Желчные кислоты
Одна из теорий предполагает увеличение уровня желчных кислот в коже пациентов с холестатическими заболеваниями, что приводит к появлению кожного зуда. Наблюдения последователей данной теории демонстрируют, что уменьшение количества желчных кислот в поверхностных слоях кожи у данной группы пациентов связано с интенсивностью зуда, хотя достоверность используемых для определения этого методов остается сомнительной [2]. Другие исследования показывают возможность того, что прием желчных кислот индуцирует и усиливает кожный зуд [3, 4].
Существуют, однако, три исследования, результаты которые не противоречат основной роли желчных кислот как причине кожного зуда:
- случайное уменьшение кожного зуда, несмотря на продолжающийся холестаз и наличие высокого уровня желчных кислот в плазме [5];
- отсутствие зуда у многих пациентов с холестазом и повышенным уровнем желчных кислот в плазме [5];
- очевидный недостаток корреляции между наличием и тяжестью кожного зуда и концентрацией желчных кислот в коже пациентов с хроническим холестазом в большинстве тщательно проведенных исследований, посвященных этой проблеме [6].
Более того, холестирамин и холестипол – препараты, используемые для лечения холестатического кожного зуда, также приводят к уменьшению зуда у пациентов с уремией и истинной полицитемией, т. е. состояниями, не связанными с задержкой солей желчных кислот.
Относительность гипотез спутывается тем, что повышенный уровень желчных кислот в плазме вследствие гепатотоксичности влияет на кожный зуд в большей степени, нежели их прямой эффект на нервные окончания [7]. Очищенные желчные кислоты повреждают мембраны гепатоцитов, позволяя содержимому клеток (большая часть которого может вызывать кожный зуд) вытекать в общий кровоток.
Эндогенные опиоиды
Все больше значения придается роли эндогенных опиоидов в патогенезе кожного холестатического зуда [8]. Назначение опиатов с агонистической активностью к опиоидным μ-рецепторам может усиливать кожный зуд у здоровых людей, предположительно за счет центрального действия. Более важно, что эндогенный уровень опиатов увеличивается (по неясному механизму) у пациентов с хроническими заболеваниями печени [9, 10], и множество исследований показывают уменьшение холестатического кожного зуда у пациентов, получающих лечение антагонистами опиоидных рецепторов [8, 11–13].
Лизофосфатидная кислота и аутотаксин
Предварительные исследования подтверждают важность роли лизофосфатидной кислоты (ЛФК) при холестатическом кожном зуде [14]. ЛФК относится к фосфолипидам, образуемым под действием аутотаксина, который отщепляет группу холина от лизофосфатидилхолина. В сравнении с контролем пациенты с холестатическим зудом имеют значимо более высокий сывороточный уровень концентрации ЛФК и активность аутотаксина. Более того, инъекции ЛФК индуцируют реакции расчесывания у мышей. Эти исследования требуют подтверждения, но указывают на потенциальную роль ингибиторов аутотаксина как вариант терапевтической стратегии.
Лечение
Вариантом выбора при кожном зуде, ассоциированном с холестазом, может быть лечение основного заболевания печени и желчевыводящих путей. При внепеченочной билиарной обструкции в случаях, при которых основная терапия невозможна, обычно билиарный дренаж весьма эффективен в прекращении кожного зуда. При внутрипеченочном холестазе в случаях, при которых основная терапия невозможна, могут быть применены некоторые медикаментозные средства, что позволяет облегчить симптомы зуда.
Достаточно сложно оценить эффективность лекарственной терапии кожного зуда в клинических исследованиях, поскольку симптомы зуда являются весьма субъективными и могут усиливаться и ослабляться спонтанно. Однако исследователи сейчас имеют современное оборудование для мониторирования активности кожного зуда, которое позволяет регистрировать интенсивность расчесывания независимо от крупных движений тела, таким образом, учитывают поведенческую методологию в клинических исследованиях зуда [15]. И все же клинические исследования в своем большинстве небольшие и используют различные шкалы для оценки зуда, поэтому ограниченно сравнимы друг с другом [16].
В легких случаях зуд может контролироваться с помощью неспецифических мероприятий, таких как теплые ванны, смягчающие и успокаивающие средства. Однако многие из этих средств часто не оказывают эффекта при умеренном и тяжелом зуде или зуде, сопровождающемся экскориациями. В таких случаях используются следующие опции лечения.
Производные желчных кислот
Холестирамин и холестипол эффективны как первая линия препаратов в лечении умеренного и тяжелого холестатического зуда на основании их благоприятного профиля безопасности и результатов клинических исследований [17]. Клинических контролируемых исследований по их применению достаточно много [16].
Эти препараты не абсорбируются и содержат основные полистерины, которые связывают анионы в просвете кишечника. Они также снижают уровень желчных кислот посредством ингибирования реабсорбции желчных кислот примерно на 90%. Тем не менее, только связывание желчных кислот, к сожалению, не может объяснить их эффект, а более мощные секвестранты желчных кислот (холесевелам) неэффективны при холестатическом зуде по сравнению с плацебо в контролируемых исследованиях [18]. Они также уменьшают зуд при нехолестатических нарушениях, таких как уремия и истинная полицитемия, подтверждая, что воздействуют и на другие механизмы зуда.
Эффективная доза холестирамина находится в интервале от 4 до 16 г/сут. Кроме этого, эффективность может быть увеличена за счет назначения дозы до и после приема пищи у пациентов с интактным желчным пузырем и повышенной секрецией зудогенных веществ, которые, возможно, накапливаются в желчном пузыре в течение ночного периода. Однако приверженность к лечению является основной проблемой использования производных желчных кислот. Эти препараты относительно неприятные на вкус, могут провоцировать запоры и усиливать абсорбцию различных лекарственных препаратов, включая дигоксин, варфарин, пропранолол и тиазидные диуретики.
Рифампицин
Некоторые результаты исследований демонстрируют уменьшение холестатического зуда на дозе от 300 до 600 мг рифампицина в сутки [16, 19, 20]. Первоначально предполагалось, что рифампицин может уменьшать зуд вследствие конкурирования с желчными кислотами за захват в печени, таким образом минимизируя токсичность желчных кислот в отношении гепатоцитов. Напротив, рифампицин может индуцировать микросомальные ферменты, что усиливает 6-альфа-гидроксиляцию и последовательно глюкуронизацию токсичных солей желчных кислот. Однако эти эффекты не подтверждены, и механизм взаимодействия остается неясным.
Хотя токсичность рифампицина не была обнаружена в этих предварительных исследованиях, следует соблюдать осторожность при использовании рифампицина при холестатических состояниях в связи с иногда возникающими гепатитами и тяжелыми идиосинкратическими реакциями [16].
Антагонисты опиоидных рецепторов
Применение антагонистов опиоидов, таких как инъекционный налоксон (применяемый болюсно 0,4 мг с последующим введение 0,2 мкг/кг/мин. в течение суток), пероральный налмефен (от 60 до 120 мг/сут), пероральный налтрексон (от 12,5 до 50 мг/сут), часто ассоциируется с частичным облегчением холестатического зуда [11, 16, 21–24]. Это иллюстрируется контролируемым перекрестным исследованием на 29 пациентах, которое показало уменьшение потребности в расчесывании на 27% и значимое снижение восприятия зуда [21]. Похожее исследование на 16 пациентах, рандомизированных в группы налтрексона или плацебо, показало, что налтрексон был ассоциирован со значительным уменьшением симптомов зуда в дневное время (изменение интенсивности зуда -54% против -8%) также эффективно, как и в ночное время (-44% против -7%) [22]. Стойкое улучшение наблюдалось спустя 2 мес. по результатам третьего плацебо-контролируемого перекрестного исследования, включающего 20 пациентов [24]. У 9 больных отмечено уменьшение зуда более чем на 50%, и у 5 пациентов симптомы зуда были купированы полностью.
Антагонисты опиоидов обычно хорошо переносятся, за исключением ограниченных «синдромов отмены», которые чаще всего разрешаются самостоятельно в течение 2 дней [24]. Эти проблемы более очевидны при приеме налмефена, который в настоящее время доступен только для экспериментального использования [23]. Возникновение и интенсивность «синдрома отмены» могут быть уменьшены путем осторожного инициирующего внутривенного введения (т. к. налоксон вводится внутривенно медленно со скоростью 0,002 мкг/кг/мин и скорость введения постепенно повышается до достижения терапевтической дозы) и перехода на последующую пероральную терапию [25]. В дополнение антагонисты опиоидов могут приводить к неконтролируемому болевому синдрому у пациентов, имеющих боли различного генеза (например, постгерпетическая невралгия) [26]. К тому времени, когда роль эндогенных опиоидов при холестатическом зуде будет лучше изучена, использование этих препаратов, в т. ч. для перорального приема, станет более распространено в клинической практике.
Урсодезоксихолевая кислота
Урсодезоксихолевая кислота (УДХК) природного происхождения – желчная кислота, назначаемая экзогенно, она изменяет пул желчных кислот на более гидрофильные [27, 28]. Остается неясным, вызван ли этот эффект конкуренцией при кишечной абсорбции эндогенных желчных кислот или повышением печеночного клиренса эндогенных желчных кислот. УДХК используется в лечении некоторых форм холестатических заболеваний печени, в т. ч. первичного билиарного цирроза.
Эффект УДХК в отношении зуда, однако, остается неясным [29]. Два больших клинических исследования по первичному билиарному циррозу, например, не показали уменьшения зуда при дозировке УДХК от 13 до 15 мг/кг/сут [30, 31]. Для сравнения: терапия высокими дозами (30 мг/кг/сут, разделенные на 3 приема) в других исследованиях показала значительное облегчение симптомов зуда [32]. В проведенных позднее исследованиях зуд исчезал у 6 из 7 пациентов менее чем за 1 мес.
Другие средства
В лечении зуда могут найти применение и множество других препаратов, однако количество исследований, проведенных с их применением, весьма ограниченно и включает лишь небольшое число пациентов.
Совместное использование колхицина и метотрексата значимо уменьшает зуд в контролируемом двойном слепом исследовании, включающем 85 пациентов с первичным билиарным циррозом, которые вели ежедневник по оценке зуда [33]. Фенобарбитал показал эффект в ряде исследований [34, 35].
Клинические примеры и небольшие контролируемые исследования подтверждают возможную эффективность селективных ингибиторов обратного захвата серотонина. Сертралин (от 75 до 100 мг/сут) был эффективен по результатам ретроспективного анализа группы пациентов с первичным билиарным циррозом, которые были частью исследования УДХК с метотрексатом и без него [36], а также в небольшом рандомизированном плацебо-контролируемом перекрестном исследовании пациентов с зудом при различных заболеваниях печени [37]. Пароксетин показал хороший результат у пациентов с тяжелым недерматологическим зудом (большинство из которых имели не связанные с заболеваниями печени причины зуда) [38].
Фототерапия с использованием ультрафиолета (UV–B) имела эффект в ряде исследований [39–41]. Механизм уменьшения зуда неясен, хотя гипотеза предполагает нарушение кожной чувствительности к веществам, вызывающим зуд, или изменение пула желчных кислот посредством мобилизации желчных кислот кожи. В нашем опыте фототерапия не имела эффекта более чем у 80% пациентов с первичным билиарным циррозом, которые не ответили на терапию холестирамином.
Некоторые исследования демонстрируют облегчение симптомов зуда после проведения плазмафереза у пациентов с холестазом [42–44]. Однако клинический опыт достаточно противоречив и неоднороден. Эта техника слишком многовариантна для оценки и трудноприменима для рутинного использования. Но плазмаферез может играть определенную роль в том случае, если остальные методы неэффективны, а также у пациентов с циррозом печени для уменьшения зуда.
Пропофол – седативный анестетик, назначали 3 пациентам внутривенно в субгипнотических дозах [45]. Было отмечено значимое уменьшение зуда без отключения седации. Предполагаемый механизм связан с ингибированием вентральных и дорсальных рогов спинного мозга, модулированным опиоидоподобными лигандами.
Андрогены (такие как норетандролон, метилтестостерон, станозолол) увеличивают содержание в сыворотке желчных кислот и ухудшают желтуху, также они парадоксально облегчают симптомы зуда у пациентов с холестазом [46]. Механизм этого воздействия остается неясным, но множество побочных эффектов ограничивают применение подобных препаратов.
Дельта-9-тетрагидроканнабинол облегчает симптомы зуда в некоторых наблюдениях [47].
Молекулярная адсорбционная система кровообращения (устройства для гемофильтрации) также была эффективна в нескольких сериях наблюдений [48–51].
Трансплантация печени
Тяжелый кожный зуд, рефрактерный к другим средствам терапии, может являться относительным показанием для трансплантации печени у пациентов с тяжелыми формами холестаза. Функционирующий трансплантат печени компенсирует основное заболевание и способствует быстрому разрешению зуда.
Стандарты Американской ассоциации по изучению печени (AASLD, 2009)
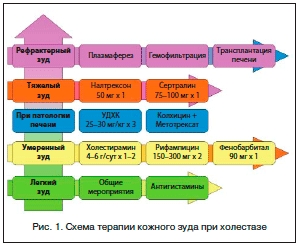
Рекомендуют следующий подход для лечения зуда при холестазе, ассоциированном с заболеваниями печени. Терапию начинают секвестрантами желчных кислот. Они назначаются от 2 до 4 р./сут до или после приема УДХК. У пациентов с зудом, рефрактерным к лечению секвестрантами желчных кислот, в качестве следующего шага терапии может быть использован: рифампицин (от 150 до 300 мг 2 р./сут ) или пероральные антагонисты опиатов, например налтрексон (50 мг/сут). Сертралин (от 75 до 100 мг/сут) может быть использован при неэффективности остальных методов (рис. 1).
Выводы и рекомендации
1. Лечение кожного зуда, ассоциированного с холестазом, в первую очередь должно быть сконцентрировано на терапии основного заболевания гепатобилиарной системы. Принципиально отличается тактика лечения внепеченочной билиарной обструкции и внутрипеченочного холестаза – основных приводящих к развитию зуда состояний.
2. Оптимальное лечение кожного зуда при холестазе окончательно не определено, хотя некоторые исследования изучили ряд возможностей для лечения (в скобках указан класс доказанности). В качестве основного критерия выбора терапии служит тяжесть и интенсивность зуда.
- Для коррекции зуда легкой степени рекомендуются общие мероприятия, такие как теплые ванны с приемом или без антигистаминных средств (Класс 2С).
- Для коррекции умеренного и тяжелого зуда или легкого зуда при неэффективности общих мероприятий рекомендуются холестирамин или холестипол (Класс 2В). Эффективная доза холестирамина – от 4 до 16 г/сут. Эффективность может повышаться при назначении до или после приема пищи у пациентов с интактным желчным пузырем.
- Для коррекции зуда у пациентов, не ответивших на холестирамин и холестипол, рекомендуется рифампицин 150 мг 2 р./сут (Класс 2В).
Он иногда используется и в первой линии терапии. У не ответивших на рифампицин пациентов рекомендуется фенобарбитал (90 мг однократно на ночь), хотя в течение первой недели приема возможна сонливость (Класс 2С).
- Для лечения зуда у пациентов с заболеваниями печени рекомендуется УДХК в высокой дозировке 25–30 мг/кг/сут, разделенная на 3 приема. Для лечения зуда у пациентов с первичным билиарным циррозом рекомендуется в добавление к УДХК назначение колхицина и метотрексата – для не ответивших пациентов (Класс 2С).
- Для лечения тяжелого зуда и у не ответивших на другую терапию рекомендуются антагонисты опиоидов (Класс 2В).