–Ъ—А–∞–њ–Є–≤–љ–Є—Ж–∞ (Urtica, –ї–∞—В. – –Ї—А–∞–њ–Є–≤–∞) – –Њ–±—Й–µ–µ –љ–∞–Ј–≤–∞–љ–Є–µ –≥—А—Г–њ–њ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —А–∞–Ј–ї–Є—З–∞—О—Й–Є—Е—Б—П –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є —А–∞–Ј–≤–Є—В–Є—П –Є —А–∞–Ј–љ—Л–Љ–Є –Љ–µ—В–Њ–і–Є—З–µ—Б–Ї–Є–Љ–Є –њ–Њ–і—Е–Њ–і–∞–Љ–Є –Ї –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є —В–µ—А–∞–њ–Є–Є.
–Ъ—А–∞–њ–Є–≤–љ–Є—Ж–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –љ–µ —В–Њ–ї—М–Ї–Њ –≤–∞–ґ–љ—Г—О –Љ–µ–і–Є—Ж–Є–љ—Б–Ї—Г—О, –љ–Њ –Є —Б–µ—А—М–µ–Ј–љ—Г—О —Б–Њ—Ж–Є–∞–ї—М–љ—Г—О –њ—А–Њ–±–ї–µ–Љ—Г –≤ —Б–≤—П–Ј–Є —Б –≤—Л—Б–Њ–Ї–Њ–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М—О, –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ —Г–љ–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ–і—Е–Њ–і–Њ–≤ –Ї –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О, –±–Њ–ї—М—И–Є–Љ–Є —Д–Є–љ–∞–љ—Б–Њ–≤—Л–Љ–Є –Ј–∞—В—А–∞—В–∞–Љ–Є –љ–∞ —В–µ—А–∞–њ–Є—О –Є —А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є—О, —А–µ–Ј–Ї–Є–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–Ю—Б–љ–Њ–≤–љ–Њ–є –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Н–ї–µ–Љ–µ–љ—В –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л – –≤–Њ–ї–і—Л—А—М. –Т–Њ–ї–і—Л—А–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —З–µ—В–Ї–Њ –Њ—В–≥—А–∞–љ–Є—З–µ–љ–љ—Л–µ, –≤–Њ–Ј–≤—Л—И–∞—О—Й–Є–µ—Б—П –љ–∞–і –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М—О –Ї–Њ–ґ–Є —Н–ї–µ–Љ–µ–љ—В—Л —А–∞–Ј–Љ–µ—А–Њ–Љ –Њ—В –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–Є–ї–ї–Є–Љ–µ—В—А–Њ–≤ –і–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —Б–∞–љ—В–Є–Љ–µ—В—А–Њ–≤, –≤–њ–ї–Њ—В—М –і–Њ –≥–Є–≥–∞–љ—В—Б–Ї–Њ–є –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л.
–Р–љ–≥–Є–Њ–љ–µ–≤—А–Њ—В–Є—З–µ—Б–Ї–Є–є –Њ—В–µ–Ї (–Р–Ю), –Є–ї–Є –Њ—В–µ–Ї –Ъ–≤–Є–љ–Ї–µ, –Њ–њ–Є—Б–∞–љ–љ—Л–є –≤ 1882 –≥. Quinke, –Ї–Њ—В–Њ—А—Л–є —З–∞—Б—В–Њ —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –Ї—А–∞–њ–Є–≤–љ–Є—Ж–µ–є –Є–ї–Є —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –Є –Њ—В–ї–Є—З–∞–µ—В—Б—П –Њ—В –њ–Њ—Б–ї–µ–і–љ–µ–є –ї–Є—И—М –≥–ї—Г–±–Є–љ–Њ–є –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ–ґ–Є. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –Њ—В–µ–Ї –Ъ–≤–Є–љ–Ї–µ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –∞—Б—Б–Є–Љ–µ—В—А–Є—З–љ—Л–Љ –Њ—В–µ–Ї–Њ–Љ –і–µ—А–Љ—Л –ї—О–±–Њ–є –Њ–±–ї–∞—Б—В–Є. –Я–∞—В–Њ–≥–µ–љ–µ–Ј –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л –Є –Њ—В–µ–Ї–∞ –Ъ–≤–Є–љ–Ї–µ –Њ–±—Й–Є–є – –љ–∞—А—Г—И–µ–љ–Є–µ –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В–Є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ —А—Г—Б–ї–∞ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –Љ–µ—Б—В–љ—Л–Љ –Њ—В–µ–Ї–Њ–Љ, –∞ –њ—А–Є –Р–Ю –≤ –њ—А–Њ—Ж–µ—Б—Б –≤–Њ–≤–ї–µ–Ї–∞—О—В—Б—П –±–Њ–ї–µ–µ –≥–ї—Г–±–Њ–Ї–Є–µ —Б–ї–Њ–Є –і–µ—А–Љ—Л.
–Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–Њ–≤–Њ–і–Є–Љ—Л—Е –≤ —А–∞–Ј–љ—Л—Е —А–µ–≥–Є–Њ–љ–∞—Е –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є, —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Ї–Њ–ґ–Є –Ї–Њ–ї–µ–±–ї–µ—В—Б—П –≤ —И–Є—А–Њ–Ї–Є—Е –њ—А–µ–і–µ–ї–∞—Е: –Њ—В 7 –і–Њ 50% –Є –±–Њ–ї–µ–µ [1,3,4].
–Ъ—А–∞–њ–Є–≤–љ–Є—Ж–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ —Б–∞–Љ—Л—Е —А–∞–Ј–љ—Л—Е –њ–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Г –Є –њ—А–Њ–≥–љ–Њ–Ј—Г –±–Њ–ї–µ–Ј–љ–µ–є (–∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ—Л–µ, –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ, —Б–Є—Б—В–µ–Љ–љ—Л–µ, –њ–∞—А–∞–Ј–Є—В–∞—А–љ—Л–µ –Є –њ—А.), —З—В–Њ –Њ–њ—А–µ–і–µ–ї—П–µ—В —Б–ї–Њ–ґ–љ–Њ—Б—В–Є –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є —В–µ—А–∞–њ–Є–Є —Н—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є.
–Ф–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В –Њ–±—Й–µ–њ—А–Є–љ—П—В–∞—П –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л, –∞ –≤—Б–µ –њ–Њ–њ—Л—В–Ї–Є –µ–µ —Б–Њ–Ј–і–∞–љ–Є—П –њ—А–Є–≤–Њ–і—П—В –Ї –њ—А–µ–і–ї–Њ–ґ–µ–љ–Є—О –≥—А–Њ–Љ–Њ–Ј–і–Ї–Є—Е —Б—Е–µ–Љ, –љ–µ —Г–і–Њ–±–љ—Л—Е –і–ї—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≤ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–Љ –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є–Є. –Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Г —А–∞–Ј–ї–Є—З–∞—О—В –њ–Њ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П: –Њ—Б—В—А–∞—П –Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞ –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞; –њ–Њ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ—Г –њ—А–Є–Ј–љ–∞–Ї—Г: —Д–Є–Ј–Є—З–µ—Б–Ї–∞—П (–Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞, –≤—Л–Ј–≤–∞–љ–љ–∞—П –і–∞–≤–ї–µ–љ–Є–µ–Љ, –≤–Є–±—А–∞—Ж–Є–Њ–љ–љ–∞—П, —Б–Њ–ї–љ–µ—З–љ–∞—П, —Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–∞—П, —В–µ–њ–ї–Њ–≤–∞—П, —Е–Њ–ї–Њ–і–Њ–≤–∞—П), –і–µ—А–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–∞—П –Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞, –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–є –≤–Є–±—А–∞—Ж–Є–Њ–љ–љ—Л–є –Њ—В–µ–Ї, –њ–Є–≥–Љ–µ–љ—В–љ–∞—П –Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞, –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П –Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞; –і—А—Г–≥–Є–µ –≤–Є–і—Л –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л: –њ–∞–њ—Г–ї–µ–Ј–љ–∞—П, –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–∞—П, –≤–∞—Б–Ї—Г–ї–Є—В, –њ–∞—А–∞–љ–µ–Њ–њ–ї–∞—Б—В–Є—З–µ—Б–Ї–∞—П, –њ—Б–Є—Е–Њ–≥–µ–љ–љ–∞—П, —Н–љ–і–Њ–Ї—А–Є–љ–љ–∞—П, –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –Є –і—А.
–Т—Л–і–µ–ї—П—О—В —В–∞–Ї–ґ–µ –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–µ —Д–Њ—А–Љ—Л –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л, –Ї –Ї–Њ—В–Њ—А—Л–Љ –Њ—В–љ–Њ—Б—П—В –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–є –∞–љ–≥–Є–Њ–љ–µ–≤—А–Њ—В–Є—З–µ—Б–Ї–Є–є –Њ—В–µ–Ї, –љ–∞—А—Г—И–µ–љ–Є–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –њ—А–Њ—В–Њ–њ–Њ—А—Д–Є—А–Є–љ–∞, —Б–Є–љ–і—А–Њ–Љ –®–љ–Є—В—Ж–ї–µ—А–∞ (–Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞, –∞–Љ–Є–ї–Њ–Є–і–Њ–Ј, –≥–ї—Г—Е–Њ—В–∞), –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–∞—П —Е–Њ–ї–Њ–і–Њ–≤–∞—П –Ї—А–∞–њ–Є–≤–љ–Є—Ж–∞, –і–µ—Д–Є—Ж–Є—В –°3–≤ –Є–љ–∞–Ї—В–Є–≤–∞—В–Њ—А–∞.
–І–∞—Й–µ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—О, –≤ –Њ—Б–љ–Њ–≤–µ –Ї–Њ—В–Њ—А–Њ–є –ї–µ–ґ–Є—В –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–є –њ—А–Є–љ—Ж–Є–њ.
–Я–Њ —Н—В–Њ–Љ—Г –њ—А–Є–љ—Ж–Є–њ—Г –≤—Л–і–µ–ї—П—О—В –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Г, –≤ –Љ–µ—Е–∞–љ–Є–Ј–Љ–µ –Ї–Њ—В–Њ—А–Њ–є –ї–µ–ґ–∞—В –љ–∞—А—Г—И–µ–љ–Є—П –≤ —Б–Є—Б—В–µ–Љ–µ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞: –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–∞—П (–њ–Є—Й–µ–≤–∞—П, –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П, –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Г–ґ–∞–ї–µ–љ–Є–є, —В—А–∞–љ—Б—Д—Г–Ј–Є–Њ–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –Є –і—А.), –∞–љ–∞—Д–Є–ї–∞–Ї—В–Њ–Є–і–љ–∞—П, –њ—Б–µ–≤–і–Њ–∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–∞—П (–њ–Є—Й–µ–≤–∞—П, –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П, –∞—Б–њ–Є—А–Є–љ–Ј–∞–≤–Є—Б–Є–Љ–∞—П).
–Ь–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–Є–µ –њ—А–Є—З–Є–љ –Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л –Њ–±—К—П—Б–љ—П–µ—В —Б–ї–Њ–ґ–љ–Њ—Б—В–Є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є —В–µ—А–∞–њ–Є–Є –∞–ї–ї–µ—А–≥–Њ–і–µ—А–Љ–∞—В–Њ–Ј–Њ–≤ –≤–Њ–Њ–±—Й–µ –Є –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є.
–Ъ –Њ—Б–љ–Њ–≤–љ—Л–Љ –њ—А–Є–љ—Ж–Є–њ–∞–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л –Њ—В–љ–Њ—Б—П—В—Б—П –≤—Л—П–≤–ї–µ–љ–Є–µ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є –њ—А–Њ–≤–Њ—Ж–Є—А—Г—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є—Е —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Я—А–Њ—В–Њ–Ї–Њ–ї –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л –≤–Ї–ї—О—З–∞–µ—В:
- –°–±–Њ—А –∞–љ–∞–Љ–љ–µ–Ј–∞ –ґ–Є–Ј–љ–Є –Є –±–Њ–ї–µ–Ј–љ–Є
- –Ъ–ї–Є–љ–Є–Ї–Њ––ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–µ –Љ–µ—В–Њ–і—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
- –†–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ, –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л–µ, —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –Є –і—А—Г–≥–Є–µ (–њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ) –Љ–µ—В–Њ–і—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
- –Р–ї–ї–µ—А–≥–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
- –Ш–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–°—Г—Й–µ—Б—В–≤—Г—О—В –Њ–±—П–Ј–∞—В–µ–ї—М–љ—Л–µ –Љ–µ—В–Њ–і—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ.
–Ю–±—П–Ј–∞—В–µ–ї—М–љ—Л–µ –Љ–µ—В–Њ–і—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–Њ–ї–ґ–љ—Л –њ—А–Њ–≤–Њ–і–Є—В—М—Б—П –љ–µ—Г–Ї–Њ—Б–љ–Є—В–µ–ї—М–љ–Њ –≤—Б–µ–Љ–Є –≤—А–∞—З–∞–Љ–Є, –µ—Б–ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–∞ –≤—Л—Б—В–∞–≤–ї—П–µ—В—Б—П –і–Є–∞–≥–љ–Њ–Ј –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л.
–Ъ –Њ–±—П–Ј–∞—В–µ–ї—М–љ—Л–Љ –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–Љ –Љ–µ—В–Њ–і–∞–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Є –Ї—А–∞–њ–Є–≤–љ–Є—Ж–µ –Њ—В–љ–Њ—Б—П—В—Б—П:
- –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є
- –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є (–Њ–±—Й–Є–є –±–µ–ї–Њ–Ї, –±–Є–ї–Є—А—Г–±–Є–љ –Њ–±—Й–Є–є –Є –њ—А—П–Љ–Њ–є, –Р–°–Ґ, –Р–Ы–Ґ, –≥–ї—О–Ї–Њ–Ј–∞, —В–Є–Љ–Њ–ї–Њ–≤–∞—П –њ—А–Њ–±–∞, CRP)
- –Њ–±—Й–Є–є –∞–љ–∞–ї–Є–Ј –Љ–Њ—З–Є
- RW, –Т–Ш–І
–Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –Љ–µ—В–Њ–і—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞–Ј–љ–∞—З–∞—О—В—Б—П –≤ —В–µ—Е —Б–ї—Г—З–∞—П—Е, –Ї–Њ–≥–і–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—В–Њ—З–љ–Є—В—М –њ—А–Є—З–Є–љ—Л –Є –Љ–µ—Е–∞–љ–Є–Ј–Љ —А–∞–Ј–≤–Є—В–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –∞ –Њ–±—П–Ј–∞—В–µ–ї—М–љ—Л–µ –Љ–µ—В–Њ–і—Л –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Є –љ–µ –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ—Л.
–Ъ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ –Љ–µ—В–Њ–і–∞–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Є –Ї—А–∞–њ–Є–≤–љ–Є—Ж–µ –Њ—В–љ–Њ—Б—П—В—Б—П:
- –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ–і–µ—А–ґ–Є–Љ–Њ–≥–Њ, —Д–µ–Ї–∞–ї–Є–є
- –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ–Њ—Б–µ–≤—Л –љ–∞ —Д–ї–Њ—А—Г —Б–Њ —Б–ї–Є–Ј–Є—Б—В–Њ–є —А–Њ—В–Њ–≥–ї–Њ—В–Ї–Є
- –њ–∞—А–∞–Ј–Є—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ (–Ї–Њ–њ—А–Њ—Ж–Є—В–Њ—Б–Ї–Њ–њ–Є—П, –Р–Ґ –Ї –Р–У —В–Њ–Ї—Б–Њ–Ї–∞—А—Л, —Н—Е–Є–љ–Њ–Ї–Њ–Ї–Ї–∞, –Њ–њ–Є—Б—В–Њ—А—Е–Є—Б–∞, —В—А–Є—Е–Є–љ–µ–ї–ї—Л)
- –£–Ч–Ш –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –і—А—Г–≥–Є—Е –Њ—А–≥–∞–љ–Њ–≤ (–њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ)
- –і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–µ –Ј–Њ–љ–і–Є—А–Њ–≤–∞–љ–Є–µ —Б –њ–Њ—Б–µ–≤–Њ–Љ –њ–Њ—А—Ж–Є–є –ґ–µ–ї—З–Є –Т –Є –°
- –≤–µ–ї–Њ—Н—А–≥–Њ–Љ–µ—В—А–Є—П
- —А–µ–љ—В–≥–µ–љ–Њ–≥—А–∞–Љ–Љ–∞ –Ю–У–Ъ –Є –Я–Я–Э
- –Ї–Њ–ї–Њ–љ–Њ—Б–Ї–Њ–њ–Є—П
- –і—А—Г–≥–Є–µ –Љ–µ—В–Њ–і—Л –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ
–Ъ–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є–Є —Б–њ–µ—Ж–Є–∞–ї–Є—Б—В–Њ–≤
- –≥–∞—Б—В—А–Њ—Н–љ—В–µ—А–Њ–ї–Њ–≥, –≥–µ–њ–∞—В–Њ–ї–Њ–≥
- –Њ—В–Њ–ї–∞—А–Є–љ–≥–Њ–ї–Њ–≥
- —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥
- –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥
- —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥
- –і—А—Г–≥–Є–µ – –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ
–Я–Њ—Б–ї–µ –∞–љ–∞–ї–Є–Ј–∞ –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±–Њ–ї—М–љ—Л—Е –Ї—А–∞–њ–Є–≤–љ–Є—Ж–µ–є –≤—А–∞—З –Њ–њ—А–µ–і–µ–ї—П–µ—В –Њ–±—К–µ–Љ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є, —Б—Е–µ–Љ—Л –Є –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П.
–Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –њ—А–Є–љ—Ж–Є–њ–∞–Љ–Є —В–µ—А–∞–њ–Є–Є, –Ї–Њ—В–Њ—А—Л–µ –Њ—В–≤–µ—З–∞—О—В –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–Љ —Б—В–∞–љ–і–∞—А—В–∞–Љ, —П–≤–ї—П—О—В—Б—П:
- —Г—Б—В—А–∞–љ–µ–љ–Є–µ (—Н–ї–Є–Љ–Є–љ–∞—Ж–Є—П) –њ—А–Є—З–Є–љ–љ—Л—Е –Є –њ—А–Њ–≤–Њ—Ж–Є—А—Г—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤
- —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П
- –ї–µ—З–µ–љ–Є–µ –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П
- –Ї–Њ—А—А–µ–Ї—Ж–Є—П —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є
- –Њ–±—Г—З–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –∞–ї–ї–µ—А–≥–Њ—И–Ї–Њ–ї–µ
–Ы–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–∞—П —В–µ—А–∞–њ–Є—П (—Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П) –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Њ–і–љ–Є–Љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л, —Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –Њ—Б–Њ–±–Њ–µ –Љ–µ—Б—В–Њ –Ј–∞–љ–Є–Љ–∞—О—В –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л [2].
–Ю–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ–µ–є—И–Є—Е –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л—Е –Ј–∞ —А–∞–Ј–≤–Є—В–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л, —П–≤–ї—П–µ—В—Б—П –≥–Є—Б—В–∞–Љ–Є–љ. –У–Є—Б—В–∞–Љ–Є–љ –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ —Б–Њ–і–µ—А–ґ–Є—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ —В—Г—З–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е –Є –±–∞–Ј–Њ—Д–Є–ї–∞—Е.
–Т—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –µ–≥–Њ –Є–Ј —В—Г—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –Є –±–∞–Ј–Њ—Д–Є–ї–Њ–≤ –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л–Ј–≤–∞–љ–Њ –Ї–∞–Ї IgE––Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –њ—А–Є –У–Э–Ґ, —В–∞–Ї –Є —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–Љ–Є –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є –љ–µ–Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є —Б—В–Є–Љ—Г–ї–∞–Љ–Є, –њ—А–Є–≤–Њ–і—П—Й–Є–Љ–Є –Ї –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Ї–ї–µ—В–Њ–Ї –Є –Ј–∞–њ—Г—Б–Ї—Г —Б–µ–Ї—А–µ—В–Њ—А–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞.
–®–Є—А–Њ–Ї–Є–є —Б–њ–µ–Ї—В—А —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –≥–Є—Б—В–∞–Љ–Є–љ–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –µ–≥–Њ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ–Љ –Є–Ј —В—Г—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї –Є –±–∞–Ј–Њ—Д–Є–ї–Њ–≤, –Є –≤–Њ–≤–ї–µ—З–µ–љ–Є–µ –≤ —А–µ–∞–Ї—Ж–Є—О —А–∞–Ј–љ—Л—Е —В–Ї–∞–љ–µ–є, –Њ—А–≥–∞–љ–Њ–≤ –Є —Б–Є—Б—В–µ–Љ. –Ґ–Є–њ–Є—З–љ—Л–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –і–µ–є—Б—В–≤–Є—П –≥–Є—Б—В–∞–Љ–Є–љ–∞ —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ї–Њ–ґ–Є —П–≤–ї—П–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ –Ј—Г–і–∞, –≥–Є–њ–µ—А–µ–Љ–Є–Є, –≤–Њ–ї–і—Л—А–љ—Л—Е –Є –љ–µ—Г—А—В–Є–Ї–∞—А–љ—Л—Е –≤—Л—Б—Л–њ–∞–љ–Є–є. –°–Њ —Б—В–Њ—А–Њ–љ—Л –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –≤–ї–Є—П–љ–Є—П –≥–Є—Б—В–∞–Љ–Є–љ–∞ —П–≤–ї—П—О—В—Б—П: –Њ—В–µ–Ї —Б–ї–Є–Ј–Є—Б—В–Њ–є –љ–Њ—Б–∞, –≥–Є–њ–µ—А—Б–µ–Ї—А–µ—Ж–Є—П —Б–ї–Є–Ј–Є –≤ –њ–Њ–ї–Њ—Б—В–Є –љ–Њ—Б–∞, –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ –Є –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є—П —Б–ї–Є–Ј–Є –±—А–Њ–љ—Е–Є–∞–ї—М–љ—Л–Љ–Є –ґ–µ–ї–µ–Ј–∞–Љ–Є.
–°—А–µ–і–Є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–Њ–ґ–љ–Њ –≤—Л–і–µ–ї–Є—В—М —В—А–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –≥—А—Г–њ–њ—Л –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л—Е –≤ –ї–µ—З–µ–љ–Є–Є –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Ї–Њ–ґ–Є:
- –њ—А–µ–њ–∞—А–∞—В—Л, –±–ї–Њ–Ї–Є—А—Г—О—Й–Є–µ –Э1––≥–Є—Б—В–∞–Љ–Є–љ–Њ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л (–∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ–µ—А–≤–Њ–є, –≤—В–Њ—А–Њ–є –Є —В—А–µ—В—М–µ–є –≥–µ–љ–µ—А–∞—Ж–Є–Є). –≠—В–∞ –≥—А—Г–њ–њ–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –≤ –њ–µ—А–Є–Њ–і –Њ–±–Њ—Б—В—А–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –і–ї—П —Б–љ—П—В–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л (—Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П);
- –њ—А–µ–њ–∞—А–∞—В—Л, –њ–Њ–≤—Л—И–∞—О—Й–Є–µ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б—Л–≤–Њ—А–Њ—В–Ї–Є –Ї—А–Њ–≤–Є —Б–≤—П–Ј—Л–≤–∞—В—М –≥–Є—Б—В–∞–Љ–Є–љ (–≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –≥–Є—Б—В–∞–≥–ї–Њ–±—Г–ї–Є–љ—Л). –≠—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –љ–∞–Ј–љ–∞—З–∞—О—В –≤ –Ї–∞—З–µ—Б—В–≤–µ –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є –≥–Є–њ–Њ—Б–µ–љ—Б–Є–±–Є–ї–Є–Ј–∞—Ж–Є–Є –Є –і–ї—П —Б–љ–Є–ґ–µ–љ–Є—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ї –≥–Є—Б—В–∞–Љ–Є–љ—Г;
- –њ—А–µ–њ–∞—А–∞—В—Л, —В–Њ—А–Љ–Њ–Ј—П—Й–Є–µ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –≥–Є—Б—В–∞–Љ–Є–љ–∞ –Є–Ј —В—Г—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї (–Ї–µ—В–Њ—В–Є—Д–µ–љ, –Ї—А–Њ–Љ–Њ–ї–Є–љ––љ–∞—В—А–Є–є –Є –і—А.). –Я—А–µ–њ–∞—А–∞—В—Л —Н—В–Њ–є –≥—А—Г–њ–њ—Л –љ–∞–Ј–љ–∞—З–∞—О—В –љ–∞ –і–ї–Є—В–µ–ї—М–љ—Л–є —Б—А–Њ–Ї, –Ї–∞–Ї –±–∞–Ј–Є—Б–љ—Г—О –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї—Г—О —В–µ—А–∞–њ–Є—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В–Є.
–Т—Л–і–µ–ї—П—О—В —В—А–Є –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –±–ї–Њ–Ї–Є—А—Г—О—Й–Є—Е –≥–Є—Б—В–∞–Љ–Є–љ–Њ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л – –±–ї–Њ–Ї–∞—В–Њ—А—Л –Э1–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤: –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ–µ—А–≤–Њ–≥–Њ, –≤—В–Њ—А–Њ–≥–Њ –Є —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П.
–Р–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ–µ—А–≤–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Њ—В–љ–Њ—Б—П—В—Б—П –Ї —З–Є—Б–ї—Г –љ–∞–Є–±–Њ–ї–µ–µ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л—Е –≤ –Љ–Є—А–µ –≤ —В–µ—З–µ–љ–Є–µ –і–µ—Б—П—В–Ї–Њ–≤ –ї–µ—В (—В–∞–±–ї. 1). –Э–µ—А–µ–і–Ї–Њ –Њ–љ–Є –Њ—В–њ—Г—Б–Ї–∞—О—В—Б—П –і–∞–ґ–µ –±–µ–Ј —А–µ—Ж–µ–њ—В–∞ –≤—А–∞—З–∞.
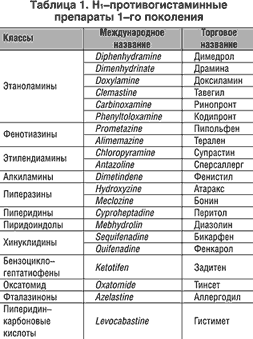
–Э1––∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Њ–±–ї–∞–і–∞—О—В —Б–ї–µ–і—Г—О—Й–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є, —Б–≤—П–Ј–∞–љ–љ—Л–Љ–Є —Б —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–Њ–є:
– –ї–Є–њ–Њ—Д–Є–ї—М–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –љ–∞–ї–Є—З–Є–µ–Љ –≤ –Љ–Њ–ї–µ–Ї—Г–ї–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Є–ї–Є –≥–µ—В–µ—А–Њ—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є—Е –Ї–Њ–ї–µ—Ж –Є –∞–ї–Ї–Є–ї—М–љ—Л—Е –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї–µ–є;
– –Њ—Б–љ–Њ–≤–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –љ–Є—В—А–Њ–≥—А—Г–њ–њ—Л;
– –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В—М «—Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ» –∞—В–Њ–Љ–∞ (–≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ—А–Є—А–Њ–і—Л —Н—В–Њ–≥–Њ –∞—В–Њ–Љ–∞ –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—В–Є–≤–Њ–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ—А–Є–љ—П—В–Њ –і–µ–ї–Є—В—М –љ–∞ 6 –Њ—Б–љ–Њ–≤–љ—Л—Е –≥—А—Г–њ–њ: —Н—В–∞–љ–Њ–ї–∞–Љ–Є–љ—Л, —Д–µ–љ–Њ—В–Є–∞–Ј–Є–љ—Л, —Н—В–Є–ї–µ–љ–і–Є–∞–Љ–Є–љ—Л, –∞–ї–Ї–Є–ї–∞–Љ–Є–љ—Л, –њ–Є–њ–µ—А–∞–Ј–Є–љ—Л, –њ–Є–њ–µ—А–Є–і–Є–љ—Л).
–Э–Њ, –Ї–∞–Ї –њ–Њ–Ї–∞–Ј–∞–ї–Є –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Э1––∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л 1––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –≤—Л–Ј—Л–≤–∞—О—В —Ж–µ–ї—Л–є —А—П–і –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ (—Б—А–µ–і–Є –Ї–Њ—В–Њ—А—Л—Е –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є – —Б–µ–і–∞—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В), –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—О—Й–Є—Е –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ –Ї–ї–Є–љ–Є–Ї–µ.
–Ю—Б–љ–Њ–≤–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Э1––∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ 1––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П:
– –±–ї–Њ–Ї–∞–і–∞ —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –і—А—Г–≥–Є—Е –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ (–љ–∞–њ—А–Є–Љ–µ—А, –Ь–—Е–Њ–ї–Є–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —З—В–Њ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –≤ –≤–Є–і–µ —Б—Г—Е–Њ—Б—В–Є —Б–ї–Є–Ј–Є—Б—В—Л—Е –њ–Њ–ї–Њ—Б—В–Є —А—В–∞, –љ–Њ—Б–∞, –≥–Њ—А–ї–∞, –±—А–Њ–љ—Е–Њ–≤; —А–µ–і–Ї–Њ – —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–Њ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є—П –Є —Г—Е—Г–і—И–µ–љ–Є–µ –Ј—А–µ–љ–Є—П);
– –Љ–µ—Б—В–љ–Њ––∞–љ–µ—Б—В–µ–Ј–Є—А—Г—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ
– —Е–Є–љ–Є–і–Є–љ–Њ––њ–Њ–і–Њ–±–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ —Б–µ—А–і–µ—З–љ—Г—О –Љ—Л—И—Ж—Г;
– –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –Є —Г—Б–Є–ї–Є–≤–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–∞–Љ;
– –њ—А–Њ—В–Є–≤–Њ—А–≤–Њ—В–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ;
– –і–µ–є—Б—В–≤–Є–µ –љ–∞ –¶–Э–° (—Б–µ–і–∞—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В, –љ–∞—А—Г—И–µ–љ–Є–µ –Ї–Њ–Њ—А–і–Є–љ–∞—Ж–Є–Є, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ, –≤—П–ї–Њ—Б—В—М, —Б–љ–Є–ґ–µ–љ–Є–µ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞—В—М –≤–љ–Є–Љ–∞–љ–Є–µ);
– –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–њ–њ–µ—В–Є—В–∞;
– —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Ц–Ъ–Ґ (—В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞, –њ–Њ–љ–Њ—Б, –њ–Њ—В–µ—А—П –∞–њ–њ–µ—В–Є—В–∞, –љ–µ–њ—А–Є—П—В–љ—Л–µ –Њ—Й—Г—Й–µ–љ–Є—П –≤ —Н–њ–Є–≥–∞—Б—В—А–Є–Є);
– —В–∞—Е–Є—Д–Є–ї–∞–Ї—Б–Є—П (—Б–љ–Є–ґ–µ–љ–Є–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є).
–Ъ–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є–µ –Э1––∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л —П–≤–ї—П—О—В—Б—П –Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ—Л–Љ–Є –±–ї–Њ–Ї–∞—В–Њ—А–∞–Љ–Є –Э1–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –њ–Њ—Н—В–Њ–Љ—Г —Б–≤—П–Ј—Л–≤–∞–љ–Є–µ –Є—Е —Б —А–µ—Ж–µ–њ—В–Њ—А–Њ–Љ –Њ–±—А–∞—В–Є–Љ–Њ. –Ф–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л —В–∞–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –њ—А–Є —Н—В–Њ–Љ –ї–µ–≥—З–µ –Є —З–∞—Й–µ –њ—А–Њ—П–≤–ї—П—О—В—Б—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є—Е –Э1––њ—А–Њ—В–Є–≤–Њ–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ–Ї–∞–Ј—Л–≤–∞—О—В –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –∞ –Ј–љ–∞—З–Є—В –Є—Е –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–љ–Є–Љ–∞—В—М 3–4 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є.
–Т –†–Њ—Б—Б–Є–Є, –≤ –ї–∞–±–Њ—А–∞—В–Њ—А–Є–Є –Ь.–Ф. –Ь–∞—И–Ї–Њ–≤—Б–Ї–Њ–≥–Њ —Б–Њ–Ј–і–∞–љ–∞ –љ–Њ–≤–∞—П –≥—А—Г–њ–њ–∞ – —Е–Є–љ—Г–Ї–ї–Є–і–Є–љ–Њ–≤—Л–µ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ: –Ї–≤–Є—Д–µ–љ–∞–і–Є–љ –Є —Б–µ–Ї–≤–Є—Д–µ–љ–∞–і–Є–љ. –Ъ–≤–Є—Д–µ–љ–∞–і–Є–љ –Њ–±–ї–∞–і–∞–µ—В –љ–Є–Ј–Ї–Њ–є –ї–Є–њ–Њ—Д–Є–ї—М–љ–Њ—Б—В—М—О, –њ–ї–Њ—Е–Њ –њ—А–Њ–љ–Є–Ї–∞–µ—В —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А –Є –њ–Њ—Н—В–Њ–Љ—Г –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –Є–Љ–µ–µ—В —Б–µ–і–∞—В–Є–≤–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞. –Ю–љ –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В –∞–і—А–µ–љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–є –Є —Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В. –Я–Њ–Љ–Є–Љ–Њ –±–ї–Њ–Ї–∞–і—Л –Э1–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –Ї–≤–Є—Д–µ–љ–∞–і–Є–љ —Г–Љ–µ–љ—М—И–∞–µ—В —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –≥–Є—Б—В–∞–Љ–Є–љ–∞ –≤ —В–Ї–∞–љ—П—Е –Ј–∞ —Б—З–µ—В –∞–Ї—В–Є–≤–∞—Ж–Є–Є –і–Є–∞–Љ–Є–љ–Њ–Ї—Б–Є–і–∞–Ј—Л, –Є–љ–∞–Ї—В–Є–≤–Є—А—Г—О—Й–µ–є –≥–Є—Б—В–∞–Љ–Є–љ. –°–µ–Ї–≤–Є—Д–µ–љ–∞–і–Є–љ, –Ї—А–Њ–Љ–µ –±–ї–Њ–Ї–∞–і—Л –Э1–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –±–ї–Њ–Ї–Є—А—Г–µ—В –Є —Б–µ—А–Њ—В–Њ–љ–Є–љ–Њ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л 1 —В–Є–њ–∞, —Б —Н—В–Є–Љ —Б–≤–Њ–є—Б—В–≤–Њ–Љ —Б–≤—П–Ј–∞–љ–Њ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –њ—А–Њ—В–Є–≤–Њ–Ј—Г–і–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –±–Є–Ї–∞—А—Д–µ–љ–∞.
–Р–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –њ–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –±–ї–Њ–Ї–Є—А–Њ–≤–∞—В—М –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–µ –Э1–—А–µ—Ж–µ–њ—В–Њ—А—Л —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л —Б –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –њ–µ—А–≤–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –љ–Њ –Њ–љ–Є –љ–µ –њ—А–Њ–љ–Є–Ї–∞—О—В —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А, –∞ –њ–Њ—В–Њ–Љ—Г –љ–µ –≤—Л–Ј—Л–≤–∞—О—В —Б–µ–і–∞—В–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞. –Р–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П —Б—В–∞–ї–Є —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –≤ –Ї–ї–Є–љ–Є–Ї–µ –≤ 80-–µ –≥–Њ–і—Л (—В–∞–±–ї. 2).
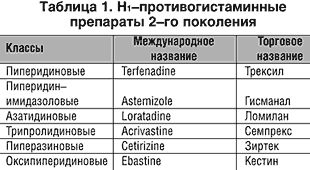
–£ —Н—В–Њ–є –≥—А—Г–њ–њ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —В–∞–Ї–ґ–µ –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л —Б–µ—А—М–µ–Ј–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Є—Е –Ї–∞—А–і–Є–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В—М—О.
–Т —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –і–Њ–Ј–∞—Е —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –Њ–±–ї–∞–і–∞—О—В —Е–Њ—А–Њ—И–Є–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є. –Ю–і–љ–∞–Ї–Њ –њ—А–Є –Ј–∞–Љ–µ–і–ї–µ–љ–Є–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Д–µ—А–Љ–µ–љ—В–∞–Љ–Є –њ–µ—З–µ–љ–Є (CYP3A4 —Б–Є—Б—В–µ–Љ—Л —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450) –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ –љ–µ–Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Е–Њ–і–љ—Л—Е —Д–Њ—А–Љ, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞—А—Г—И–µ–љ–Є—О —Б–µ—А–і–µ—З–љ–Њ–≥–Њ —А–Є—В–Љ–∞ (–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–∞—П «–≤–µ—А–µ—В–µ–љ–Њ–Њ–±—А–∞–Ј–љ–∞—П» —В–∞—Е–Є–Ї–∞—А–і–Є—П, –љ–∞ –≠–Ъ–У – —Г–і–ї–Є–љ–µ–љ–Є–µ –Є–љ—В–µ—А–≤–∞–ї–∞ Q–Ґ). –Ґ–∞–Ї–Њ–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–µ –Љ–Њ–ґ–µ—В –≤–Њ–Ј–љ–Є–Ї–љ—Г—В—М —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Љ–∞–Ї—А–Њ–ї–Є–і–Њ–≤, –њ—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤—Л—Е –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е –Є–Љ–Є–і–∞–Ј–Њ–ї–∞, –і—А—Г–≥–Є—Е –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–≤ –Є –њ–Є—Й–µ–≤—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —В–Њ—А–Љ–Њ–Ј—П—В –Њ–Ї—Б–Є–≥–µ–љ–∞–Ј–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М CYP3A4 —Б–Є—Б—В–µ–Љ—Л —Ж–Є—В–Њ—Е—А–Њ–Љ–∞ –†450. –£–Ї–∞–Ј–∞–љ–љ—Л–є –њ–Њ–±–Њ—З–љ—Л–є —Н—Д—Д–µ–Ї—В —Е–∞—А–∞–Ї—В–µ—А–µ–љ –і–ї—П —В–µ—А—Д–µ–љ–∞–і–Є–љ–∞, –∞—Б—В–µ–Љ–Є–Ј–Њ–ї–∞ –Є –ї–Њ—А–∞—В–∞–і–Є–љ–∞.
–Т—Б–µ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤ —А–∞–≤–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –±–ї–Њ–Ї–Є—А—Г—О—В –≥–Є—Б—В–∞–Љ–Є–љ–Њ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л (–Э1–—А–µ—Ж–µ–њ—В–Њ—А—Л), –љ–Њ –Њ—В–ї–Є—З–∞—О—В—Б—П –њ—А–Њ—Д–Є–ї–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є.
–Э–∞–Є–±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Њ–±–ї–∞–і–∞–ї–Є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П – —В–µ—А—Д–µ–љ–∞–і–Є–љ –Є –∞—Б—В–µ–Љ–Є–Ј–Њ–ї.
–Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –і–ї—П –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П —П–≤–ї—П—О—В—Б—П:
– –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б –Ї–µ—В–Њ–Ї–Њ–љ–∞–Ј–Њ–ї–Њ–Љ, –Є–љ—В—А–∞–Ї–Њ–љ–Њ–Ј–Њ–ї–Њ–Љ –Є–ї–Є –Љ–Є–Ї–Њ–љ–∞–Ј–Њ–ї–Њ–Љ
– –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б –Љ–∞–Ї—А–Њ–ї–Є–і–∞–Љ–Є
– –њ—А–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Б —Е–Є–љ–Є–љ–Њ–Љ
– –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є, —Б–њ–Њ—Б–Њ–±–љ—Л–Љ–Є —Г–і–ї–Є–љ—П—В—М –Є–љ—В–µ—А–≤–∞–ї QT, –≤–Ї–ї—О—З–∞—П –∞–љ—В–Є–∞—А–Є—В–Љ–Є—З–µ—Б–Ї–Є–µ —Б—А–µ–і—Б—В–≤–∞
– –±–Њ–ї—М–љ—Л–µ —Б –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —Б–µ—А–і–µ—З–љ–Њ–≥–Њ —А–Є—В–Љ–∞
– –љ–µ–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є, –љ–µ–є—А–Њ—Н–љ–і–Њ–Ї—А–Є–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –њ–µ—З–µ–љ–Є, –њ–Њ—З–µ–Ї
– –±–Њ–ї—М–љ—Л–µ —Б –≤—А–Њ–ґ–і–µ–љ–љ—Л–Љ —Г–і–ї–Є–љ–µ–љ–Є–µ–Љ –Є–љ—В–µ—А–≤–∞–ї–∞ QT –љ–∞ –≠–Ъ–У
– –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М –Є –њ–µ—А–Є–Њ–і –ї–∞–Ї—В–∞—Ж–Є–Є.
–Т 1997 –≥–Њ–і—Г –Р–і–Љ–Є–љ–Є—Б—В—А–∞—Ж–Є—П –њ–Њ –Ї–Њ–љ—В—А–Њ–ї—О –њ–Є—Й–µ–≤—Л—Е –Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –°–®–Р (FDA) –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–∞ –Ј–∞–њ—А–µ—В–Є—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —В–µ—А—Д–µ–љ–∞–і–Є–љ–∞ – –њ–µ—А–≤–Њ–≥–Њ –љ–µ—Б–µ–і–∞—В–Є–≤–љ–Њ–≥–Њ –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –Я–Њ–Ј–ґ–µ –±—Л–ї –Ј–∞–њ—А–µ—Й–µ–љ –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Є –∞—Б—В–µ–Љ–Є–Ј–Њ–ї. –Ъ–∞–Ї —Г–ґ–µ –≥–Њ–≤–Њ—А–Є–ї–Њ—Б—М –≤—Л—И–µ, —Н—В–Њ –±—Л–ї–Њ —Б–≤—П–Ј–∞–љ–Њ —Б —В–µ–Љ, —З—В–Њ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞, —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ–≥–Њ —Б –і—А—Г–≥–Є–Љ–Є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є, –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —В–µ—А—Д–µ–љ–∞–і–Є–љ–∞ –Є –∞—Б—В–µ–Љ–Є–Ј–Њ–ї–∞ –Њ—В–Љ–µ—З–∞–ї—Б—П –≤—Л—Б–Њ–Ї–Є–є –Ї–Њ—Н—Д–Є—Ж–Є–µ–љ—В —А–Є—Б–Ї–∞ –Ї–∞—А–і–Є–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞. –° 2001 –≥–Њ–і–∞ —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –Ј–∞–њ—А–µ—Й–µ–љ—Л –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Є –≤ –†–Њ—Б—Б–Є–Є.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Ї –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –њ—А–µ–і—К—П–≤–ї—П—О—В —Б—В—А–Њ–≥–Є–µ —В—А–µ–±–Њ–≤–∞–љ–Є—П, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –Њ–љ–Є –і–Њ–ї–ґ–љ—Л –Њ–±–ї–∞–і–∞—В—М:
– –≤—Л—Б–Њ–Ї–Њ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–є –±–ї–Њ–Ї–Є—А—Г—О—Й–µ–є –Э1– –≥–Є—Б—В–∞–Љ–Є–љ–Њ–≤–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О,
– –≤—Л—Б–Њ–Ї–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –њ—А–Є –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е (–Ъ–Р–†, –°–Р–†, –•–†–Ъ –Є –і—А.),
– –≤—Л—Б–Њ–Ї–Є–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є,
– –±—Л—Б—В—А—Л–Љ –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ–Љ –Є –љ–∞—З–∞–ї–Њ–Љ –і–µ–є—Б—В–≤–Є—П,
– –≤—Л—Б–Њ–Ї–Њ–є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М—О –Є –і–ї–Є—В–µ–ї—М–љ—Л–Љ –њ–µ—А–Є–Њ–і–Њ–Љ –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В –і–Њ–±–Є—В—М—Б—П –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ–Њ—Б–ї–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П (–љ–µ –Љ–µ–љ–µ–µ 24 —З–∞—Б–Њ–≤),
– –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –≤–Љ–µ—Б—В–µ —Б –і—А—Г–≥–Є–Љ–Є –≥—А—Г–њ–њ–∞–Љ–Є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–≤ (–∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є, –њ—А–Њ—В–Є–≤–Њ–≥—А–Є–±–Ї–Њ–≤—Л–µ, —Б–µ—А–і–µ—З–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –Є –і—А.), –∞ —В–∞–Ї–ґ–µ –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є:
– –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Є–Ј–Љ–µ–љ—П—В—М –і–Њ–Ј—Г –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є –љ–∞—А—Г—И–µ–љ–Є—П—Е —Д—Г–љ–Ї—Ж–Є–Є –Ц–Ъ–Ґ, –≥–µ–њ–∞—В–Њ––±–Є–ї–ї–Є–∞—А–љ–Њ–є, –Љ–Њ—З–µ–≤—Л–і–µ–ї–Є—В–µ–ї—М–љ–Њ–є, —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ –Є –і—А., –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –Є —Б—В–∞—А—З–µ—Б–Ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ,
– —В–∞—Е–Є—Д–Є–ї–∞–Ї—Б–Є–Є,
– –Ї—Г–Љ—Г–ї—П—Ж–Є–Є –Є –њ—А.
–Э–∞–Є–±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є —Б—А–µ–і–Є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Њ–±–ї–∞–і–∞–µ—В —Н–±–∞—Б—В–Є–љ. –Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞–Љ–Є –≠–±–∞—Б—В–Є–љ–∞ —П–≤–ї—П—О—В—Б—П: –±—Л—Б—В—А—Л–є, –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ—Л–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В, –≤—Л—Б–Њ–Ї–∞—П –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –Є –і–ї–Є—В–µ–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є–є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є –Є —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –≤ —В–µ—З–µ–љ–Є–µ 24 —З–∞—Б–Њ–≤, –Њ—В—Б—Г—В—Б—В–≤–Є–µ —В–∞—Е–Є—Д–Є–ї–∞–Ї—Б–Є–Є, –≤—Л—Б–Њ–Ї–Є–є –њ—А–Њ—Д–Є–ї—М –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є, –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б–µ–і–∞—В–Є–≤–љ–Њ–≥–Њ –Є –Ї–∞—А–і–Є–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –≥–Є–±–Ї–Њ–≥–Њ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П. –≠–±–∞—Б—В–Є–љ –љ–µ —Г—Б–Є–ї–Є–≤–∞–µ—В –і–µ–є—Б—В–≤–Є–µ –∞–ї–Ї–Њ–≥–Њ–ї—П –Є –і–Њ—Б—В—Г–њ–µ–љ –њ–Њ —Ж–µ–љ–µ.
–Ґ–∞–Ї –ґ–µ —Е–Њ—А–Њ—И–Њ –Ј–∞—А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–ї —Б–µ–±—П –њ—А–µ–њ–∞—А–∞—В –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–є –§–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ–Љ–њ–∞–љ–Є–Є Lek (–°–ї–Њ–≤–µ–љ–Є—П) – –ї–Њ—А–∞—В–∞–і–Є–љ (–Ы–Њ–Љ–Є–ї–∞–љ).
–Ы–Њ—А–∞—В–∞–і–Є–љ (–Ы–Њ–Љ–Є–ї–∞–љ) –±—Л—Б—В—А–Њ –≤—Б–∞—Б—Л–≤–∞–µ—В—Б—П –Є–Ј –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –њ–Њ—Б–ї–µ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞. –•–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –≤—Л—Б–Њ–Ї–Њ–є —Б—В–µ–њ–µ–љ—М—О —Б–≤—П–Ј—Л–≤–∞–љ–Є—П —Б –±–µ–ї–Ї–∞–Љ–Є –њ–ї–∞–Ј–Љ—Л –Є —Е–Њ—А–Њ—И–Є–Љ –Њ–±—К–µ–Љ–Њ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П. –≠—Д—Д–µ–Ї—В –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —З–µ—А–µ–Ј –њ–Њ–ї—З–∞—Б–∞ –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –Є —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 24 —З–∞—Б–Њ–≤. –Ь–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ –њ–µ—З–µ–љ–Є. –•–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ «–њ–µ—А–≤–Њ–≥–Њ –њ—А–Њ—Е–Њ–ґ–і–µ–љ–Є—П —З–µ—А–µ–Ј –њ–µ—З–µ–љ—М». –Я–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–ї—П–µ—В –і–ї—П –ї–Њ—А–∞—В–∞–і–Є–љ–∞ 7–11 —З–∞—Б–Њ–≤, –і–ї—П –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є—В–∞ – 17–24 —З–∞—Б–∞. –Т—Л–≤–Њ–і–Є—В—Б—П –≤ –≤–Є–і–µ –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –њ–Њ—З–Ї–∞–Љ–Є (–Њ–Ї–Њ–ї–Њ 40%) –Є –Ї–Є—И–µ—З–љ–Є–Ї–Њ–Љ (–Њ–Ї–Њ–ї–Њ 41%). –§–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–∞—А–∞–Љ–µ—В—А—Л –ї–Њ—А–∞—В–∞–і–Є–љ–∞ (–Ы–Њ–Љ–Є–ї–∞–љ–∞) —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ—П—О—В—Б—П —Г –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О.
–Т 90–—Е –≥–Њ–і–∞—Е —Б—В–∞–ї–Є —В—Й–∞—В–µ–ї—М–љ–Њ –Њ—Ж–µ–љ–Є–≤–∞—В—М –Ї–Њ—Н—Д–Є—Ж–Є–µ–љ—В —А–Є—Б–Ї/–њ–Њ–ї—М–Ј–∞ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –±–Њ–ї—М–љ—Л–Љ —Б –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є [5,6,7,8].
–£—З–Є—В—Л–≤–∞—П, —З—В–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Љ–µ—В–∞–±–Њ–ї–Є—В—Л –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —В–µ—А—Д–µ–љ–∞–і–Є–љ–∞ –Є –∞—Б—В–µ–Љ–Є–Ј–Њ–ї–∞, –Њ–±–ї–∞–і–∞—О—В –і–∞–ґ–µ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –±–ї–Њ–Ї–Є—А–Њ–≤–∞—В—М –≥–Є—Б—В–∞–Љ–Є–љ–Њ–≤—Л–µ –Э1–—А–µ—Ж–µ–њ—В–Њ—А—Л, —З–µ–Љ —Б–∞–Љ–Є –њ—А–µ–њ–∞—А–∞—В—Л, –њ–Њ—П–≤–Є–ї–∞—Б—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —А–∞–Ј—А–∞–±–Њ—В–Ї–Є –љ–Њ–≤–Њ–≥–Њ – —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤.
–Ю—Б–љ–Њ–≤–љ–Њ–є –Ј–∞–і–∞—З–µ–є –њ—А–Є —Б–Њ–Ј–і–∞–љ–Є–Є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П —П–≤–ї—П–ї–Њ—Б—М –њ–Њ–ї—Г—З–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ, –љ–Њ –ї–Є—И–µ–љ–љ—Л—Е –Є–Ј–≤–µ—Б—В–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є—Е –≥—А—Г–њ–њ –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤ [8].
–†–∞–Ј—А–∞–±–Њ—В–Ї–∞ –Э1––∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–≤ 3––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –љ–∞–њ—А–∞–≤–ї–µ–љ–∞ –љ–∞ –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ —Б–ї–µ–і—Г—О—Й–Є—Е –ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ —Г –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Њ–є –≥—А—Г–њ–њ—Л: –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б–µ–і–∞—В–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞, –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Ї–∞—А–і–Є–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є, –±—Л—Б—В—А–Њ–µ –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ –њ–µ—А–Њ—А–∞–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –≤ –Њ—А–≥–∞–љ—Л––Љ–Є—И–µ–љ–Є, –≤—Л—Б–Њ–Ї–∞—П –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –Є –і–ї–Є—В–µ–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є–є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Є–µ–Љ–∞ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є –Є —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –≤ —В–µ—З–µ–љ–Є–µ 24 —З–∞—Б–Њ–≤, –Њ—В—Б—Г—В—Б—В–≤–Є–µ —В–∞—Е–Є—Д–Є–ї–∞–Ї—Б–Є–Є, –Њ—В—Б—Г—В—Б—В–≤–Є–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –≤ –Є–Ј–Љ–µ–љ–µ–љ–Є–Є –і–Њ–Ј—Л —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–∞—А—Г—И–µ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–µ–є –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ–Ї, –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б –і—А—Г–≥–Є–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є, –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М.
–Т 1996 –≥–Њ–і—Г –≤ –Р–і–Љ–Є–љ–Є—Б—В—А–∞—Ж–Є–Є –њ–Њ –Ї–Њ–љ—В—А–Њ–ї—О –њ–Є—Й–µ–≤—Л—Е –Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤ –°–®–Р –≤–њ–µ—А–≤—Л–µ –±—Л–ї –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ –љ–Њ–≤—Л–є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П – —Д–µ–Ї—Б–Њ—Д–µ–љ–∞–і–Є–љ. –Я–Њ–Ј–ґ–µ —Б—В–∞–ї–Є —А–∞–Ј—А–∞–±–∞—В—Л–≤–∞—В—М—Б—П –і—А—Г–≥–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л: –і–µ—Б–Ї–∞—А–±–Њ—Н—В–Њ–Ї—Б–Є–ї–Њ—А–∞—В–∞–і–Є–љ –Є –љ–Њ—А–∞—Б—В–µ–Љ–Є–Ј–Њ–ї [8].
–§–µ–Ї—Б–Њ—Д–µ–љ–∞–і–Є–љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —А–∞—Ж–µ–Љ–Є—З–µ—Б–Ї—Г—О —Б–Љ–µ—Б—М –і–≤—Г—Е —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ—Л—Е –Є–Ј–Њ–Љ–µ—А–Њ–≤ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є—В–∞ —В–µ—А—Д–µ–љ–∞–і–Є–љ–∞, –Э1––≥–Є—Б—В–∞–Љ–Є–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–∞ 2––≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П. –Ш—Е –њ—А–Њ—В–Є–≤–Њ–≥–Є—Б—В–∞–Љ–Є–љ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞—З–Є–љ–∞–µ—В –њ—А–Њ—П–≤–ї—П—В—М—Б—П —З–µ—А–µ–Ј 30 –Љ–Є–љ—Г—В –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ per os, –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤ –Ї—А–Њ–≤–Є –і–Њ—Б—В–Є–≥–∞–µ—В –Љ–∞–Ї—Б–Є–Љ—Г–Љ–∞ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е —З–∞—Б–Њ–≤, –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П – –і–Њ 24 —З–∞—Б–Њ–≤. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б–њ—Л—В–∞–љ–Є—П —Д–µ–Ї—Б–Њ—Д–µ–љ–∞–і–Є–љ–∞ –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –і–∞–ґ–µ –і–≤—Г—Е– –Є —В—А–µ—Е–Ї—А–∞—В–љ–Њ–µ –њ—А–µ–≤—Л—И–µ–љ–Є–µ —Б—А–µ–і–љ–µ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –љ–µ –≤—Л–Ј—Л–≤–∞–ї–Њ —Б–µ–і–∞—В–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ [5,6,7,8].
–Т –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –њ—А–Є–љ—Ж–Є–њ–∞–Љ–Є –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л, –±—Л–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤—Л—Б–Њ–Ї–∞—П –њ—А–Њ—В–Є–≤–Њ–≥–Є—Б—В–∞–Љ–Є–љ–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ —Д–µ–Ї—Б–Њ—Д–µ–љ–∞–і–Є–љ —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–љ—Л–Љ–Є –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–µ–є –Ї—А–∞–њ–Є–≤–љ–Є—Ж–µ.
–Ъ –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –Њ—В–љ–Њ—Б—П—В —В–∞–Ї–ґ–µ –Э1––∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л, –Њ–±–ї–∞–і–∞—О—Й–Є–µ –Љ–µ–Љ–±—А–∞–љ–Њ—Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Ъ —Н—В–Є–Љ –Э1––њ—А–Њ—В–Є–≤–Њ–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –Њ—В–љ–Њ—Б—П—В –Ї–µ—В–Њ—В–Є—Д–µ–љ, –Њ–Ї—Б–∞—В–Њ–Љ–Є–і, –∞–Ј–µ–ї–∞—Б—В–Є–љ, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –њ—А–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Д–Њ—А–Љ–∞—Е –∞–ї–ї–µ—А–≥–Њ–і–µ—А–Љ–∞—В–Њ–Ј–Њ–≤, –љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –Ї—А–∞–њ–Є–≤–љ–Є—Ж–µ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є –њ—Б–µ–≤–і–Њ–∞–ї–ї–µ—А–≥–Є–Є.
–Я—А–Є –≤—Л–±–Њ—А–µ –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ–∞—Ж–Є–µ–љ—В–∞ –Ї –њ—А–Њ—В–Є–≤–Њ–≥–Є—Б—В–∞–Љ–Є–љ–љ–Њ–Љ—Г –і–µ–є—Б—В–≤–Є—О –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–∞.
–Ф—А—Г–≥–Є–Љ –≤–∞–ґ–љ–µ–є—И–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ –≤—Л–±–Њ—А–∞ —П–≤–ї—П–µ—В—Б—П –Њ—Ж–µ–љ–Ї–∞ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, —В.–µ. –њ—А–Њ—Д–Є–ї—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є.
1. –Ш–ї—М–Є–љ–∞ –Э.–Ш. –Р–ї–ї–µ—А–≥–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—П –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ–≥–Є–Њ–љ–∞—Е –†–Њ—Б—Б–Є–Є –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Ї–ї–Є–љ–Є–Ї–Њ–—Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є.// –∞–≤—В–Њ—А–µ—Д–µ—А–∞—В –і–Њ–Ї—В. –і–Є—Б—Б. –Ь. 1996, 24 —Б.
2. –Ш.–°. –У—Г—Й–Є–љ// –Р–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ –Є –µ–≥–Њ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –Ї–Њ–љ—В—А–Њ–ї—М//1998, –Ь.,–§–Р–Ь–Р–†–£–° –Я–†–Ш–Э–Ґ, 251 —Б.
3. –Ы—Г—Б—Б –Ы.–Т. –Р–ї–ї–µ—А–≥–Є—П –Є –њ—Б–µ–≤–і–Њ–∞–ї–ї–µ—А–≥–Є—П –≤ –Ї–ї–Є–љ–Є–Ї–µ. –Ф–Њ–Ї—В. –і–Є—Б—Б. –Ь., 1993. 220 —Б.
4. –•–∞–Є—В–Њ–≤ –†.–Ь., –Я–Є–љ–µ–≥–Є–љ –Т.–С., –Ш—Б—В–∞–Љ–Њ–≤ –•.–Ш. –≠–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—П. – –Ь. –Т–Э–Ш–†–Ю. 1995, —Б. 178 – 207
5. E. Paul, J. Berth–Jones, J–P. Ortonne, M. Stern// –§–µ–Ї—Б–∞—Д–µ–љ–∞–і–Є–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і –≤ –ї–µ—З–µ–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л: –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ, –њ–∞—А–∞–ї–ї–µ–ї—М–љ–Њ–µ –Є—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Њ–Ј –њ—А–µ–њ–∞—А–∞—В–∞// J. Dermatol. Treat., 1998, 143–149/
6. A. Finn, A. Kaplan, R. Fretwell, R. Qu// –Ф–≤–Њ–є–љ–Њ–µ —Б–ї–µ–њ–Њ–µ, –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –§–µ–Ї—Б–∞—Д–µ–љ–∞–і–Є–љ–∞ HCI –≤ –ї–µ—З–µ–љ–Є–Є –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л// J. Allergy Clin. Immunol.,1999, 103, 1071–1078/
7. H. Nelson, R. Reynolds, J. Mason// –§–µ–Ї—Б–∞—Д–µ–љ–∞–і–Є–љ –Э–°I – –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–µ –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ —Б—А–µ–і—Б—В–≤–Њ –ї–µ—З–µ–љ–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –Ї—А–∞–њ–Є–≤–љ–Є—Ж—Л// Ann. Allergy Asthma Jmmunol., 2000, 84, 517 – 522.
8. D. Handley, A. Magnetti, A. Higgins// –Ґ–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —В—А–µ—В—М–µ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П// Exp. Clin. Invest. Drags// 1998, 7(7), 1045 – 1054.












