–Т–≤–µ–і–µ–љ–Є–µ
–Ф–Є—Б–Љ–µ–љ–Њ—А–µ—П вАФ —Н—В–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, —З–∞—Й–µ –≤—Б–µ–≥–Њ –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є—Е –Ј–∞ –і–µ–љ—М –і–Њ –Є–ї–Є –≤ –њ–µ—А–≤—Л–µ –і–љ–Є –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–Є. –Т –Њ—Б–љ–Њ–≤–љ–Њ–Љ –і–Є—Б–Љ–µ–љ–Њ—А–µ—П –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —В—П–љ—Г—Й–Є–Љ–Є –Є–ї–Є —Б—Е–≤–∞—В–Ї–Њ–Њ–±—А–∞–Ј–љ—Л–Љ–Є –±–Њ–ї—П–Љ–Є –≤–љ–Є–Ј—Г –ґ–Є–≤–Њ—В–∞ –Є –њ–Њ—П—Б–љ–Є—Ж–µ. –Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–∞—П –±–Њ–ї—М –њ–Њ—П–≤–ї—П–µ—В—Б—П —З–µ—А–µ–Ј 1вАУ2 –≥–Њ–і–∞ –њ–Њ—Б–ї–µ –Љ–µ–љ–∞—А—Е–µ, –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –≤–∞—А—М–Є—А—Г–µ—В –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П, –љ–∞—Б—В—А–Њ–µ–љ–Є—П, —Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е –љ–∞–≥—А—Г–Ј–Њ–Ї [1].
–Ь–µ–љ—Б—В—А—Г–∞–ї—М–љ—Г—О —В–∞–Ј–Њ–≤—Г—О –±–Њ–ї—М –Љ–Њ–ґ–љ–Њ —В—А–∞–Ї—В–Њ–≤–∞—В—М –Ї–∞–Ї –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ. –Я–µ—А–≤–Є—З–љ–∞—П, –Є–ї–Є –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П, –і–Є—Б–Љ–µ–љ–Њ—А–µ—П –Њ—Б—В–∞–µ—В—Б—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –Њ–±—А–∞—Й–µ–љ–Є—П –Ї –≤—А–∞—З—Г –∞–Ї—Г—И–µ—А—Г-–≥–Є–љ–µ–Ї–Њ–ї–Њ–≥—Г –ґ–µ–љ—Й–Є–љ —А–∞–љ–љ–µ–≥–Њ –Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ [2, 3]. –Т—В–Њ—А–Є—З–љ–∞—П –і–Є—Б–Љ–µ–љ–Њ—А–µ—П –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ —А—П–і–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Ь–µ—Е–∞–љ–Є–Ј–Љ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ—А–Є –≤—В–Њ—А–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ, –Ї–Њ—В–Њ—А–Њ–µ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–µ—В—Б—П —Н—Б—В—А–Њ–≥–µ–љ–∞–Љ–Є. –Я—А–Њ–ї–Њ–љ–≥–∞—Ж–Є—П –і–∞–љ–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–≤—П–Ј–∞–љ–∞ —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —В–∞–Ј–Њ–≤–Њ–є –±–Њ–ї–Є –љ–∞ —Д–Њ–љ–µ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є —Б–µ–љ—Б–Є—В–Є–Ј–∞—Ж–Є–Є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є–ї–Є –њ—А–Њ–≥—А–µ—Б—Б–Є–µ–є –∞–і–µ–љ–Њ–Љ–Є–Њ–Ј–∞, —Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ —Н—Б—В—А–Њ–≥–µ–љ-–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ [2]. –Я–Њ—Н—В–Њ–Љ—Г —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –∞—Б–њ–µ–Ї—В—Л –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞—О—В –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї—Г —А–∞–Ј–≤–Є—В–Є—П —Б–Є–љ–і—А–Њ–Љ–∞ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —В–∞–Ј–Њ–≤–Њ–є –±–Њ–ї–Є –Є —Н–љ–і–Њ–Љ–µ—В—А–Є–Њ–Ј–∞.
–Ф–Є—Б–Љ–µ–љ–Њ—А–µ—П –Ї–∞–Ї –≥–ї–Њ–±–∞–ї—М–љ–∞—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–∞—П –Є —Б–Њ—Ж–Є–∞–ї—М–љ–∞—П –њ—А–Њ–±–ї–µ–Љ–∞
–Ь–µ–љ—Б—В—А—Г–∞–ї—М–љ–∞—П –±–Њ–ї—М –≤—Б—В—А–µ—З–∞–µ—В—Б—П —Г 50вАУ90% –љ–µ—Б–Њ–≤–µ—А—И–µ–љ–љ–Њ–ї–µ—В–љ–Є—Е –њ–Њ–і—А–Њ—Б—В–Ї–Њ–≤ –Є –ґ–µ–љ—Й–Є–љ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –Є —П–≤–ї—П–µ—В—Б—П –≤–µ–і—Г—Й–µ–є –њ—А–Є—З–Є–љ–Њ–є –њ—А–Њ–њ—Г—Б–Ї–∞ —Г—З–µ–±–љ—Л—Е –Ј–∞–љ—П—В–Є–є –Є –љ–µ–≤—Л—Е–Њ–і–∞ –љ–∞ —А–∞–±–Њ—В—Г [4вАУ6]. –Я–Њ–Љ–Є–Љ–Њ –±–Њ–ї–Є, –њ—А–Є –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ –Є–Љ–µ–µ—В –Љ–µ—Б—В–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б —Н–љ–і–Њ–Ї—А–Є–љ–љ—Л—Е, —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ-–њ—Б–Є—Е–Є—З–µ—Б–Ї–Є—Е –Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –≤–ї–Є—П—О—Й–Є—Е –љ–∞ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Ї–Є [4, 5, 7].
–£ –љ–µ—Б–Њ–≤–µ—А—И–µ–љ–љ–Њ–ї–µ—В–љ–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –±–Њ–ї–µ–≤–∞—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ –Љ–Њ–ґ–µ—В —Б–Њ—З–µ—В–∞—В—М—Б—П —Б —А–≤–Њ—В–Њ–є, –і–Є–∞—А–µ–µ–є, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ–Љ, –Њ–±–Љ–Њ—А–Њ–Ї–∞–Љ–Є, –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї—М—О [7вАУ9]. –Э–Њ –Є –њ—А–Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –±–Њ–ї–Є, –Ї–Њ–≥–і–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –љ–µ –њ—А–Њ–њ—Г—Б–Ї–∞—В—М —Г—З–µ–±—Г –Є–ї–Є —А–∞–±–Њ—В—Г, –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ –≤–љ–Є–Љ–∞–љ–Є—П –Є –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В–µ–ї—М–љ–Њ—Б—В–Є —В—А—Г–і–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї. –Я–Њ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Њ—Ж–µ–љ–Ї–∞–Љ, –≤ –°–®–Р –µ–ґ–µ–≥–Њ–і–љ–Њ —В–µ—А—П–µ—В—Б—П 2 –Љ–ї—А–і –і–Њ–ї–ї–∞—А–Њ–≤ (600 –Љ–ї–љ —З–∞—Б–Њ–≤ —А–∞–±–Њ—З–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є) –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Њ–њ—Г—Б–Ї–∞ —А–∞–±–Њ—В—Л –Є–ї–Є —Б–љ–Є–ґ–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є —А–∞–±–Њ—В–љ–Є—Ж –Є–Ј-–Ј–∞ —В–∞–Ј–Њ–≤–Њ–є –±–Њ–ї–Є –≤–Њ –≤—А–µ–Љ—П –Љ–µ—Б—П—З–љ—Л—Е –Є –і—А—Г–≥–Њ–є —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –љ–Є–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є [6]. –Ю—Ж–µ–љ–Ї–∞ —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е –≤ –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є –Ј–∞—В—А—Г–і–љ–µ–љ–∞, —В–∞–Ї –Ї–∞–Ї –ї–Є—И—М 15% –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ–є –Њ–±—А–∞—Й–∞—О—В—Б—П –Ј–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й—М—О, —Е–Њ—В—П –њ—А–Є —Б–±–Њ—А–µ –∞–љ–∞–Љ–љ–µ–Ј–∞ –Њ–Ї–Њ–ї–Њ 90% –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В, —З—В–Њ –Є—Б–њ—Л—В—Л–≤–∞—О—В –±–Њ–ї–Є –≤–Њ –≤—А–µ–Љ—П –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–Є [10]. –І—А–µ–Ј–≤—Л—З–∞–є–љ–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–∞ –і–Є—Б–Љ–µ–љ–Њ—А–µ—П –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є —Б—В—Г–і–µ–љ—В–Њ–Ї [11, 12]. –Ґ–∞–Ї, 47вАУ70% —Б—В—Г–і–µ–љ—В–Њ–Ї —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–Њ–≤ —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –њ—А–Є–Љ–µ–љ—П—О—В –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Є –і–ї—П –Њ–±–ї–µ–≥—З–µ–љ–Є—П –±–Њ–ї–Є, –і–Њ 30% вАФ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П –Є —В–Њ–ї—М–Ї–Њ 15вАУ20% вАФ –Њ–±—А–∞—Й–∞—О—В—Б—П –Ї –≤—А–∞—З—Г [13]. –Ф–Є—Б–Љ–µ–љ–Њ—А–µ—П –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –Ј–љ–∞—З–Є–Љ–Њ —З–∞—Й–µ —Г —Б—В—Г–і–µ–љ—В–Њ–Ї –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –Љ–Є–ї–ї–µ–љ–Є—Г–Љ–∞ (¬Ђ–Љ–Є–ї–ї–µ–љ–Є–∞–ї–Њ–≤¬ї), —З–µ–Љ –≤ –њ–Њ–Ї–Њ–ї–µ–љ–Є–Є ¬Ђ–Ј—Г–Љ–µ—А–Њ–≤¬ї (84,4% –њ—А–Њ—В–Є–≤ 65,45%, p<0,05) [14]. –Х–µ —А–µ–∞–ї—М–љ–∞—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Љ–Њ–ґ–µ—В –љ–µ–і–Њ–Њ—Ж–µ–љ–Є–≤–∞—В—М—Б—П, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Љ–љ–Њ–≥–Є–µ –ґ–µ–љ—Й–Є–љ—Л —Б—З–Є—В–∞—О—В –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ–µ —В–µ—З–µ–љ–Є–µ –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞ –≤–∞—А–Є–∞–љ—В–Њ–Љ –љ–Њ—А–Љ—Л –Є –Є–Ј–±–µ–≥–∞—О—В –≤–Є–Ј–Є—В–∞ –Ї –≤—А–∞—З—Г –і–∞–ґ–µ –њ—А–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В–µ [8, 15]. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ 58,2% —Г—З–∞—Й–Є—Е—Б—П –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 16 –ї–µ—В –і–Њ 21 –≥–Њ–і–∞ –њ—А–Њ–њ—Г—Б–Ї–∞—О—В –њ–Њ –і–∞–љ–љ–Њ–є –њ—А–Є—З–Є–љ–µ –Њ—В –Њ–і–љ–Њ–≥–Њ –Є –±–Њ–ї–µ–µ —Г—З–µ–±–љ—Л—Е –і–љ–µ–є –≤ –≥–Њ–і—Г (n=783, p=0,005) [16]. –†–∞—Б—Е–Њ–і—Л –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П –љ–∞ –ї–µ—З–µ–љ–Є–µ —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –≤ 2,2 —А–∞–Ј–∞ –њ—А–µ–≤—Л—И–∞—О—В –Ј–∞—В—А–∞—В—Л –љ–∞ –ї–µ—З–µ–љ–Є–µ –ґ–µ–љ—Й–Є–љ –±–µ–Ј –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є [17]. –Я—А–Є –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ —Б–љ–Є–ґ–∞–µ—В—Б—П –њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ—Б—В—М —А–∞–±–Њ—В—Л, —Г—Е—Г–і—И–∞–µ—В—Б—П —Б–Њ—Ж–Є–∞–ї—М–љ–∞—П –ґ–Є–Ј–љ—М, –љ–∞—А—Г—И–∞—О—В—Б—П –Њ—В–љ–Њ—И–µ–љ–Є—П —Б –Ї–Њ–ї–ї–µ–≥–∞–Љ–Є, —Б —Б–µ–Љ—М–µ–є [18].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –і–Є—Б–Љ–µ–љ–Њ—А–µ—П —П–≤–ї—П–µ—В—Б—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –Є —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–µ–є –љ–µ–≥–∞—В–Є–≤–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –ґ–µ–љ—Й–Є–љ—Л –≤ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ –њ–Њ –≤—Б–µ–Љ—Г –Љ–Є—А—Г.
–Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –і–ї—П –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є –њ–∞—Ж–Є–µ–љ—В–Ї–Є –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Э–Я–Т–Я), —В–∞–Ї–Є–µ –Ї–∞–Ї –Є–±—Г–њ—А–Њ—Д–µ–љ [19] –Є–ї–Є —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Є [5]. –Ф–µ–є—Б—В–≤–Є–µ –Э–Я–Т–Я —А–µ–∞–ї–Є–Ј—Г–µ—В—Б—П –њ—Г—В–µ–Љ —Б–љ–Є–ґ–µ–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ вАФ –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П [2].
–Ю—В–Љ–µ—З–µ–љ –Є–љ—В–µ—А–µ—Б –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є –Ї —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П–Љ –Э–Я–Т–Я –Є–ї–Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ –Є –Љ–Є–Њ-—В—А–Њ–њ–љ—Л—Е —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Њ–≤ –і–ї—П –њ–Њ–≤—Л—И–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞–љ–∞–ї—М–≥–µ–Ј–Є–Є [1, 20]. –Ю–і–љ–Є–Љ –Є–Ј —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –і–Њ—Б—В—Г–њ–љ—Л—Е –≤ –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є, —П–≤–ї—П–µ—В—Б—П —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –Є–±—Г–њ—А–Њ—Д–µ–љ–∞, –њ–Є—В–Њ—Д–µ–љ–Њ–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і–∞ (–Љ–Є–Њ—В—А–Њ–њ–љ–Њ–µ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–µ —Б—А–µ–і—Б—В–≤–Њ) –Є —Д–µ–љ–њ–Є–≤–µ—А–Є–љ–Є—П –±—А–Њ–Љ–Є–і–∞ (M-—Е–Њ–ї–Є–љ–Њ–±–ї–Њ–Ї–Є—А—Г—О—Й–µ–µ —Б—А–µ–і—Б—В–≤–Њ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П).
–Ф–Є—Б–Љ–µ–љ–Њ—А–µ—П вАФ –љ–µ —В–Њ–ї—М–Ї–Њ –±–Њ–ї—М
–Ґ—П–ґ–µ–ї–∞—П —Б—В–µ–њ–µ–љ—М –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є —Б–≤—П–Ј–∞–љ–∞ —Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –±–Њ–ї–µ–≤–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Њ–є, —А–µ–Ј–Ї–Є–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –љ–∞–ї–Є—З–Є–µ–Љ —А—П–і–∞ –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ [8, 13]. –Т—Б–µ —Н—В–Њ —В—А–µ–±—Г–µ—В –љ–µ–Њ—В–ї–Њ–ґ–љ–Њ–≥–Њ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–љ–Є–ґ–∞–µ—В –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–Ї [21].
–Ш–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –±–Њ–ї–Є –њ—А–Є –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ –Њ–±—Л—З–љ–Њ –і–Њ—Б—В–Є–≥–∞–µ—В –њ–Є–Ї–∞ —З–µ—А–µ–Ј 24вАУ36 —З –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–Є, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —А–µ–і–Ї–Њ –њ—А–µ–≤—Л—И–∞–µ—В –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –і–љ–µ–є [6]. –Я—А–Є—Б—В—Г–њ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ—Л–µ –±–Њ–ї–Є –Љ–Њ–≥—Г—В –і–ї–Є—В—М—Б—П –њ–µ—А–Є–Њ–і–∞–Љ–Є –њ–Њ 2вАУ3 –Љ–Є–љ, –Њ—В–і–∞–≤–∞—В—М –Є–Ј –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є –ґ–Є–≤–Њ—В–∞ –≤ –њ–Њ—П—Б–љ–Є—Ж—Г, —В–Є–њ–Є—З–љ—Л –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–Є–µ –±–Њ–ї–Є [1]. –Ф–Њ –љ–∞—З–∞–ї–∞ –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–Є –љ–µ–Ї–Њ—В–Њ—А—Л–µ –њ–∞—Ж–Є–µ–љ—В–Ї–Є —З—Г–≤—Б—В–≤—Г—О—В –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В –≤–љ–Є–Ј—Г –ґ–Є–≤–Њ—В–∞. –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Г –љ–Є—Е –љ–∞–±–ї—О–і–∞–µ—В—Б—П –≥–Є–њ–µ—А–∞–ї—М–≥–µ–Ј–Є—П –Є –∞–ї–ї–Њ–і–Є–љ–Є—П –≤ –і—А—Г–≥–Є—Е —З–∞—Б—В—П—Е —В–µ–ї–∞, –≤–Ї–ї—О—З–∞—П –њ—А–µ–і–њ–ї–µ—З—М—П, –Ј–∞–њ—П—Б—В—М—П, –љ–Є–ґ–љ–Є–µ –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є, –≤–µ—А—Е–љ—О—О —З–∞—Б—В—М —Б–њ–Є–љ—Л, —А–Њ—В–Њ–≤—Г—О –њ–Њ–ї–Њ—Б—В—М, –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞ [22вАУ25]. –Я–Њ–Љ–Є–Љ–Њ –±–Њ–ї–Є, –њ–∞—Ж–Є–µ–љ—В–Ї–Є —Б—В–∞–ї–Ї–Є–≤–∞—О—В—Б—П —Б —А–µ–Ј–Ї–Є–Љ–Є –њ–µ—А–µ–Љ–µ–љ–∞–Љ–Є –љ–∞—Б—В—А–Њ–µ–љ–Є—П, —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О, –њ–ї–∞–Ї—Б–Є–≤–Њ—Б—В—М—О. –Ъ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Б –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ–є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є —Б—Д–µ—А—Л –Є –њ–Њ–≤–µ–і–µ–љ–Є—П —В–∞–Ї–ґ–µ –Љ–Њ–≥—Г—В –Њ—В–љ–Њ—Б–Є—В—М—Б—П –∞–љ–Њ—А–µ–Ї—Б–Є—П, –і–µ–њ—А–µ—Б—Б–Є—П, —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М, –±–µ—Б—Б–Њ–љ–љ–Є—Ж–∞, –±—Г–ї–Є–Љ–Є—П, –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –Ј–∞–њ–∞—Е–Њ–≤, –Є–Ј–≤—А–∞—Й–µ–љ–Є–µ –≤–Ї—Г—Б–∞ [5]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –і–µ–њ—А–µ—Б—Б–Є—П –Є –±–Њ–ї—М –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—В –і—А—Г–≥ –і—А—Г–≥–∞: —Б—В—А–µ—Б—Б, –љ–µ–≥–∞—В–Є–≤–љ—Л–µ —Н–Љ–Њ—Ж–Є–Є –њ–Њ–≤—Л—И–∞—О—В –≤–Њ—Б–њ—А–Є–Є–Љ—З–Є–≤–Њ—Б—В—М —З–µ–ї–Њ–≤–µ–Ї–∞ –Ї –±–Њ–ї–Є [26].
–Т—Б–ї–µ–і—Б—В–≤–Є–µ —Б–њ–∞–Ј–Љ–∞ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –Њ—А–≥–∞–љ–Њ–≤ –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ (–Ц–Ъ–Ґ) –≤–Њ–Ј–Љ–Њ–ґ–љ—Л —В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞, –≤–Ј–і—Г—В–Є–µ –ґ–Є–≤–Њ—В–∞, –і–Є–∞—А–µ—П. –Ю—В–і–µ–ї—М–љ—Л–є –±–ї–Њ–Ї –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П—О—В –∞–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–µ —А–µ–∞–Ї—Ж–Є–Є, –њ—А–Њ—П–≤–ї—П—О—Й–Є–µ—Б—П –≤ –≤–Є–і–µ –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є, —Б–ї–∞–±–Њ—Б—В–Є, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є—П, –±–ї–µ–і–љ–Њ—Б—В–Є –Ї–Њ–ґ–Є, –Є–љ–Њ–≥–і–∞ —Б –Ј–Њ–љ–∞–Љ–Є –≥–Є–њ–µ—А–µ–Љ–Є–Є –љ–∞ –≥—А—Г–і–Є –Є —И–µ–µ [5, 6, 27].
–Ъ–∞–Ї —Г–ґ–µ –±—Л–ї–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –≤—Л—И–µ, –њ—А–Є –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–µ –і–Є–∞–≥–љ–Њ–Ј–∞ –≤—Л–і–µ–ї—П—О—В –њ–µ—А–≤–Є—З–љ—Г—О –Є –≤—В–Њ—А–Є—З–љ—Г—О –і–Є—Б–Љ–µ–љ–Њ—А–µ—О. –†–∞–Ј–љ–Њ-–Њ–±—А–∞–Ј–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –њ–µ—А–≤–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є, –њ–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ—Г –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—О, –Є–Љ–µ—О—В —Б–≤—П–Ј—М —Б –∞–љ–Њ–Љ–∞–ї—М–љ–Њ–є —Н–Ї—Б–њ—А–µ—Б—Б–Є–µ–є –Ї–ї–µ—В–Њ—З–љ—Л—Е –≥–Њ—А–Љ–Њ–љ–Њ–≤ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ [4вАУ6, 27, 28]. –Т—В–Њ—А–Є—З–љ–∞—П –і–Є—Б–Љ–µ–љ–Њ—А–µ—П –Љ–Њ–ґ–µ—В –≤–Ї–ї—О—З–∞—В—М –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –њ–µ—А–≤–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є, –љ–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –Є–љ—Л–Љ–Є —Б–Њ—Б—В–Њ—П–љ–Є—П–Љ–Є –Є –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —В—А–µ–±—Г–µ—В —В–µ—А–∞–њ–Є–Є –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –І–∞—Й–µ —А–∞–Ј–≤–Є—В–Є–µ –≤—В–Њ—А–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є —Б–≤—П–Ј—Л–≤–∞—О—В —Б —Н–љ–і–Њ–Љ–µ—В—А–Є–Њ–Ј–Њ–Љ, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Њ—А–≥–∞–љ–Њ–≤ –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞, –ї–µ–є–Њ–Љ–Є–Њ–Љ–Њ–є –Є –Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ—Л–Љ —Ж–Є—Б—В–Є—В–Њ–Љ [4, 7]. –Т—В–Њ—А–Є—З–љ–∞—П –і–Є—Б–Љ–µ–љ–Њ—А–µ—П –љ–µ—А–µ–і–Ї–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М—О –Ї –∞–≥—А–µ—Б—Б–Є–≤–љ–Њ–Љ—Г –њ–Њ–≤–µ–і–µ–љ–Є—О –Ї–ї–µ—В–Њ–Ї —Н–љ–і–Њ–Љ–µ—В—А–Є—П –њ—А–Є —Б–љ–Є–ґ–µ–љ–Є–Є —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞ –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–Є [29]. –£ 10вАУ20% –ґ–µ–љ—Й–Є–љ —Н—В–Њ—В –њ—А–Њ—Ж–µ—Б—Б —Б–≤—П–Ј–∞–љ —Б –∞–і–µ–љ–Њ–Љ–Є–Њ–Ј–Њ–Љ [30].
–Ь–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ-–Ї–ї–µ—В–Њ—З–љ—Л–µ –њ—А–µ–і–њ–Њ—Б—Л–ї–Ї–Є —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є
–Т –Њ—Б–љ–Њ–≤–µ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є –ї–µ–ґ–Є—В –љ–∞—А—Г—И–µ–љ–Є–µ —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Љ–Є–Њ–Љ–µ—В—А–Є—П [31]. –Я—А–Є –њ–µ—А–≤–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ –Љ–∞—В–Њ—З–љ—Л–є —В–Њ–љ—Г—Б –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є –њ–Њ–Ї–Њ—П —Б–Њ—Б—В–∞–≤–ї—П–µ—В –±–Њ–ї–µ–µ 10 –Љ–Љ —А—В. —Б—В., –∞ –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ вАФ —Б–≤—Л—И–µ 120 –Љ–Љ —А—В. —Б—В., –≤ –Љ–Њ–Љ–µ–љ—В —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –Њ–љ–Њ –Љ–Њ–ґ–µ—В –њ–Њ–≤—Л—И–∞—В—М—Б—П –і–Њ 300 –Љ–Љ —А—В. —Б—В. [32].
–Ъ–ї—О—З–µ–≤–∞—П —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є –њ–µ—А–≤–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є –Њ—В–≤–Њ–і–Є—В—Б—П –і–Є—Б–±–∞–ї–∞–љ—Б—Г –≤ –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л вАФ –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤ (–њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤, –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞) [6]. –Ю–≤—Г–ї—П—В–Њ—А–љ—Л–µ —Г—А–Њ–≤–љ–Є –њ—А–Њ–≥–µ—Б—В–µ—А–Њ–љ–∞ —Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—В –Ї–ї–µ—В–Њ—З–љ—Л–µ –ї–Є–Ј–Њ—Б–Њ–Љ—Л, –љ–Њ –≤ –Ї–Њ–љ—Ж–µ –ї—О—В–µ–Є–љ–Њ–≤–Њ–є —Д–∞–Ј—Л, –Ї–Њ–≥–і–∞ —Г—А–Њ–≤–µ–љ—М –њ—А–Њ–≥–µ—Б—В–µ—А–Њ–љ–∞ —Б–љ–Є–ґ–∞–µ—В—Б—П, –ї–Є–Ј–Њ—Б–Њ–Љ—Л —А–∞–Ј—А—Г—И–∞—О—В—Б—П –Є –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞—О—В —Д–Њ—Б—Д–Њ–ї–Є–њ–∞–Ј—Г –Р2. –≠—В–Њ—В —Д–µ—А–Љ–µ–љ—В –Є–љ–Є—Ж–Є–Є—А—Г–µ—В –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –њ—Г—В–Є, –њ—А–Є–≤–Њ–і—П—Й–Є–µ –Ї —Б–Є–љ—В–µ–Ј—Г –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤ (—А–Є—Б. 1).
![–†–Є—Б. 1. –Я–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —А–∞–Ј–≤–Є—В–Є—П –±–Њ–ї–Є –Є –і—А—Г–≥–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ—А–Є –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ [6] Fig. 1. Pathogenic mechanisms of pain and other symptoms in dysmenorrhea [6] –†–Є—Б. 1. –Я–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —А–∞–Ј–≤–Є—В–Є—П –±–Њ–ї–Є –Є –і—А—Г–≥–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ—А–Є –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ [6] Fig. 1. Pathogenic mechanisms of pain and other symptoms in dysmenorrhea [6]](/upload/medialibrary/218/146-1.png)
–Я—А–Њ—Б—В–∞–љ–Њ–Є–і—Л —Б–∞–Љ–Є –љ–µ –≤—Л–Ј—Л–≤–∞—О—В –±–Њ–ї–µ–≤—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є –Є –љ–∞—Е–Њ–і—П—В—Б—П –≤ –Ї—А–Њ–≤–Є –Є —В–Ї–∞–љ—П—Е –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є. –Ю–і–љ–∞–Ї–Њ –Њ–љ–Є –≤–ї–Є—П—О—В –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л –≤ –Ї–ї–µ—В–Ї–∞—Е. –С–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ —Б–≤—П–Ј–∞–љ —Б –і–µ–є—Б—В–≤–Є–µ–Љ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ [33]. –Я—А–Є –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, –≤ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞ –Х2 (–Я–У –Х2) –Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞ F2ќ± (–Я–У F2ќ±), –љ–∞–±–ї—О–і–∞–µ—В—Б—П –і–Є—Б–±–∞–ї–∞–љ—Б —А–µ–≥—Г–ї—П—В–Њ—А–љ—Л—Е –Љ–Њ–ї–µ–Ї—Г–ї –≤ —Н–љ–і–Њ–Љ–µ—В—А–Є–Є, –Љ–Є–Њ–Љ–µ—В—А–Є–Є, –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А–µ –Њ—А–≥–∞–љ–Њ–≤ –Ц–Ъ–Ґ –Є –Ї—А–Њ–≤–µ–љ–Њ—Б–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –≤ –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–є –Ї—А–Њ–≤–Є. –Я–У F2ќ± –Є –Я–У –Х2 –Љ–Њ–≥—Г—В –≤–ї–Є—П—В—М –љ–∞ —Б–Њ—Б—В–Њ—П–љ–Є–µ –і—А—Г–≥–Є—Е –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–Њ–≤, –≤—Л–Ј—Л–≤–∞—П –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Г—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї—Г, —Б–≤—П–Ј–∞–љ–љ—Г—О —Б –±—А–Њ–љ—Е–Њ—Б–њ–∞–Ј–Љ–Њ–Љ, —В–Њ—И–љ–Њ—В–Њ–є, —А–≤–Њ—В–Њ–є, –і–Є–∞—А–µ–µ–є, –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є [34].
–Ф–Є—Б–Ї–Њ–Њ—А–і–Є–љ–∞—Ж–Є—П –Љ—Л—И–µ—З–љ—Л—Е —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є –њ–µ—А–µ—А–∞—Б—В–∞–µ—В –≤ —Б–њ–∞–Ј–Љ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –Є —Б–Њ—Б—Г–і–Њ–≤, —З—В–Њ –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –≤—Л–Ј—Л–≤–∞–µ—В –Є—И–µ–Љ–Є—О —В–Ї–∞–љ–µ–є –Є –≤—В–Њ—А–Є—З–љ–Њ–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ –Ї–ї–µ—В–Њ–Ї —Б –≤—Л–±—А–Њ—Б–Њ–Љ —Д–Њ—Б—Д–Њ–ї–Є–њ–∞–Ј—Л –Є –љ–Њ–≤—Л–є —Б–Є–љ—В–µ–Ј –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ –≤–Њ–≤–ї–µ—З–µ–љ–Є–µ –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –і–Є—Б–±–∞–ї–∞–љ—Б–∞: –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞—Б—Б—В—А–Њ–є—Б—В–≤—Г –≤–∞–Ј–Њ–њ—А–µ—Б—Б–Є–љ-–Њ–Ї—Б–Є—В–Њ—Ж–Є–љ–Њ–≤–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є —А–Є—В–Љ–∞ –Љ—Л—И–µ—З–љ—Л—Е —Б–Њ–Ї—А–∞—Й–µ–љ–Є–є. –°–њ–∞–Ј–Љ –Є –Є—И–µ–Љ–Є—П –њ—А–Є–≤–Њ–і—П—В –Ї —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –±–Њ–ї–µ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ї–∞–Ї –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞–Љ–Є, —В–∞–Ї –Є –і—А—Г–≥–Є–Љ–Є –∞–Ї—В–Є–≤–љ—Л–Љ–Є –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є (–Є–Њ–љ–∞–Љ–Є –Ї–∞–ї–Є—П –Є –Ї–∞–ї—М—Ж–Є—П, –ї–µ–є–Ї–Њ—В—А–Є–µ–љ–∞–Љ–Є) вАФ –њ–Њ—П–≤–ї—П–µ—В—Б—П –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–∞—П –±–Њ–ї—М. –†–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ –њ–Њ–≤—Л—И–µ–љ–Є—П —Н–Ї—Б–њ—А–µ—Б—Б–Є–Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ —П–≤–ї—П–µ—В—Б—П —Б–Є—Б—В–µ–Љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ—А–Њ–≥–∞ –±–Њ–ї–Є (–њ–Њ–≤—Л—И–µ–љ–Є–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –±–Њ–ї–Є). –Я–Њ–≤—Л—И–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –∞–Ї—В–Є–≤–љ—Л—Е –∞–ї—М–≥–Њ–≥–µ–љ–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ –≤ –Ї—А–Њ–≤–Є –Љ–Њ–ґ–µ—В –≤—Л–Ј—Л–≤–∞—В—М –≥–Њ–ї–Њ–≤–љ—Г—О –±–Њ–ї—М –Є –і—А—Г–≥–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л вАФ —А–≤–Њ—В—Г, –і–Є–∞—А–µ—О, –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ —Б–µ—А–і—Ж–∞ [5, 6, 28]. –Э–∞ –њ—А–∞–Ї—В–Є–Ї–µ —Г—А–Њ–≤–µ–љ—М –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –≤ –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–є –Ї—А–Њ–≤–Є –њ—А—П–Љ–Њ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї–µ–љ —А–Є—Б–Ї—Г —А–∞–Ј–≤–Є—В–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ [28]. –Т—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–є –±–Њ–ї–Є –Є —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –љ–µ–є —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ—А—П–Љ–Њ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞–µ–Љ—Л—Е –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ [9]. –Т—Л—Б–Њ–Ї–Њ–µ –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ, –њ–µ—А–Є—Б—В–∞–ї—М—В–Є–Ї–∞ –Є —Б–њ–∞–Ј–Љ –Љ–Є–Њ–Љ–µ—В—А–Є—П, –Њ–±—К—П—Б–љ—П—О—Й–Є–µ –њ–µ—А–≤–Є—З–љ—Г—О –і–Є—Б–Љ–µ–љ–Њ—А–µ—О, –њ—А–Є–≤–Њ–і—П—В –Ї –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Њ–Љ—Г –љ–∞–њ—А—П–ґ–µ–љ–Є—О –Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—О –Љ–∞—В–Ї–Є –Є –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ —Б—З–µ—В–µ –Љ–Њ–≥—Г—В —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞—В—М —А–∞–Ј–≤–Є—В–Є–µ –∞–і–µ–љ–Њ–Љ–Є–Њ–Ј–∞ [9]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Љ–Є–Ї—А–Њ—В—А–∞–≤–Љ–∞ –≤ –Њ–±–ї–∞—Б—В–Є –Ј–Њ–љ—Л —Н–љ–і–Њ–Љ–Є–Њ–Љ–µ—В—А–Є–∞–ї—М–љ–Њ–≥–Њ –њ–µ—А–µ—Е–Њ–і–∞ (junctional zone) —Б–ї—Г–ґ–Є—В –Њ–і–љ–Є–Љ –Є–Ј –Ї–ї—О—З–µ–≤—Л—Е –Ј–≤–µ–љ—М–µ–≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ —Н–љ–і–Њ–Љ–µ—В—А–Є–Њ–Ј–∞ [35].
–Ъ–∞—Б–Ї–∞–і–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —А–∞–Ј–≤–Є—В–Є—П –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –≤–∞–ґ–љ–Њ—Б—В—М –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ—Б—В–Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –њ—А–Є –њ–Њ—П–≤–ї–µ–љ–Є–Є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є, –∞ –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г—З–∞—П—Е –Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П.
–Ф–Є—Б–Љ–µ–љ–Њ—А–µ—О —Б–≤—П–Ј—Л–≤–∞—О—В –Є —Б –≤–ї–Є—П–љ–Є–µ–Љ –њ–Њ–ї–Њ–≤—Л—Е –≥–Њ—А–Љ–Њ–љ–Њ–≤ –љ–∞ —Б–Є–љ—В–µ–Ј –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –Є —А–∞–Ј–ї–Є—З–љ—Л–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л, –∞ —В–∞–Ї–ґ–µ –љ–∞ —А–∞–±–Њ—В—Г —А–∞–Ј–ї–Є—З–љ—Л—Е —Б–Є—Б—В–µ–Љ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –љ–µ–є—А–Њ–≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–є –Є —А–µ–љ–Є–љ-–∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ-–∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–Њ–≤–Њ–є. –Ш–Ј–Љ–µ–љ–µ–љ–Є–µ —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Н—В–Є—Е —Б–Є—Б—В–µ–Љ –≤ –Њ—В–≤–µ—В –љ–∞ –Ї–Њ–ї–µ–±–∞–љ–Є—П –њ–Њ–ї–Њ–≤—Л—Е –≥–Њ—А–Љ–Њ–љ–Њ–≤ –≤–Њ –≤—А–µ–Љ—П –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞ –Є –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М —Б–∞–Љ–Њ–≥–Њ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Љ–Њ–≥—Г—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М –њ–Њ—П–≤–ї–µ–љ–Є—О —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ—А–µ–і–Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –њ–µ—А–≤–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є. –°–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –љ–∞—А—Г—И–µ–љ–Є–µ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞ –Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–∞—П –∞–і–∞–њ—В–∞—Ж–Є—П –Љ–Њ–≥—Г—В –±—Л—В—М –Ї–ї—О—З–µ–≤—Л–Љ–Є –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є, –ї–µ–ґ–∞—Й–Є–Љ–Є –≤ –Њ—Б–љ–Њ–≤–µ —Н—В–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є [36].
–Ъ–∞–Ї –Є —З–µ–Љ –ї–µ—З–Є—В—М –і–Є—Б–Љ–µ–љ–Њ—А–µ—О
–†–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —Н–љ–і–Њ–Љ–µ—В—А–Є–Њ–Ј–∞ —П–≤–ї—П–µ—В—Б—П –µ—Й–µ –Њ–і–љ–Є–Љ –≤–µ—Б¬≠–Ї–Є–Љ –і–Њ–≤–Њ–і–Њ–Љ –≤ –њ–Њ–ї—М–Ј—Г –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є —А–∞–љ–љ–µ–є –Є –∞–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–µ—А–≤–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є [37].
–Ъ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Л–Љ —Б—А–µ–і—Б—В–≤–∞–Љ –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –Њ—В–љ–Њ—Б—П—В –Э–Я–Т–Я, –Ї–Њ—В–Њ—А—Л–µ –±—Л—Б—В—А–Њ –Є –њ–Њ–ї–љ–Њ—Б—В—М—О –Ї—Г–њ–Є—А—Г—О—В –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ—Г—О –±–Њ–ї—М —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї [38вАУ40]. –Ф–µ–є—Б—В–≤–Є–µ –Э–Я–Т–Я —Б–ї–µ–і—Г–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –Ї–∞–Ї –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–µ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –Њ–љ–Є —Б–љ–Є–ґ–∞—О—В –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –Я–У F2ќ± –Є –Я–У E2 –≤ –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–Љ —Б–µ–Ї—А–µ—В–µ. –Ю–і–љ–∞–Ї–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є –≤ —Н—В–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є –±—Г–і—Г—В —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є–Ї–Є [41]. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –Њ—Б–Њ–±—Г—О –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М –њ—А–Є–Њ–±—А–µ—В–∞–µ—В —А–∞–љ–љ–µ–µ –≤—Л—П–≤–ї–µ–љ–Є–µ –њ–µ—А–≤–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є –Ї–∞–Ї –њ—А–µ–і–Є–Ї—В–Њ—А–∞ —Е—А–Њ–љ–Є–Ј–∞—Ж–Є–Є –±–Њ–ї–Є –Є —В—А–µ–±—Г–µ—В –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї —В–µ—А–∞–њ–Є–Є [42].
–Я–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—П –њ–µ—А–≤–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Є–Ј—Г—З–µ–љ–∞, –Є –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–Њ—Б—А–µ–і–Њ—В–Њ—З–µ–љ—Л –љ–∞ –Љ–µ—В–Њ–і–∞—Е –ї–µ—З–µ–љ–Є—П, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є—О —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–Ї. –Я—А–Є –≤–µ–і–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ–є –њ—А–Є–Љ–µ–љ—П—О—В —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є –љ–µ—Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ (—Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П, —В–µ–њ–ї–Њ–≤–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ) –Љ–µ—В–Њ–і—Л, –љ–Њ –љ–∞ –Љ–Њ–Љ–µ–љ—В –љ–∞–њ–Є—Б–∞–љ–Є—П —Б—В–∞—В—М–Є –≤ –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –Њ–±–ї–µ–≥—З–µ–љ–Є—П –±–Њ–ї–Є —П–≤–ї—П–µ—В—Б—П –њ—А–Є–µ–Љ –Э–Я–Т–Я [4, 7, 43, 44].
–°–Є—Б—В–µ–Љ–∞—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–є –Њ–±–Ј–Њ—А, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л–є —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ—Г –∞–љ–∞–ї–Є–Ј—Г —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–µ—В–Њ–і–Њ–≤ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –њ–µ—А–≤–Є—З–љ–Њ–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –≤ –њ–Њ–ї—М–Ј—Г –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Э–Я–Т–Я –њ—А–Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –Є —В—П–ґ–µ–ї–Њ–є —В–∞–Ј–Њ–≤–Њ–є –±–Њ–ї–Є [43]. –Т –Њ—Б–љ–Њ–≤–µ –і–µ–є—Б—В–≤–Є—П –Э–Я–Т–Я –ї–µ–ґ–Є—В –њ—А–Є–љ—Ж–Є–њ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –і–µ—Б–µ–љ—Б–Є—В–Є–Ј–∞—Ж–Є–Є –Ї–∞–Ї –ї–µ–≥–Ї–Њ–є —В–∞–Ј–Њ–≤–Њ–є –±–Њ–ї–Є (–Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П), —В–∞–Ї –Є —В—П–ґ–µ–ї–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (–≤ —Б–Њ—Б—В–∞–≤–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є) [2].
–Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±–Ј–Њ—А–∞ –Є —Б–µ—В–µ–≤–Њ–≥–Њ –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј–∞ 35 –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —В–µ—А–∞–њ–Є–Є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є, –≤ –Ї–Њ—В–Њ—А—Л—Е —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Њ –≤ –Њ–±—Й–µ–є —Б–ї–Њ–ґ–љ–Њ—Б—В–Є 4383 –њ–∞—Ж–Є–µ–љ—В–Ї–Є, –Є–±—Г–њ—А–Њ—Д–µ–љ –њ—А–Є–Ј–љ–∞–љ –Њ–і–љ–Є–Љ –Є–Ј –і–≤—Г—Е –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е (–Њ—В–љ–Њ—И–µ–љ–Є–µ —И–∞–љ—Б–Њ–≤ (–Ю–®) —Б–Њ—Б—В–∞–≤–Є–ї–Њ 10,08, 95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї (–Ф–Ш) 3,29вАУ30,85) –Є –Њ–і–љ–Є–Љ –Є–Ј –і–≤—Г—Е –љ–∞–Є–±–Њ–ї–µ–µ –±–µ–Ј–Њ–њ–∞—Б–љ—Л—Е –Э–Я–Т–Я (–Њ—Ж–µ–љ–Ї–∞ –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Љ–µ—В–Њ–і–∞ –Ї—А–Є–≤—Л—Е SUCRA 79,7%). –Ш–±—Г–њ—А–Њ—Д–µ–љ –≤–Њ –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –≤ –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤ –і–Њ–Ј–∞—Е 200вАУ400 –Љ–≥, —Б–µ—В–µ–≤–Њ–є –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј –њ—А–Њ–≤–Њ–і–Є–ї—Б—П —Б –Ї–µ—В–Њ–њ—А–Њ—Д–µ–љ–Њ–Љ (50вАУ75 –Љ–≥), –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–Њ–Љ (25вАУ50 –Љ–≥), –љ–∞–њ—А–Њ–Ї—Б–µ–љ–Њ–Љ (250вАУ550 –Љ–≥) –Є –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є (500вАУ650 –Љ–≥) [45]. –°–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є –Њ–±–Ј–Њ—А –і–≤–Њ–є–љ—Л—Е —Б–ї–µ–њ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–ї –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–є –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –Э–Я–Т–Я –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ –њ—А–Є –Ю–® 4,50 –Є 95% –Ф–Ш 3,85вАУ5,27 –±–µ–Ј —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–є —А–∞–Ј–љ–Є—Ж—Л –Љ–µ–ґ–і—Г –Њ—В–і–µ–ї—М–љ—Л–Љ–Є –њ—А–µ–і—Б—В–∞–≤–Є—В–µ–ї—П–Љ–Є –≥—А—Г–њ–њ—Л [33].
–Ф–µ–є—Б—В–≤–Є–µ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Є–±—Г–њ—А–Њ—Д–µ–љ–∞, –њ–Є—В–Њ—Д–µ–љ–Њ–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і–∞ –Є —Д–µ–љ–њ–Є–≤–µ—А–Є–љ–Є—П –±—А–Њ–Љ–Є–і–∞ (–°–Я–Р–Ч–У–Р–Э –Э–Х–Ю) –љ–∞ –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —А–∞–Ј–≤–Є—В–Є—П –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є вАФ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ (—А–Є—Б. 2).
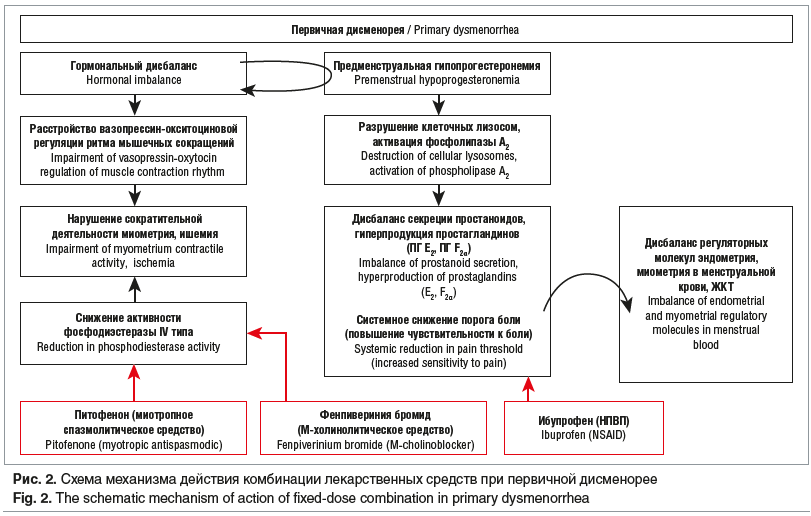
–Ф–µ–є—Б—В–≤–Є–µ –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –Њ—Б–љ–Њ–≤—Л–≤–∞–µ—В—Б—П –љ–∞ –њ–Њ–і–∞–≤–ї–µ–љ–Є–Є –≤—Л—А–∞–±–Њ—В–Ї–Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –њ—Г—В–µ–Љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є—П —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј–љ–Њ–≥–Њ –њ—Г—В–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –°–љ–Є–ґ–∞–µ—В—Б—П —Б—В–Є–Љ—Г–ї—П—Ж–Є—П —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –Љ–Є–Њ–Љ–µ—В—А–Є—П –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞–Љ–Є, –њ–Њ–≤—Л—И–∞–µ—В—Б—П –±–Њ–ї–µ–≤–Њ–є –њ–Њ—А–Њ–≥ [45].
–§–µ–љ–њ–Є–≤–µ—А–Є–љ–Є—П –±—А–Њ–Љ–Є–і –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –±–Њ–ї–µ–µ —Ж–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –≥–ї–∞–і–Ї—Г—О –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Г –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–Њ–≤, —З—В–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Њ–±–ї–µ–≥—З–∞–µ—В —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї. –С–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–Є–µ –Љ—Г—Б–Ї–∞—А–Є–љ–Њ–≤—Л—Е —Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї –Ј–∞—В—А—Г–і–љ–µ–љ–Є—О –і–µ–њ–Њ–ї—П—А–Є–Ј–∞—Ж–Є–Є –Љ–µ–Љ–±—А–∞–љ –Љ–Є–Њ—Ж–Є—В–Њ–≤, —Б–љ–Є–ґ–µ–љ–Є—О –њ–Њ—В–Њ–Ї–∞ –Є–Њ–љ–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –≤ —Н—В–Є –Ї–ї–µ—В–Ї–Є –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, –Ї —Б–љ–Є–ґ–µ–љ–Є—О —В–Њ–љ—Г—Б–∞ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Д–µ–љ–њ–Є–≤–µ—А–Є–љ–Є—П –±—А–Њ–Љ–Є–і –Њ–±–ї–µ–≥—З–∞–µ—В —Б–њ–∞–Ј–Љ—Л, –Є–Ј-–Ј–∞ –Ї–Њ—В–Њ—А—Л—Е —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Є —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–∞—П –±–Њ–ї—М.
–Ю–±–ї–µ–≥—З–∞–µ—В —Б–њ–∞–Ј–Љ—Л –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–Њ–≤ –Є —Б–Њ—Б—Г–і–Њ–≤ —В–∞–Ї–ґ–µ –Љ–Є–Њ—В—А–Њ–њ–љ–Њ–µ —Б–њ–∞–Ј–Љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–µ —Б—А–µ–і—Б—В–≤–Њ –њ–Є—В–Њ—Д–µ–љ–Њ–љ. –Ф–µ–є—Б—В–≤–Є–µ –њ–Є—В–Њ—Д–µ–љ–Њ–љ–∞ —Б—Д–Њ–Ї—Г—Б–Є—А–Њ–≤–∞–љ–Њ –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Д–Њ—Б—Д–Њ–і–Є—Н—Б—В–µ—А–∞–Ј—Л IV —В–Є–њ–∞. –Т–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ —Д–Њ—Б—Д–Њ–і–Є—Н—Б—В–µ—А–∞–Ј—Г IV —В–Є–њ–∞ —В–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —В–Њ–љ—Г—Б–∞ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л, —В–∞–Ї –Ї–∞–Ї —Н—В–Њ—В —Д–µ—А–Љ–µ–љ—В —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ—Б–љ–Њ–≤–љ–Њ–µ –Ј–≤–µ–љ–Њ –≥–Є–і—А–Њ–ї–Є–Ј–∞ —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–і–µ–љ–Њ–Ј–Є–љ–Љ–Њ–љ–Њ—Д–Њ—Б—Д–∞—В–∞ –≤ –Ї–ї–µ—В–Ї–∞—Е –≥–ї–∞–і–Ї–Є—Е –Љ—Л—И—Ж –Љ–∞—В–Ї–Є, –Љ–Њ—З–µ—В–Њ—З–љ–Є–Ї–Њ–≤, –ґ–µ–ї—З–µ–≤—Л–≤–Њ–і—П—Й–Є—Е –њ—Г—В–µ–є, –Њ—А–≥–∞–љ–Њ–≤ –Ц–Ъ–Ґ, –Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е —Б–Њ—Б—Г–і–Њ–≤ –Є —Б–µ–Ї—А–µ—В–Њ—А–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е, —П–≤–ї—П—П—Б—М –Є–љ–і—Г–Ї—В–Њ—А–Њ–Љ —Б–Њ–Ї—А–∞—Й–µ–љ–Є—П –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –≤ –і–∞–љ–љ–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є [5].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤, –≤—Е–Њ–і—П—Й–Є—Е –≤ —Б–Њ—Б—В–∞–≤ –њ—А–µ–њ–∞—А–∞—В–∞ –°–Я–Р–Ч–У–Р–Э –Э–Х–Ю, —Г—Б—В—А–∞–љ—П–µ—В —Б–њ–∞–Ј–Љ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л, –∞ —В–∞–Ї–ґ–µ –Є—И–µ–Љ–Є—О, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—О –±–Њ–ї–Є –њ—А–Є –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–Є.
–Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Є–±—Г–њ—А–Њ—Д–µ–љ–∞, –њ–Є—В–Њ—Д–µ–љ–Њ–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і–∞ –Є —Д–µ–љ–њ–Є–≤–µ—А–Є–љ–Є—П –±—А–Њ–Љ–Є–і–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Љ–Њ–љ–Њ–њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Є–Ј –≥—А—Г–њ–њ—Л –Э–Я–Т–Я –њ—А–Є —В–µ—А–∞–њ–Є–Є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є –Њ—В–Љ–µ—З–µ–љ—Л –≤ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–є –љ–∞—Г—З–љ–Њ–є –ї–Є—В–µ—А–∞—В—Г—А–µ. –†—П–і –∞–≤—В–Њ—А–Њ–≤ –і–∞–љ–љ—Г—О —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Г—О –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В –≤—Л–±–Њ—А–∞ [46].
–Ґ–∞–Ї –Ї–∞–Ї –і–Є—Б–Љ–µ–љ–Њ—А–µ—П –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б, —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –Є–±—Г–њ—А–Њ—Д–µ–љ–∞, –њ–Є—В–Њ—Д–µ–љ–Њ–љ–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і–∞ –Є —Д–µ–љ–њ–Є–≤–µ—А–Є–љ–Є—П –±—А–Њ–Љ–Є–і–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–∞–Ј–љ–∞—З–µ–љ–∞ —Б –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є —Ж–µ–ї—М—О –Ј–∞ 2вАУ3 –і–љ—П –і–Њ –Љ–µ–љ—Б—В—А—Г–∞—Ж–Є–Є –Є–ї–Є –њ—А–Є –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–є –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Є–µ–Љ–∞ –љ–µ –і–Њ–ї–ґ–љ–∞ –њ—А–µ–≤—Л—И–∞—В—М 5 –і–љ–µ–є. –°–Я–Р–Ч–У–Р–Э –Э–Х–Ю —П–≤–ї—П–µ—В—Б—П –±–µ–Ј—А–µ—Ж–µ–њ—В—Г—А–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –њ–Њ—Н—В–Њ–Љ—Г –і–Њ—Б—В—Г–њ–µ–љ –і–ї—П –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –Њ–Ї–∞–Ј–∞–љ–Є—П –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й–Є –њ—А–Є –њ–Њ—П–≤–ї–µ–љ–Є–Є —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є.
–Ю–і–љ–∞–Ї–Њ —Е–Њ—В–µ–ї–Њ—Б—М –±—Л –љ–∞–њ–Њ–Љ–љ–Є—В—М, —З—В–Њ –Э–Я–Т–Я –Љ–Њ–≥—Г—В –Њ–Ї–∞–Ј—Л–≤–∞—В—М –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –Ц–Ъ–Ґ. –Я–Њ—Б–ї–µ–і–љ–Є–µ –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–Њ–ґ–µ—В —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є, –Њ—Б—В—А–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞, –≤–µ–љ–Њ–Ј–љ–Њ–є —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є–Є [8]. –°–Я–Р–Ч–У–Р–Э –Э–Х–Ю –≤—Л–њ—Г—Б–Ї–∞–µ—В—Б—П –≤ —Д–Њ—А–Љ–µ —В–∞–±–ї–µ—В–Њ–Ї, –њ–Њ–Ї—А—Л—В—Л—Е –Њ–±–Њ–ї–Њ—З–Ї–Њ–є, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–љ–Є–Ј–Є—В—М —А–Є—Б–Ї –њ—А—П–Љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –Є—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О –ґ–µ–ї—Г–і–Ї–∞.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Я–µ—А–≤–Є—З–љ–∞—П –і–Є—Б–Љ–µ–љ–Њ—А–µ—П —П–≤–ї—П–µ—В—Б—П –Ї—А—Г–њ–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –Є —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є, —В–∞–Ї –Ї–∞–Ї –Ј–∞—В—А–∞–≥–Є–≤–∞–µ—В –Њ–±—И–Є—А–љ—Г—О –Ї–∞—В–µ–≥–Њ—А–Є—О –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –≥–ї–∞–≤–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–∞—П –±–Њ–ї—М –≤ –ґ–Є–≤–Њ—В–µ –Є –њ–Њ—П—Б–љ–Є—Ж–µ вАФ —В—П–љ—Г—Й–∞—П, —А–µ–ґ—Г—Й–∞—П, —Б—Е–≤–∞—В–Ї–Њ–Њ–±—А–∞–Ј–љ–∞—П, вАФ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В, –њ–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П–Љ, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –∞–љ–Њ–Љ–∞–ї—М–љ–Њ –≤—Л—Б–Њ–Ї–Њ–є —Б–Њ–Ї—А–∞—В–Є–Љ–Њ—Б—В–Є –Љ–Є–Њ–Љ–µ—В—А–Є—П, —Б—Г–ґ–µ–љ–Є—П –∞—А—В–µ—А–Є–Њ–ї –Є —В–Ї–∞–љ–µ–≤–Њ–є –≥–Є–њ–Њ–Ї—Б–Є–Є. –Ъ–ї—О—З–µ–≤—Л–Љ–Є –Љ–Њ–ї–µ–Ї—Г–ї–∞–Љ–Є –≤ —А–∞–Ј–≤–Є—В–Є–Є –і–∞–љ–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П —З–∞—Б—В–Њ —П–≤–ї—П—О—В—Б—П –Я–У –Х2 –Є –Я–У F2ќ±. –°–Я–Р–Ч–У–Р–Э –Э–Х–Ю —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –≤ —Б–љ–Є–ґ–µ–љ–Є–Є –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–є –±–Њ–ї–Є –Є –і—А—Г–≥–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є –±–ї–∞–≥–Њ–і–∞—А—П —Б–Њ—З–µ—В–∞–љ–Є—О —В—А–µ—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –њ—А–µ–њ–∞—А–∞—В–∞, –Ї–Њ—В–Њ—А—Л–µ –≤–ї–Є—П—О—В –љ–∞ –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л —А–∞–Ј–≤–Є—В–Є—П –і–Є—Б–Љ–µ–љ–Њ—А–µ–Є. –°–Я–Р–Ч–У–Р–Э –Э–Х–Ю —Е–Њ—А–Њ—И–Њ –њ–Њ–і—Е–Њ–і–Є—В –і–ї—П –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞–љ–Є—П, —В–∞–Ї –Ї–∞–Ї –Њ—В–њ—Г—Б–Ї–∞–µ—В—Б—П –±–µ–Ј —А–µ—Ж–µ–њ—В–∞. –Т–Њ–≤–ї–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ–Њ-–Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, –≥–ї–∞–≤–љ—Л–Љ–Є –Є–Ј –Ї–Њ—В–Њ—А—Л—Е —П–≤–ї—П—О—В—Б—П –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –≤—Л—А–∞–±–Њ—В–Ї–Є –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –Є –њ—А–µ–њ—П—В—Б—В–≤–Є–µ —Б–њ–∞–Ј–Љ—Г –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –≤–љ—Г—В—А–µ–љ–љ–Є—Е –Њ—А–≥–∞–љ–Њ–≤ –Є —Б–Њ—Б—Г–і–Њ–≤, –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї—Г—О –Њ–њ—А–∞–≤–і–∞–љ–љ–Њ—Б—В—М –Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –°–Я–Р–Ч–У–Р–Э –Э–Х–Ю –њ—А–Є –і–Є—Б–Љ–µ–љ–Њ—А–µ–µ.
–°–≤–µ–і–µ–љ–Є—П –Њ–± –∞–≤—В–Њ—А–∞—Е:
–І–µ–±–Њ—В–∞—А–µ–≤–∞ –Ѓ–ї–Є—П –Ѓ—А—М–µ–≤–љ–∞ вАФ –і.–Љ.–љ., –і–Њ—Ж–µ–љ—В, –і–Њ—Ж–µ–љ—В –Ї–∞—Д–µ–і—А—Л –∞–Ї—Г—И–µ—А—Б—В–≤–∞ –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є вДЦ 2 –У–С–Ю–£ –Т–Я–Ю –†–Њ—Б—В–У–Ь–£ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є; 344022, –†–Њ—Б—Б–Є—П, –≥. –†–Њ—Б—В–Њ–≤-–љ–∞-–Ф–Њ–љ—Г, –њ–µ—А. –Э–∞—Е–Є—З–µ–≤–∞–љ—Б–Ї–Є–є, –і. 29; ORCID iD 0000-0001-9609-0917.
–Я–µ—В—А–Њ–≤ –Ѓ—А–Є–є –Р–ї–µ–Ї—Б–µ–µ–≤–Є—З вАФ –і.–Љ.–љ., –њ—А–Њ—Д–µ—Б—Б–Њ—А, –Ј–∞–≤–µ–і—Г—О—Й–Є–є –Ї–∞—Д–µ–і—А–Њ–є –∞–Ї—Г—И–µ—А—Б—В–≤–∞ –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є вДЦ 2 –У–С–Ю–£ –Т–Я–Ю –†–Њ—Б—В–У–Ь–£ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є; 344022, –†–Њ—Б—Б–Є—П, –≥. –†–Њ—Б—В–Њ–≤-–љ–∞-–Ф–Њ–љ—Г, –њ–µ—А. –Э–∞—Е–Є—З–µ–≤–∞–љ—Б–Ї–Є–є, –і. 29; ORCID iD 0000-0002-2348-8809.
–Ъ–Њ–љ—В–∞–Ї—В–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П: –І–µ–±–Њ—В–∞—А–µ–≤–∞ –Ѓ–ї–Є—П –Ѓ—А—М–µ–≤–љ–∞, e-mail: chebotarevajulia@inbox.ru.
–Я—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є: –љ–Є–Ї—В–Њ –Є–Ј –∞–≤—В–Њ—А–Њ–≤ –љ–µ –Є–Љ–µ–µ—В —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –Ј–∞–Є–љ—В–µ—А–µ—Б–Њ–≤–∞–љ–љ–Њ—Б—В–Є –≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–∞—Е –Є –Љ–µ—В–Њ–і–∞—Е.
–Ъ–Њ–љ—Д–ї–Є–Ї—В –Є–љ—В–µ—А–µ—Б–Њ–≤ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В.
–°—В–∞—В—М—П –њ–Њ—Б—В—Г–њ–Є–ї–∞ 14.03.2022.
–Я–Њ—Б—В—Г–њ–Є–ї–∞ –њ–Њ—Б–ї–µ —А–µ—Ж–µ–љ–Ј–Є—А–Њ–≤–∞–љ–Є—П 06.04.2022.
–Я—А–Є–љ—П—В–∞ –≤ –њ–µ—З–∞—В—М 29.04.2022.
About the authors:
Yuliya Yu. Chebotareva вАФ Dr. Sc. (Med.), Associate Professor, associate professor of the Department of Obstetrics & Gynecology, Rostov State Medical University; 29, Nakhichevanskiy lane, Rostov-on-Don, 344022, Russian Federation; ORCID iD 0000-0001-9609-0917.
Yuriy A. Petrov вАФ Dr. Sc. (Med.), Professor, Head of the Department of Obstetrics & Gynecology, Rostov State Medical University; 29, Nakhichevanskiy lane, Rostov-on-Don, 344022, Russian Federation; ORCID iD 0000-0002-2348-8809.
Contact information: Yuliya Yu. Chebotareva, e-mail: chebotarevajulia@inbox.ru.
Financial Disclosure: the authors have no a financial or property interest in any material or method mentioned.
There is no conflict of interests.
Received 14.03.2022.
Revised 06.04.2022.
Accepted 29.04.2022.








.gif)



