–Т–≤–µ–і–µ–љ–Є–µ
–Т–њ–µ—А–≤—Л–µ –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л–µ —Б–Є–љ–µ—Е–Є–Є (–Т–Ь–°) –±—Л–ї–Є –Њ–њ–Є—Б–∞–љ—Л –≤ 1894 –≥. Fritsch H. [1] —Г –њ–∞—Ж–Є–µ–љ—В–Ї–Є —Б–Њ –≤—В–Њ—А–Є—З–љ–Њ–є –∞–Љ–µ–љ–Њ—А–µ–µ–є, —А–∞–Ј–≤–Є–≤—И–µ–є—Б—П –њ–Њ—Б–ї–µ –≤—Л—Б–Ї–∞–±–ї–Є–≤–∞–љ–Є—П –≤ –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤–Њ–Љ –њ–µ—А–Є–Њ–і–µ. –°–њ—Г—Б—В—П 33 –≥–Њ–і–∞ Bass –Т. —Г 20 –Є–Ј 1500 –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е –ґ–µ–љ—Й–Є–љ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–ї –∞—В—А–µ–Ј–Є—О —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, –≤–Њ–Ј–љ–Є–Ї—И—Г—О –њ–Њ—Б–ї–µ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–≥–Њ –∞–±–Њ—А—В–∞ [2]. –Т 1946 –≥. Stamer S. –Ї 37 —Б–ї—Г—З–∞—П–Љ, –Њ–њ–Є—Б–∞–љ–љ—Л–Љ –≤ –ї–Є—В–µ—А–∞—В—Г—А–µ, –і–Њ–±–∞–≤–Є–ї 24 —Б–ї—Г—З–∞—П –Є–Ј —Б–Њ–±—Б—В–≤–µ–љ–љ–Њ–≥–Њ –Њ–њ—Л—В–∞ [3]. –Т 1948 –≥. –Ф–ґ–Њ–Ј–µ—Д–Њ–Љ –Р—И–µ—А–Љ–∞–љ–Њ–Љ –±—Л–ї –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ —А—П–і —Б—В–∞—В—М–µ–є, –≤ –Ї–Њ—В–Њ—А—Л—Е –≤–њ–µ—А–≤—Л–µ —Г–Ї–∞–Ј–∞–ї —З–∞—Б—В–Њ—В—Г –Т–Ь–°, –њ–Њ–і—А–Њ–±–љ–Њ –Њ–њ–Є—Б–∞–ї —Н—В–Є–Њ–ї–Њ–≥–Є—О, —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї—Г, –∞ —В–∞–Ї–ґ–µ –њ—А–µ–і—Б—В–∞–≤–Є–ї —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –Ї–∞—А—В–Є–љ—Г –Т–Ь–°. –Я–Њ—Б–ї–µ –µ–≥–Њ –њ—Г–±–ї–Є–Ї–∞—Ж–Є–є —В–µ—А–Љ–Є–љ ¬Ђ—Б–Є–љ–і—А–Њ–Љ –Р—И–µ—А–Љ–∞–љ–∞¬ї –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –і–ї—П –Њ–њ–Є—Б–∞–љ–Є—П –Т–Ь–° –і–Њ –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –≤—А–µ–Љ–µ–љ–Є. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ —З—В–Њ –Њ —Б–Є–љ–µ—Е–Є—П—Е –Є–Ј–≤–µ—Б—В–љ–Њ –±–Њ–ї—М—И–µ –≤–µ–Ї–∞, –њ—А–Њ–±–ї–µ–Љ–∞ –і–Њ —Б–Є—Е –њ–Њ—А –Њ—Б—В–∞–µ—В—Б—П –љ–µ—А–µ—И–µ–љ–љ–Њ–є, –Є –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤–µ–і—Г—В—Б—П —А–∞–±–Њ—В—Л, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л–µ –љ–∞ –Є–Ј—Л—Б–Ї–∞–љ–Є–µ –Љ–µ—А –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –і–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є.–Я—Г—Б–Ї–Њ–≤—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –і–ї—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –Т–Ь–° —П–≤–ї—П–µ—В—Б—П —В—А–∞–≤–Љ–∞ –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Б–ї–Њ—П —Н–љ–і–Њ–Љ–µ—В—А–Є—П, –Ї–Њ—В–Њ—А–∞—П –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л–Ј–≤–∞–љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є. –Ю—Б–љ–Њ–≤–љ–Њ–є –Є–Ј –љ–Є—Е вАУ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –≤–Њ –≤—А–µ–Љ—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –Є–ї–Є –≤ –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤–Њ–Љ –њ–µ—А–Є–Њ–і–µ. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ —З—В–Њ —Б–Є–љ–і—А–Њ–Љ –Р—И–µ—А–Љ–∞–љ–∞ –±—Л–ї –Њ–њ–Є—Б–∞–љ –њ–Њ—Б–ї–µ –њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–љ–Њ–≥–Њ –≤—Л—Б–Ї–∞–±–ї–Є–≤–∞–љ–Є—П –њ–Њ –њ–Њ–≤–Њ–і—Г –∞–Ї—Г—И–µ—А—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є, –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ—Л –Є –і—А—Г–≥–Є–µ –њ—А–Є—З–Є–љ—Л –Т–Ь–°. –Ґ–∞–Ї, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —З–Є—Б–ї–∞ –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –њ–Њ –њ–Њ–≤–Њ–і—Г —Б—Г–±–Љ—Г–Ї–Њ–Ј–љ—Л—Е –Љ–Є–Њ–Љ–∞—В–Њ–Ј–љ—Л—Е —Г–Ј–ї–Њ–≤, –∞–љ–Њ–Љ–∞–ї–Є–є —А–∞–Ј–≤–Є—В–Є—П –Љ–∞—В–Ї–Є –Є —В. –і. –і–∞–ї–Њ –µ—Й–µ –Њ–і–љ—Г –≥—А—Г–њ–њ—Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї, –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –Т–Ь–°.
–†–Њ–ї—М –Є–љ—Д–µ–Ї—Ж–Є–Є –≤ —А–∞–Ј–≤–Є—В–Є–Є –Т–Ь–° вАУ —Б–њ–Њ—А–љ–∞—П. –Т —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Њ–і–љ–Є –∞–≤—В–Њ—А—Л —Б—З–Є—В–∞—О—В, —З—В–Њ –Є–љ—Д–µ–Ї—Ж–Є–Є –љ–µ –њ—А–Є—З–∞—Б—В–љ—Л –Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –Т–Ь–°, –і—А—Г–≥–Є–µ —Г—В–≤–µ—А–ґ–і–∞—О—В, —З—В–Њ –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –і–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —П–≤–ї—П–µ—В—Б—П –Є–Љ–µ–љ–љ–Њ –Є–љ—Д–µ–Ї—Ж–Є—П, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –≥–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–љ–Њ–Љ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ –Є–ї–Є –њ–Њ–і–Њ—Б—В—А–Њ–Љ —Н–љ–і–Њ–Љ–µ—В—А–Є—В–µ, –і–∞–ґ–µ –±–µ–Ј –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л (–ї–Є—Е–Њ—А–∞–і–Ї–Є, –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–Ј–∞, –≥–љ–Њ–є–љ—Л—Е –≤—Л–і–µ–ї–µ–љ–Є–є).
–£ –±–Њ–ї—М–љ—Л—Е —Б –Т–Ь–° –Ї–∞—А—В–Є–љ–∞ –њ—А–Є –≥–Є—Б—В–µ—А–Њ—Б–Ї–Њ–њ–Є–Є (–У–°) –Љ–Њ–ґ–µ—В –±—Л—В—М —А–∞–Ј–ї–Є—З–љ–Њ–є: –Њ—В —А—Л—Е–ї—Л—Е, –µ–і–Є–љ–Є—З–љ—Л—Е —Б–њ–∞–µ–Ї –і–Њ –њ–Њ–ї–љ–Њ–є –Њ–±–ї–Є—В–µ—А–∞—Ж–Є–Є –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є –њ–ї–Њ—В–љ—Л–Љ–Є —Б–Є–љ–µ—Е–Є—П–Љ–Є. –†—П–і –∞–≤—В–Њ—А–Њ–≤ —Г—В–≤–µ—А–ґ–і–∞—О—В, —З—В–Њ –Ї—А–Є—В–Є—З–µ—Б–Ї–Є–є –њ–µ—А–Є–Њ–і, –≤ —В–µ—З–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –њ–Њ—П–≤–ї—П—О—В—Б—П —Б–њ–∞–є–Ї–Є, вАУ –Њ—В 3-—Е –і–Њ 5 –і–љ–µ–є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є [4]. –≠—В–Њ—В –њ—А–Њ—Ж–µ—Б—Б —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П —А—П–і–Њ–Љ —Д–∞–Ї—В–Њ—А–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –љ–∞—А—Г—И–∞—О—В —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Д–Є–±—А–Є–љ–Њ–ї–Є–Ј: –Є—И–µ–Љ–Є—П, –њ–Њ—Б—В—В—А–∞–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, –љ–∞–ї–Є—З–Є–µ –Ї—А–Њ–≤–Є, –Є–љ–Њ—А–Њ–і–љ—Л–µ —В–µ–ї–∞ [5]. –°–њ–∞–є–Ї–Є –Љ–Њ–≥—Г—В –≤–Њ–≤–ї–µ–Ї–∞—В—М —А–∞–Ј–ї–Є—З–љ—Л–µ —Б–ї–Њ–Є –Ї–∞–Ї —Н–љ–і–Њ–Љ–µ—В—А–Є—П, —В–∞–Ї –Є –Љ–Є–Њ–Љ–µ—В—А–Є—П. –°—А–∞—Й–µ–љ–Є—П —Н—В–Є—Е —В–Ї–∞–љ–µ–є –≥–Є—Б—В–µ—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є –њ—А–Њ—П–≤–ї—П—О—В—Б—П —Е–∞—А–∞–Ї—В–µ—А–љ–Њ–є –Ї–∞—А—В–Є–љ–Њ–є: —Н–љ–і–Њ–Љ–µ—В—А–Є–∞–ї—М–љ—Л–µ —Б–њ–∞–є–Ї–Є —Б—Е–Њ–ґ–Є —Б –Њ–Ї—А—Г–ґ–∞—О—Й–µ–є –Ј–і–Њ—А–Њ–≤–Њ–є —В–Ї–∞–љ—М—О, –Љ–Є–Њ—Д–Є–±—А–Є–∞–ї—М–љ—Л–µ —Б–њ–∞–є–Ї–Є –≤—Б—В—А–µ—З–∞—О—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–љ—Л–Љ —В–Њ–љ–Ї–Є–Љ —Б–ї–Њ–µ–Љ —Н–љ–і–Њ–Љ–µ—В—А–Є—П —Б –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –ґ–µ–ї–µ–Ј–∞–Љ–Є.
–Э–∞—А—Г—И–µ–љ–Є—П –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є, –≤–Ї–ї—О—З–∞—П –≥–Є–њ–Њ–Љ–µ–љ–Њ—А–µ—О –Є –∞–Љ–µ–љ–Њ—А–µ—О, –Њ—Б—В–∞—О—В—Б—П –Њ–±—Й–Є–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –Т–Ь–° [6]. –Я—А–Є –Т–Ь–° –∞–Љ–µ–љ–Њ—А–µ—П –Љ–Њ–ґ–µ—В –±—Л—В—М –≤—Л–Ј–≤–∞–љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є: —Н–љ–і–Њ—Ж–µ—А–≤–Є–Ї–∞–ї—М–љ—Л–Љ–Є —Б–њ–∞–є–Ї–∞–Љ–Є, –њ—А–Є–≤–Њ–і—П—Й–Є–Љ–Є –Ї –Њ–±—Б—В—А—Г–Ї—Ж–Є–Є —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞, –Њ–±—И–Є—А–љ—Л–Љ —Б–њ–∞–µ—З–љ—Л–Љ –њ—А–Њ—Ж–µ—Б—Б–Њ–Љ –≤ –њ–Њ–ї–Њ—Б—В–Є —В–µ–ї–∞ –Љ–∞—В–Ї–Є –Є–Ј-–Ј–∞ —А–∞–Ј—А—Г—И–µ–љ–Є—П –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Б–ї–Њ—П —Н–љ–і–Њ–Љ–µ—В—А–Є—П. –Я—А–Є –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–є –∞–Љ–µ–љ–Њ—А–µ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –Њ—В–Љ–µ—З–∞—О—В—Б—П —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–є –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В –Є–ї–Є –±–Њ–ї–Є –≤–љ–Є–Ј—Г –ґ–Є–≤–Њ—В–∞, –≥–µ–Љ–∞—В–Њ–Љ–µ—В—А–∞ –Є –і–∞–ґ–µ –≥–µ–Љ–∞—В–Њ—Б–∞–ї—М–њ–Є–љ–Ї—Б. –Ю—В–Љ–µ—З–∞–µ—В—Б—П —В–∞–Ї–ґ–µ –і–Є—Б–Љ–µ–љ–Њ—А–µ—П –Є –±–µ—Б–њ–ї–Њ–і–Є–µ [6]. –Я–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –∞–Љ–µ–љ–Њ—А–µ–µ–є –Є –±–µ—Б–њ–ї–Њ–і–Є–µ–Љ –љ–µ–≤—Л–љ–∞—И–Є–≤–∞–љ–Є–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –±–Њ–ї–µ–µ –ї–µ–≥–Ї–Є–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П–Љ –Т–Ь–°. –Т–Њ–Ј–Љ–Њ–ґ–љ—Л–µ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Д–∞–Ї—В–Њ—А—Л –≤–Ї–ї—О—З–∞—О—В –≤ —Б–µ–±—П: —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є, –Њ—В—Б—Г—В—Б—В–≤–Є–µ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є —В–Ї–∞–љ–Є —Н–љ–і–Њ–Љ–µ—В—А–Є—П –і–ї—П –Є–Љ–њ–ї–∞–љ—В–∞—Ж–Є–Є –Є –њ–Њ–і–і–µ—А–ґ–Ї–Є –њ–ї–∞—Ж–µ–љ—В—Л, –љ–µ–њ–Њ–ї–љ–Њ—Ж–µ–љ–љ—Г—О –≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є—О —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А—Г—О—Й–µ–≥–Њ —Н–љ–і–Њ–Љ–µ—В—А–Є—П –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Д–Є–±—А–Њ–Ј–∞ –Є —В. –і. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Schenker J.G., Margalioth E.J. –љ–∞–±–ї—О–і–∞–ї–Є—Б—М 165 –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–µ–є —Г –ґ–µ–љ—Й–Є–љ —Б –љ–µ–ї–µ—З–µ–љ–Њ–є —Д–Њ—А–Љ–Њ–є —Б–Є–љ–і—А–Њ–Љ–∞ –Р—И–µ—А–Љ–∞–љ–∞. –І–∞—Б—В–Њ—В–∞ —Б–њ–Њ–љ—В–∞–љ–љ–Њ–≥–Њ –≤—Л–Ї–Є–і—Л—И–∞ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 40%, –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ—Л—Е —А–Њ–і–Њ–≤ 23%, —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ—Л–µ —А–Њ–і—Л –њ—А–Њ–Є–Ј–Њ—И–ї–Є –≤ 30% —Б–ї—Г—З–∞–µ–≤, –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Ї—А–µ–њ–ї–µ–љ–Є–µ –њ–ї–∞—Ж–µ–љ—В—Л –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г 13% –ґ–µ–љ—Й–Є–љ, –≤–љ–µ–Љ–∞—В–Њ—З–љ–∞—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М вАУ —Г 12% –±–Њ–ї—М–љ—Л—Е [6].
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П —В–µ—Б–љ–Њ —Б–≤—П–Ј–∞–љ—Л —Б —В–∞–Ї–Є–Љ–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є, –Ї–∞–Ї –≥–ї—Г–±–Є–љ–∞ —Д–Є–±—А–Њ–Ј–∞, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ —Б–њ–∞–µ–Ї (—А–Є—Б. 1), –Є –і–µ–ї—П—В—Б—П –љ–∞ 3 —В–Є–њ–∞.
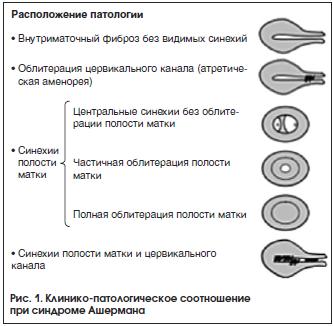
–Ґ–Є–њ 1. –Р–Љ–µ–љ–Њ—А–µ—П —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Б–њ–∞–µ–Ї –Є–ї–Є —Б—В–µ–љ–Њ–Ј–∞ —Ж–µ—А–≤–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞. –Т —В–∞–Ї–Є—Е —Б–ї—Г—З–∞—П—Е, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –≤—Л—П–≤–ї—П–µ—В—Б—П –љ–Њ—А–Љ–∞–ї—М–љ–∞—П –њ–Њ–ї–Њ—Б—В—М –Љ–∞—В–Ї–Є –≤—Л—И–µ —Б–њ–∞–µ–Ї, –њ—А–Њ–≥–љ–Њ–Ј –і–Њ–≤–Њ–ї—М–љ–Њ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є.
–Ґ–Є–њ 2. –°–њ–∞–є–Ї–Є –≤—Л—П–≤–ї—П—О—В—Б—П –≤ –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є. –≠—В–∞ –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–∞—П —Д–Њ—А–Љ–∞ –Т–Ь–° –Є–Љ–µ–µ—В 3 —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є: —Ж–µ–љ—В—А–∞–ї—М–љ—Л–µ –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л–µ —Б–Є–љ–µ—Е–Є–Є –±–µ–Ј —Б—Г–ґ–µ–љ–Є—П –њ–Њ–ї–Њ—Б—В–Є, —З–∞—Б—В–Є—З–љ–∞—П –Њ–±–ї–Є—В–µ—А–∞—Ж–Є—П —Б —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –Є –њ–Њ–ї–љ–∞—П –Њ–±–ї–Є—В–µ—А–∞—Ж–Є—П –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є. –Я—А–Њ–≥–љ–Њ–Ј –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –љ–∞–њ—А—П–Љ—Г—О –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б—В–µ–њ–µ–љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б —Ж–µ–љ—В—А–∞–ї—М–љ—Л–Љ–Є –Т–Ь–° –Є —Б–Њ—Е—А–∞–љ–µ–љ–љ—Л–Љ–Є –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ —Н–љ–і–Њ–Љ–µ—В—А–Є–µ–Љ –Є –њ–Њ–ї–Њ—Б—В—М—О –Љ–∞—В–Ї–Є –њ—А–Њ–≥–љ–Њ–Ј –ї–µ—З–µ–љ–Є—П –і–Њ–≤–Њ–ї—М–љ–Њ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є. –Я—А–Њ–≥–љ–Њ–Ј –ї–µ—З–µ–љ–Є—П –Ј–∞—З–∞—Б—В—Г—О –љ–µ—Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–є —Г –±–Њ–ї—М–љ—Л—Е —Б —З–∞—Б—В–Є—З–љ–Њ–є –Є–ї–Є –њ–Њ–ї–љ–Њ–є –∞—В—А–µ–Ј–Є–µ–є –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є.
–Ґ–Є–њ 3. –°–њ–∞–є–Ї–Є –Љ–Њ–≥—Г—В –≤—Л—П–≤–ї—П—В—М—Б—П –Ї–∞–Ї –≤ –Ї–∞–љ–∞–ї–µ —И–µ–є–Ї–Є, —В–∞–Ї –Є –≤ –њ–Њ–ї–Њ—Б—В–Є —В–µ–ї–∞ –Љ–∞—В–Ї–Є.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Т–Ь–°
–У–Є—Б—В–µ—А–Њ—Б–∞–ї—М–њ–Є–љ–≥–Њ–≥—А–∞—Д–Є—П (–У–°–У) –і–Њ –Є–Ј–Њ–±—А–µ—В–µ–љ–Є—П –≥–Є—Б—В–µ—А–Њ—Б–Ї–Њ–њ–∞ –±—Л–ї–∞ –Є –і–Њ —Б–Є—Е –њ–Њ—А –і–ї—П –Љ–љ–Њ–≥–Є—Е –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Њ–≤ –Њ—Б—В–∞–µ—В—Б—П –Љ–µ—В–Њ–і–Њ–Љ –≤—Л–±–Њ—А–∞. –У–°–У —Б–њ–Њ—Б–Њ–±–љ–∞ –Њ—Ж–µ–љ–Є—В—М —Д–Њ—А–Љ—Г –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є –Є —Б–Њ—Б—В–Њ—П–љ–Є–µ –Љ–∞—В–Њ—З–љ—Л—Е —В—А—Г–±. Wamsteker –Ъ. –Њ–њ–Є—Б–∞–ї –У–°–У-–Ї–∞—А—В–Є–љ—Г –њ—А–Є –Т–Ь–° –Ї–∞–Ї –і–µ—Д–µ–Ї—В—Л –љ–∞–њ–Њ–ї–љ–µ–љ–Є—П —Б —А–µ–Ј–Ї–Њ –Њ—З–µ—А—З–µ–љ–љ—Л–Љ–Є –≥—А–∞–љ–Є—Ж–∞–Љ–Є, —Б —Ж–µ–љ—В—А–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л–Љ –Є/–Є–ї–Є –њ—А–Є—Б—В–µ–љ–Њ—З–љ—Л–Љ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ–Љ [7].–£–Ч–Ш –≤–≤–Є–і—Г –љ–µ–Є–љ–≤–∞–Ј–Є–≤–љ–Њ—Б—В–Є —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –Ї–∞–Ї —Б –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–є, —В–∞–Ї –Є, –Є–љ—В—А–∞–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ, —Б –≤—Б–њ–Њ–Љ–Њ–≥–∞—В–µ–ї—М–љ–Њ–є —Ж–µ–ї—М—О.
–°–Њ–љ–Њ–≥–Є—Б—В–µ—А–Њ–≥—А–∞—Д–Є—П —Б–Њ—З–µ—В–∞–µ—В –≤ —Б–µ–±–µ –£–Ч–Ш —Б –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л–Љ –≤–≤–µ–і–µ–љ–Є–µ–Љ –Є–Ј–Њ—В–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–ї–µ–≤–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞. –Я—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є –Њ–і–љ–Њ–є –Є–ї–Є –±–Њ–ї–µ–µ —Н—Е–Њ–≥–µ–љ–љ—Л—Е –Њ–±–ї–∞—Б—В–µ–є –Љ–µ–ґ–і—Г –њ–µ—А–µ–і–љ–µ–є –Є –Ј–∞–і–љ–µ–є —Б—В–µ–љ–Ї–∞–Љ–Є –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є –Љ–Њ–ґ–љ–Њ –Ј–∞–њ–Њ–і–Њ–Ј—А–Є—В—М –Т–Ь–°.
–Ю—Б–љ–Њ–≤–љ—Л–Љ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ–Љ –Ь–†–Ґ —П–≤–ї—П—О—В—Б—П –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є—П –≤ –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ—Л—Е —Б–њ–∞–µ–Ї –Є –Њ—Ж–µ–љ–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П —Н–љ–і–Њ–Љ–µ—В—А–Є—П, —З—В–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–ї—П —А–µ—И–µ–љ–Є—П –≤–Њ–њ—А–Њ—Б–∞ –Њ –і–∞–ї—М–љ–µ–є—И–µ–є —В–∞–Ї—В–Є–Ї–µ –≤–µ–і–µ–љ–Є—П –±–Њ–ї—М–љ–Њ–є. –Ь–†–Ґ –Є–≥—А–∞–µ—В –≤—Б–њ–Њ–Љ–Њ–≥–∞—В–µ–ї—М–љ—Г—О —А–Њ–ї—М –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –њ–Њ–ї–љ–Њ–є –Њ–±–ї–Є—В–µ—А–∞—Ж–Є–Є –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є, –Ї–Њ–≥–і–∞ –≥–Є—Б—В–µ—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–∞—П –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є—П –љ–µ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є.
–С–ї–∞–≥–Њ–і–∞—А—П –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–є –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є –њ—А–Є –У–° –Љ–Њ–ґ–љ–Њ –±–Њ–ї–µ–µ —В–Њ—З–љ–Њ –њ–Њ–і—В–≤–µ—А–і–Є—В—М –љ–∞–ї–Є—З–Є–µ –Є –Њ—Ж–µ–љ–Є—В—М —Б—В–µ–њ–µ–љ—М —Б–њ–∞–µ—З–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є. Al-Inany –Э. –Њ–њ–Є—Б–∞–ї —А–∞–Ј–ї–Є—З–љ—Л–µ –≤–Є–і—Л –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л—Е —Б–њ–∞–µ–Ї, –Ї–Њ—В–Њ—А—Л–µ –≤–Є–Ј—Г–∞–ї–Є–Ј–Є—А—Г—О—В—Б—П –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –≥–Є—Б—В–µ—А–Њ—Б–Ї–Њ–њ–∞: 1) —Ж–µ–љ—В—А–∞–ї—М–љ—Л–µ —Б–њ–∞–є–Ї–Є –≤—Л–≥–ї—П–і—П—В –≤ –≤–Є–і–µ –Ї–Њ–ї–Њ–љ–Њ–Ї —Б —А–∞—Б—И–Є—А–µ–љ–љ—Л–Љ–Є –Ї–Њ–љ—Ж–∞–Љ–Є –Є —Б–≤—П–Ј—Л–≤–∞—О—В –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ—Л–µ —Б—В–µ–љ–Ї–Є –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є; 2) –њ—А–Є—Б—В–µ–љ–Њ—З–љ—Л–µ —Б–њ–∞–є–Ї–Є –≤—Л–≥–ї—П–і—П—В –Ї–∞–Ї –њ–Њ–ї—Г–Љ–µ—Б—П—Ж –Є –Ј–∞–љ–∞–≤–µ—Б, —Б–Ї—А—Л–≤–∞—П –і–љ–Њ –Є–ї–Є –±–Њ–Ї–Њ–≤—Л–µ —Б—В–µ–љ–Ї–Є, –Њ–љ–Є –Љ–Њ–≥—Г—В –њ—А–Є–і–∞—В—М –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є –∞—Б–Є–Љ–Љ–µ—В—А–Є—З–љ—Г—О —Д–Њ—А–Љ—Г; 3) –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–µ —Б–њ–∞–є–Ї–Є, –Ї–Њ—В–Њ—А—Л–µ –і–µ–ї—П—В –њ–Њ–ї–Њ—Б—В—М –Љ–∞—В–Ї–Є –љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –±–Њ–ї–µ–µ –Љ–µ–ї–Ї–Є—Е –њ–Њ–ї–Њ—Б—В–µ–є [8].
–Э–Є –≤ –Њ–і–љ–Њ–є –Є–Ј –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–є –Т–Ь–° –љ–µ —Г—З–Є—В—Л–≤–∞—О—В—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П, –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є. –Ш–Ј –≤—Б–µ—Е –Є–Ј–≤–µ—Б—В–љ—Л—Е –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–є –љ–∞ –і–∞–љ–љ—Л–є –Љ–Њ–Љ–µ–љ—В —Б–∞–Љ–Њ–є –Њ–±—К–µ–Ї—В–Є–≤–љ–Њ–є —Б—З–Є—В–∞–µ—В—Б—П –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ —Д–µ—А—В–Є–ї—М–љ–Њ—Б—В–Є (AFS) 1988 –≥., —Е–Њ—В—П –Њ–љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б–ї–Њ–ґ–љ–∞ –Є –≥—А–Њ–Љ–Њ–Ј–і–Ї–∞ (—В–∞–±–ї. 1) [9].
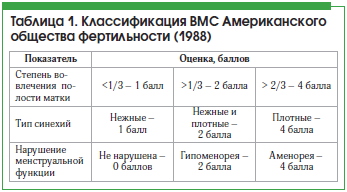
–Я–Њ –і–∞–љ–љ–Њ–є –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є —Б—В–∞–і–Є—П –Т–Ь–° –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —Б—Г–Љ–Љ–Њ–є –±–∞–ї–ї–Њ–≤:
1) —Б—В–∞–і–Є—П I вАУ 1вАУ4 –±–∞–ї–ї–∞;
2) —Б—В–∞–і–Є—П II вАУ 5вАУ8 –±–∞–ї–ї–Њ–≤;
3) —Б—В–∞–і–Є—П III вАУ 9вАУ12 –±–∞–ї–ї–Њ–≤.
–Ы–µ—З–µ–љ–Є–µ
–Ы–µ—З–µ–љ–Є–µ —Б–Є–љ–і—А–Њ–Љ–∞ –Р—И–µ—А–Љ–∞–љ–∞ –љ–∞–њ—А–∞–≤–ї–µ–љ–Њ –љ–∞ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —А–∞–Ј–Љ–µ—А–Њ–≤ –Є —Д–Њ—А–Љ—Л –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є, –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–є –Є —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є, –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї—Г —А–µ—Ж–Є–і–Є–≤–∞ —Б–њ–∞–µ–Ї. –Э–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ —Б—В–Њ–ї–µ—В–Є—П –±—Л–ї–Є –Њ–њ–Є—Б–∞–љ—Л —А–∞–Ј–ї–Є—З–љ—Л–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П.1. –Т—Л–ґ–Є–і–∞—В–µ–ї—М–љ–∞—П —В–∞–Ї—В–Є–Ї–∞. Schenker –Є Margalioth –љ–∞–±–ї—О–і–∞–ї–Є 23 –ґ–µ–љ—Й–Є–љ—Л —Б –∞–Љ–µ–љ–Њ—А–µ–µ–є, –Ї–Њ—В–Њ—А—Л–µ –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, —Г 18 –Є–Ј –љ–Є—Е –≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є–ї—Б—П —А–µ–≥—Г–ї—П—А–љ—Л–є –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ—Л–є —Ж–Є–Ї–ї –≤ –њ–µ—А–Є–Њ–і –Њ—В 1 –≥–Њ–і–∞ –і–Њ 7 –ї–µ—В [6].
2. –°–ї–µ–њ–Њ–µ —А–∞—Б—И–Є—А–µ–љ–Є–µ –Є –Ї—О—А–µ—В–∞–ґ. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Н—В–Њ—В –Љ–µ—В–Њ–і —З—А–µ–≤–∞—В –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є –Љ–∞–ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–µ–љ.
3. –У–Є—Б—В–µ—А–Њ—В–Њ–Љ–Є—П. –Т–њ–µ—А–≤—Л–µ –≥–Є—Б—В–µ—А–Њ—В–Њ–Љ–Є—О –і–ї—П —А–∞–Ј–і–µ–ї–µ–љ–Є—П –Т–Ь–° –њ—А–µ–і–ї–Њ–ґ–Є–ї –Ф. –Р—И–µ—А–Љ–∞–љ. –Я—А–Є –∞–љ–∞–ї–Є–Ј–µ 31 —Б–ї—Г—З–∞—П –≥–Є—Б—В–µ—А–Њ—В–Њ–Љ–Є–Є –Ј–∞–±–µ—А–µ–Љ–µ–љ–µ–ї–Є 16 –ґ–µ–љ—Й–Є–љ (52%), 8 (25,8%) –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –±–ї–∞–≥–Њ–њ–Њ–ї—Г—З–љ–Њ —А–Њ–і–Њ—А–∞–Ј—А–µ—И–µ–љ—Л. –Ю–і–љ–∞–Ї–Њ —Н—В–Њ—В –Љ–µ—В–Њ–і –ї–µ—З–µ–љ–Є—П —Б–ї–µ–і—Г–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М —В–Њ–ї—М–Ї–Њ –≤ —Б–∞–Љ—Л—Е —Н–Ї—Б—В—А–µ–Љ–∞–ї—М–љ—Л—Е —Б–Є—В—Г–∞—Ж–Є—П—Е.
4. –У–Є—Б—В–µ—А–Њ—Б–Ї–Њ–њ–Є—П (–У–°) –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —П–≤–ї—П–µ—В—Б—П –Љ–µ—В–Њ–і–Њ–Љ –≤—Л–±–Њ—А–∞ –њ—А–Є —Б–Є–љ–і—А–Њ–Љ–µ –Р—И–µ—А–Љ–∞–љa –±–ї–∞–≥–Њ–і–∞—А—П –Љ–∞–ї–Њ–є –Є–љ–≤–∞–Ј–Є–≤–љ–Њ—Б—В–Є –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –њ—А–Є —А–µ—Ж–Є–і–Є–≤–µ. –Я—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –љ–Њ–ґ–љ–Є—Ж –Є–ї–Є —Й–Є–њ—Ж–Њ–≤ –і–ї—П —А–∞–Ј—А—Г—И–µ–љ–Є—П —Б–Є–љ–µ—Е–Є–є —Б—Г—Й–µ—Б—В–≤—Г–µ—В –Љ–µ–љ—М—И–Є–є —А–Є—Б–Ї –њ–µ—А—Д–Њ—А–∞—Ж–Є–Є –Љ–∞—В–Ї–Є –Є —А–∞–Ј—А—Г—И–µ–љ–Є—П –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Б–ї–Њ—П —Н–љ–і–Њ–Љ–µ—В—А–Є—П –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –≤–Є–і–Њ–≤ —Н–љ–µ—А–≥–Є–Є. –Ю–і–љ–∞–Ї–Њ –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ–∞—П —Е–Є—А—Г—А–≥–Є—П —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Н–љ–µ—А–≥–Є–Є –Љ–Њ–ґ–µ—В —Б–Њ–Ј–і–∞—В—М —Г—Б–ї–Њ–≤–Є—П –і–ї—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –Є —В–Њ—З–љ–Њ–є —А–µ–Ј–Ї–Є, –∞ —В–∞–Ї–ґ–µ –≥–∞—А–∞–љ—В–Є—А–Њ–≤–∞—В—М –≥–µ–Љ–Њ—Б—В–∞–Ј, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—П –Њ–њ—В–Є—З–µ—Б–Ї—Г—О –њ—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М –Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ–Њ–ї—П.
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Б–Є–љ–і—А–Њ–Љ–∞ –Р—И–µ—А–Љ–∞–љ–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —Г–ї—Г—З—И–µ–љ–∞, –µ—Б–ї–Є –У–° —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –Њ–і–љ–Є–Љ –Є–Ј –Љ–µ—В–Њ–і–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—П: —А–µ–љ—В–≥–µ–љ–Њ—Б–Ї–Њ–њ–Є–µ–є, –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є–µ–є, —В—А–∞–љ—Б–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ—Л–Љ –£–Ч–Ш. –Э–µ–і–Њ—Б—В–∞—В–Њ–Ї —А–µ–љ—В–≥–µ–љ–Њ—Б–Ї–Њ–њ–Є–Є –Ј–∞–Ї–ї—О—З–∞–µ—В—Б—П –≤ –ї—Г—З–µ–≤–Њ–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–Є. –Ы–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є—П —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –і–ї—П –Ї–Њ–љ—В—А–Њ–ї—П –≥–Є—Б—В–µ—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–і–≥–µ–Ј–Є–Њ–ї–Є–Ј–Є—Б–∞ –Є –і–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Њ—Ж–µ–љ–Є—В—М —Б–Њ—Б—В–Њ—П–љ–Є–µ –Њ—А–≥–∞–љ–Њ–≤ –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞, –≤—Л–њ–Њ–ї–љ–Є—В—М —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –њ—А–Є —А–∞–Ј–ї–Є—З–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Ґ—А–∞–љ—Б–∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–µ –£–Ч–Ш –≤—Б–µ —З–∞—Й–µ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –њ—А–Є –≥–Є—Б—В–µ—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–Љ —А–∞–Ј–і–µ–ї–µ–љ–Є–Є –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л—Е —Б–њ–∞–µ–Ї –Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї –њ–µ—А—Д–Њ—А–∞—Ж–Є–Є –Љ–∞—В–Ї–Є.
–Ю —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–Љ —Г—Б–њ–µ—Е–µ –Љ–Њ–ґ–љ–Њ —Б—Г–і–Є—В—М –њ–Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –∞–љ–∞—В–Њ–Љ–Є–Є –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є, –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О –Љ–µ–љ—Б—В—А—Г–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є, –љ–∞—Б—В—Г–њ–ї–µ–љ–Є—О –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –Є –ґ–Є–≤–Њ—А–Њ–ґ–і–∞–µ–Љ–Њ—Б—В–Є. –Ю—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є –њ–Њ—Б–ї–µ –њ–µ—А–≤–Њ–є –њ—А–Њ—Ж–µ–і—Г—А—Л —Б–Њ—Б—В–∞–≤–ї—П–µ—В 57,8вАУ97,5% [10]. –Ю–і–љ–∞–Ї–Њ —А–µ–њ—А–Њ–і—Г–Ї—В–Є–≤–љ—Л–є –Є—Б—Е–Њ–і –Ј–∞–≤–Є—Б–Є—В –љ–µ —В–Њ–ї—М–Ї–Њ –Њ—В —Б–Њ—Б—В–Њ—П–љ–Є—П –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є, –љ–Њ –Є –Њ—В —Б–Њ—Б—В–Њ—П–љ–Є—П —Н–љ–і–Њ–Љ–µ—В—А–Є—П.
–Я–Њ –і–∞–љ–љ—Л–Љ –ї–Є—В–µ—А–∞—В—Г—А—Л, —З–∞—Б—В–Њ—В–∞ –љ–∞—Б—В—Г–њ–ї–µ–љ–Є—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –њ–Њ—Б–ї–µ –≥–Є—Б—В–µ—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–Є–Ј–Є—Б–∞ –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л—Е —Б–њ–∞–µ–Ї —Г –ґ–µ–љ—Й–Є–љ —Б–Њ—Б—В–∞–≤–Є–ї–∞ –Њ–Ї–Њ–ї–Њ 74% (468 –Є–Ј 632), —З—В–Њ –љ–∞–Љ–љ–Њ–≥–Њ –≤—Л—И–µ, —З–µ–Љ —Г –љ–µ–Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ [11]. –†–µ—Ж–Є–і–Є–≤ –Т–Ь–° вАУ –Њ—Б–љ–Њ–≤–љ–Њ–є —Д–∞–Ї—В–Њ—А –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Њ–њ–µ—А–∞—Ж–Є–Є –Є –љ–∞–њ—А—П–Љ—Г—О —Б–≤—П–Ј–∞–љ —Б —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М—О —Б–њ–∞–µ–Ї. –Ю—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ —З–∞—Б—В–Њ—В–∞ —А–µ—Ж–Є–і–Є–≤–Њ–≤ –≤ –і–Є–∞–њ–∞–Ј–Њ–љ–µ 3,1вАУ28,7% —Е–∞—А–∞–Ї—В–µ—А–љ–∞ –і–ї—П –≤—Б–µ—Е —Б–ї—Г—З–∞–µ–≤ —Б–њ–∞–µ–Ї –Є 20вАУ62,5% вАУ –і–ї—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е —Б–њ–∞–µ–Ї [12].
–Ґ–∞–Ї –Ї–∞–Ї —А–µ—Ж–Є–і–Є–≤ –Т–Ь–° –љ–∞—Б—В—Г–њ–∞–µ—В –≤ —А–∞–љ–љ–µ–Љ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ, –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –Є–Љ–µ–µ—В –≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є.
–Я—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ —А–µ—Ж–Є–і–Є–≤–∞ –Т–Ь–°
–Т–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–Ј–∞—З–∞—В–Њ—З–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–µ—В–Њ–і–∞ –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —А–µ—Ж–Є–і–Є–≤–∞ –Т–Ь–°. –Т –Њ–±–Ј–Њ—А–µ –ї–Є—В–µ—А–∞—В—Г—А—Л March C.M. –Ј–∞–Ї–ї—О—З–Є–ї, —З—В–Њ –Ґ-–Њ–±—А–∞–Ј–љ—Л–µ –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л–µ —Б–њ–Є—А–∞–ї–Є –Є–Љ–µ—О—В —Б–ї–Є—И–Ї–Њ–Љ –Љ–∞–ї—Г—О –њ–ї–Њ—Й–∞–і—М –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є, —З—В–Њ–±—Л –њ—А–µ–і–Њ—В–≤—А–∞—В–Є—В—М –њ—А–Є–ї–Є–њ–∞–љ–Є–µ —Б—В–µ–љ–Њ–Ї –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є [13]. –Т –ї–Є—В–µ—А–∞—В—Г—А–µ –µ—Б—В—М –і–∞–љ–љ—Л–µ –Њ–± –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Ї–∞—В–µ—В–µ—А–∞ Foley, –≤–≤–µ–і–µ–љ–љ–Њ–≥–Њ –≤ –њ–Њ–ї–Њ—Б—В—М –Љ–∞—В–Ї–Є –љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –і–љ–µ–є –њ–Њ—Б–ї–µ –ї–Є–Ј–Є—Б–∞ —Б–њ–∞–µ–Ї –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П —А–µ—Ж–Є–і–Є–≤–∞. –Т –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Amer M.I. et al. –Њ—Ж–µ–љ–Є–ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—В–Њ–≥–Њ –Љ–µ—В–Њ–і–∞, –Њ—Б—В–∞–≤–Є–≤ –≤ –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є –Ї–∞—В–µ—В–µ—А Foley –љ–∞ –Њ–і–љ—Г –љ–µ–і–µ–ї—О –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є —Г 32 –±–Њ–ї—М–љ—Л—Е. –Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–∞—П –У–° –≤—Л–њ–Њ–ї–љ–µ–љ–∞ –љ–∞ —Б—А–Њ–Ї–µ –Њ—В 6 –і–Њ 8 –љ–µ–і. –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є. –Т–Ь–° –±—Л–ї–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ—Л —Г 7 –њ–∞—Ж–Є–µ–љ—В–Њ–Ї –≤ –≥—А—Г–њ–њ–µ —Б –±–∞–ї–ї–Њ–љ–Њ–Љ (7 –Є–Ј 32; 21,9%) –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б 9 –њ–∞—Ж–Є–µ–љ—В–Ї–∞–Љ–Є –≤ –≥—А—Г–њ–њ–µ –±–µ–Ј –±–∞–ї–ї–Њ–љ–∞ (9 –Є–Ј 18; 50%) [14]. –Ю–і–љ–∞–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –±–∞–ї–ї–Њ–љ–∞ —Б–Њ–Ј–і–∞–µ—В ¬Ђ–Њ—В–Ї—А—Л—В—Л–µ –≤–Њ—А–Њ—В–∞¬ї –≤ –њ–Њ–ї–Њ—Б—В—М –Љ–∞—В–Ї–Є –і–ї—П –Є–љ—Д–µ–Ї—Ж–Є–Є –Є–Ј –≤–ї–∞–≥–∞–ї–Є—Й–∞. –С–Њ–ї—М—И–Њ–≥–Њ —А–∞–Ј–Љ–µ—А–∞ –±–∞–ї–ї–Њ–љ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ, –Ї–Њ—В–Њ—А–Њ–µ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї —Б–љ–Є–ґ–µ–љ–Є—О –њ—А–Є—В–Њ–Ї–∞ –Ї—А–Њ–≤–Є –Ї —Б—В–µ–љ–Ї–∞–Љ –Љ–∞—В–Ї–Є –Є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–Љ—Г –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О –љ–∞ —А–µ–≥–µ–љ–µ—А–∞—Ж–Є—О —Н–љ–і–Њ–Љ–µ—В—А–Є—П. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Н—В–Њ—В –Љ–µ—В–Њ–і –Љ–Њ–ґ–µ—В —Б–Њ–Ј–і–∞—В—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Ї–Є.J. Wood –Є G. Pena –њ—А–µ–і–ї–Њ–ґ–Є–ї–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н—Б—В—А–Њ–≥–µ–љ–Њ–≤ –і–ї—П —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є —А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є —Н–љ–і–Њ–Љ–µ—В—А–Є—П –љ–∞ —В—А–∞–≤–Љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—П—Е [15]. –Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 60 –ґ–µ–љ—Й–Є–љ–∞–Љ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –≤—Л—Б–Ї–∞–±–ї–Є–≤–∞–љ–Є–µ –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ I —В—А–Є–Љ–µ—Б—В—А–∞ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –Є –њ—А–Њ–≤–µ–і–µ–љ–∞ —Н—Б—В—А–Њ–≥–µ–љ-–њ—А–Њ–≥–µ—Б—В–Є–љ–Њ–≤–∞—П —В–µ—А–∞–њ–Є—П –њ–Њ—Б–ї–µ –∞–і–≥–µ–Ј–Є–Њ–ї–Є–Ј–Є—Б–∞. –£ —Н—В–Њ–є –≥—А—Г–њ–њ—Л –±–Њ–ї—М–љ—Л—Е —В–Њ–ї—Й–Є–љ–∞ (0,84 —Б–Љ –њ—А–Њ—В–Є–≤ 0,67 —Б–Љ; P1/4.02) –Є –Њ–±—К–µ–Љ —Н–љ–і–Њ–Љ–µ—В—А–Є—П (3,85 —Б–Љ2 –њ—А–Њ—В–Є–≤ 1,97 —Б–Љ2) –±—Л–ї–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ –±–Њ–ї—М—И–µ, —З–µ–Љ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ. –≠—В–Є –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М–љ–∞—П –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —В–Њ–ї—Й–Є–љ—Г –Є –Њ–±—К–µ–Љ —Н–љ–і–Њ–Љ–µ—В—А–Є—П, —Б—В–Є–Љ—Г–ї–Є—А—Г—П –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –Є —Ж–Є–Ї–ї–Є—З–µ—Б–Ї—Г—О —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є—О.
–Т —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –Ъ–Њ—А–Њ–ї–µ–≤—Б–Ї–Њ–≥–Њ –Ї–Њ–ї–ї–µ–і–ґ–∞ –∞–Ї—Г—И–µ—А—Б—В–≤–∞ –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л—Е –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —Б–њ–∞–µ—З–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ [16], –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –ї—О–±–Њ–µ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–Њ –љ–∞ –Њ—А–≥–∞–љ–∞—Е –ґ–Є–≤–Њ—В–∞ –Є –Љ–∞–ї–Њ–≥–Њ —В–∞–Ј–∞ –≤–µ–і–µ—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О —Б–њ–∞–µ–Ї –Є —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –љ–Є–Љ–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤ –Њ—В–і–∞–ї–µ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ. –Т–Њ –Є–Ј–±–µ–ґ–∞–љ–Є–µ —В–∞–Ї–Є—Е —А–Є—Б–Ї–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–Њ—В–Є–≤–Њ—Б–њ–∞–µ—З–љ—Л—Е –±–∞—А—М–µ—А–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Э–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є –њ—А–Њ—В–Є–≤–Њ—Б–њ–∞–µ—З–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є –≤ –∞–Ї—Г—И–µ—А—Б—В–≤–µ –Є –≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Є–Є –њ—А–Є–Ј–љ–∞–љ—Л –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ –≥–Є–∞–ї—Г—А–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (–У–Ъ). –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–∞—П –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є—П –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є—Е —Е–Є—А—Г—А–≥–Њ–≤-–≥–Є–љ–µ–Ї–Њ–ї–Њ–≥–Њ–≤ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В –њ—А–Є–Љ–µ–љ—П—В—М –±–∞—А—М–µ—А–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ—Б–њ–∞–µ—З–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ (–≥–µ–ї–Є), –≤ —Б–Њ—Б—В–∞–≤ –Ї–Њ—В–Њ—А—Л—Е –≤—Е–Њ–і–Є—В –У–Ъ, –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –ї—О–±—Л—Е –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤, —В. –Ї. –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Н—В–Є —Б—А–µ–і—Б—В–≤–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞—О—В —А–Є—Б–Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —Б–њ–∞–µ—З–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є [17].
–Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≥–µ–ї–µ–≤—Л—Е —Д–Њ—А–Љ –њ—А–Њ—В–Є–≤–Њ—Б–њ–∞–µ—З–љ—Л—Е —Б—А–µ–і—Б—В–≤ —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ—Л–Љ –њ—А–Є –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≥–µ–ї—М —А–∞–≤–љ–Њ–Љ–µ—А–љ–Њ —А–∞—Б–њ—А–µ–і–µ–ї—П–µ—В—Б—П –њ–Њ –≤—Б–µ–є —Б—Д–µ—А–µ, –Ј–∞–њ–Њ–ї–љ—П—П –Ї–Њ–љ–≥—А—Г—Н–љ—В–љ—Л–µ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Є —В—А—Г–і–љ–Њ–і–Њ—Б—В—Г–њ–љ—Л–µ –Њ–±–ї–∞—Б—В–Є –≤ –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є. –У–µ–ї–Є –њ—А–Њ—Б—В—Л –≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є, –Њ–±—А–∞–Ј—Г—О—В –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Њ—А–≥–∞–љ–∞ —В–Њ–љ–Ї—Г—О –њ–ї–µ–љ–Ї—Г, –Ї–Њ—В–Њ—А–∞—П –≤—Л–њ–Њ–ї–љ—П–µ—В —Д—Г–љ–Ї—Ж–Є—О –њ—А–Њ—В–Є–≤–Њ—Б–њ–∞–µ—З–љ–Њ–≥–Њ –±–∞—А—М–µ—А–∞ –љ–∞ –≤—А–µ–Љ—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–≥–Њ –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П —В–Ї–∞–љ–µ–є. –Я–Њ—Н—В–Њ–Љ—Г –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–µ—Ж–Є–і–Є–≤–∞ –њ–Њ—Б–ї–µ –∞–і–≥–µ–Ј–Є–Њ–ї–Є–Ј–Є—Б–∞ –≤ –њ–Њ–ї–Њ—Б—В—М –Љ–∞—В–Ї–Є –≤–≤–Њ–і—П—В—Б—П –≥–µ–ї–µ–Њ–±—А–∞–Ј–љ—Л–µ –љ–∞–њ–Њ–ї–љ–Є—В–µ–ї–Є, –њ—А–µ–њ—П—В—Б—В–≤—Г—О—Й–Є–µ –Ї–Њ–љ—В–∞–Ї—В—Г –µ–µ —Б—В–µ–љ–Њ–Ї, —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Т–Ь–°. –Э–∞–Є–±–Њ–ї—М—И–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –њ–Њ–ї—Г—З–Є–ї–Є –±–∞—А—М–µ—А—Л –Є–Ј –±–Є–Њ—А–∞–Ј–ї–∞–≥–∞–µ–Љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї–љ–Њ—Б—В—М—О –≤—Л–≤–Њ–і—П—В—Б—П –Є–Ј –Њ—А–≥–∞–љ–Є–Ј–Љ–∞.
–Ю—Б–љ–Њ–≤–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ —В–∞–Ї–Є—Е –±–∞—А—М–µ—А–Њ–≤ —Б–ї—Г–ґ–Є—В –У–Ъ (–њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –і–Є—Б–∞—Е–∞—А–Є–і–љ—Г—О –Љ–Њ–ї–µ–Ї—Г–ї—Г), –Њ–љ–∞ –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Ї–∞–Ї –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –≤–љ–µ–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Љ–∞—В—А–Є–Ї—Б–∞. –У–Ъ –±—Л–ї–∞ –њ—А–µ–і–ї–Њ–ґ–µ–љ–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ –±–∞—А—М–µ—А–љ–Њ–≥–Њ –∞–≥–µ–љ—В–∞ –і–ї—П –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П –∞–і–≥–µ–Ј–Є–Є –Є –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–∞ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ –і–ї—П –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞. –Ь–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –У–Ъ —А–µ–∞–ї–Є–Ј—Г–µ—В—Б—П –љ–∞ –Њ—З–µ–љ—М —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–Є –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П —В–Ї–∞–љ–µ–є (–њ–µ—А–≤—Л–µ 3вАУ4 –і–љ—П) –њ—Г—В–µ–Љ –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –∞–і–≥–µ–Ј–Є–Є —Д–Є–±—А–Њ–±–ї–∞—Б—В–Њ–≤ –Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤, –∞ —В–∞–Ї–ґ–µ –њ—Г—В–µ–Љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —Д–Є–±—А–Є–љ–∞ –Є —Б–Њ–Ј–і–∞–љ–Є—П –Ј–∞—Й–Є—В–љ–Њ–≥–Њ –±–∞—А—М–µ—А–∞ –љ–∞ –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ–Њ–Љ —Г—З–∞—Б—В–Ї–µ —В–Ї–∞–љ–Є. –Я–µ—А–Є–Њ–і –њ–Њ–ї—Г—А–∞—Б–њ–∞–і–∞ –У–Ъ вАУ –Њ–Ї–Њ–ї–Њ 1вАУ3-—Е –і–љ–µ–є. –Я–Њ–ї–љ–Њ—Б—В—М—О —А–∞—Б—Й–µ–њ–ї—П–µ—В—Б—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –≤ —В–µ—З–µ–љ–Є–µ 4-—Е —Б—Г—В–Њ–Ї —Б –њ–Њ–Љ–Њ—Й—М—О —Д–µ—А–Љ–µ–љ—В–∞ –≥–Є–∞–ї—Г—А–Њ–љ–Є–і–∞–Ј—Л.
–Ф—А—Г–≥–Њ–є –∞–љ—В–Є–∞–і–≥–µ–Ј–Є–≤–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –њ–Њ–і –љ–∞–Ј–≤–∞–љ–Є–µ–Љ –Ї–∞—А–±–Њ–Ї—Б–Є–Љ–µ—В–Є–ї—Ж–µ–ї–ї—О–ї–Њ–Ј–∞ (–Ъ–Ь–¶) –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В —Б–Њ–±–Њ–є –≤—Л—Б–Њ–Ї–Њ–Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–є –њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і, –Ї–Њ—В–Њ—А—Л–є —В–∞–Ї–ґ–µ —Б–ї—Г–ґ–Є—В —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –њ—А–Њ—В–Є–≤–Њ—Б–њ–∞–µ—З–љ—Л–Љ —Б—А–µ–і—Б—В–≤–Њ–Љ. –Ъ–Ь–¶ –љ–µ—В–Њ–Ї—Б–Є—З–љ–∞, –љ–µ–Ї–∞–љ—Ж–µ—А–Њ–≥–µ–љ–љ–∞. –Т –њ–Є—Й–µ–≤–Њ–є –њ—А–Њ–Љ—Л—И–ї–µ–љ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –Ї–∞–Ї –Ј–∞–≥—Г—Б—В–Є—В–µ–ї—М, –љ–∞–њ–Њ–ї–љ–Є—В–µ–ї—М –Є –њ–Є—Й–µ–≤–∞—П –і–Њ–±–∞–≤–Ї–∞. –Т —Е–Є—А—Г—А–≥–Є–Є –Ъ–Ь–¶ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—Г–±—Б—В—А–∞—В–∞ –і–ї—П –Ј–∞–Ї—А–µ–њ–ї–µ–љ–Є—П –Є –њ—А–Њ–ї–Њ–љ–≥–Є—А–Њ–≤–∞–љ–Є—П –і–µ–є—Б—В–≤–Є—П –У–Ъ –љ–∞ –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є —В–Ї–∞–љ–Є. –Ф–µ–є—Б—В–≤—Г–µ—В –Ї–∞–Ї –Љ–µ—Е–∞–љ–Є—З–µ—Б–Ї–Є—Е –±–∞—А—М–µ—А.
–Ъ–Њ–Љ–±–Є–љ–∞—Ж–Є—П –≤—Л—Б–Њ–Ї–Њ–Њ—З–Є—Й–µ–љ–љ–Њ–є –љ–∞—В—А–Є–µ–≤–Њ–є —Б–Њ–ї–Є –У–Ъ —Б –Ъ–Ь–¶ –≤ –≤–Є–і–µ –≥–µ–ї—П (–Р–љ—В–Є–∞–і–≥–µ–Ј–Є–љ¬Ѓ (–У–µ–љ—М—О—Н–ї –Ъ–Њ., –Ы—В–і., –Ъ–Њ—А–µ—П)) –њ—А–µ–і–љ–∞–Ј–љ–∞—З–µ–љ–∞ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б–њ–∞–є–Ї–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –њ–Њ—Б–ї–µ –ї—О–±—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є –љ–∞ –Њ—А–≥–∞–љ–∞—Е –Є —В–Ї–∞–љ—П—Е, –≥–і–µ –Є–Љ–µ–µ—В—Б—П —А–Є—Б–Ї —Б–њ–∞–є–Ї–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П, –≤ —В. —З. –њ–Њ—Б–ї–µ –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є [18]. –°–Њ–≥–ї–∞—Б–љ–Њ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ—Г —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О J.W. Do et al., —А–∞–Ј–≤–Є—В–Є–µ –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ–Њ–≥–Њ —Б–њ–∞–µ—З–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ —З–µ—А–µ–Ј 4 –љ–µ–і. –њ–Њ—Б–ї–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –≤ 2 —А–∞–Ј–∞ —А–µ–ґ–µ –≤ –≥—А—Г–њ–њ–µ —Б –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Р–љ—В–Є–∞–і–≥–µ–Ј–Є–љ–∞, —З–µ–Љ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є: 13% –њ—А–Њ—В–Є–≤ 26% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [19]. –Я—А–Њ—В–Є–≤–Њ—Б–њ–∞–µ—З–љ—Л–є –≥–µ–ї—М –Њ–±–ї–∞–і–∞–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ–Є —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞–Љ–Є: —Г–і–Њ–±—Б—В–≤–Њ –Є –њ—А–Њ—Б—В–Њ—В–∞ –≤ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–Є –≤–љ—Г—В—А–Є–Љ–∞—В–Њ—З–љ–Њ–Љ, –Њ—В–Ї—А—Л—В–Њ–Љ –Є –ї–∞–њ–∞—А–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Њ–Љ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–µ, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Њ—В–Є–≤–Њ—Б–њ–∞–µ—З–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ (–і–Њ 7 –і–љ–µ–є), —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ї —А–∞—Б—Б–∞—Б—Л–≤–∞–љ–Є—О (–±–Є–Њ–і–µ–≥—А–∞–і–∞—Ж–Є–Є), –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М, –Є–Љ–Љ—Г–љ–Њ—Б–Њ–≤–Љ–µ—Б—В–Є–Љ–Њ—Б—В—М, –Є–љ–µ—А—В–љ–Њ—Б—В—М (–≥–µ–ї—М –љ–µ —П–≤–ї—П–µ—В—Б—П –Њ—З–∞–≥–Њ–Љ –Є–љ—Д–µ–Ї—Ж–Є–Є, —Д–Є–±—А–Њ–Ј–∞, –∞–љ–≥–Є–Њ–≥–µ–љ–µ–Ј–∞ –Є –њ—А.), –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –±–∞—А—М–µ—А–љ—Л–є (—А–∞–Ј–≥—А–∞–љ–Є—З–Є–≤–∞—О—Й–Є–є) —Н—Д—Д–µ–Ї—В. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≥–µ–ї—М –Р–љ—В–Є–∞–і–≥–µ–Ј–Є–љ¬Ѓ –Є–Љ–µ–µ—В –Њ–њ—В–Є–Љ–∞–ї–љ—Г—О —Б—В–µ–њ–µ–љ—М —В–µ–Ї—Г—З–µ—Б—В–Є –Є –≤—П–Ј–Ї–Њ—Б—В–Є, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –µ–Љ—Г –Њ–±–≤–Њ–ї–∞–Ї–Є–≤–∞—В—М –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –ї—О–±–Њ–є —Д–Њ—А–Љ—Л, —Б–Њ–Ј–і–∞–≤–∞—П –≥–µ–ї–µ–≤—Г—О –њ–ї–µ–љ–Ї—Г, —Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ—Г—О –Ї —А–∞–љ–µ–≤–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є, –∞ —В–∞–Ї–ґ–µ –љ–µ –≤–ї–Є—П–µ—В –љ–∞ –љ–Њ—А–Љ–∞–ї—М–љ–Њ –њ—А–Њ—В–µ–Ї–∞—О—Й–Є–µ –њ—А–Њ—Ж–µ—Б—Б—Л —А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є –Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –≤—Б–µ–Љ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ—Л–Љ —Б—В–∞–љ–і–∞—А—В–∞–Љ –Ї–∞—З–µ—Б—В–≤–∞.
–°–ї–µ–і—Г–µ—В –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –Т–Ь–° –≤—Б–µ–≥–і–∞ –њ–Њ–ї–µ–Ј–љ–µ–µ –Є –ї–µ–≥—З–µ, —З–µ–Љ –ї–µ—З–µ–љ–Є–µ. –° —Н—В–Њ–є —Ж–µ–ї—М—О –≤–∞–ґ–љ–Њ –Є–Ј–±–µ–≥–∞—В—М –ї—О–±—Л—Е —В—А–∞–≤–Љ –Љ–∞—В–Ї–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –Є –≤ –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤–Њ–Љ –њ–µ—А–Є–Њ–і–µ. –Я—А–Є –љ–∞–ї–Є—З–Є–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ–Њ–ї–Њ—Б—В–Є –Љ–∞—В–Ї–Є –≤ –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Є–ї–Є –њ–Њ—Б–ї–µ –∞–±–Њ—А—В–∞ –У–° —Б–ї–µ–і—Г–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –Ї–∞–Ї —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –Љ–µ—В–Њ–і –і–ї—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –Ї–Њ–љ—В—А–Њ–ї—П –ї–µ—З–µ–љ–Є—П, —В. –Ї. –Њ–љ–∞ –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–µ –Њ–±—Л—З–љ–Њ–≥–Њ –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–≥–Њ, —Б–ї–µ–њ–Њ–≥–Њ –≤—Л—Б–Ї–∞–±–ї–Є–≤–∞–љ–Є—П.












