–Ґ–∞–Ї–∞—П –≤—Л—Б–Њ–Ї–∞—П —А–µ–њ—Г—В–∞—Ж–Є—П –Ї–ї–∞—Б—Б–∞ –С–Р–†, –Њ—В–Љ–µ—З–µ–љ–љ–∞—П –≤ –Х–≤—А–Њ–њ–µ–є—Б–Ї–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –њ–Њ –Р–У 2007 –≥., –±—Л–ї–∞ «–Ј–∞—А–∞–±–Њ—В–∞–љ–∞» –≤ —Е–Њ–і–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Њ—Е–≤–∞—В—Л–≤–∞—О—Й–Є—Е —И–Є—А–Њ–Ї–Є–є —Б–њ–µ–Ї—В—А –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є, —Н–љ–і–Њ–Ї—А–Є–љ–љ—Л–Љ–Є, —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л–Љ–Є –Є –њ–Њ—З–µ—З–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є [4].
–Ю—Б–љ–Њ–≤–Њ–њ–Њ–ї–∞–≥–∞—О—Й–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–њ–Њ –Є–Ј—Г—З–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –С–Р–†
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ LIFE. –Я–µ—А–≤—Л–Љ –Є —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –≤–∞–ґ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ, –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—Й–Є–Љ –Њ–≥—А–Њ–Љ–љ—Л–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Ї–ї–∞—Б—Б–∞ c–∞—А—В–∞–љ–Њ–≤, —Б—В–∞–ї–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ LIFE [7]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є LIFE –њ—А–Є–љ—П–ї–Є —Г—З–∞—Б—В–Є–µ 9193 –њ–∞—Ж–Є–µ–љ—В–∞ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 55 –і–Њ 80 –ї–µ—В —Б –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Є–Љ –Р–Ф 95–115 –Љ–Љ —А—В. —Б—В. –Є/–Є–ї–Є —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Є–Љ –Р–Ф 160–200 –Љ–Љ —А—В. —Б—В. –њ–ї—О—Б —Б –љ–∞–ї–Є—З–Є–µ–Љ –≠–Ъ–У –Ї—А–Є—В–µ—А–Є–µ–≤ –У–Ы–Ц. –С–Њ–ї—М–љ—Л–µ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ—А–Є —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є –њ–Њ–ї—Г—З–∞–ї–Є –ї–Є–±–Њ –ї–Њ–Ј–∞—А—В–∞–љ 50 –Љ–≥, –ї–Є–±–Њ –∞—В–µ–љ–Њ–ї–Њ–ї 50 –Љ–≥ —Б –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ –і—А—Г–≥–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Р–Ф. –Т —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–≥–Њ 5––ї–µ—В–љ–µ–≥–Њ –љ–∞–±–ї—О–і–µ–љ–Є—П —Г –ї–Њ–Ј–∞—А—В–∞–љ––ї–µ—З–µ–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –∞—В–µ–љ–Њ–ї–Њ–ї–∞ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М 13%––љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є (–њ–µ—А–≤–Є—З–љ–∞—П –Ї–Њ–љ–µ—З–љ–∞—П —В–Њ—З–Ї–∞) –±–µ–Ј —А–∞–Ј–ї–Є—З–Є–є –≤ —А–Є—Б–Ї–µ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ (–Ш–Ь), –љ–Њ —Б 25% —А–∞–Ј–ї–Є—З–Є–µ–Љ –≤ —З–∞—Б—В–Њ—В–µ –Є–љ—Б—Г–ї—М—В–Њ–≤ (—А–Є—Б. 1). –≠—В–Є –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –љ–∞ —Д–Њ–љ–µ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є —А–µ–≥—А–µ—Б—Б–Є–Є –У–Ы–Ц –њ–Њ –і–∞–љ–љ—Л–Љ –≠–Ъ–У –≤ –≥—А—Г–њ–њ–µ, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–Њ–Ј–∞—А—В–∞–љ.
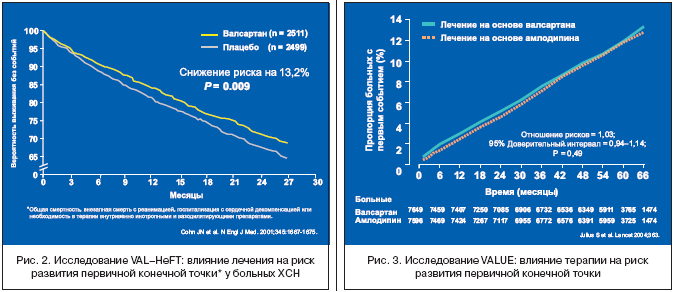
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ Val–HeFT. –Т–∞–ї—Б–∞—А—В–∞–љ —Б—В–∞–ї –њ–µ—А–≤—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Є–Ј –Ї–ї–∞—Б—Б–∞ –С–Р–†, –Ї–Њ—В–Њ—А—Л–є –±—Л–ї –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ –і–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О (–•–°–Э). –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Valsartan in Heart Failure Trial (Val–HeFT) –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 5010 –±–Њ–ї—М–љ—Л—Е –•–°–Э —Б–Њ II, III –Є IV —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –Ї–ї–∞—Б—Б–Њ–Љ NYHA, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–∞–ї–Є —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ—Г—О —В–µ—А–∞–њ–Є—О [8]. –Ъ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є, –≤–Ї–ї—О—З–∞—П –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —Г 93% –±–Њ–ї—М–љ—Л—Е, –±—Л–ї –і–Њ–±–∞–≤–ї–µ–љ –ї–Є–±–Њ –≤–∞–ї—Б–∞—А—В–∞–љ –≤ —Б—В–∞—А—В–Њ–≤–Њ–є –і–Њ–Ј–µ 40–80 –Љ–≥ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –і–Њ 160 –Љ–≥ 2 —А–∞–Ј–∞/—Б—Г—В., –ї–Є–±–Њ –њ–ї–∞—Ж–µ–±–Њ. –Я—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –≤–∞–ї—Б–∞—А—В–∞–љ–∞ –Ї –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є, –≤–Ї–ї—О—З–∞—П –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§, –њ—А–Є–≤–µ–ї–Њ –Ї —Б–љ–Є–ґ–µ–љ–Є—О —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є (—Б–Љ–µ—А—В–љ–Њ—Б—В—М –Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–∞—П –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М) –љ–∞ 13,2% (—А=0,009) –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Ј–∞ —Б—З–µ—В —Б–љ–Є–ґ–µ–љ–Є—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (—А–Є—Б. 2).
–Э–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –≤ –≥—А—Г–њ–њ–µ –Є–Ј 366 –±–Њ–ї—М–љ—Л—Е, –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ–Њ –њ—А–Є—З–Є–љ–µ –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§: —Б–Љ–µ—А—В–љ–Њ—Б—В—М –Њ—В –≤—Б–µ—Е –њ—А–Є—З–Є–љ –±—Л–ї–∞ –љ–∞ 33,1% –љ–Є–ґ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –њ–ї–∞—Ж–µ–±–Њ. –Ю—В–Љ–µ—З–∞–ї–Є—Б—М –Є –і—А—Г–≥–Є–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л, –≤–Ї–ї—О—З–∞—П —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –Є —Ж–µ–ї–Њ–≥–Њ —А—П–і–∞ –љ–µ–є—А–Њ–≥–Њ—А–Љ–Њ–љ–Њ–≤ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤–∞–ї—Б–∞—А—В–∞–љ–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤–∞–ї—Б–∞—А—В–∞–љ —Б—В–∞–ї —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –Ј–∞–Љ–µ–љ–Њ–є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ (–њ—А–Є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є) —Г –±–Њ–ї—М–љ—Л—Е –•–°–Э.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ CHARM. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є CHARM (Candesartan in Heart Failure Assessment of Reduction in Mortality and Morbidity) –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –С–Р–† –Ї–∞–љ–і–µ—Б–∞—А—В–∞–љ —Г –±–Њ–ї—М–љ—Л—Е –•–°–Э –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–Ј–Є–ї —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —Б–Љ–µ—А—В–Є –Њ—В –≤—Б–µ—Е –њ—А–Є—З–Є–љ –љ–∞ 10% (—А=0,032) –Є —Б–Љ–µ—А—В–Є –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ –љ–∞ 13% (—А=0,006) [9].
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ VALIANT. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є VALIANT (Valsartan in Acute Myocardial Infarction Trial) –Є–Ј—Г—З–∞–ї–Њ—Б—М –≤–ї–Є—П–љ–Є–µ –≤–∞–ї—Б–∞—А—В–∞–љ–∞ –љ–∞ —В–µ—З–µ–љ–Є–µ –Њ—Б—В—А–Њ–≥–Њ –Ш–Ь [10]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–∞–ї–Є—Б—М –±–Њ–ї—М–љ—Л–µ –≤ —В–µ—З–µ–љ–Є–µ 0,5–10 –і–љ–µ–є –њ–Њ—Б–ї–µ —А–∞–Ј–≤–Є—В–Є—П –Ш–Ь. –Я–Њ –і–∞–љ–љ—Л–Љ —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –≤–∞–ї—Б–∞—А—В–∞–љ–Њ–Љ –≤ –і–Њ–Ј–µ 160 –Љ–≥ 2 —А–∞–Ј–∞/—Б—Г—В. –Њ–Ї–∞–Ј–∞–ї–∞—Б—М —В–∞–Ї–Њ–є –ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –≤ –ї–µ—З–µ–љ–Є–Є –њ–Њ—Б—В–Є–љ—Д–∞—А–Ї—В–љ—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ –Є/–Є–ї–Є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О, –Ї–∞–Ї –Є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –Ї–∞–њ—В–Њ–њ—А–Є–ї–Њ–Љ –≤ –і–Њ–Ј–µ 50 –Љ–≥ 3 —А–∞–Ј–∞/—Б—Г—В. , —Ж–µ–љ–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–Њ—В–Њ—А–Њ–≥–Њ –≤ –њ–Њ–і–Њ–±–љ–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є –±—Л–ї–∞ –і–Њ–Ї–∞–Ј–∞–љ–∞ —А–∞–љ–µ–µ. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М –ї—Г—З—И—Г—О –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –≤–∞–ї—Б–∞—А—В–∞–љ–∞.
–Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ –Р–Я–§ –Є –С–Р–† –љ–µ –і–∞–≤–∞–ї–∞ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ —Г–ї—Г—З—И–µ–љ–Є—П –њ—А–Њ–≥–љ–Њ–Ј–∞ —Г –±–Њ–ї—М–љ—Л—Е –њ–Њ—Б–ї–µ –Ш–Ь –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–µ–є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ –Р–Я–§.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ MARVAL. –Ь–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—П (–Ь–Р–£) —П–≤–ї—П–µ—В—Б—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Р–Ї—В–Є–≤–∞—Ж–Є—П –†–Р–Р–° —П–≤–ї—П–µ—В—Б—П –Ї–ї—О—З–µ–≤—Л–Љ —Н—В–∞–њ–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–Њ—З–µ–Ї [11]. –С–ї–Њ–Ї–∞—В–Њ—А—Л –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —Г–Љ–µ–љ—М—И–∞—П –њ–Њ—В–µ—А–Є –±–µ–ї–Ї–∞ —Б –Љ–Њ—З–Њ–є, –Њ–Ї–∞–Ј—Л–≤–∞—О—В –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –љ–µ—Д—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Т –Њ–і–љ–Њ–Љ –Є–Ј –њ–µ—А–≤—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є the MicroAlbuminuria Reduction with VALsartan (MARVAL) —Г 332 –±–Њ–ї—М–љ—Л—Е –°–Ф 2––≥–Њ —В–Є–њ–∞ –Є –Ь–Р–£ –Є–Ј—Г—З–∞–ї–Њ—Б—М –≤–ї–Є—П–љ–Є–µ –≤–∞–ї—Б–∞—А—В–∞–љ–∞ –≤ –і–Њ–Ј–µ 80 –Љ–≥ –њ—А–Њ—В–Є–≤ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –≤ –і–Њ–Ј–µ 5 –Љ–≥ –љ–∞ –≤–µ–ї–Є—З–Є–љ—Г —Н–Ї—Б–Ї—А–µ—Ж–Є–Є –±–µ–ї–Ї–∞ —Б –Љ–Њ—З–Њ–є –≤ —В–µ—З–µ–љ–Є–µ 24 –љ–µ–і–µ–ї—М [12]. –Т –Ї–Њ–љ—Ж–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–∞ —Д–Њ–љ–µ –≤–∞–ї—Б–∞—А—В–∞–љ–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ –љ–∞ 44% —Б–љ–Є–Ј–Є–ї–∞—Б—М —Н–Ї—Б–Ї—А–µ—Ж–Є—П –±–µ–ї–Ї–∞ —Б –Љ–Њ—З–Њ–є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –∞–Љ–ї–Њ–і–Є–њ–Є–љ–Њ–Љ, –љ–∞ —Д–Њ–љ–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ —Б–Њ—Б—В–∞–≤–Є–ї–Њ —В–Њ–ї—М–Ї–Њ 8%. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –±—Л–ї–Њ –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–Љ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е, –∞–љ—В–Є–њ—А–Њ—В–µ–Є–љ—Г—А–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –≤–∞–ї—Б–∞—А—В–∞–љ–∞ –±—Л–ї –Р–Ф––љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ.
–†–µ–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Є –С–Р–† —Г –±–Њ–ї—М–љ—Л—Е —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–Њ—З–µ–Ї –±—Л–ї–Є –Њ–±–Њ–±—Й–µ–љ—Л –≤ –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј–µ 127 —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б –≤–Ї–ї—О—З–µ–љ–Є–µ–Љ 73 514 –±–Њ–ї—М–љ—Л—Е [13]. –Т —Н—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±—Л–ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л –љ–µ—Д—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–µ –≤—Л–≥–Њ–і—Л, –Њ–і–љ–∞–Ї–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П, —З—В–Њ, –≤–µ—А–Њ—П—В–љ–µ–µ –≤—Б–µ–≥–Њ, –Њ–љ–Є —Б–≤—П–Ј–∞–љ—Л —Б –Р–Ф–—Б–љ–Є–ґ–∞—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –І—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –≤–ї–Є—П–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –±–ї–Њ–Ї–Є—А—Г—О—Й–Є—Е –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –†–Р–Р–°, –≤–Ї–ї—О—З–∞—П –С–Р–†, –≤ –і—А—Г–≥–Њ–Љ –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј–µ –≤ –њ–Њ–і–≥—А—Г–њ–њ–∞—Е –±–Њ–ї—М–љ—Л—Е —Б –°–Ф –Є –±–µ–Ј –љ–µ–≥–Њ, —Г—З–∞—Б—В–≤—Г—О—Й–Є—Е –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ–Њ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–∞ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є, —В–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ, –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –і—А—Г–≥–Є–Љ–Є –Ї–ї–∞—Б—Б–∞–Љ–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ [14]. –°–ї–µ–і—Г–µ—В –Є–Љ–µ—В—М –≤ –≤–Є–і—Г, —З—В–Њ —Н—В–Є –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ –њ–Њ–і–≥—А—Г–њ–њ–∞—Е –±–Њ–ї—М–љ—Л—Е –≤ –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј–∞—Е –Є –Ї –љ–Є–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–љ–Њ—Б–Є—В—М—Б—П –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ VALUE. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ VALUE –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ –±–Њ–ї–µ–µ 15 —В—Л—Б. –±–Њ–ї—М–љ—Л—Е –Р–У >50 –ї–µ—В —Б –≤—Л—Б–Њ–Ї–Є–Љ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —А–Є—Б–Ї–Њ–Љ, –Ї–Њ—В–Њ—А—Л–Љ –љ–∞–Ј–љ–∞—З–∞–ї–Є –ї–µ—З–µ–љ–Є–µ –ї–Є–±–Њ –љ–∞ –Њ—Б–љ–Њ–≤–µ –≤–∞–ї—Б–∞—А—В–∞–љ–∞, –ї–Є–±–Њ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ [15]. –Ю–±–µ —Б—Е–µ–Љ—Л —В–µ—А–∞–њ–Є–Є –±—Л–ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –≤ —Б–љ–Є–ґ–µ–љ–Є–Є –Р–Ф, —Е–Њ—В—П —Б–љ–Є–ґ–µ–љ–Є–µ –±—Л–ї–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –±–Њ–ї—М—И–µ –≤ –≥—А—Г–њ–њ–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ —Б —А–∞–Ј–ї–Є—З–Є–µ–Љ –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є 1,5/1,3 –Љ–Љ —А—В.—Б—В. –њ–Њ—Б–ї–µ –≥–Њ–і–∞ –ї–µ—З–µ–љ–Є—П. –Я—А–Є 5––ї–µ—В–љ–µ–Љ –љ–∞–±–ї—О–і–µ–љ–Є–Є —З–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є (–њ–µ—А–≤–Є—З–љ–∞—П –Ї–Њ–љ–µ—З–љ–∞—П —В–Њ—З–Ї–∞) —Б–Њ—Б—В–∞–≤–Є–ї–∞ 10,4% –≤ –≥—А—Г–њ–њ–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –Є 10,6% –≤ –≥—А—Г–њ–њ–µ –≤–∞–ї—Б–∞—А—В–∞–љ–∞ (—А–∞–Ј–ї–Є—З–Є–µ –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ–Њ) (—А–Є—Б. 3). –°—А–µ–і–Є –≤—В–Њ—А–Є—З–љ—Л—Е –Ї–Њ–љ–µ—З–љ—Л—Е —В–Њ—З–µ–Ї –≤ –≥—А—Г–њ–њ–µ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–∞ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Љ–µ–љ—М—И–µ —Б–ї—Г—З–∞–µ–≤ –Ш–Ь –Є —В–µ–љ–і–µ–љ—Ж–Є—П –≤ —Б–љ–Є–ґ–µ–љ–Є–Є —Б–ї—Г—З–∞–µ–≤ —Д–∞—В–∞–ї—М–љ—Л—Е –Є –љ–µ—Д–∞—В–∞–ї—М–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤–∞–ї—Б–∞—А—В–∞–љ —Б–љ–Є–Ј–Є–ї –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А –≤ —Б–≤—П–Ј–Є —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є.
–Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞, –Ї–Њ—В–Њ—А—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є VALUE —Б –њ–Њ–Љ–Њ—Й—М—О —В–µ—А–∞–њ–Є–Є, –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є –љ–∞ –≤–∞–ї—Б–∞—А—В–∞–љ–µ –Є –љ–∞ –∞–Љ–ї–Њ–і–Є–њ–Є–љ–µ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —Б—В–∞–ї–Є –Њ—Б–љ–Њ–≤–Њ–є –і–ї—П —Б–Њ–Ј–і–∞–љ–Є—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Н—В–Є—Е –і–≤—Г—Е –≤—Л—Б–Њ–Ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –Є —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –≤–Є–і–µ –Љ–љ–Њ–≥–Њ—Ж–µ–ї–µ–≤–Њ–є —В–µ—А–∞–њ–Є–Є.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ JIKEY HEART. –Т —П–њ–Њ–љ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є JIKEY HEART —Г 3081 –±–Њ–ї—М–љ–Њ–≥–Њ —Б –Р–У –Є –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (—Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–∞—П –Ш–С–°, –•–°–Э, –°–Ф –Є–ї–Є –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 65 –ї–µ—В, —Б—А–µ–і–љ—П—П –Љ–∞—Б—Б–∞ —В–µ–ї–∞ 24 –Ї–≥/–Љ2) –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –Ї –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є –±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є (67% –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П; 35% –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§; 32% b––±–ї–Њ–Ї–∞—В–Њ—А—Л –Є –і—А. –њ—А–µ–њ–∞—А–∞—В—Л) –≤–∞–ї—Б–∞—А—В–∞–љ–∞ –≤ –і–Њ–Ј–µ 40–160 –Љ–≥ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ —Б–љ–Є–ґ–µ–љ–Є—О –Р–Ф —Б–Њ 139/81 –і–Њ 132/78 –Љ–Љ —А—В.—Б—В. [16]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –Њ—В–Ї—А—Л—В–Њ–µ; –≥—А—Г–њ–њ–Њ–є —Б—А–∞–≤–љ–µ–љ–Є—П –±—Л–ї–Є –±–Њ–ї—М–љ—Л–µ, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –≤—Б–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –љ–Њ –±–µ–Ј –С–Р–†.
–Ч–∞ 3,1 –≥–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –ї–µ—З–µ–љ–Є–µ –≤–∞–ї—Б–∞—А—В–∞–љ–Њ–Љ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–µ—А–≤–Є—З–љ–Њ–є —Б—Г–Љ–Љ–∞—А–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є, –≤–Ї–ї—О—З–∞—О—Й–µ–є —Б–µ—А–і–µ—З–љ—Л–µ, —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л–µ –Є –њ–Њ—З–µ—З–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П. –Ю—Б–љ–Њ–≤–љ–Њ–є —Н—Д—Д–µ–Ї—В –Ј–∞–Ї–ї—О—З–∞–ї—Б—П –≤ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Б—Г–ї—М—В–∞ –љ–∞ 40% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –±–Њ–ї—М–љ—Л—Е, —Г –Ї–Њ—В–Њ—А—Л—Е –Р–Ф –±—Л–ї–Њ —В–Њ–ї—М–Ї–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –≤—Л—И–µ, —З–µ–Љ 132/78 –Љ–Љ —А—В. —Б—В., –љ–Њ –±—Л–ї–Њ –і–Њ—Б—В–Є–≥–љ—Г—В–Њ —Б –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ–Љ –і—А—Г–≥–Є—Е, –Ї—А–Њ–Љ–µ –С–Р–†, –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (—А–Є—Б. 4).
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ ONTARGET. –†–∞–љ–µ–µ –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —А–∞–Љ–Є–њ—А–Є–ї (–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ HOPE) –Є –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї (–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ EUROPA) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є —Б—В–∞–±–Є–ї—М–љ–Њ–є –Ш–С–° –±–µ–Ј –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Б–љ–Є–ґ–∞—О—В —А–∞–Ј–≤–Є—В–Є–µ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ [17,18]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ONTARGET (Ongoing Telmisartan Alone and in Combination with Ramipril Global End–point Trial) –Є–Ј—Г—З–∞–ї–Є –≤–ї–Є—П–љ–Є–µ –С–Р–† —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ –Р–Я–§ —А–∞–Љ–Є–њ—А–Є–ї–Њ–Љ, –∞ —В–∞–Ї–ґ–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Н—В–Є—Е –і–≤—Г—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –љ–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —В–µ—З–µ–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є [19]. –Т–Ї–ї—О—З–∞–ї–Є—Б—М –±–Њ–ї—М–љ—Л–µ —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е, –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –Є —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є, –°–Ф, —Б –Њ—А–≥–∞–љ–љ—Л–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є. –Я–Њ—Б–ї–µ —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є –≤ —А–∞–Љ–Ї–∞—Е –і–≤–Њ–є–љ–Њ–≥–Њ —Б–ї–µ–њ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –≤ —В–µ—З–µ–љ–Є–µ 56 –Љ–µ—Б. 8576 –±–Њ–ї—М–љ—Л—Е –њ–Њ–ї—Г—З–∞–ї–Є —А–∞–Љ–Є–њ—А–Є–ї –≤ –і–Њ–Ј–µ 10 –Љ–≥; 8542 –±–Њ–ї—М–љ—Л—Е –њ–Њ–ї—Г—З–∞–ї–Є —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ –≤ –і–Њ–Ј–µ 80 –Љ–≥; 8502 –±–Њ–ї—М–љ—Л—Е –њ–Њ–ї—Г—З–∞–ї–Є –Њ–±–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –і–Њ–Ј–∞—Е –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –Ї —А–∞–љ–µ–µ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Т –Ї–∞—З–µ—Б—В–≤–µ –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є –±—Л–ї–∞ –≤—Л–±—А–∞–љ–∞ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Б–ї–µ–і—Г—О—Й–Є—Е —Б–Њ–±—Л—В–Є–є: —Б–Љ–µ—А—В—М –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ, –Ш–Ь, –Є–љ—Б—Г–ї—М—В –Є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є—П –≤ —Б–≤—П–Ј–Є —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О.
–Т —В–µ—З–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–Њ–±—Л—В–Є—П –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є –≤–Њ–Ј–љ–Є–Ї–ї–Є —Г 1412 –±–Њ–ї—М–љ—Л—Е –≤ –≥—А—Г–њ–њ–µ —А–∞–Љ–Є–њ—А–Є–ї–∞ (16,5%) –Є —Г 1423 –±–Њ–ї—М–љ—Л—Е –≤ –≥—А—Г–њ–њ–µ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ (16,7%) –±–µ–Ј –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є. –Я–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —А–∞–Љ–Є–њ—А–Є–ї–Њ–Љ —Г –±–Њ–ї—М–љ—Л—Е –љ–∞ —Д–Њ–љ–µ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ –±—Л–ї–∞ –љ–Є–ґ–µ —З–∞—Б—В–Њ—В–∞ –Ї–∞—И–ї—П (1,1% –њ—А–Њ—В–Є–≤ 4,2%; —А<0,001) –Є –∞–љ–≥–Є–Њ—В–µ–Ї–∞ (0,1% –њ—А–Њ—В–Є–≤ 0,3%; —А=0,01), –љ–Њ –≤—Л—И–µ —З–∞—Б—В–Њ—В–∞ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ (2,6% –њ—А–Њ—В–Є–≤ 1,7%; —А<0,001).
–Т –≥—А—Г–њ–њ–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–є —З–∞—Б—В–Њ—В–µ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є —А–∞–Љ–Є–њ—А–Є–ї–∞ (–љ–µ—В –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –Њ—В–ї–Є—З–Є–є) –±—Л–ї–∞ —Е—Г–ґ–µ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М: –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є (4,8% –њ—А–Њ—В–Є–≤ 1,7%; —А<0,001), —Б–Є–љ–Ї–Њ–њ–∞–ї—М–љ—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є (0,3% –њ—А–Њ—В–Є–≤ 0,2; —А=0,03) –Є –њ–Њ—З–µ—З–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є (13,5% –њ—А–Њ—В–Є–≤ 10,2%; —А<0,001).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–∞—А—В–∞–љ—Л –Њ–Ї–∞–Ј–∞–ї–Є—Б—М –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є —Б –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ–Є –Р–Я–§ —Г —Н—В–Њ–є –Ї–Њ–≥–Њ—А—В—Л –±–Њ–ї—М–љ—Л—Е –њ—А–Є –ї—Г—З—И–µ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є. –Р –≤–Њ—В –і–∞–≤–љ–Њ –Њ–±—Б—Г–ґ–і–∞–µ–Љ–∞—П –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є —Б–Њ—З–µ—В–∞–љ–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ —Б –С–Р–†, –Њ—Б–Њ–±–µ–љ–љ–Њ –і–ї—П —Г—Б–Є–ї–µ–љ–Є—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –Њ—В –Р–Ф –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤, –љ–µ —В–Њ–ї—М–Ї–Њ –љ–µ –њ–Њ–і—В–≤–µ—А–і–Є–ї–∞—Б—М, –љ–Њ –Є –Њ–Ї–∞–Ј–∞–ї–∞—Б—М –±–Њ–ї–µ–µ –Њ–њ–∞—Б–љ–Њ–є –≤ –њ–ї–∞–љ–µ —А–∞–Ј–≤–Є—В–Є—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ TRANSCEND. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —Б–љ–Є–ґ–∞—О—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –Њ–і–љ–∞–Ї–Њ, –њ–Њ —А–∞–Ј–љ—Л–Љ –Њ—Ж–µ–љ–Ї–∞–Љ, –і–Њ 20% –±–Њ–ї—М–љ—Л—Е –љ–µ –њ–µ—А–µ–љ–Њ—Б—П—В —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л. –С—Л–ї–Њ –Њ—А–≥–∞–љ–Є–Ј–Њ–≤–∞–љ–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ TRANSCEND (Telmisartan Randomised Assessment Study in ACE intolerant subjects with cardiovascular Disease) –і–ї—П –Є–Ј—Г—З–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –С–Р–† —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Є–ї–Є –°–Ф —Б –Њ—А–≥–∞–љ–љ—Л–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є [20].
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 5926 –±–Њ–ї—М–љ—Л—Е —Б —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є —А–∞–љ–µ–µ –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Г—О –і–Њ–Ї–∞–Ј–∞–љ–љ—Г—О —В–µ—А–∞–њ–Є—О, –Ї–Њ—В–Њ—А—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–ї–Є –љ–∞ 2 –≥—А—Г–њ–њ—Л – —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ 80 –Љ–≥ (n=2954) –Є –њ–ї–∞—Ж–µ–±–Њ (n=2972). –Я–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Њ–є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±—Л–ї–∞ —Б—Г–Љ–Љ–∞ —Б–Љ–µ—А—В–µ–є –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ, –Ш–Ь, –Є–љ—Б—Г–ї—М—В–Њ–≤ –Є –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –њ–Њ –њ–Њ–≤–Њ–і—Г —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є. –°—А–µ–і–љ—П—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ 56 –Љ–µ—Б. –Р–Ф –±—Л–ї–Њ –љ–Є–ґ–µ –≤ –≥—А—Г–њ–њ–µ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (–≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 4,0/2,2 –Љ–Љ —А—В.—Б—В.). –Т –≥—А—Г–њ–њ–µ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ 465 (15,7%) —Б–Њ–±—Л—В–Є–є –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б 504 (17,0%) —Б–Њ–±—Л—В–Є—П–Љ–Є –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ (–Њ—В–љ–Њ—И–µ–љ–Є–µ —А–Є—Б–Ї–Њ–≤ 0,91; 95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї 0,81–1,05; —А=0,216), —З—В–Њ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ.
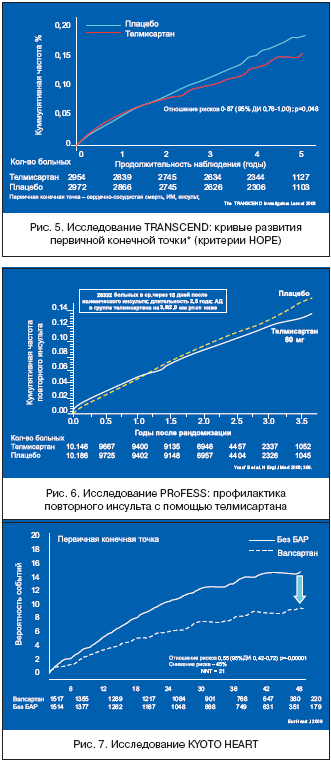
–Ю–і–љ–∞–Ї–Њ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Њ–і–љ–∞ –Є–Ј –≤—В–Њ—А–Є—З–љ—Л—Е –Ї–Њ–љ–µ—З–љ—Л—Е —В–Њ—З–µ–Ї – —Б—Г–Љ–Љ–∞ —Б–Љ–µ—А—В–µ–є –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ, –Ш–Ь –Є –Є–љ—Б—Г–ї—М—В–Њ–≤ – –±—Л–ї–∞ —Г 384 (13,0%) –±–Њ–ї—М–љ—Л—Е –љ–∞ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–µ –Є —Г 440 (14,8%) –±–Њ–ї—М–љ—Л—Е –љ–∞ –њ–ї–∞—Ж–µ–±–Њ (–Њ—В–љ–Њ—И–µ–љ–Є–µ —А–Є—Б–Ї–Њ–≤ 0,87; 95% –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–≤–∞–ї 0,76–1,00; —А=0,048), —З—В–Њ –±—Л–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Љ–µ–љ—М—И–µ (—А–Є—Б. 5). –Э–∞–њ–Њ–Љ–Є–љ–∞–µ–Љ, —З—В–Њ –Є–Љ–µ–љ–љ–Њ –њ–Њ —В–∞–Ї–Њ–Љ—Г –Ї—А–Є—В–µ—А–Є—О –±—Л–ї–∞ –і–Њ–Ї–∞–Ј–∞–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —А–∞–Љ–Є–њ—А–Є–ї–∞ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є HOPE [17]. –С–Њ–ї—М–љ—Л–µ, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —А–µ–ґ–µ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є—Б—М –њ–Њ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ –њ—А–Є—З–Є–љ–∞–Љ – –љ–∞ 15% (—А=0,028). –Ґ–µ–ї–Љ–Є—Б–∞—А—В–∞–љ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї —Е–Њ—А–Њ—И—Г—О —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –Є –Љ–Њ–ґ–µ—В –±—Л—В—М –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ –≤ —Н—В–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ PROFESS. –†–∞–љ–µ–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є PROGRESS –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф –њ–Њ—Б–ї–µ –Є–љ—Б—Г–ї—М—В–∞ —Г–Љ–µ–љ—М—И–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ —Б–Њ–±—Л—В–Є—П [21]. –Ш–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ –†–Р–Р–° —Г –±–Њ–ї—М–љ—Л—Е —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ —Б–љ–Є–ґ–∞–µ—В –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –≤–Ї–ї—О—З–∞—П –Є–љ—Б—Г–ї—М—В. –Ю–і–љ–∞–Ї–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–љ–Є–ґ–µ–љ–Є—П –Р–Ф —Б –њ–Њ–Љ–Њ—Й—М—О –±–ї–Њ–Ї–∞–і—Л –†–Р–Р–° –≤ –±–ї–Є–ґ–∞–є—Й–Є–µ —Б—А–Њ–Ї–Є –њ–Њ—Б–ї–µ –Є–љ—Б—Г–ї—М—В–∞ –Є–Ј—Г—З–µ–љ–∞ –±—Л–ї–∞ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є PROFESS –±—Л–ї–Є –Њ—Ж–µ–љ–µ–љ—Л —Н—Д—Д–µ–Ї—В—Л —В–µ—А–∞–њ–Є–Є –С–Р–† —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–Њ–Љ, –љ–∞–Ј–љ–∞—З–µ–љ–љ–Њ–≥–Њ –≤—Б–Ї–Њ—А–µ –њ–Њ—Б–ї–µ –Є–љ—Б—Г–ї—М—В–∞. –Т –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ (—Б —Г—З–∞—Б—В–Є–µ–Љ —А–Њ—Б—Б–Є–є—Б–Ї–Є—Е —Ж–µ–љ—В—А–Њ–≤) –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 20 332 –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–і–∞–≤–љ–Њ –њ–µ—А–µ–љ–µ—Б–µ–љ–љ—Л–Љ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ (–≤ —Б—А–µ–і–љ–µ–Љ —З–µ—А–µ–Ј 15 –і–љ–µ–є), –Ї–Њ—В–Њ—А—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–ї–Є –љ–∞ 2 –≥—А—Г–њ–њ—Л – –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ 80 –Љ–≥ –≤ –і–µ–љ—М –Є –њ–ї–∞—Ж–µ–±–Њ [22]. –Я–µ—А–≤–Є—З–љ–∞—П –Ї–Њ–љ–µ—З–љ–∞—П —В–Њ—З–Ї–∞ –±—Л–ї–∞ –њ–Њ–≤—В–Њ—А–љ—Л–є –Є–љ—Б—Г–ї—М—В, –≤—В–Њ—А–Є—З–љ—Л–µ – —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–µ —Б–Њ–±—Л—В–Є—П (—Б–Љ–µ—А—В—М, –Є–љ—Б—Г–ї—М—В, –Ш–Ь, —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М) –Є –љ–Њ–≤—Л–µ —Б–ї—Г—З–∞–Є –°–Ф.
–Т —В–µ—З–µ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (—Б—А–µ–і–љ—П—П –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М 2,5 –≥) –≤ –≥—А—Г–њ–њ–µ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ –Р–Ф –±—Л–ї–Њ –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 3,8/2,0 –Љ–Љ —А—В. —Б—В. –љ–Є–ґ–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ. –Ч–∞ –≤—А–µ–Љ—П –љ–∞–±–ї—О–і–µ–љ–Є—П —Г 880 –±–Њ–ї—М–љ—Л—Е (8,7%) –≤ –≥—А—Г–њ–њ–µ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ –Є —Г 934 –±–Њ–ї—М–љ—Л—Е (9,2%) –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ —А–∞–Ј–≤–Є–ї—Б—П –њ–Њ–≤—В–Њ—А–љ—Л–є –Є–љ—Б—Г–ї—М—В: —Н—В–Њ —А–∞–Ј–ї–Є—З–Є–µ –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ, —А=0,23 (—А–Є—Б. 6). –Ю—Б–љ–Њ–≤–љ—Л–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–µ —Б–Њ–±—Л—В–Є—П —Б–ї—Г—З–Є–ї–Є—Б—М —Г 1367 –±–Њ–ї—М–љ—Л—Е (13,5%) –≤ –≥—А—Г–њ–њ–µ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ –Є —Г 1463 –±–Њ–ї—М–љ—Л—Е (14,4%) –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ, —А=0,11. –Э–Њ–≤—Л–µ —Б–ї—Г—З–∞–Є –°–Ф –±—Л–ї–Є –Њ—В–Љ–µ—З–µ–љ—Л —Г 1,7% –≤ –≥—А—Г–њ–њ–µ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–∞ –Є —Г 2,1% –±–Њ–ї—М–љ—Л—Е –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ, —А=0,10. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –ї–µ—З–µ–љ–Є–µ —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–Њ–Љ, –Є–љ–Є—Ж–Є–Є—А–Њ–≤–∞–љ–љ–Њ–µ –≤—Б–Ї–Њ—А–µ –њ–Њ—Б–ї–µ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ –Є –њ—А–Њ–і–Њ–ї–ґ–∞—О—Й–µ–µ—Б—П 2,5 –≥–Њ–і–∞, –љ–µ —Б–љ–Є–ґ–∞–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —А–Є—Б–Ї –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞, –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є –Є —А–∞–Ј–≤–Є—В–Є—П –°–Ф [22].
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ KYOTO HEART. –Ю—Б–љ–Њ–≤–љ–Њ–є —Ж–µ–ї—М—О —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Ї–Њ—В–Њ—А–Њ–µ –±—Л–ї–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –љ–∞ –Њ–і–љ–Њ–є –Є–Ј —Б–µ—Б—Б–Є–є –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–≥–Њ –Ї–Њ–љ–≥—А–µ—Б—Б–∞ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤ –≤ –С–∞—А—Б–µ–ї–Њ–љ–µ –≤ —Б–µ–љ—В—П–±—А–µ 2009 –≥., –±—Л–ї–∞ –Њ—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤–∞–ї—Б–∞—А—В–∞–љ–∞ –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–љ–Њ–≥–Њ –Ї –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –Р–У —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [23]. –Т —Н—В–Њ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –Њ—В–Ї—А—Л—В–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б –Ј–∞—Б–ї–µ–њ–ї–µ–љ–љ—Л–Љ–Є –Ї–Њ–љ–µ—З–љ—Л–Љ–Є —В–Њ—З–Ї–∞–Љ–Є (PROBE –і–Є–Ј–∞–є–љ) –±—Л–ї –≤–Ї–ї—О—З–µ–љ 3031 –±–Њ–ї—М–љ–Њ–є (43% –ґ–µ–љ—Й–Є–љ, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 66 –ї–µ—В, —П–њ–Њ–љ—Б–Ї–∞—П –њ–Њ–њ—Г–ї—П—Ж–Є—П) —Б –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–є –Р–У, –Ї–Њ—В–Њ—А—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–ї–Є –љ–∞ –≥—А—Г–њ–њ—Г –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –≤–∞–ї—Б–∞—А—В–∞–љ –≤ –і–Њ–Ј–µ –і–Њ 320 –Љ–≥ –Є –≥—А—Г–њ–њ—Г –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –і—А—Г–≥–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л –Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –С–Р–†. –Т –Ї–∞—З–µ—Б—В–≤–µ –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є –±—Л–ї–∞ —Б—Г–Љ–Љ–∞ –≤—Б–µ—Е —Д–∞—В–∞–ї—М–љ—Л—Е –Є –љ–µ—Д–∞—В–∞–ї—М–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є. –Т —Б—А–µ–і–љ–µ–Љ –њ–µ—А–Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї 3,3 –≥–Њ–і–∞. –Т –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –±—Л–ї –і–Њ—Б—В–Є–≥–љ—Г—В –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –Ј–∞ —Г—А–Њ–≤–љ–µ–Љ –Р–Ф: –і–∞–≤–ї–µ–љ–Є–µ —Б–љ–Є–Ј–Є–ї–Њ—Б—М —Б–Њ 157/88 –і–Њ 133/76 –Љ–Љ —А—В. —Б—В. –£ –±–Њ–ї—М–љ—Л—Е –≥—А—Г–њ–њ—Л –≤–∞–ї—Б–∞—А—В–∞–љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і—А—Г–≥–Њ–є –≥—А—Г–њ–њ–Њ–є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–Ј–Є–ї—Б—П —А–∞–Ј–≤–Є—В–Є—П —Б–Њ–±—Л—В–Є–є –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є –љ–∞ 45% (—А–Є—Б. 7). –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –≤–∞–ї—Б–∞—А—В–∞–љ–∞ –Ї –ї–µ—З–µ–љ–Є—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –±–Њ–ї—М–љ—Л—Е –Р–У –љ–µ —В–Њ–ї—М–Ї–Њ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –і–Њ–±–Є—В—М—Б—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П, –љ–Њ –Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–ї—Г—З—И–Є–ї–Њ –њ—А–Њ–≥–љ–Њ–Ј.
–Я–Њ—Б–ї–µ—Б–ї–Њ–≤–Є–µ
–Ї –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ
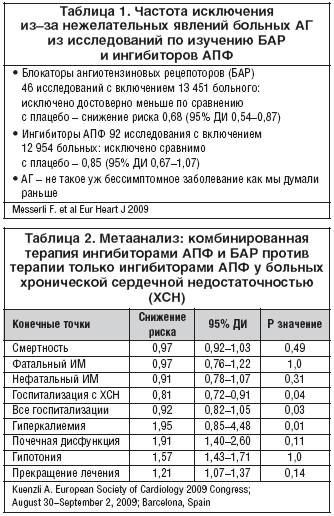
–Т —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і–љ–Є—Е –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –ї–µ—В –Ј–∞–≤–µ—А—И–Є–ї–Њ—Б—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Ї—А—Г–њ–љ–Њ–Љ–∞—Б—И—В–∞–±–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б –Њ—Ж–µ–љ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б–∞—А—В–∞–љ–Њ–≤ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є—В—Г–∞—Ж–Є—П—Е. –Я–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П KYOTO HEART –≥—А—Г–њ–њ–∞ –њ—А–Њ—Д. F. Messerli –њ—А–µ–і—Б—В–∞–≤–Є–ї–∞ –љ–Њ–≤—Л–є –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б–∞—А—В–∞–љ–Њ–≤ –њ—А–Њ—В–Є–≤ –њ–ї–∞—Ж–µ–±–Њ –Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П —Г –±–Њ–ї—М–љ—Л—Е —Б –Р–У, –≤—Л—Б–Њ–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є –і—А—Г–≥–Є—Е, –љ–Њ –±–µ–Ј –≤–Ї–ї—О—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О [24]. –Ш–Ј –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –≤–Є–і–љ–Њ, –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –С–Р–† –Њ—В–Љ–µ—З–∞–µ—В—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Б—Г–ї—М—В–∞ –љ–∞ 13% (—А–Є—Б. 8), –љ–Њ –±–µ–Ј –≤–ї–Є—П–љ–Є—П –љ–∞ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ш–Ь (—А–Є—Б. 9). –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –±—Л–ї –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –С–Р–† –Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –Р–Я–§ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ. –Ю–Ї–∞–Ј–∞–ї–Њ—Б—М, —З—В–Њ –µ—Б–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —В–∞–Ї–Њ–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М, –Ї–∞–Ї –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є—Б–Ї–ї—О—З–µ–љ–љ—Л—Е –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ –њ—А–Є—З–Є–љ–µ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –±–Њ–ї—М–љ—Л—Е, —В–Њ –С–Р–† –њ–µ—А–µ–љ–Њ—Б—П—В—Б—П –ї—Г—З—И–µ, —З–µ–Љ –њ–ї–∞—Ж–µ–±–Њ, –∞ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —В–∞–Ї –ґ–µ, –Ї–∞–Ї –њ–ї–∞—Ж–µ–±–Њ (—В–∞–±–ї. 1).
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ONTARGET –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П —А–∞–Љ–Є–њ—А–Є–ї–∞ —Б —В–µ–ї–Љ–Є—Б–∞—А—В–∞–љ–Њ–Љ –≤—Л–Ј—Л–≤–∞–µ—В –њ–Њ—З–µ—З–љ—Г—О –і–Є—Б—Д—Г–љ–Ї—Ж–Є—О –Є –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –±–Њ–ї—М–љ—Л–Љ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –±–µ–Ј –•–°–Э. –С—Л–ї –њ—А–Њ–≤–µ–і–µ–љ –Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –љ–∞ –Ї–Њ–љ–≥—А–µ—Б—Б–µ –≤ –С–∞—А—Б–µ–ї–Њ–љ–µ –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ –Њ—Ж–µ–љ–Ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ –њ–ї—О—Б –С–Р–† –њ—А–Њ—В–Є–≤ –Є–љ–≥–Є–±–Є—В–Њ—А –Р–Я–§ —Г –±–Њ–ї—М–љ—Л—Е –•–°–Э. –Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –≤ —В–∞–±–ї–Є—Ж–µ 2 –і–∞–љ–љ—Л—Е, –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤–Њ–њ—А–Њ—Б –Њ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —В–∞–Ї–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е –•–°–Э, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –њ–Њ–Ј–Є—В–Є–≤ –≤ –≤–Є–і–µ —Б–љ–Є–ґ–µ–љ–Є—П –њ–Њ–≤—В–Њ—А–љ—Л—Е –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є —П–≤–љ–Њ —Г—Б—В—Г–њ–∞–µ—В –Љ–љ–Њ–≥–Є–Љ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П–Љ.
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–С–ї–Њ–Ї–∞–і–∞ –†–Р–Р–° —Б –њ–Њ–Љ–Њ—Й—М—О –С–Р–† —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –Р–Ф –Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ–Љ —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П —Г –±–Њ–ї—М–љ—Л—Е –Р–У, –љ–Њ –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е, —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л—Е (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ–Њ–≤—В–Њ—А–љ—Л—Е –Є–љ—Б—Г–ї—М—В–Њ–≤) –Є –њ–Њ—З–µ—З–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –њ—А–Њ–≥–љ–Њ–Ј–∞ –С–ї–Њ–Ї–∞—В–Њ—А—Л –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ј–∞–љ–Є–Љ–∞—О—В –≤–∞–ґ–љ–Њ–µ –Љ–µ—Б—В–Њ —Б—А–µ–і–Є –і—А—Г–≥–Є—Е —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е —Б—В—А–∞—В–µ–≥–Є–є –≤ –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Є –њ–Њ—З–µ—З–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, —Б–Њ–µ–і–Є–љ—П—П –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М.



–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Staessen JA, Li Y, Thijs L, et al. Blood pressure reduction and cardiovascular prevention: An update including the 2003–2004 secondary prevention trials. Hypertens Res 2005; 28: 385–407.
2. Lewington S, Clarke R, Qizilbash N, et al. For the Prospective Studies Collaboration. Age–specific relevance of usual blood pressure to vascular mortality: A meta–analysis of individual data for one million adults in 61 prospective studies. Lancet 2002; 360: 1903–1913.
3. EI Fakiri F, Bruijnzeels MA, Hoes AW. Prevention of cardiovascular disease: focus on modifiable cardiovascular risk. Heart 2006; 92 (6): 741–745.
4. The Task Force for the management of arterial hypertension of the European Society of Hypertension and of the European Society of Cardiolody. 2007 Guidelines for the management of arterial hypertension. J Hypertens 2007; 25: 1105–1187.
5. Dzau V, Bernstein K, Celermaier D, et al. The relevance of tissue angiotensin– converting enzyme: manifestations in mechanistic and endpoint data. Am J Cardiol 2001; 88 (Suppl L): 1–20.
6. –Ъ–∞—А–њ–Њ–≤ –Ѓ.–Р. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–°: –њ—А–Є –≤—Л—Б–Њ–Ї–Њ–Љ —А–Є—Б–Ї–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Є–ї–Є –≤—Б–µ–Љ. –Ъ–∞—А–і–Є–Њ–ї–Њ–≥–Є—П 2005; 9: 4–10.
7. Dahl–Њf B, Devereux RB, Kjeldsen SE, et al. Cardiovascular morbidity and mortality in the Losartan Intervention for Endpoint reduction in hypertension study (LIFE): a randomized trial against atenolol. Lancet 2002; 359: 995–1003.
8. Maggioni AP, Anand I, Gottlieb SO et al. Effects of valsartan on morbidity and mortality in patients with heart failure not receiving angiotensin–converting enzyme inhibitors. J Am Coll Cardiol 2002; 40: 1414–1421.
9. Pfeffer MA, Swedberg K Granger CB, et al. Effect of candesartan on mortality and morbidity in patients with chronic heart failure: the CHARM–Overall programme. Lancet 2003; 362: 759–66.
10. Pfeffer MA, McMurray JJ, Velazquez EJ et al. Valsartan, captopril, or both in myocardial infarction complicated by heart failure, left ventricular dysfunction, or both. N Engl J Med 2003; 349: 1893–1906.
11. Scmieder RE, Hilgers KF, Schlaich MP, et al. Renin–angiotensin system and cardiovascular risk. Lancet 2007; DOI: 1016/S0140–6736(07)60242–6.
12. Viberti G, Wheeldon NM. Microalbuminuria reduction with valsartan in patients with type 2 diabetes mellitus: a blood pressure–independent effect. Circulation 2002; 106: 672–678.
13. Casas JP, Chua W, Loukogeorgakis S, et al. Effect of inhibitors of the rennin–angiotensin system and other antihypertensive drugs on renal outcomes: systematic review and meta–analysis. Lancet 2005; 366: 2026–2033.
14. Turnbull F, Neal B, Algert C, et al. Effects of different blood pressure–lowering regimens on major cardiovascular events in individuals with and without diabetes mellitus: results of prospectively designed overviews of randomized trials. Arch Intern Med. 2005; 165: 1410–1419.
15. Julius S, Kjeldsen SE, Weber M et al. Outcomes in hypertensive patients at high cardiovascular risk treated with regimens based on valsartan or amlodipine: the VALUE randomised trial. Lancet 2004; 363: 2022–2031.
16. Mochizuki S, Dahlof B, Shimizu M, et al. Valsartan in a Japanese population with hypertension and other cardiovascular disease (Jikei Heart Study) a randomized, open–label, blinded endpoint morbidity–mortality study. Lancet 2007; 369: 1431–1439.
17. The HOPE Study Investigators. Effects of an angiotensin–converting enzyme inhibitor, ramipril, on death from cardiovascular causes, myocardial infarction, and stroke in high–risk patients. N Engl J Med 2000; 342: 145–53.
18. The EUROPA investigators. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomased, double–blind, placebo–controlled, multicentre trial (the EUROPA study). Lancet 2003; 362; 782–788.
19. The ONTARGET investigators. Telmisartan, ramipril or both in patients at high risk for vascular events. N Engl J Med 2008; 358: 1547–1559.
20. The TRANSCEND investigators. Effects of the angiotensin–receptor blocker telmisartan on cardiovascular events in high–risk patients intolerant to angiotensin–converting enzyme inhibitors: a randomised controlled trial. Lancet 2008, 372: 1174–1183.
21. PROGRESS Collaborative group. Effects of a perindopril–based blood pressure lowering regimen on cardiac outcomes among patients with cerebrovascular disease. Eur Heart J 2003; 24: 475–484.
22. Yusuf S, Diener H–C, Sacco RL, et al. for the PRoFESS study group. Telmisartan to prevent recurrent stroke and cardiovascular events. N Engl J Med 2008; 359: 1225–1237..
23. Samada T, Yamada H, Dahlof B, et al. Effects of valsartan on morbidity and mortality in uncontrolled hypertensive patients with high cardiovascular risks: KYOTO HEART Study. Eur Heart J August 31, 2009: doi: 10.1093/eurheartj/ehp363.
24. Messerli FH, Bangalore S, Ruschitzka F. Angiotensin receptor blockers: baseline therapy in hypertension?. Eur Heart J August 31, 2009: doi: 10.1093/eurheartj/ehp363.








.gif)



