В настоящее время в патогенезе ишемической болезни сердца (ИБС) и инфаркта миокарда (ИМ) ведущая роль отводится дисфункции эндотелия сосудов (ДЭ). ДЭ является ключевым моментом, инициирующим атерогенез и способствующим прогрессии атеросклероза, что в конечном итоге приводит к дестабилизации атеросклеротической бляшки, ее разрыву и развитию ИМ [1]. Дисфункция эндотелия тесным образом связана с нарушениями метаболизма липидов [2,3,4,5,6,7]. Влиянию нарушений липидного обмена, в частности, воздействию окисленных липопротеидов низкой плотности (ЛПНП) на функциональное состояние эндотелия сосудов посвящено много работ. Доказано, что окисленные ЛПНП обладают высокой токсичностью, вызывают апоптоз сосудистых клеток, вазоконстрикторные реакции, то есть способствуют развитию ДЭ [8,9,10].
Установлено, что некоторые виды терапии оказывают отчетливое влияние на функциональное состояние эндотелия. При однократном воздействии хороший эффект оказался при проведении афереза ЛПНП, применении ингибиторов ангиотензинпревращающего фермента, антиоксидантов, эстрогенов, L–аргинина, и антагонистов кальциевых каналов. При хроническом применении лучший эффект на функциональное состояние эндотелия оказывали гиполипидемические препараты, в частности статины. В связи с этим цель настоящего исследования состояла в изучении функционального состояния эндотелия сосудов у больных ИБС и оценке влияния препарата симвастатин (торговое название – Симгал) на дисфункцию эндотелия у этих пациентов.
Материалы и методы
В исследование было включено 30 больных ИБС. Критериями включения в исследование были: документированная ИБС (стабильная стенокардия напряжения, постинфарктный кардиосклероз), уровень общего холестерина (ОХ) более 5,0 ммоль/л, содержание холестерина ЛПНП более 3,0 ммоль/л, концентрация триглицеридов (ТГ) сыворотки крови не более 3,5 ммоль/л.
Диагноз ИБС был верифицирован на основании анамнеза и данных велоэргометрии. Инфаркт миокарда в анамнезе был у 21 больного (70,0%). У 27 человек (90,0%) на момент исследования была стенокардия II–III функционального класса. У 25 пациентов (83,3%) сопутствующей патологией была гипертоническая болезнь. 9 больных (30,0%) на момент включения в исследование курили. Отягощенный наследственный анамнез по ИБС был выявлен у 9 человек (30,0%). Средний возраст больных на момент обследования составил 62,2±1,9 года (от 38 до 82 лет).
Забор крови проводился утром, после 12–часового голодания. После отделения форменных элементов сыворотка хранилась 1–3 дня при температуре +4°С. Концентрацию ОХ, ТГ, ХС ЛПВП (после осаждения из плазмы крови ХС ЛПНП и ХС ЛПОНП) определяли ферментативным методом на автоанализаторе ФП–901.
Фракции холестерина ЛПНП и ЛПОНП определялись на основании расчетных формул («Дислипопротеинемии и ишемическая болезнь сердца», 1980) в ммоль/л.
Коэффициент атерогенности (КА) рассчитывался по формуле:
КА = (OX - XC ЛПВП) / XC ЛПВП
На момент включения в исследование средние значения уровня общего холестерина составили 6,0±0,1 ммоль/л, холестерина ЛПНП 4,0±0,1 ммоль/л, триглицеридов 1,8±0,1 ммоль/л, холестерина ЛПВП 1,6±0,3 ммоль/л, холестерина ЛПОНП 0,8±0,05 ммоль/л.
Всем больным также определялись следующие показатели, отражающие функциональное состояние эндотелия сосудов [11,12,13]: количество десквамированных эндотелиоцитов в крови (методом Hladovec J., 1978), концентрация фактора Виллебранда методом иммуноферментного анализа с использованием моноклональных антител (Торопов Б.Г. и соавт., 1990), уровень фибриногена плазмы крови гравиметрическим методом (Петрищев Н.Н., Папаян Л.П., 1999), эндотелийзависимая вазодилатация по результатам пробы с реактивной гиперемией (Celermajer D.S. et al., 1992).
При оценке показателей функционального состояния эндотелия у больных ИБС до терапии симвастатином было установлено увеличение количества циркулирующих в крови десквамированных эндотелиоцитов до 7,5±1,4 кл/100 мкл. У здоровых людей по данным J. Hladovec (1978) количество циркулирующих в крови десквамированных эндотелиоцитов составляет от 2 до 4 кл на 100 мкл.
Известно, что у здоровых людей прирост диаметра плечевой артерии должен быть более 10%. Если данный показатель составляет менее 10%, это свидетельствует о наличии ДЭ [14]. У пациентов, включенных в исследование, этот показатель был снижен и составлял 8,3±1,6%. Более того, у 10% больных при проведении пробы с реактивной гиперемией определялась парадоксальная вазоконстрикторная реакция, которая свидетельствует о более выраженной дисфункции эндотелия. Вероятно, наличие вазоконстрикторной реакции связано с тем, что в условиях нарушения липидного обмена происходит снижение выработки и избыточное разрушение одного из основных вазодилататоров – оксида азота. Таким образом, наблюдается дисбаланс между синтезом вазодилататорных и вазоконстрикторных веществ, в пользу последних. С другой стороны, установлено, что у больных ишемической болезнью сердца повышена активность симпатической нервной системы, что увеличивает чувствительность сосудистой стенки к прессорным воздействиям.
Уровень фибриногена у пациентов, включенных в исследование, был несколько выше нормы и составил 4,4±0,3 г/л. По данным Петрищева Н.Н. и Папаян Л.П. (1999), уровень этого показателя в норме колеблется от 2 до 4 г/л.
Содержание фактора Виллебранда было в пределах нормальных значений 109,1±8,2%.
Все больные получали 20–40 мг симвастатина (препарат Симгал; производитель – компания Айвэкс А.С.) в течение 12 недель.
Полученные результаты обрабатывались с помощью методов математической статистики, представленных в пакетах Statisics ver. 5.5. и SPSS ver. 10.0.
Результаты
За 6 недель лечения Симгалом у 21 больного были достигнуты целевые уровни холестерина ЛПНП (менее 3,0 ммоль/л), у 7 больных отмечалось снижение холестерина ЛПНП без достижения целевого уровня. Этим больным доза препарата была увеличена в 2 раза (40 мг). Один пациент выведен из исследования в связи с отказом от дальнейшего приема препарата.
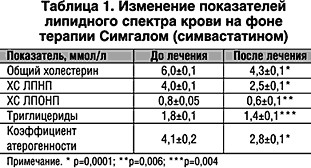
Через 12 недель терапии Симгалом у 22 больных (75,9%) были достигнуты целевые уровни холестерина ЛПНП. У 6 больных (20,6%) терапия была частично эффективна (уровень холестерина ЛПНП снизился более чем на 10%) (табл. 1). Только у одного больного терапия оказалась неэффективной.
Мы проанализировали динамику показателей, отражающих функциональное состояние эндотелия сосудов в 2–х группах больных: в группах с эндотелийзависимой вазодилатацией плечевой артерии (ЭЗВД) менее 10% и более или равной 10%. Показатели липидного спектра в этих группах до начала и через 12 недель терапии Симгалом были сопоставимы. Вместе с тем через 12 недель приема препарата эндотелийзависимая вазодилатация в значительно большей степени возросла в группе больных, у которых до начала терапии ЭЗВД плечевой артерии при пробе с реактивной гиперемией была менее 10%, т.е. дисфункция эндотелия была выражена в большей степени (табл. 2).

В данной работе у 30 мужчин, больных ИБС, были оценены показатели липидного спектра сыворотки крови и функционального состояния эндотелия сосудов до и после 12–недельного курса терапии препаратом Симгал (симвастатин). Выбор данного препарата был продиктован тем, что гиполипидемическая терапия оказывает отчетливое влияние на функциональное состояние эндотелия, а также появлением в литературе данных о том, что симвастатин в большей степени, чем другие статины, в частности, аторвастатин, увеличивает уровень холестерина ЛПВП [15,16]. Кроме того, дополнительной задачей было подтверждение клинической эффективности этого препарата, которое особенно актуально при наличии у Симгала такого важного преимущества, как доступная (по сравнению с большинством других статинов) стоимость лечения.
В данной работе у 30 мужчин, больных ИБС, были оценены показатели липидного спектра сыворотки крови и функционального состояния эндотелия сосудов до и после 12–недельного курса терапии препаратом (симвастатин). Выбор данного препарата был продиктован тем, что гиполипидемическая терапия оказывает отчетливое влияние на функциональное состояние эндотелия, а также появлением в литературе данных о том, что симвастатин в большей степени, чем другие статины, в частности, аторвастатин, увеличивает уровень холестерина ЛПВП [15,16]. Кроме того, дополнительной задачей было подтверждение клинической эффективности этого препарата, которое особенно актуально при наличии у Симгала такого важного преимущества, как доступная (по сравнению с большинством других статинов) стоимость лечения.У больных, вошедших в исследование, трехмесячный курс терапии Симгалом сопровождался значительным улучшением липидного состава сыворотки крови. Так, уровень общего холестерина снизился на 28,4%, уровень холестерина ЛПНП снизился на 37,5%.
Известно, что механизм действия статинов связан с обратимым ингибированием ГМГ–КоА–редуктазы – ключевого фермента эндогенного биосинтеза холестерина. В результате этого на поверхности гепатоцитов появляется дополнительное количество ЛПНП–рецепторов и катаболизм ХС ЛПНП усиливается [17]. Главный гиполипидемический эффект статинов выражается в снижении общего ХС за счет ХС ЛПНП, что обосновано при лечении первичной гиперхолестеринемии IIа типа и других типов гиперхолестеринемий с преимущественным повышением ХС ЛПНП в плазме крови (комбинированная ГЛП, ремнантная ГЛП III типа, полигенная гиперхолестеринемия).
Действие статинов на содержание ТГ зависит от исходного уровня последних. При исходных значениях ТГ более 2,8 ммоль/л снижение их уровня может составить 22–45%. Этот эффект связан как с усилением катаболизма триглицериднасыщенных частиц, так и с угнетением синтеза апобелков, являющихся субстратом для сборки ЛПОНП (содержание ТГ в ЛПОНП составляет до 55%).
В данном исследовании терапия симвастатином (Симгалом) сопровождалась достоверным снижением уровня ТГ (на 22,2%).
Многие годы считалось, что гиполипидемическая терапия приводит к регрессии атеросклероза за счет снижения уровней липидов. Результаты первых крупных исследований статинов с использованием ангиографии (MARS, CCAIT, MAAS, PLAC–1), предпринятых для оценки влияния статинов на прогрессирование коронарного атеросклероза, оказались парадоксальными [18,19,20,21]. Терапия статинами по сравнению с группой контроля в среднем сопровождалась небольшим, но достоверным замедлением прогрессирования стеноза коронарных артерий. Однако небольшое (0,03–0,06 мм) отличие в изменении диаметра просвета сосуда не могло объяснить значительного (на 24–42%) снижения кардиальных событий.
В проспективных плацебо–контролируемых исследованиях с применением статинов (4S, CARE, LIPID, WOSCOPS, AFCAPS) было установлено, что значительное (на 25–30%) снижение уровня ХС ЛПНП сопровождалось достоверным снижением фатальных и нефатальных кардиальных событий без увеличения или со снижением общей смертности [22,23,24,25,26].
Грацианский Н.А. (1997) в обзоре, посвященном анализу эффективности статинов у больных ИБС, пишет о том, что клинический эффект статинов (в частности, уменьшение риска развития инфаркта миокарда) наступает быстрее, чем достигается стабилизация атеросклеротической бляшки по данным повторных ангиографий [1].
Одним из оснований для такого мнения явилась относительная быстрота наступления клинического эффекта статинов: через 6 месяцев после начала лечения в WOSCOPS и через 7 месяцев для фатальных и нефатальных ИМ в LIPID. В более мелких исследованиях уменьшение числа различных «коронарных» событий среди больных, получавших статины, по сравнению с контролем происходило еще быстрее – через 6 и даже 3 месяца (PLAC). Считается, что само по себе снижение уровней липидов сказалось бы на клиническом течении заболевания существенно позже. Это предположение основывается на результатах исследования POSCH. В данном исследовании снижение уровней ХС на 23% и ХС ЛПНП – на 38% у больных ИБС с гиперлипидемией было достигнуто без лекарственного вмешательства с помощью хирургического выключения из пищеварения части тонкой кишки. Только через 10 лет наблюдения снижение ХС и ХС ЛПНП в этом исследовании сопровождалось уменьшением числа летальных исходов от ИБС на 35%.
С чем связано быстрое улучшение функции эндотелия при приеме статинов? Исходя из анализа данных литературы, наиболее вероятной причиной быстрого эффекта этих препаратов является не только снижение уровней ОХ и холестерина ЛПНП, но и так называемые нелипидные или плеотропные эффекты.
Быстрый клинический эффект статинов связан, прежде всего, со стабилизацией атеросклеротической бляшки, в том числе за счет улучшения функционального состояния эндотелия сосудов, с уменьшением вероятности спастических реакций, с влиянием статинов на гемостаз и процессы воспаления. Причем стабилизация атеросклеротической бляшки происходит при снижении уровня холестерина ЛПНП не менее чем на 20–25% (Грацианский Н.А., 1997) [1].
Основным механизмом, лежащим в основе изменения реакции сосудов на различные стимулы, включая реактивную гиперемию, у больных ИБС принято считать сниженное содержание NO, выделяемого эндотелиальными клетками или быструю инактивацию его в результате высокого содержания супероксидных анионов [27,28,29,30]. Помимо этого, супероксидные анионы могут подавлять активность NO–синтазы [31], угнетать выработку одного из кофакторов этого фермента, способствуя, тем самым, снижению выработки NO [32,33].
Установлено, что статины, в том числе и симвастатин, способствуют высвобождению NO за счет активации NO–синтазы [34]. Доказано, что применение статинов сопровождается снижением уровней провоспалительных цитокинов [35] и С–реактивного белка [36], снижением количества макрофагов и секреции ими металлопротеиназ и тканевого фактора [37], подавлением накопления эфиров холестерина в макрофагах и образования пенистых клеток [38].
Кроме того, известно, что при гиперхолестеринемии имеется резистентность тромбоцитов к ингибирующему действию оксида азота. Было установлено, что статины уменьшают эту резистентность тромбоцитов [39].
Все вышеперечисленные эффекты статинов приводят к улучшению функционального состояния эндотелия и способствуют стабилизации ИБС.
Снижение ЭЗВД плечевой артерии у больных ИБС было выявлено в работах многих исследователей [40,41]. O’Driscoll и соавт. (1997) отметили улучшение ЭЗВД плечевой артерии уже через 4 недели лечения симвастатином.
Одним из маркеров повреждения эндотелия является степень его десквамации, которая оценивалась по количеству циркулирующих (десквамированных) эндотелиоцитов в крови (Hladovec J., 1978). У мужчин, перенесших ИМ, выявлено увеличение числа циркулирующих в крови десквамированных эндотелиоцитов по сравнению со здоровыми людьми. Подобные результаты были получены и в работах других исследователей [42]. Это дает возможность рассматривать увеличение числа циркулирующих эндотелиальных клеток как показатель степени повреждения сосудистой стенки [43].
У вошедших в настоящее исследование больных ИБС были выявлены признаки дисфункции эндотелия сосудов: снижение эндотелийзависимой вазодилатации плечевой артерии; у части больных определялись вазоспастические реакции при проведении пробы с реактивной гиперемией. По мнению многих авторов, появление вазоспастических реакций при проведении пробы с реактивной гиперемией отражает более тяжелое нарушение функции эндотелия [44,45]. Существует обоснованное мнение, что нарушение сосудодвигательной функции в виде вазоспазма у больных с фиксированной коронарной обструкцией может играть решающую роль в развитии острых коронарных синдромов [46].
По нашим данным, трехмесячная терапия симвастатином у больных ИБС сопровождалась достоверным увеличением ЭЗВД плечевой артерии, снижением количества циркулирующих в крови десквамированных эндотелиоцитов, уровней фибриногена и фактора Виллебранда.
Заключение
1. Применение Симгала (симвастатина) у больных ИБС оказывает выраженное гиполипидемическое действие.
2. Прием Симгала приводит к значительному улучшению функционального состояния эндотелия сосудов. Причем лучший эффект в плане функционального состояния эндотелия сосудов наблюдается у пациентов с более выраженной дисфункцией эндотелия.
1. Грацианский Н. А. Нестабильная стенокардия – острый коронарный синдром. III. Предупреждение обострений ишемической болезни сердца. Статины и антибиотики // Кардиология. – 1997. – Т. 37, № 11. – С. 4 – 17.
2. Celermajer D. S., Sorensen K. E., Gooch V. M. et al. Non–invasive detection of endothelial dysfunction in children and adults at risk of atherosclerosis // Lancet. – 1992. – Vol. 340, № 8828. – Р. 1111 –1115.
3. Celermajer D. S. Endothelial dysfunction: does it matter? Is it reversible? // J. Am. Coll. Cardiol. – 1997. – Vol. 30, № 3. – Р. 325 – 333.
4. Vita J.A., Treasure C.B., Nabel E.G. et al. Coronary vasomotor responses to acetylcholine relate to risk factors for coronary artery disease. //Circulation. 1990; 81: pp. 491–497.
5. Casino P.R., Kilcoyne C.M., Quyyumi A.A., Hoeg J.M., Panza J.A. The role of nitric oxide in endothelium–dependent vasodilation of hypercholesterolemic patients. //Circulation. 1993, 88: pp. 2541–2547.
6. Seiler C., Hess O.M., Buechi M., Suter T.M., Krayenbuehl H.P. Influence of serum cholesterol and other risk factors on vasomotion of angiographically normal coronary arteries. //Circulation. 1993; 88(part 1): pp. 2139–2148.
7. Sorensen K.E., Celenmajer D.S., Georgakopoulos D. Impairment of endothelium– dependent dilation is an early event in children with familial hypercholesterolemia an is related to the lipoprotein level. //J Clin Invest. 1994; 93: pp. 50–55.
8. Berliner J.A., Navab M., Fogelman A.M. Atherosclerosis: basic mechanisms. Oxidation, inflammation and genetics. //Circulation 1995; 91: pp. 2488–2496.
9. Siow R.C.M., Redley K.C., Richards J.P., Leake D.S., Mann G.E. Vitamin C protects human vascular smooth mucle cells against apoptosis induced by moderatery oxidized LDL containing high levels of lipid hydroperoxides. //Atheroscler Tromb Vasc Biol. 1999; 19: pp. 2387–2394. 65.
10. Shoji T., Nishizawa J., Fukumoto M., Shimamura K. Inverse relationsip between circulating oxidized low density lipoprotein and anti–oxLDL antibody levels in healthy subjects. //Atherosclerosis. 2000; 148: pp. 171–177.
11. Торопова Б. Г., Горностаев В. С., Данилов А. О. и др. Иммуноферментный анализ фактора Виллебранда с использованием моноклональных антител // Лабор. дело. – 1990. – № 12. – С. 52 – 55.
12. Гемостаз: Физиологические механизмы, принципы диагностики основных форм геморрагических заболеваний / Под ред. Н. Н. Петрищева, Л. П. Папаян; Санкт–Петерб. гос. мед. ун–т им акад. И. П. Павлова, Рос. НИИ гематологии и трансфузиологии. – СПб., 1999. – С. 22.
13. Hladovec J. Circulating endothelial cells as a sign of vessel wall lesions // Physiol. Bohemoslov. – 1978. – Vol. 27, № 2. – Р. 140 – 144.
14. Vogel R. A. Coronary risk factors, endothelial function, and atherosclerosis: a review // Clin. Cardiol. – 1997. – Vol. 20, № 5. – Р. 426 – 432.
15. Branchi A., Fiorenza A. M., Torri A. et al. Effects of low doses of simvaststin and atorvastatin on high–density lipiprotein cholesterol levels in patients with hypercholrsterolemia // Clin. Ther. – 2001. – Vol. 23, № 6. – Р. 851– 857.
16. Geiss H. C., Otto C., Schwandt P., Parhofer K. G. Effect of atorvastatin on low–density lipiprotein subtypes in patients with different forms of hyperlipoproteinemia and control subjects // Metabolism. – 2001. – Vol. 50, № 8. – Р. 983 – 988.
17. Сусеков А.В. Обоснование повышения доз статинов в клинической практике // Терапевтический архив. 2001, –Том 73, – №4, с. 76–80.
18. Blakenhorn D.H., Azen S.P., Kramsch D.M. et al. Coronary angiographic changes with lovastatin therapy. The Monitored Atherosclerosis Regression Study (MARS). The MARS Research Group.// Ann Intern Med 1993; Vol. 119, № 10. – P. 969–976.
19. MAAS Investigators. Effect of simvastatin on coronary atheroma: the Multicentre Anti– atheroma Study (MAAS). Lancet. 1994; 344:633–638.
20. Blakenhorn D. H., Azen S. P., Kramsch D. M. et al. Coronary angiographic changes with lovastatin therapy. The Monitored Atherosclerosis Regression Study (MARS). The MARS Research Group // Ann. Intern. Med. – 1993. – Vol.119, № 10. – P. 969 – 976.
21. Pitt B., Mancini G.B.J., Ellis S.G. et al. Pravastatin limitation of Atherosclerosis in the Coronary Arteries (PLAC–1); reduction in atherosclerosis progression and clinical events. J Am Col Cardiol 1995; 26:133–1139.
22. Downs J.R., Clearfield M., Weis S. et al., et al., for the AFCAPS/TexCAPS Research Group. Primary prevention of acute coronary events with lovastatin in men and women with average cholesterol levels: results of AFCAPS/TexCAPS. JAMA. 1998; 279: 1615–1622.
23. Scandinavian Simvaststin Survival Study Group. Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: the Scandinavian Simvaststin Survival Study (4S). Lancet. 1994; 344: 1383–1389.
24. Long–term Intervention with Pravastatin in Ischaemic Disease (LIPID) Stttudy Group. Prevention of cardiovascular events and death with pravastatin in patients with coronary heart disease and a broad range of initial cholesterol levels. N Engl J Med 1998; 339: 1349–1357.
25. Sacks F.M., Preffer M.A., Moye L.A. et al. For the Cholesterol and Recurrent Events Trial Investigators. The effect of pravastatin on coronary events after myocardial infarction in patients with average cholesterol levels. N Engl J Med. 1996; 335: 1001–1009.
26. Shepard J., Cobb S.M., Ford I. et al., for the West of Scotland Coronary Prevention Study Group. Prevention of coronary heart disease with pravastatin in men with hypercholesterolemia. N Engl J Med 1995; 333: 1301–1307.
27. Сорокин Е. В., Карпов Ю. А. Статины, эндотелий и сердечно–сосудистый риск // Рус. мед. журн. – 2001. – Т. 9, № 9. – С. 352 – 353.
28. Ohara Y., Peterson T. E., Harrison D. G. Hypercholesterolemia increases endothelial superoxide anion production // J. Clin. Invest. – 1993. – Vol. 91, № 6. – Р. 2546 – 2551.
29. Quyyumi A. A. Endothelial function in health and disease: new insights into the genesis of cardiovascular disease //Am. J. Med. – 1998. – Vol. 105, № 1A. – P. 32S – 39S.
30. Feron O., Dessy C., Moniotte S. et al. Hypercholesterolemia decreases nitric oxide production by promoting the interaction of caveolin and endothelial nitric oxide synthase // J. Clin. Invest. – 1999. – Vol. 103, № 6. – Р. 897 – 905.
31. Rubanyi G. M., Vanhoutte P. M. Superoxide anions and hyperoxia inactivate endothelium–derived relaxing factor // Am. J. Physiol. – 1986. – Vol. 250, № 5, pt. 2. – Р. H822 – 827.
32. Schini–Kerth V. B., Vanhoutte P. M. Nitric oxide synthases in vascular cells // Exp. Physiol. – 1995. – Vol. 80, № 6. – Р. 885 – 905.
33. Harrison D. G., Sayegh H., Ohara Y. et al. Regulation of expression of the endothelial cell nitric oxide synthase // Clin. Exp. Pharmacol. Physiol. – 1996. – Vol. 23, № 3. – Р. 251 – 255.
34. Dobrucki L. W., Kalinowski L., Dobrucki I. T., Malinski T. Statin–stimulated nitric oxide release from endothelium // Med. Sci. Monit. – 2001. – Vol.7, № 4. – Р. 622 – 627.
35. Rosensen R.S., Tangney C.C., Casey L.C. Inhibition of pro–inflammatory cytocine production by pravastatin. Laancet. 1999;353: 983–984.
36. Ridker P.M., Rifai N., Pfeffer M.A. et al. Inflammation, pravastatin, and the risk of coronary events after myocardial infarction in patients with average cholesterol levels. Circulation. 1998;98: 839–844.
37. Aikawa M., Rabkin E., Sugiyama S., Libby P. An HMG–KoA reductase inhibitor, cerivaststin, suppresses growth of macrophages expressing matrix metalloproteinases and tissue factor in vivo and in vitro. Circulation. 2001; 103: 276–283.
38. Keidar S., Aviram M., Maor I. et al. Pravastatin inhibits cellular cholesterol synthesis and increases low density lipoprotein receptor activity in macrophages: in vitro and in vivo studies. Br J Clin Pharmac 1994; 39: 513–519.
39. Chirkov Y. Y., Hons A. S. H., Willoughby S. R. et al. Stable angina and acute coronary syndromes are associated with nitric oxide resistance in platelets // J. Am. Coll. Cardiol. – 2001. – Vol. 37, № 7. – Р. 1851 – 1857.
40. Lieberman E. H., Gerhard M. D., Uehata A. et al. Flow–induced vasodilatation of the human brachial artery is impaired in patients < 40 years of age with coronary artery disease //Am. J. Cardiol. –1996. – Vol. 78, № 11. – Р. 1210 – 1214.
41. Rubenfire M., Cao N., Smith D. E., Mosca L. Usefulness of brachial artery reactivity to isometric handgrip exercise in identifying patients at risk and with coronary artery disease //Am. J. Cardiol. – 2000. – Vol. 86, № 11. – Р. 1161–1165.
42. Bory M., Sampol J., Yvorra S. et al. Detection des cellules endotheliales circulantes: un nouveau test diagniostique de l` angor de repos // Arch. Mal. Coeur. Vaiss. – 1995. – Vol. 88, № 12. – Р. 1827 – 1831.
43. Vanhoutte P. M. How to assess endothelial function in human blood vessels // J. Hypertens. – 1999. – Vol. 17, № 8. – Р. 1047 – 1058.
44. Nabel E. G., Selwyn A. P., Ganz P. et al. Large coronary arteries in humans are responsive to changing blood flow: an endothelium–dependent mechanism that fails in patients with atherosclerosis // J. Am. Coll. Cardiol. – 1990. – Vol.16, № 2. – Р. 349 – 356.
45. Yeung A. C., Vekshtein V. I., Krantz D. S. et al. The effect of atherosclerosis on the vasomotor response of coronary arteries to mental stress // N. Engl. J. Med. – 1991. – Vol. 325, № 22. – Р. 1551 – 1556.
46. Noll G., Lusher T.E. The endothelium in acute coronary syndromes // Eur. Heart J. – 1998. – Vol. 19, Suppl. C: – Р. C30 – C38.












