Что общего у промышленных инцидентов в Бхопале, Чернобыле и Три-Майл-Айленде?
Все это произошло ночью (случайная находка в Интернете)
Введение
Медицина доступна пациентам круглосуточно, без выходных, и врачи постоянно работают много часов днем и ночью. При судебно-медицинской оценке ошибка переутомленного и уставшего врача все еще остается ошибкой. Истощение и усталость — не защита от неправильного принятия решений. Многие исследования человеческой работоспособности и умственных возможностей показали значительные спады между 22:00 и 06:00, а риск травм в ночную смену на 30% выше, чем в утреннюю. Усталость при работе в течение 20–25 ч без сна и без отдыха в течение дня перед началом смены снижает психомоторные характеристики до состояния человека с концентрацией алкоголя в крови 0,1% [1]. Ночная работа требует от врачей бодрствования и бдительности в тот период, когда они физиологически запрограммированы на сон.
Хорошо известно, что усталость снижает работоспособность [2]. Усталость — это риск возникновения проблем со здоровьем для врачей, работающих в ночное время, особенно с учетом того, что метаболизм и бдительность самые низкие между 03:00 и 05:00. Переход с ночных смен на дневные, а также продолжительность смены (ночной или дневной) также могут способствовать утомлению. Известно, что недостаток сна снижает способность рассуждать и концентрировать внимание. Даже после окончания ночной смены остаются негативные последствия усталости, включая снижение способности принимать решения и нарушение памяти. В ночную смену человек обычно работает против своих внутренних биологических часов, может страдать от сонливости, вызванной рассинхронизацией внутренних циркадных ритмов и нарушением режима сна и бодрствования.
Основная причина нарушений при сменной работе — снижение количества и качества сна. Многие биологические функции, помимо сна, регулируются циркадными ритмами, и их характеристики могут различаться у разных людей. Циркадные предпочтения определяются внутренними факторами (например, генетическими особенностями, уровнем кортизола и мелатонина) и факторами окружающей среды (например, социальными привычками, циклом света/темноты, временем года) [3]. У людей циркадная система состоит из нескольких осцилляторов, распределенных по всему организму, и центрального водителя ритма в супрахиазматическом ядре гипоталамуса, который координирует всю систему. Хроническое нарушение циркадного ритма связано со множеством рисков для здоровья, включая нарушение сна, желудочно-кишечные расстройства и сердечно-сосудистые заболевания [4, 5]. Такие риски для здоровья часто усугубляются снижением уровня активности [6]. Частичная депривация сна нарушает деятельность ЦНС — от основных функций регуляции аппетита и температуры до более важных когнитивных функций, негативно сказывается на бдительности и быстроте реакций [7]. Более того, медики, работающие в ночную смену, часто жалуются на повышенную утомляемость [8]. Это ассоциируется с увеличением числа непреднамеренных происшествий, таких как производственные травмы, и повышенным риском для здоровья как медицинских работников, так и пациентов [9].
Есть сообщения о взаимосвязи между ограничением/лишением сна, способностью генерировать мышечную силу и усталостью [10], снижением субмаксимальной и максимальной мышечной силы после недосыпания [11, 12]. Группа итальянских исследователей выявила нарушение нервно-мышечной функции у медицинских работников независимо от их графика ночных дежурств. Нервно-мышечные изменения, а именно снижение максимального уровня мышечной активации, выходной силы мышц-сгибателей пальцев, раннее и выраженное проявление миоэлектрической усталости и низкая мышечная мелкая моторика, регистрировались на фоне уменьшения количества сна и ухудшения его качества. Интересно, что процентное снижение максимальной активации и силы мышц коррелировало с параметрами сна, описывающими общее время сна и его качество [13].
Ряд исследований выявили связь между недосыпанием и патологическими признаками болезни Альцгеймера, для которой пожилой возраст и наличие аллели аполипопротеина E ε4 являются одними из самых сильных факторов риска [13]. Американское поперечное исследование показало, что взрослые, сообщавшие об уменьшении продолжительности сна, имели более высокие концентрации амилоида β в головном мозге [14]. Кроме того, нарушение сна и его недостаток были связаны с увеличением заболеваемости деменцией [15, 16]. Датское когортное исследование с участием 28 731 медсестры, которое изучало влияние сменной работы на смертность от конкретных причин, показало высокую корреляцию чередования дневной, вечерней или ночной смены со смертностью от болезни Альцгеймера и деменции, а также повышенную смертность от сердечно-сосудистых заболеваний и сахарного диабета [17]. Результаты шведского исследования по изучению связи между сменной работой и случайной деменцией в двух популяционных когортах из Шведского реестра близнецов (STR), включающего 36 536 человек, показало, что сменная работа, в т. ч. ночная, в среднем возрасте была в значительной степени связана с увеличением заболеваемости деменцией в более позднем возрасте. Кроме того, повышенный риск деменции коррелировал с длительным стажем сменной работы [18].
«Аммиак, одновременно и свидетель, и актер, сам является причиной утомления», — подчеркивал профессор P. Vanuxem [19]. Исходя из вышенаписанного, мы сформулировали гипотезу, что у медицинских работников, которые часто дежурят, на фоне переутомления, астении и мышечных изменений может возникнуть гипераммониемия.
Гипераммониемия формируется под воздействием различных факторов, ее наиболее распространенные причины связаны с нарушениями работы печени. Этиология ее сложна, и исследователи продолжают изучать этот феномен. Патофизиологические механизмы нецирротической гипераммониемической энцефалопатии также являются многофакторными. Несмотря на редкость диагноза, эта патология заслуживает изучения [20]. Русский ученый профессор И.П. Павлов с коллегами впервые описали связь между аммиаком и печеночной энцефалопатией еще в 1893 г., но подробное исследование изменений биохимии аммиака при болезнях печени началось в 1950-х годах [21, 22]. Несмотря на многочисленные исследования, многогранная патофизиология гипераммониемии, в т. ч. роль аммиака, остается недостаточно понятной и сегодня [23, 24].
Гипераммониемия считается основной причиной снижения уровня аминокислот с разветвленной цепью — валина, лейцина и изолейцина. В исследовании M. Holecek et al. [25] изучали влияние аммиака на уровень аминокислот с разветвленной цепью и белковый обмен в различных типах скелетных мышц. Аммиак также вызывал значительное увеличение концентрации глутамина в скелетных мышцах. Гипераммониемия непосредственно влияла на метаболизм аминокислот с разветвленной цепью в скелетных мышцах, что приводило к снижению их уровня во внеклеточной жидкости. Эффект был связан с активированием синтеза глутамина, увеличением окисления аминокислот с разветвленной цепью и снижением их содержания в мышцах. Влияние аммиака было более выраженным в мышцах с высоким содержанием белых волокон, которые выполняют быструю и высокоинтенсивную работу.
Недавние исследования выявили еще несколько механизмов формирования саркопении вследствие гипераммониемии. Скелетные мышцы становятся основным органом метаболизма аммиака, что приводит к истощению субстратов данного метаболизма и снижению мышечной массы [26]. Миостатин является мощным ингибитором аутокринного роста производства миоцитов, он ингибирует рост мышц и уменьшает мышечную массу при гипераммониемии [27]. Гипераммониемия индуцирует аутофагию, посредством которой поврежденные белки расщепляются или перерабатываются для поддержания клеточной функции [28]. J. McDaniel et al. [29] представили непосредственные доказательства того, что гипераммониемия снижает силу скелетных мышц и усиливает мышечное утомление, приводя к выраженной мышечной дисфункции. Относительная значимость каждого из этих новых механизмов функциональных и органических нарушений мышечной системы при гипераммониемии пока не ясна. Однако совокупные данные подчеркивают необходимость выявления и минимизации влияния аммиака не только на когнитивные функции, но и на профилактику и лечение саркопении и мышечной дисфункции [30]. Эти механизмы изучались у пациентов с циррозом печени, но гипераммониемия, особенно латентная, может возникнуть у людей и без серьезной патологии печени. Длительная минимальная гипераммониемия может быть связана с нейродегенеративными заболеваниями, такими как болезнь Альцгеймера или болезнь Паркинсона [31]. Поэтому поддержание низких уровней содержания аммиака в крови будет важно не только для лечения гипераммониемии, но также для предотвращения или замедления развития нейродегенеративных заболеваний.
Цель исследования: оценить степень астении и когнитивных нарушений, уровень аммониемии, а также изучить влияние L-орнитина-L-аспартата (LOLA) при гипераммониемии у часто дежурящих медицинских работников городской больницы скорой помощи.
Материал и методы
Под наблюдением находился 31 врач (12 женщин и 19 мужчин) терапевтического и хирургического профиля в возрасте от 22 до 45 лет (средний возраст 32,29±6,11 года), без вредных привычек. Индекс массы тела составил 25,27±3,93 кг/м2. Все врачи работали в дневную смену и имели 8–12 ночных дежурств в месяц. В исследование не включали лиц с хроническими заболеваниями легких, сердечно-сосудистой системы, органов пищеварения, эндокринной системы, онкологическими заболеваниями.
У всех врачей до и после дежурства исследовали аммониемию экспресс-методом (PocketChem BA PA-4140: норма аммиака в крови 15–45 мкг/дл), предлагали пройти тест связи чисел и заполнить субъективную шкалу оценки астении (МFI-20), в которой в норме общее количество баллов не должно превышать 20–30 [32].
Восемь врачей, имевших самые высокие значения аммиака в крови, в течение следующего дежурства принимали 3 саше LOLA (Гепа-Мерц, «Мерц Фарма ГмбХ и Ко. КГаА», Германия), после дежурства у них снова исследовали уровень аммиака крови, и они вновь проходили тест и заполняли шкалу МFI-20.
Обработку данных проводили с помощью пакета прикладных программ Statistica 10.0. Количественные показатели представлены в виде среднего значения и стандартного отклонения, качественные — в виде частот (процентов). При анализе средних значений количественных показателей в группах оценивали соответствие фактического распределения показателя нормальному распределению с помощью критерия Пирсона. Для оценки различий количественных показателей использовали параметрические критерии: при двух группах сравнения — t-критерий Стьюдента. Анализ различий частот в сравниваемых группах проводили с помощью критерия χ2 Пирсона. При количестве наблюдений менее 10 в какой-либо ячейке таблицы сопряженности применяли критерий Йетса. Критический уровень значимости нулевой статистической гипотезы был принят равным 0,05.
Исследование проведено в соответствии с принципами Хельсинкской декларации Всемирной медицинской ассоциации (в редакции 2000 г. с разъяснениями, данными на Генеральной ассамблее ВМА, Токио, 2004), правилами качественной клинической практики Международной конференции по гармонизации (ICH GCP), этическими принципами, изложенными в Директиве Европейского союза 2001/20/ЕС и требованиями национального российского законодательства. Протокол исследования одобрен комитетом по этике ФГБОУ ВО КемГМУ Минздрава России. Все врачи подписали информированное согласие на участие в исследовании.
Результаты и обсуждение
В данных врачей разного профиля (хирурги и терапевты), а также женщин и мужчин статистически значимых различий не выявлено, поэтому при статистической обработке материала отдельные подгруппы не выделяли.
При измерении аммониемии до дежурного дня (утром натощак) обратило на себя внимание то, что почти у всех врачей был повышен уровень аммиака в капиллярной крови. Все доктора, кроме работы днем (часто более 8 ч), еще дежурили 2–3 раза в неделю, поэтому у них не было возможности полноценно отдохнуть и восстановиться, следствием чего, вероятно, стала гипераммониемия. Такая же ситуация наблюдалась и с результатами тестирования по шкале астении МFI-20: полученные данные указывали на наличие астении у подавляющего большинства участников наблюдения.
Как видно из таблицы 1 и рисунка 1, выраженность гипераммониемии после дежурства весьма разнилась. Мы отметили тенденцию: чем выше ИМТ (причем у мужчин за счет мышечной массы), тем выше аммониемия. Например, у врача 26 лет с ИМТ 31,2 кг/м2 уровень аммиака в крови был более 400 мкг/дл и до, и после дежурства, уровень астении — 30 баллов до дежурства и 38 — после, а тест связи чисел он заполнял за 26 с без динамики. Пока мы не можем объяснить данный феномен.

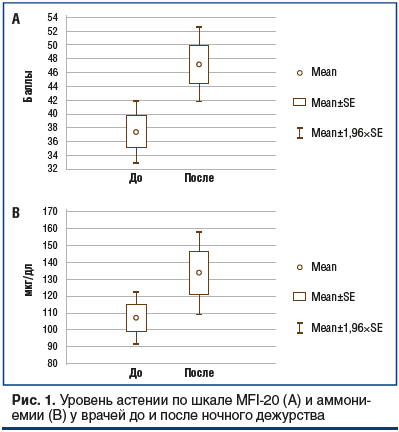
Врачи, которые принимали LOLA в течение следующего дежурства, продемонстрировали показатели, которые представлены в таблице 2 и на рисунке 2.
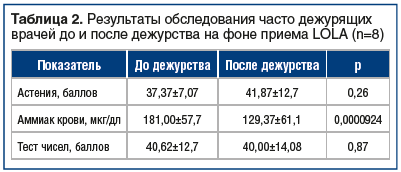
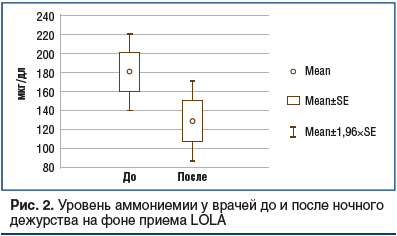
Таким образом, мы получили статистически значимые различия по уровню аммониемии у врачей, работающих в дневную смену, ночную смену и далее опять в дневную (34–36 ч) без отдыха на фоне приема LOLA 9 г в 3 приема.
Заключение
Сложный график работы медиков по разным причинам — дефицит кадров, желание больше заработать и т. п. — приводит к серьезным нарушениям здоровья. Такая работа обусловливает нарушение циркадных ритмов, ускоряет развитие различных заболеваний, таких как сердечно-сосудистые, сахарный диабет, деменция, приводит к ранней смерти. При этом у этих медиков никогда не исследовался в динамике на фоне работы уровень аммониемии.
Гипераммониемия, даже минимальная, при длительном течении наносит организму серьезный вред, в первую очередь на уровне головного мозга, приводя к серьезным когнитивным и двигательным нарушениям, раннему формированию деменции и болезни Альцгеймера [32]. Гипотетически мы можем предположить, что во время принудительного бодрствования возникает повышенная потребность в нейротрансмиттерах, отвечающих за этот процесс, — глутамине и глутамате, которые напрямую связаны с эндогенным аммиаком. Однако в имеющейся литературе прямого подтверждения этой гипотезе мы не нашли.
В настоящем клиническом наблюдении мы впервые обнаружили повышенный уровень аммиака в крови у врачей различных специальностей, которые работают ежедневно и дежурят до 2–3 раз в неделю, продолжительность их работы может составлять 68–82 ч в неделю, включая ночные 16–24 ч. Полноценно адаптироваться к такому графику работы невозможно. LOLA — одно из средств, которое способствует эффективному снижению уровня аммиака крови в сложившейся ситуации [33]. В России более 20 лет представлен на фармацевтическом рынке препарат Гепа-Мерц в инфузионной и пероральной формах. Саше Гепа-Мерц — очень удобная форма для профилактики и лечения гипераммониемии как у пациентов с заболеваниями печени, так и в случаях непеченочных форм повышения содержания аммиака в крови. Мы рекомендуем всем людям, профессия которых связана с нарушением циркадных ритмов и продолжительным рабочим временем, ночными сменами, усталостью и астенией, контролировать уровень аммониемии и снижать его медикаментозно до нормального.
Благодарность
Редакция благодарит компанию Merz за оказанную помощь в технической редактуре настоящей публикации.








.gif)



