• выраженность симптомов достигает тяжелой степени;
• пролонгируется длительность симптомов;
• симптомы развиваются при отсутствии стрессорных факторов;
• симптомы нарушают физическое, социальное или профессиональное функционирование индивидуума.
Клинически значимая тревога встречается у 5–7% в общей популяции и у 25% или более пациентов, наблюдающихся врачами общей практики. Заболеваемость в течение жизни тревожными расстройствами может составлять свыше 30%. Тревога в подростковом и молодом взрослом возрасте часто в дальнейшем перерастает в депрессию. Грань между «нормальным» ответом на угрозу и патологическим тревожным расстройством часто весьма размыта и, возможно, существует континум от личностного дистресса до психического расстройства. Определенную помощь в диагностике патологической тревоги могут оказать надежные диагностические критерии тревожных расстройств, изложенные в МКБ–10. Согласно современным классификациям психических расстройств, тревожные расстройства распределены в восемь дискретных категорий: паническое расстройство, генерализованное тревожное расстройство, агорафобия с паническим расстройством, обсессивно–компульсивное расстройство, социальная фобия, специфические фобии, посттравматическое стрессорное расстройство, острое стрессорное расстройство. Среди хронических форм тревоги паническое расстройство и генерализованное тревожное расстройство наиболее часто диагностируются врачами общей практики. Любое из перечисленных тревожных расстройств может протекать в субклинической форме.
Врач–невролог в своей повседневной практике встречается с тревожными расстройствами, находящимися в различных причинно–следственных отношениях с основным (неврологическим) заболеванием. Можно выделить как минимум три такие категории:
• Первичная патологическая тревога, проявляющаяся «неврологическими» знаками и симптомами.
• Тревожное расстройство коморбидное с текущим неврологическим заболеванием или смешанное тревожно–депрессивное расстройство коморбидное с текущим неврологическим заболеванием.
• Лекарственно индуцированная тревога, возникшая в результате терапии основного заболевания.
Пациенты, страдающие первичной хронической тревогой, наблюдаются врачами неврологами чаще всего с диагнозами: вегетативная дистония, нейроциркуляторная дистония, вегетативные кризы, симпто–адреналовые кризы. Для категории пациентов, обращающихся к неврологу, характерно жаловаться на «соматические» симптомы тревоги, которые являются в большинстве своем следствием активации симпатического отдела вегетативной нервной системы. Психические симптомы могут не осознаваться больным или расцениваться как нормальная реакция на «непонятное» болезненное состояние. Только активный расспрос пациентов позволяет выявить наряду с вегетативной дисфункцией психические тревожные симптомы. Наиболее часто в поле зрения невролога попадают пациенты, страдающие генерализованным тревожным расстройством (ГТР) и паническими атаками (ПА).
ГТР обычно возникает, как правило, до 40 лет (наиболее типичное начало – между подростковым возрастом и третьим десятилетием жизни), течет хронически годами с выраженной флуктуацией симптомов. Женщины заболевают ГТР в два и более раз чаще, чем мужчины. Основным проявлением заболевания является чрезмерная тревога или беспокойство по поводу обыденных событий, которые пациент не может контролировать. Тревога ассоциирована с тремя или более и из представленных в таблице 2 симптомов.
Кроме того, неограниченно могут быть представлены неспецифические симптомы тревоги: вегетативные (головокружение, тахикардия, эпигастральный дискомфорт, сухость во рту, потливость и др); мрачные предчувствия (беспокойство о будущем, предчувствие «конца», трудности концентрации); моторное напряжение (двигательное беспокойство, суетливость, невозможность расслабиться, головные боли напряжения, озноб). Именно неспецифические соматические (вегетативные) симптомы часто становятся ведущими жалобами больных с ГТР, что объясняет принятые ранее термины «вегетативная дистония», «нейроциркуляторная дистония». Ранее ГТР большинством экспертов рассматривалось как мягкое расстройство, которое достигает клинической значимости только в случае коморбидности с депрессией. Но увеличение фактов, свидетельствующих о нарушении социальной и профессиональной адаптации больных с ГТР, заставляет более серьезно относиться к этому заболеванию.
Паническое расстройство (ПР) – крайне распространенное, склонное к хронизации заболевание, манифестирующее в молодом, социально активном возрасте. Распространенность ПР, по данным эпидемиологических исследований, составляет 1,9–3,6% [1]. ПР в 2–3 раза чаще наблюдается у женщин. Основным проявлением ПР являются повторяющиеся пароксизмы тревоги (панические атаки). Паническая атака (ПА) представляет собой необъяснимый мучительный для больного приступ страха или тревоги в сочетании с различными вегетативными (соматическими) симптомами. В отечественной литературе долгое время использовался термин – «вегетативный криз», отражающий представления о первичности дисфункции вегетативной нервной системы.
Диагностика панической атаки основывается на определенных клинических критериях. Паническая атака характеризуется пароксизмальным страхом (часто сопровождающимся чувством неминуемой гибели) или тревогой и/или ощущением внутреннего напряжения в сочетании с 4 или более из списка паникоассоциированных симптомов (табл. 3).
Интенсивность основного критерия ПА – пароксизмальной тревоги – может варьировать в широких пределах: от выраженного аффекта паники до ощущения внутреннего напряжения. В последнем случае, когда на первый план выступает вегетативная составляющая, говорят о «нестраховой» ПА или о «панике без паники». Атаки, обедненные эмоциональными проявлениями, чаще встречаются в терапевтической и неврологической практике. Паникоассоциированные симптомы развиваются внезапно и достигают своего пика в течение 10 минут. Послеприступный период характеризуется общей слабостью, разбитостью.
ПР имеет особый стереотип становления и развития симптоматики. Первые атаки оставляют неизгладимый след в памяти больного, что ведет к появлению синдрома тревоги «ожидания» приступа, который в свою очередь закрепляет повторяемость атак. Повторение атак в сходных ситуациях (в транспорте, пребывании в толпе и т.д.) способствует формированию ограничительного поведения, т.е. избегания потенциально опасных для развития ПА мест и ситуаций. Трактовка пациентом ПА как проявления какого–либо соматического заболевания приводит к частым посещениям врача, консультациям у специалистов различного профиля, неоправданным диагностическим исследованиям и создает у пацента впечатление о сложности и уникальности его заболевания. Неверные представления пациента о сути заболевания ведут к появлению ипохондрических симптомов, способствующих утяжелению течения болезни.
Коморбидность ПР психопатологическим синдромам имеет тенденцию нарастать по мере длительности заболевания. Лидирующее положение по коморбидности с ПР занимают агорафобия, депрессия, генерализованная тревога. Многими исследователями доказано, что при сочетании ПР и ГТР оба заболевания проявляются в более тяжелой форме, взаимно отягощают прогноз и снижают вероятность ремиссии.
Тревожное расстройство у пациентов с коморбидным неврологическим или соматическим заболеванием может проявляться различными симптомами, которые описаны при первичной патологической тревоге. Тревога особенно часто ассоциирована со следующими хроническими неврологическими заболеваниями: эпилепсия, инсульт, рассеянный склероз, хронические болевые синдромы, мигрень, болезнь Паркинсона и другие дегенеративные заболевания. Необходимость дифференцировать многие соматические симптомы тревоги от симптомов соматического или неврологического заболевания в некоторых случаях становится значительной проблемой. Тревожные симптомы могут быть ошибочно расценены как признаки неврологического заболевания, что часто влечет за собой необоснованную терапию.
Клиническая манифестация тревожных симптомов часто не удовлетворяет критериям очерченного тревожного расстройства и представляет собой рекуррентную группу симптомов с меньшей длительностью и выраженностью, чем это требуется для синдромальной классификации. Эти субсиндромально выраженные тревожные нарушения наиболее трудны для диагностики, часто остаются нелечеными, при этом оказывая крайне негативное влияние на качество жизни пациента и окружающих его лиц. Часто субсиндромальное тревожное расстройство является фактором риска развития тяжелой депрессии. Коморбидное тревожное расстройство независимо от степени выраженности оказывает существенное негативное влияние на течение основного (неврологического) заболевания. Например, тревога может привести к учащению эпилептических припадков или срыву лекарственной ремиссии, удлинить период реабилитации у пациентов, перенесших инсульт. Мягкие тревожные расстройства соответствуют синдромальным по продолжительности, но включают меньшее количество (от 2 до 4) тревожных симптомов или более четырех симптомов, незначительная выраженность (тяжесть) которых не удовлетворяет полностью диагностическим критериям. Изучение качества жизни у пациентов, страдающих субсиндромальной или мягкой тревогой, показало, что по параметрам профессиональной и социальной активности снижение качества жизни у них сопоставимо с пациентами, имеющими развернутое тревожное расстройство, и значительно хуже, чем у лиц, имеющих хроническое заболевание, не осложненное психопатологическими синдромами [3].
Эпидемиологические исследования показывают, что у пациентов, страдающих неврологическими заболеваниями, имется высокое превалирование сочетания симптомов тревоги или тревожных расстройств с депрессией. Например, эпидемиологическое исследование «RAPSODY» показало, что среди пациентов, страдающих хроническими болевыми синдромами, у 14% имелось только тревожное расстройство, у 17% – только депрессивное расстройство, а у 36% – сочетание тревоги и депрессии [4]. Среди пациентов, страдающих эпилепсией и имеющих депрессию, 73% имели конкурирующее тревожное расстройство [2]. Сочетание тревоги и депрессии взаимно утяжеляет течение каждого синдрома и собственно неврологического заболевания (табл. 4).
Дополнительное диагностирование тревоги, безусловно, влияет на выбор терапии смешанного тревожно–депрессивного синдрома. Однако вычленение тревожных и депрессивных симптомов по большей части оказывается весьма сложной задачей, поскольку многие симптомы не обладают специфичностью (табл. 5). Не только общие симптомы, но и некоторые общие психобиологические звенья патогенеза позволяют обсуждать некий континеум: тревога–депрессия. Патогенное влияние тревоги и депрессии на течение и прогноз соматического (неврологического) заболевания также реализуется по общим механизмам, которые условно разделяют на психологические и биологические. К наиболее важным психологическим механизмам относят ухудшение соблюдения режима терапии основного заболевания, нарушение альянса «врач–пациент» (тревога и депрессия снижают коммуникативные возможности), склонность к злоупотреблению алкоголем и табакокурению. Биологическое влияние тревоги и депрессии на соматическое заболевание осуществляется через активацию гипоталамо–гипофизарно–надпочечниковой системы, приводящей к повышению уровня кортизола, и гиперактивацию симпато–адреналовой системы, приводящей к дисбалансу симпатического и парасимпатического отделов вегетативной нервной системы.
Многие лекарственные препараты и другие химические субстанции могут стать причиной тревожных симптомов. Чрезмерное употребление кофеина или резкое прекращение его употребления вызывает значимые тревожные симптомы [1]. Различные рецепторные медикаменты вызывают манифестацию тревоги, что трактуется как побочный эффект препарата. Способностью вызывать тревогу обладают: адренергические агонисты, бронходилататоры, кортикостероиды, препараты, влияющие на функцию щитовидной железы, антигипертензивные препараты, кардиоваскулярные препараты, особенно дериваты дегиталиса. Психотропные препараты, такие как нейролептики и реже селективные ингибиторы обратного захвата серотонина, могут быть причиной акатизии, которая ассоциирована с тревогой. Все антидепрессанты при длительном использовании демонстрируют противотревожный эффект. Однако в инициальном периоде лечения все антидепрессанты без исключения могут индуцировать тревогу, что во многих случаях является причиной отказа пациента от терапии. Комбинация антидепрессанта с противотревожным препаратом на инициальный период лечения делает терапию в целом более успешной.
Хорошо известно, что отмена алкоголя вызывает тревогу и ажитацию. Многие патологические тревожные симптомы дебютируют в период абстиненции. Симптомы отмены седативных и снотворных препаратов близки по патогенезу и клиническим проявлениям к симптомам отмены алкоголя, но часто недооцениваются клиницистами как потенциальная причина тревоги. Оба эти состояния характеризуются следующими тревожными симптомами: нервозность, тахикардия, дрожь, потливость и тошнота. В то же время седативные препараты (бензодиазепины) используют для лечения тревожных симптомов. Поэтому возникают трудности при дифференцировке симптомов основного тревожного расстройства от симптомов отмены ассоциированных с использованием этих медикаментов.
Тревожные расстройства диагностируются лишь у 50% пациентов с очевидными симптомами [5]. Меньше чем 50% пациентов получают какое–либо лечение, и меньше 30% – адекватную терапию. Мягкие и субпороговые тревожные расстройства часто вообще не рассматриваются как мишень для лечения. Вероятность лечения повышается по мере утяжеления симптоматики (табл. 6). В то же время неадекватное лечение депрессии может спровоцировать появление тревоги как симптома частично леченной депрессии. Тревожное расстройство, являющееся остаточным проявлением леченой депрессии, большинством экспертов рассматривается как индикатор повышенного риска рекурентной депрессии.
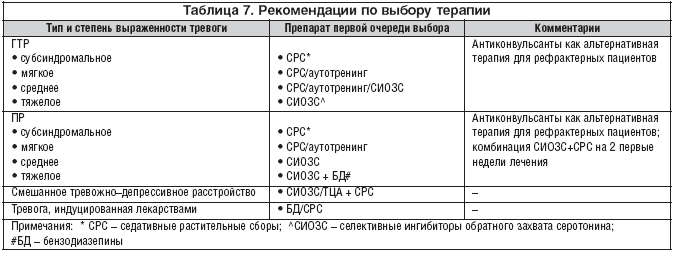
Несмотря на облигатность вегетативной дисфункции и часто маскированный характер эмоциональных расстройств, базовым методом лечения тревоги является психофармакологическое лечение. Терапевтическую стратегию необходимо выстраивать в зависимости от типа доминирующего расстройства и степени его выраженности. Выбор препарата зависит от степени выраженности уровня тревоги и длительности заболевания. Препаратами первой очереди выбора для лечения хронических тревожных расстройств являются селективные ингибиторы обратного захвата серотонина (СИОЗС). Бензодиазепиновые анксиолитики используются для купирования острых симптомов тревоги и не должны применяться более 4–х недель из–за угрозы формирования синдрома зависимости. При кратковременных субсиндромальном или мягком тревожном расстройстве используются растительные успокаивающие сборы или препараты на их основе, антигистаминные препараты (гидроксизин). Валериана на протяжении многих лет используется в традиционной медицине благодаря гипнотическому и седативному эффектам и до настоящего времени остается высоко востребованным лекарством. Особо успешными оказались препараты, содержащие валериану и дополнительные фито–экстракты, усиливающие анксиолитический эффект валерианы. Широкое применение нашел препарат Персен, который содержит, помимо валерианы, экстракт мелиссы и мяты, что усиливает анксиолитический эффект валерианы и добавляет спазмолитическое действие. Особенно хорошо зарекомендовал себя в лечении субсиндромальных тревожных и мягких тревожных расстройств Персен Форте, в каждой капсуле которого содержится 125 мг экстракта валерианы против 50 мг в таблетке Персена, благодаря чему Персен Форте обеспечивает высокий и быстрый анксиолитический эффект. Более низкое содержание валерианы в таблетках Персена позволяет использовать эту форму в педиатрическй практике. Успех Персена в немалой степени связан с его спектром переносимости. Препарат практически не вызывает побочных эффектов, в то время как большинство анксиолитиков (бензодиазепины, антигистаминные препараты, антидепрессанты) обладают значительным спектром побочных эффектов: от развития зависимости до индуцирования сексуальной дисфункции. Спектр применения Персена Форте в практике клинициста–невролога чрезвычайно широк: от применения в монотерапии для лечения субсиндромальных и мягких тревожных нарушений до комбинации с антидепрессантами для нивелирования индуцированной тревоги в инициальный период лечения (табл. 7). Учитывая отсутствие каких–либо противопоказаний для использования Персена во взрослой практике, препарат может рассматриваться как альтернативное лечение у пациентов, имеющих противопоказания для использования анксиолитиков бензодиазепинового ряда или антидепрессантов. Например, многие антидепрессанты обладают конвульсогенным действием и не всегда могут быть назначены пациентам, страдающим эпилепсией.
Не существует четких рекомендаций по длительности терапии мягких и субсиндромальных тревожных синдромов. Тем не менее большинством исследований доказана польза длительных курсов терапии. Считается, что после редукции всех симптомов должно пройти не менее четырех недель лекарственной ремиссии, после чего делается попытка отмены препарата. В среднем лечение седативными растительными сборами составляет 2–4 месяца.





Литература
1. Bruce M, Scott N, Shine P, Lader M. Anxiogenic effects of caffeine in patients with anxiety disorders. // Arch Gen Psychiatry 1992;49:867–869.
2. Jones J, Hermann BP, Barry J et al. Clinical assessment of Axis I psychiatric morbidity in chronic epilepsy: a multicenter investigation. // J Neuropsychiatry Clin Neurisci 2005;17:172–179.
3. Katon W, Hollifield M, Chapman T et al. Infrequent panic attacks: psychiatric comorbidity, personal characterisitics and functional disability. // J Psych Research 1995; 29: 121–131.
4. Mignon A, Linkowski P, Van Heeringen C, Dramaix M. Registry of patients with painful symptoms and observation of depression and anxiety. // 19th Congress of European college of Neuropsychopharmacology Paris, France, 16–20 sep. 2006.
5. Sartorius N, Ustun TB, Lecrubier Y, Wittchen HU. Depression comorbid with anxiety: results from the WHO study on psychological disorders in primary health care. Br J Psychiatry 1996 ; 168: 38–43.








.gif)



