* Department of Clinical Pharmacology Russian State Medical University
** Municipal Clinical Hospital named after Filatov O.M., Moscow Glaucoma Center
*** Department of Ophthalmology of Medical faculty Russian State Medical University
Data gained during multicenter studies showed efficacy and safety of ranibizumab, used in injections, in treatment of neovascular form of AMD. But taking into consideration high price of the drug, the question of economic practicability of including it into the scheme of treatment of patients with wet type of AMD is still opened.
Возрастная макулярная дегенерация (ВМД) характеризуется необратимым прогрессирующим поражением центральной фотоактивной зоны сетчатки. Это заболевание признано одной из основных причин необратимого снижения зрения среди пациентов старшей возрастной группы в экономически развитых странах мира [1,2]. Отмечено, что данная патология встречается у 25% лиц старше 65 лет. В России заболеваемость ВМД составляет более 15 на 1000 населения [3]. Социально–медицинская значимость этой патологии обусловлена быстрой потерей центрального зрения с утратой общей трудоспособности. У лиц работоспособного возраста выход на первичную инвалидность вследствие возрастной макулярной дегенерации наблюдается в 11% случаев, а у пожилых людей старше 60 лет – в 28% случаев.
Классификация ВМД строится в основном на этапах развития дистрофического процесса. Наиболее часто встречается «сухая» (неэкссудативная, атрофическая) форма ВМД – в 80% случаев, оставшиеся 20% приходятся на «влажную» (экссудативную, неоваскулярную) форму, при которой происходит формирование субретинальной неоваскулярной мембраны (СНМ), характеризующейся врастанием новообразованных сосудов через дефекты мембраны Бруха под пигментный эпителий сетчатки или нейроэпителий. Повышенная проницаемость сосудов приводит к пропотеванию жидкости и скоплению ее в субретинальном пространстве, отеку сетчатки и появлению субретинальных кровоизлияний.
Одним из основных медиаторов, участвующих в патогенетических процессах хориоидальной неоваскуляризации, является фактор роста эндотелия сосудов (Vascular Endothelial Growth Factor–А – VEGF). Его выделение провоцируют гипоксия, окислительный стресс и воспалительные реакции пигментного эпителия сетчатки. VEGF воздействует на пролиферацию клеток эндотелия сосудов, приводит к изменению состояния плотных контактов между ними, что, в свою очередь, обусловливает повышение проницаемости сосудистой стенки [4].
С целью уменьшения неоваскуляризации были разработаны препараты, обладающие анти–VEGF–активностью, одним из которых является ранибизумаб (Луцентис, Novartis Pharma). Он представляет собой Fab–фрагмент рекомбинантного моноклонального антитела к фактору роста эндотелия сосудов [5]. Благодаря высокоаффинному связыванию с фактором роста сосудистого эндотелия, ранибизумаб эффективно подавляет пролиферацию эндотелиальных клеток и неоваскуляризацию сетчатки, а также уменьшает опосредованную VEGF проницаемость сосудов [6].
Эффективность и безопасность Луцентиса при ВМД сетчатки изучена в рандомизированных двойных слепых контролируемых многоцентровых клинических исследованиях III фазы [7–9].
Результаты проведенных клинических исследований MARINA и ANCHOR продемонстрировали, что применение Луцентиса позволяет добиться улучшения или стабилизации остроты зрения у большинства пациентов, имеющих «влажную» форму ВМД.
В рамках двухгодичного исследования MARINA (Minimally Classic/Occult Trial of the Anti–VEGF Antibody Ranibizumab in the Treatment of Neovascular Age–Related Macular Degeneration), в котором приняло участие 716 пациентов с минимальной классической и скрытой субретинальной неоваскулярной мембраной при ВМД, улучшение остроты зрения на 15 и более букв наблюдалось у 26–33% пациентов, получавших Луцентис (а в группе контроля – 3,8%) [7]. В исследовании ANCHOR (The Anti–VEGF Antibody for the Treatment of Predominantly Classic Choroidal Neovascularization in Age–Related Macular Degeneration) приняло участие 432 пациента с преимущественно классической СНМ. Основной задачей этого исследования была оценка эффективности Луцентиса в сравнении с фотодинамической терапией (ФДТ). Через 24 мес. терапии прибавка в остроте зрения на 15 и более букв наблюдалась у 34–41% пациентов, которым проводились инъекции Луцентиса, и только у 6% пациентов из группы ФДТ [8, 9]. Эти данные послужили основанием для регистрации ранибизумаба в США (в 2006 г.), Европе (в 2007 г.) и Японии (в 2009 г.) для использования при лечении неоваскулярной ВМД. В России препарат зарегистрирован в 2008 г. и вошел в повседневную практику ведущих офтальмологических клиник.
Подробный анализ данных клинических исследований III фазы позволил выработать основанные на принципах доказательной медицины рекомендации по применению ранибизумаба для лечения неоваскулярной формы ВМД. Лечение Луцентисом эффективно при всех трех главных подтипах хориоидальной неоваскуляризации (преимущественно классической, скрытой и минимально классической). Ранибизумаб показан, в первую очередь, при субфовеальных (в которые также могут быть включены юкстафовеальные) поражениях с признаками активности заболевания [10]:
• выходящее за пределы нормы утолщение сетчатки, особенно при наличии признаков интраретинального, субретинального или субпигментного накопления жидкости, по возможности подтвержденное оптической когерентной томографией;
• наличие (или рецидив) интраретинальных или субретинальных кровоизлияний;
• новые или персистирующие участки просачивания, выявленные при флюоресцентной ангиографии;
• увеличение хориоидальной неоваскуляризации при флюоресцентной ангиографии, если это не исключительно сухие, фибротические участки;
• снижение остроты зрения, возникшее вследствие активной хориоидальной неоваскуляризации.
Согласно условиям регистрации в Европе, ранибизумаб вводится в дозе 0,5 мг ежемесячно, в течение 3 последовательных месяцев; после этого начинается фаза поддерживающей терапии, в течение которой производится регулярный мониторинг остроты зрения, а продолжение лечения выполняется при снижении остроты зрения на 5 и более букв или при наличии других признаков активности заболевания. В США рекомендуется выполнение ежемесячных инъекций препарата, однако в случаях, когда это не является возможным, допустимо удлинение интервалов между введениями по результатам оценки остроты зрения и оптической когерентной томографии. В России и европейских странах препарат применяется в индивидуализированном режиме: выполняются три ежемесячные инъекции фазы стабилизации, после чего лечение препаратом прекращают и выполняют ежемесячную оценку остроты зрения. При снижении остроты зрения более чем на 5 букв по таблице ETDRS или на одну строку по таблице Снеллена лечение препаратом возобновляют.
Учитывая необходимость многократных повторных интравитреальных инъекций Луцентиса, особое внимание следует уделить оценке его безопасности.
В ходе проведения исследования MARINA предполагаемый эндофтальмит был констатирован у 5 (1%) из 477 пациентов, которым были выполнены суммарно 10443 инъекции Луцентиса (частота на инъекцию — 0,05%) [7]. Воспалительные явления глазного яблока отмечались у 30 (12,7%) пациентов, получавших инъекции плацебо, и у 40 (16,8%) и 50 (20,8%) пациентов, которым вводили Луцентис в дозе 0,3 и 0,5 мг соответственно. Во всех группах в большинстве случаев воспаление было определено как минимальное или 1+ степени. У небольшого количества пациентов наблюдалось повышение внутриглазного давления (ВГД), однако степень повышения данного показателя после инъекции относительно значений, регистрировавшихся до этого, была небольшой и транзиторной во всех группах: при использовании 0,3 мг Луцентиса – на 1,9–3,5 мм рт.ст., 0,5 мг Луцентиса – на 2,1–3,4 мм рт.ст. и при выполнении имитации внутриглазной инъекции – на 0,8–1,5 мм рт.ст. Частота развития катаракты среди пациентов, получавших инъекции Луцентиса и плацебо, была сопоставимой, достигая 15,5% (в обеих группах ранибизумаба) и 15,7%.
Значительное количество опубликованных серий клинических наблюдений и ретроспективных исследований также позволяют оценить безопасность ранибизумаба со стороны органа зрения. В рамках ретроспективного анализа 14 320 инъекций ранибизумаба в стекловидное тело была констатирована частота эндофтальмита, соответствующая 0,02% (1 на 4500 инъекций), что соответствует значению аналогичного показателя в 0,05%, полученному в исследовании MARINA, и < 0,1%, полученному в исследовании ANCHOR [7,9]. Аналогичные значения частоты предполагаемого эндофтальмита в диапазоне от 0,03% до 0,077% были получены и в других недавно опубликованных ретроспективных исследованиях введения ингибиторов VEGF, в том числе ранибизумаба, в стекловидное тело [11,12]. При ретроспективном анализе медицинской документации было установлено, что у 1,2% из 210 пациентов отмечалось повышение ВГД на 21 мм рт.ст. и более, а у 0,5% пациентов – на 30 мм рт.ст. и более [13]. Kim et al. привели сведения о том, что повышение ВГД происходит непосредственно после инъекции ранибизумаба, является транзиторным и редко требует проведения длительного мониторинга [14]. В нескольких сериях наблюдений сообщалось о развитии разрывов сетчатки у пациентов, получавших инъекции Луцентиса. При оценке ретроспективных данных 164 глаз после интравитреального введения Луцентиса у одного (0,6%) пациента отмечался разрыв пигментного эпителия сетчатки после первой инъекции [15].
Введение ранибизумаба в стекловидное тело ассоциировалось с низким риском системных нежелательных явлений. Частота артериальных тромбоэмболий на фоне терапии Луцентисом длительностью 1 год была номинально выше, нежели у пациентов, получавших имитацию инъекции в исследовании MARINA, однако это различие нивелировалось в течение 2 лет наблюдения [7]. Частота тромбоэмболических состояний как у пациентов, которым вводился ранибизумаб, так и в группе контроля в исследовании PIER была ниже, нежели в исследованиях ANCHOR и MARINA, что может свидетельствовать в пользу того, что ежеквартальное введение ранибизумаба по сравнению с ежемесячным введением эффективно снижает частоту этих нежелательных явлений до фонового уровня [16]. Хотя частота инсультов у пациентов, получавших ранибизумаб в дозе 0,5 мг, была выше по сравнению с получавшими его в дозе 0,3 мг в исследовании SAILOR, общая частота артериальных тромбоэмболий в клинических исследованиях (2,5%) не была выше наблюдающейся в общей популяции больных ВМД. Увеличение возраста и наличие ВМД ассоциировались с повышением риска сосудистых изменений, в частности, инсульта и инфаркта миокарда, и в целом представляется маловероятным, что терапия ранибизумабом значительно повышает этот риск, хотя имеются опасения возможного повышения данного риска у пациентов, имеющих инсульт в анамнезе. Хотя пациенты, имеющие в анамнезе сердечно–сосудистую, цереброваскулярную патологию и патологические изменения периферических сосудов, не исключались специально из исследований ANCHOR и MARINA, полученные данные о риске инсульта должны интерпретироваться с учетом небольшого числа наблюдаемых случаев данной патологии. Риск этих нежелательных явлений должен тщательно мониторироваться в продолжающихся клинических исследованиях, и пациенты должны получать полную информацию о возможных видах и вероятности рисков, связанных с введением ранибизумаба в стекловидное тело [4].
Таким образом, в ходе многоцентровых исследований были получены убедительные доказательства эффективности и безопасности инъекций Луцентиса, однако, учитывая высокую стоимость препарата, остается открытым вопрос об экономической целесообразности его включения в схему лечения пациентов с «влажной» формой ВМД.
С целью фармакоэкономической оценки целесообразности использования препарата Луцентис компании Новартис было проведено модельное исследование, предполагающее сравнение результатов наблюдения за пациентами с ВМД с использованием Луцентиса и рутинной практики ведения пациентов, средний возраст которых составляет 70 лет, на протяжении 10 лет терапии.
Был построен прогноз терапии ВМД отдельно для каждой группы.
Общие затраты на ведение пациентов складывались из двух составляющих: медицинских затрат (МЗ) и социальных затрат (СЗ).
Медицинские затраты на терапию Луцентисом включали в себя стоимость лекарственного препарата 51,7 тыс. руб. (включая НДС) за инъекцию, а также затраты на проведение инъекции – стоимость одного амбулаторного визита. Инъекции получали пациенты с остротой зрения выше 20/400. В течение первого года терапии пациент получал 8 инъекций, последующих – 6. Также в стоимость терапии были включены проведение оптической когерентной томографии (ОКТ) – однократно, флюоресцентной ангиографии глазного дна (ФАГД) – ежегодно.
Стоимость рутинной терапии включала в себя стоимость медикаментозного лечения в соответствии с отечественными клиническими рекомендациями ведения больных с ВМД, проведение оптической когерентной томографии (однократно), флюоресцентной ангиографии глазного дна (однократно), а также один амбулаторный визит и семь койко–дней в офтальмологическом стационаре за квартал.
Стоимость медицинских услуг (МУ) рассчитывалась на основании утвержденных Правительством РФ тарифов (в ред. Постановления Правительства РФ от 05.12.2008 № 913 «О программе государственных гарантий оказания гражданам Российской Федерации бесплатной медицинской помощи на 2009 год») с учетом методических рекомендаций в (в ред. Письма ФФОМС от 24.08.2005 № 4085/40–3/И «О формировании и экономическом обосновании территориальной программы государственных гарантий оказания гражданам Российской Федерации бесплатной медицинской помощи на 2006 год»). При расчете стоимости медицинских услуг базовые тарифы умножались на средневзвешенный региональный коэффициент 1,144 и коэффициенты по профилю заболевания («Офтальмология») для каждого типа оказываемых услуг: стоимость амбулаторного визита – 139,9 руб.; стоимость койко–дня в офтальмологическом отделении – 1637,4 руб.; стоимость исследования ФАГД – 1300,7 руб.; стоимость исследования ОКТ – 526,9 руб. Предполагалось ежегодная индексация затрат на медицинские услуги в размере 15%. Проводилось дисконтирование стоимости лекарственных средств, медицинских услуг, социальных затрат и потерь: 7 лет – 11,2%, 10 лет – 10%.1
К социальным затратам и потерям при ВМД относятся: дополнительные социальные выплаты (пенсионные, ДЛО–ОНЛС дополнительное лекарственное обеспечение – обеспечение необходимыми лекарственными средствами), временные и финансовые потери родственников и социальных служб, связанные с необходимостью обеспечения требуемого уровня бытовых условий пациентов, затраты, связанные с возможным помещением пациентов в интернат для лиц с потерей зрения, прочие дополнительные затраты пациентов, связанные с частичной или полной потерей зрения. К сожалению, данных, оценивающих объем и стоимость социальных затрат среди больных с ВМД в РФ, найти не удалось. Возможно, какие–то крупицы подобных сведений могут содержаться в ведомственных отчетах Министерства здравоохранения и социального развития, недоступных для открытого использования.
Тем не менее размер социальных затрат и потерь пациентов может лежать в достаточно широком интервале: от 50–100 руб. в день (дополнительные выплаты вследствие инвалидности) до 1200–1500 руб. в случае содержания пациента в интернате. В ходе моделирования проводилась оценка социальных затрат и потерь для пациентов. Расчеты проводились по следующему алгоритму: оценивалась доля пациентов, потерявших зрение, и умножалась на величину выбранного порога ежедневных социальных затрат и потерь и долю пациентов, достигших этого порога.
Прогноз исходов терапии для каждой альтернативы был основан на описывающей процесс терапии модели Маркова. Построение модели и моделирование осуществлялось с использованием программного пакета DATA 3.0 TreeAge Inc.
Моделирование проводилось в расчете на пациента. Были выделены состояния с различной остротой зрения, характеризующиеся различным объемом получаемых медицинских услуг и полезностью: 20/40 и выше; от 20–60 до 20/100; от 20/125 до 20/160; от 20/200 до 20/400; ниже 20/400; смерть.
Состояния с остротой зрения ниже 20/200 соответствовали потере зрения. Частоты перехода из состояния в состояние оценивались по данным исследований MARINA, ANCHOR, TAP и изменялись во времени.
Результаты моделирования
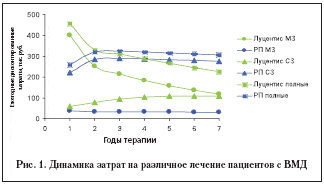
Необходимо обратить внимание, что при оценке динамики медицинских затрат и социальных издержек на ведение больных с классической формой ВМД, получающих Луцентис в сравнении с рутинной практикой (РП), наблюдается следующая тенденция, представленная на рисунке 1.
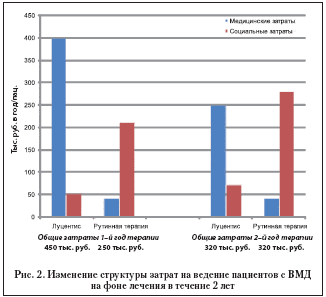
Уже через год предполагаемого наблюдения в группе Луцентиса наблюдается сокращение общих затрат на лечение до 20%, что становится примерно таковым же, как при использовании рутинной практики. В большей мере это обусловлено резким снижением социальных затрат, которые, для сравнения, уже через год после начала лечения в 5 раз ниже социальных затрат, сопутствующих традиционному ведению больных. Изменение структуры затрат обеих групп представлена на рисунке 2.
Кроме того, наиболее важным последствием проводимого лечения является то, что при длительной терапии, несмотря на несравнимо высокую стоимость Луцентиса, его использование приводит к экономии бюджетных средств, как минимум на 20% по сравнению с традиционным лечением пациентов с данной патологией.
Таким образом, использование Луцентиса для лечения больных ВМД является экономически обоснованной альтернативой, что способствует не только рациональному распределению средств на ведение больных, но и их экономии в будущем.
1 7 лет (Минфин РФ, облигации федерального займа с постоянным
купонным доходом, документарные именные, выпуск ОФЗ–26202–ПД.
Дата начала размещения: 23.09.2009. Дата погашения: 17.12.2012).
10 лет (Минфин РФ, облигации федерального займа с постоянным
купонным доходом, документарные именные, выпуск ГСО–39004–ПД.
Дата начала размещения: 30.10.2008. Дата погашения: 18.04.2024).
Литература
1. Ермакова Н.А., Рабданова О.Ц. Основные этиологические факторы и патогенетические механизмы развития возрастной макулярной дегенерации // Клиническая офтальмология. – 2007. – Т. 8. – №3. – С. 125–128.
2. Ding X., Patel M., Chan C.C. Molecular pathology of age–related macular degeneration // Prog. Retin. Eye Res.– 2009.– Vol. 28.– № 1.– P. 1–18.
3. Клинические рекомендации. Офтальмология / Под ред. Л.К. Мошетовой, А.П. Нестерова, Е.А. Егорова. – М.: ГЭОТАР–Медиа, 2007. – 256 с.
4. Schmidt–Erfurth U. Clinical safety of ranibizumab in age–related macular degeneration // Expert. Opin. Drug. Saf.– 2010.– Vol. 9.– № 1.– P. 149–165.
5. Gaudreault J., Fei D., Rusit J. et al. Preclinical pharmacokinetics of Ranibizumab (rhuFabV2) after a single intravitreal administration // Invest. Ophthalmol. Vis. Sci.– 2005.– Vol. 46.– P. 726–733.
6. Singh RP, Kaiser PK Role of ranibizumab in management of macular degeneration //Indian J Ophthalmol. 2007 Nov–Dec; 55(6): 421–425.
7. Rosenfeld P.J., Brown D.M., Heier J.S. et al. Ranibizumab for neovascular age–related macular degeneration // N. Eng. J. Med.– 2006.– Vol. 355.– P. 1419–1431.
8. Brown D.M., Kaiser P.K., Michels M. et al. Ranibizumab versus verteporfin for neovascular age–related macular degeneration // N. Eng. J. Med.– 2006.– Vol. 355.– P. 1432–1444.
9. Brown D.M., Michels M., Kaiser P.K. et al. Ranibizumab versus verteporfin photodynamic therapy for neovascular age–related macular degeneration: two–year results of the ANCHOR study // Ophthalmology.– 2009.– Vol. 116.– P. 57–65.
10. Mitchell P., Korobelnik J.F., Lanzetta P. et al. Ranibizumab (Lucentis) in neovascular age–related macular degeneration: evidence from clinical trials // Br. J. Ophthalmol.– 2010.– Vol. 94.– № 1.– P. 2–13.
11. Diago T., McCannel C.A., Bakri S.J. et al. Infectious endophthalmitis after intravitreal injection of antiangiogenic agents // Retina.– 2009.– Vol. 29.– P. 601–605.
12. Pilli S., Kotsolis A., Spaide R.F. et al. Endophthalmitis associated with intravitreal anti–vascular endothelial growth factor therapy injections in an office setting // Am. J. Ophthalmol.– 2008.– Vol. 145.– P. 879–882.
13. Larson T.A., Bakri S.J., McCannel C.A. et al. The effect of ranibizumab (Lucentis) on intraocular pressure // Invest. Ophthalmol. Vis. Sci.– 2009.– Vol. 50.– P. 256.
14. Kim J.E., Mantravadi A.V., Hur E.Y., Covert D.J. Short–term intraocular pressure changes immediately after intravitreal injections of anti–vascular endothelial growth factor agents // Am. J. Ophthalmol.– 2008.– Vol. 146.– P. 930–934.
15. Smith B.T., Kraus C.L., Apte R.S. Retinal pigment epithelial tears in ranibizumab–treated eyes // Retina.– 2009.– Vol. 29.– P. 335–339.
16. Regillo C.D., Brown D.M., Abraham P. et al. Randomized, double–masked, sham–controlled trial of ranibizumab for neovascular age–related macular degeneration: PIER study year 1 // Am. J. Ophthalmol.– 2008.– Vol. 145.– P. 239–248.
17. Будзинская М.В., Воробьева М.В., Киселева Т.Н., Лагутина Ю.М., Полунин Г.С. Современные подходы к лечению и профилактике возрастной макулярной дегенерации // Клиническая офтальмология. – 2007. – Т. 8. – № 2. – С. 78–82.
18. Еднева Я.Н., Миронова Э.М., Абрамова О.С. Гемодинамика глаза у больных «сухой» формой склеротической макулодистрофии до и после комбинированной аргонлазерной стимуляции // Лазерные методы лечения и ангиографические исследования в офтальмологии: Сб. науч. тр. – М., 1983. – С. 8
19. Ермакова Н.А., Рабданова О.Ц. Современные методы диагностики и лечения возрастной макулярной дистрофии // VI Всероссийск. школа офтальмол.: Сб. науч. тр. – М., 2007. – С. 416–422.
20. Журавлева Л.В., Бойко Э.В., Чурилова И.В. и др. // VI Всероссийск. школа офтальмол.: Сб. науч. тр. – М., 2007. – С. 275–283.
21. Нащенкова О.В. Медикаментозное лечение возрастных макулярных дегенераций // III Всероссийск. школа офтальмол.: Сб. науч. тр. – М., 2004. – С. 281–289.
22. Age–Related Eye Disease Study Research Group. A randomized, placebo–controlled, clinical trial of high–dose supplementation with vitamins C and E and beta carotene for age–related cataract and vision loss: AREDS report no. 9 // Arch Ophthalmol. – 2001. – Vol. 119. – № 10. – Р. 1439–1452.
23. Cherney E.F. Патогенез сосудистой макулодистрофии // Офтальмологический конгресс «Белые ночи», 28–31 мая 2001. Тез. докладов. – 2001. – С. 3 –5.
24. Ferrara N., Damico L., Shams N. et al. Development of Ranibizumab, An Anti–Vascular Endothelial Growth Factor Antigen Binding Fragment, As Therapy For Neovascular Age–Related Macular Degeneration // Retina, The Journal of Retinal and Vitreous Diseases. – 2006. – Vol. 26. – N8. – P. 859–870
25. Bourla D.H., Young T.A. Age–Related Macular Degeneration: A Practical Approach to a Challenging Disease // The American Geriatrics Society. – 2006.
26. Brown GC, Brown MM, Sharma S. Difference between ophthalmologists’ and patients’ perceptions of quality of life associated with age–related macular degeneration. // Can J Ophthalmol. – 2000. 35:127–133.
27. Демографический ежегодник России. 2008. Статистический сборник. Росстат. – M., 2008. – 557 c.












