–Ю–і–љ–Є–Љ –Є–Ј –њ–µ—А–≤—Л—Е –∞–≤—В–Њ—А–Њ–≤, –Њ–њ–Є—Б–∞–≤—И–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л –≥–µ–њ–∞—В–Њ–≥–µ–љ–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є, —П–≤–ї—П–µ—В—Б—П –Ъ–Є—В–∞–љ–Є –Ґ–∞–Ї—Н–Њ [2] (—А–Є—Б. 1).
–Ф–∞–љ–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л –≤–Ї–ї—О—З–∞–ї–Є –≤ —Б–µ–±—П –≤—Б–µ —Д–Њ—А–Љ—Л –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –љ–∞—З–Є–љ–∞—П —Б –≥–µ–њ–∞—В–Њ—Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є –Ш–љ–Њ—Б—Н –Є —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В—А–∞–≤–ї–µ–љ–Є—П. –£—З–Є—В—Л–≤–∞—П —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є, –њ—А–Њ–Є—Б—Е–Њ–і—П—Й–Є—Е –≤ –њ–µ—З–µ–љ–Є, –љ–µ –±—Л–ї–Њ –Њ—Б–љ–Њ–≤–∞–љ–Є–є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞—В—М, —З—В–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–љ–Њ–µ –≤–µ—Й–µ—Б—В–≤–Њ —П–≤–ї—П–µ—В—Б—П –µ–і–Є–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є [1].
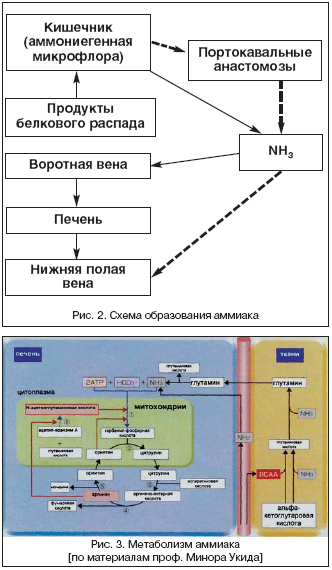
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б—З–Є—В–∞–µ—В—Б—П, —З—В–Њ –Њ—Б–љ–Њ–≤–љ—Л–Љ –≤–µ—Й–µ—Б—В–≤–Њ–Љ, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–Љ —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ, —П–≤–ї—П–µ—В—Б—П –∞–Љ–Љ–Є–∞–Ї. –Р–Љ–Љ–Є–∞–Ї –Њ–±—А–∞–Ј—Г–µ—В—Б—П –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Ї–∞—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –±–µ–ї–Ї–∞ (—А–Є—Б. 2).
–Э–µ–є—В—А–∞–ї–Є–Ј–∞—Ж–Є—П –∞–Љ–Љ–Є–∞–Ї–∞ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –≤ –≥–ї—Г—В–∞–Љ–Є–љ–Њ–≤–Њ–Љ —Ж–Є–Ї–ї–µ, –њ—А–Њ—В–µ–Ї–∞—О—Й–µ–Љ –≤ –Ї–∞–ґ–і–Њ–Љ –Њ—А–≥–∞–љ–µ. –Я—А–Є —Н—В–Њ–Љ –∞–Љ–Љ–Є–∞–Ї —Б–Њ–µ–і–Є–љ—П–µ—В—Б—П —Б –≥–ї—Г—В–∞–Љ–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В–Њ–є –Є –Њ–±—А–∞–Ј—Г–µ—В—Б—П –≥–ї—Г—В–∞–Љ–Є–љ (—А–Є—Б. 3). –Э–µ–є—В—А–∞–ї–Є–Ј–Њ–≤–∞—В—М –Њ–≥—А–Њ–Љ–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –∞–Љ–Љ–Є–∞–Ї–∞ –њ–Њ—Б—А–µ–і—Б—В–≤–Њ–Љ –≥–ї—Г—В–∞–Љ–Є–љ–Њ–≤–Њ–≥–Њ —Ж–Є–Ї–ї–∞ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ. –Я–Њ—Н—В–Њ–Љ—Г –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ —Б—Г—Й–µ—Б—В–≤—Г–µ—В —В–∞–Ї–ґ–µ —Ж–Є–Ї–ї –Љ–Њ—З–µ–≤–Є–љ—Л.
–Ь–Њ—З–µ–≤–Є–љ–∞ —П–≤–ї—П–µ—В—Б—П –і–Є–∞–Љ–Є–і–Њ–Љ —Г–≥–Њ–ї—М–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Т –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ–Њ—Б—В—М –∞–Љ–Љ–Є–∞–Ї—Г, —Н—В–Њ –љ–µ–є—В—А–∞–ї—М–љ–Њ–µ –Є –љ–µ—В–Њ–Ї—Б–Є—З–љ–Њ–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є–µ. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –љ–µ–±–Њ–ї—М—И–∞—П –Љ–Њ–ї–µ–Ї—Г–ї–∞ –Љ–Њ—З–µ–≤–Є–љ—Л –Љ–Њ–ґ–µ—В –њ—А–Њ—Е–Њ–і–Є—В—М —З–µ—А–µ–Ј –Љ–µ–Љ–±—А–∞–љ—Л. –Я–Њ —Н—В–Њ–є –њ—А–Є—З–Є–љ–µ, –∞ —В–∞–Ї–ґ–µ –Є–Ј––Ј–∞ –µ–µ —Е–Њ—А–Њ—И–µ–є —А–∞—Б—В–≤–Њ—А–Є–Љ–Њ—Б—В–Є –≤ –≤–Њ–і–µ –Љ–Њ—З–µ–≤–Є–љ–∞ –ї–µ–≥–Ї–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –Ї—А–Њ–≤—М—О –Є –≤—Л–≤–Њ–і–Є—В—Б—П —Б –Љ–Њ—З–Њ–є.
–Ь–Њ—З–µ–≤–Є–љ–∞ –Њ–±—А–∞–Ј—Г–µ—В—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Њ–є –њ–Њ—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ—Б—В–Є —А–µ–∞–Ї—Ж–Є–є, –њ—А–Њ—В–µ–Ї–∞—О—Й–Є—Е –≤ –њ–µ—З–µ–љ–Є. –Ю–±–∞ –∞—В–Њ–Љ–∞ –∞–Ј–Њ—В–∞ –±–µ—А—Г—В—Б—П –Є–Ј —Б–≤–Њ–±–Њ–і–љ–Њ–≥–Њ –∞–Љ–Љ–Є–∞–Ї–∞ –Є –Ј–∞ —Б—З–µ—В –і–µ–Ј–∞–Љ–Є–љ–Є—А–Њ–≤–∞–љ–Є—П –∞—Б–њ–∞—А—В–∞—В–∞, –Ї–∞—А–±–Њ–љ–Є–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞ – –Є–Ј –≥–Є–і—А–Њ–Ї–∞—А–±–Њ–љ–∞—В–∞. –Э–∞ –њ–µ—А–≤–Њ–є —Б—В–∞–і–Є–Є –Є–Ј –≥–Є–і—А–Њ–Ї–∞—А–±–Њ–љ–∞—В–∞ (–Э–°–Ю3–) –Є –∞–Љ–Љ–Є–∞–Ї–∞ —Б –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ 2 –Љ–Њ–ї–µ–Ї—Г–ї –Р–Ґ–§ –Њ–±—А–∞–Ј—Г–µ—В—Б—П –Ї–∞—А–±–∞–Љ–Њ–Є–ї—Д–Њ—Б—Д–∞—В. –Ъ–∞–Ї –∞–љ–≥–Є–і—А–Є–і, —Н—В–Њ —Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –Њ–±–ї–∞–і–∞–µ—В –≤—Л—Б–Њ–Ї–Є–Љ —А–µ–∞–Ї—Ж–Є–Њ–љ–љ—Л–Љ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–Љ. –Э–∞ —Б–ї–µ–і—Г—О—Й–µ–є —Б—В–∞–і–Є–Є, –Ї–∞—А–±–∞–Љ–Њ–Є–ї—М–љ—Л–є –Њ—Б—В–∞—В–Њ–Ї –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –љ–∞ –Њ—А–љ–Є—В–Є–љ —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ —Ж–Є—В—А—Г–ї–ї–Є–љ–∞. –Т—В–Њ—А–∞—П –∞–Љ–Є–љ–Њ–≥—А—Г–њ–њ–∞ –Љ–Њ–ї–µ–Ї—Г–ї—Л –Љ–Њ—З–µ–≤–Є–љ—Л –њ–Њ—Б—В–∞–≤–ї—П–µ—В—Б—П –Ј–∞ —Б—З–µ—В —А–µ–∞–Ї—Ж–Є–Є –∞—Б–њ–∞—А—В–∞—В–∞ —Б —Ж–Є—В—А—Г–ї–ї–Є–љ–Њ–Љ. –Ф–ї—П –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –љ–µ–Њ–±—А–∞—В–Є–Љ–Њ—Б—В–Є —А–µ–∞–Ї—Ж–Є–Є –і–Є—Д–Њ—Б—Д–∞—В –≥–Є–і—А–Њ–ї–Є–Ј—Г–µ—В—Б—П –њ–Њ–ї–љ–Њ—Б—В—М—О. –Ю—В—Й–µ–њ–ї–µ–љ–Є–µ —Д—Г–Љ–∞—А–∞—В–∞ –Њ—В –∞—А–≥–Є–љ–Є–љ–Њ—Б—Г–Ї—Ж–Є–љ–∞—В–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї –∞—А–≥–Є–љ–Є–љ—Г, –Є–Ј –Ї–Њ—В–Њ—А–Њ–≥–Њ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –≥–Є–і—А–Њ–ї–Є–Ј–∞ –Њ–±—А–∞–Ј—Г–µ—В—Б—П –Є–Ј–Њ–Љ–Њ—З–µ–≤–Є–љ–∞, —Б—А–∞–Ј—Г –ґ–µ –њ—А–µ–≤—А–∞—Й–∞—О—Й–∞—П—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–µ—А–µ–≥—А—Г–њ–њ–Є—А–Њ–≤–Ї–Є –≤ –Љ–Њ—З–µ–≤–Є–љ—Г. –Ю—Б—В–∞—О—Й–Є–є—Б—П –Њ—А–љ–Є—В–Є–љ –≤–љ–Њ–≤—М –≤–Ї–ї—О—З–∞–µ—В—Б—П –≤ —Ж–Є–Ї–ї –Љ–Њ—З–µ–≤–Є–љ—Л. –§—Г–Љ–∞—А–∞—В, –Њ–±—А–∞–Ј—Г—О—Й–Є–є—Б—П –≤ —Ж–Є–Ї–ї–µ –Љ–Њ—З–µ–≤–Є–љ—Л, –Љ–Њ–ґ–µ—В –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –і–≤—Г—Е —Б—В–∞–і–Є–є —Ж–Є—В—А–∞—В–љ–Њ–≥–Њ —Ж–Є–Ї–ї–∞ —З–µ—А–µ–Ј –Љ–∞–ї–∞—В –њ–µ—А–µ—Е–Њ–і–Є—В—М –≤ –Њ–Ї—Б–∞–ї–Њ–∞—Ж–µ—В–∞—В, –Ї–Њ—В–Њ—А—Л–є –Ј–∞ —Б—З–µ—В —В—А–∞–љ—Б–∞–Љ–Є–љ–Є—А–Њ–≤–∞–љ–Є—П –і–∞–ї–µ–µ –њ—А–µ–Ї—А–∞—Й–∞–µ—В—Б—П –≤ –∞—Б–њ–∞—А—В–∞—В. –Я–Њ—Б–ї–µ–і–љ–Є–є —В–∞–Ї–ґ–µ –≤–љ–Њ–≤—М –≤–Њ–≤–ї–µ–Ї–∞–µ—В—Б—П –≤ —Ж–Є–Ї–ї –Љ–Њ—З–µ–≤–Є–љ—Л (—А–Є—Б. 4) [3].
–£–Љ–µ–љ—М—И–µ–љ–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є —Ж–Є–Ї–ї–∞ –Љ–Њ—З–µ–≤–Є–љ—Л –≤ –њ–µ—З–µ–љ–Є –њ—А–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –љ–µ–Є–Ј–±–µ–ґ–љ–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –≥–ї—Г—В–∞–Љ–Є–љ–Њ–≤–Њ–≥–Њ —Ж–Є–Ї–ї–∞ –≤ –і—А—Г–≥–Є—Е –Њ—А–≥–∞–љ–∞—Е –Є —В–Ї–∞–љ—П—Е (–Ї—А–Њ–Љ–µ –њ–µ—З–µ–љ–Є). –Я—А–Є —Н—В–Њ–Љ –Њ—З–µ–љ—М –∞–Ї—В–Є–≤–љ–Њ —А–∞—Б—Е–Њ–і—Г—О—В—Б—П –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л —Б —А–∞–Ј–≤–µ—В–≤–ї–µ–љ–љ—Л–Љ–Є –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–Љ–Є —Ж–µ–њ—П–Љ–Є –Є –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Л–є –і–Є—Б–±–∞–ї–∞–љ—Б. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –≤ –Ї—А–Њ–≤–Є –њ–Њ–≤—Л—И–∞–µ—В—Б—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≥–ї—Г—В–∞–Љ–Є–љ–∞, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –∞–Ј–Њ—В–љ–∞—П –љ–∞–≥—А—Г–Ј–Ї–∞ –љ–∞ —В–Ї–∞–љ–Є, –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –Ї—А–Њ–≤–Є, –≤ –≤–µ–љ–Њ–Ј–љ–Њ–є –Ї—А–Њ–≤–Є –њ–Њ–≤—Л—И–∞–µ—В—Б—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≥–ї—Г—В–∞–Љ–Є–љ–∞. –Ф–∞–ї—М–љ–µ–є—И–µ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є —Ж–Є–Ї–ї–∞ –Љ–Њ—З–µ–≤–Є–љ—Л –њ—А–Є–≤–Њ–і–Є—В –Ї –і–µ–њ—А–µ—Б—Б–Є–Є —А–µ–∞–Ї—Ж–Є–Є: NH4 + HCO3 + AT–§ = –Ї–∞—А–±–∞–Љ–∞–Є–ї–—Д–Њ—Б—Д–Њ—А–љ–∞—П –Ї–Є—Б–ї–Њ—В–∞, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —З–µ–≥–Њ –љ–∞–Ї–∞–њ–ї–Є–≤–∞—О—В—Б—П –Є–Њ–љ—Л HCO3, –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –∞–ї–Ї–∞–ї–Њ–Ј, –њ—А–Є —Н—В–Њ–Љ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Г—Б–Ї–Њ—А–µ–љ–љ–Њ–µ –њ—А–µ–≤—А–∞—Й–µ–љ–Є–µ NH4 –≤ NH3, –љ–∞—А–∞—Б—В–∞–µ—В —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ –Ї–ї–µ—В–Њ–Ї –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. «–Я–Њ—А–Њ—З–љ—Л–є –Ї—А—Г–≥» –Ј–∞–Љ—Л–Ї–∞–µ—В—Б—П.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –≤–Њ–Ј–љ–Є–Ї–∞—О—В –Њ—З–µ–љ—М –≥–ї—Г–±–Њ–Ї–Є–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П, —В—А–µ–±—Г—О—Й–Є–µ –њ—А–Є—Б—В–∞–ї—М–љ–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П –Ї–ї–Є–љ–Є—Ж–Є—Б—В–∞.
–Э—Г—В—А–Є—В–Є–≤–љ–∞—П –њ–Њ–і–і–µ—А–ґ–Ї–∞ –њ—А–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —П–≤–ї—П–µ—В—Б—П –∞–Ї—В—Г–∞–ї—М–љ–Њ–є —Б–Њ—Б—В–∞–≤–ї—П—О—Й–µ–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Н—В–Њ–≥–Њ –Њ–њ–∞—Б–љ–Њ–≥–Њ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є, —Г—Б–Є–ї–Є–≤–∞—О—Й–Є–Љ –љ—Г—В—А–Є—В–Є–≤–љ—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е —Б –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О, —П–≤–ї—П—О—В—Б—П:
1. –Р–љ–Њ—А–µ–Ї—Б–Є—П
2. –Ґ–Њ—И–љ–Њ—В–∞
3. –†–≤–Њ—В–∞
4. –Я–Њ–љ–Њ—Б
5. –Я–∞–љ–Ї—А–µ–∞—В–Є—З–µ—Б–Ї–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М
6. –Ф–µ—Д–Є—Ж–Є—В –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В
7. –≠–љ—В–µ—А–Њ–њ–∞—В–Є—П
8. –Р—Б—Ж–Є—В
9. –Ш–љ—Д–µ–Ї—Ж–Є–Є
10. –Э–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї
11. –£–≤–µ–ї–Є—З–µ–љ–љ—Л–є —А–∞—Б–њ–∞–і –±–µ–ї–Ї–∞
12. –°–љ–Є–ґ–µ–љ–љ—Л–є —Б–Є–љ—В–µ–Ј –±–µ–ї–Ї–∞
–•–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—П –њ—А–µ–њ–∞—А–∞—В—Л –і–ї—П –ї–µ—З–µ–љ–Є—П –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –Љ–Њ–ґ–љ–Њ —Г—Б–ї–Њ–≤–љ–Њ —А–∞–Ј–і–µ–ї–Є—В—М –Є—Е –љ–∞ —Б–ї–µ–і—Г—О—Й–Є–µ –≥—А—Г–њ–њ—Л:
1. «–Ь–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ» —Б—А–µ–і—Б—В–≤–∞ (–љ–∞–њ—А–Є–Љ–µ—А, –У–µ–њ–∞—Б–Њ–ї®––Э–µ–Њ, –≥—А–∞–љ—Г–ї—Л –Т–°–Р–Р);
2. –Я–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ (–љ–∞–њ—А–Є–Љ–µ—А: –Р–Љ–Є–љ–Њ—Б–Њ–ї®––Э–µ–Њ, –Ш–љ—Д–µ–Ј–Њ–ї 40, 100 –Є –і—А.);
3. –°–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ – «–≥–µ–њ–∞» (–љ–∞–њ—А–Є–Љ–µ—А: –У–µ–њ–∞—Б–Њ–ї®-–Э–µ–Њ, –Р–Љ–Є–љ–Њ—Б—В–µ—А–Є–ї––≥–µ–њ–∞, –Р–Љ–Є–љ–Њ–њ–ї–∞–Ј–Љ–∞–ї—М––≥–µ–њ–∞);
4. –≠–љ—В–µ—А–∞–ї—М–љ—Л–µ —Б–Љ–µ—Б–Є: —Б –њ–Є—Й–µ–≤—Л–Љ–Є –≤–Њ–ї–Њ–Ї–љ–∞–Љ–Є (fiber) –Є–ї–Є —Б –њ—А–Є—Б—В–∞–≤–Ї–Њ–є «–≥–µ–њ–∞» (–љ–∞–њ—А–Є–Љ–µ—А: –Э—Г—В—А–Є–Ї–Њ–Љ–њ–—Д–∞–є–±–µ—А, –Э—Г—В—А–Є—Н–љ –У–µ–њ–∞ –Є –і—А.).
–Ш–љ—В–µ—А–µ—Б–љ—Л–Љ –≤ —В–µ—А–∞–њ–Є–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ «–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е» –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ъ–Њ–љ–µ—З–љ–Њ, —В–µ—А–Љ–Є–љ «–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ» —П–≤–ї—П–µ—В—Б—П –і–Є—Б–Ї—Г—В–∞–±–µ–ї—М–љ—Л–Љ, –Њ–і–љ–∞–Ї–Њ —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –Љ–Њ–≥—Г—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –Ї–∞–Ї —Г –±–Њ–ї—М–љ—Л—Е —Б –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є, —В–∞–Ї –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є.
–У–µ–њ–∞—Б–Њ–ї®––Э–µ–Њ – —Н—В–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В, –њ—А–µ–і—Б—В–∞–≤–ї—П—О—Й–Є–є —Б–Њ–±–Њ–є —А–∞—Б—В–≤–Њ—А –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В. –Т —Б–Њ—Б—В–∞–≤ –У–µ–њ–∞—Б–Њ–ї–∞®––Э–µ–Њ –≤—Е–Њ–і—П—В –≤—Б–µ 8 –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, –Ї–Њ—В–Њ—А—Л–µ –Њ—А–≥–∞–љ–Є–Ј–Љ —З–µ–ї–Њ–≤–µ–Ї–∞ –љ–µ –Љ–Њ–ґ–µ—В —Б–Є–љ—В–µ–Ј–Є—А–Њ–≤–∞—В—М (L––≤–∞–ї–Є–љ, L––Є–Ј–Њ–ї–µ–є—Ж–Є–љ, L––ї–µ–є—Ж–Є–љ, L––ї–Є–Ј–Є–љ, L––Љ–µ—В–Є–Њ–љ–Є–љ, L–—В—А–µ–Њ–љ–Є–љ, L–—Д–µ–љ–Є–ї–∞–ї–∞–љ–Є–љ, L–—В—А–Є–њ—В–Њ—Д–∞–љ), 2 —Г—Б–ї–Њ–≤–љ–Њ–Ј–∞–Љ–µ–љ–Є–Љ—Л–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л (L––∞—А–≥–Є–љ–Є–љ –Є L––≥–Є—Б—В–Є–і–Є–љ), –Ї–Њ—В–Њ—А—Л–µ —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В—Б—П –≤ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ –њ—А–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е, –Є 5 –Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є—Е –∞–і–µ–Ї–≤–∞—В–љ—Л–є –Њ–±–Љ–µ–љ –≤–µ—Й–µ—Б—В–≤ —Г –±–Њ–ї—М–љ—Л—Е —Б –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–µ—З–µ–љ–Є. –Р–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л –љ–∞—Е–Њ–і—П—В—Б—П –≤ L–—Д–Њ—А–Љ–µ, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Є—Е –њ—А—П–Љ–Њ–≥–Њ —Г—З–∞—Б—В–Є—П –≤ –±–Є–Њ—Б–Є–љ—В–µ–Ј–µ –±–µ–ї–Ї–Њ–≤ (—Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –∞–Ј–Њ—В–∞ – –≤—Б–µ–≥–Њ 12,9 –≥/–ї). L––∞—А–≥–Є–љ–Є–љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ—А–µ–≤—А–∞—Й–µ–љ–Є—О –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Љ–Њ—З–µ–≤–Є–љ—Г, —Б–≤—П–Ј—Л–≤–∞–µ—В —В–Њ–Ї—Б–Є—З–љ—Л–µ –Є–Њ–љ—Л –∞–Љ–Љ–Њ–љ–Є—П, –Њ–±—А–∞–Ј—Г—О—Й–Є–µ—Б—П –њ—А–Є –Ї–∞—В–∞–±–Њ–ї–Є–Ј–Љ–µ –±–µ–ї–Ї–Њ–≤ –≤ –њ–µ—З–µ–љ–Є. L––∞–ї–∞–љ–Є–љ –Є L––њ—А–Њ–ї–Є–љ —Г–Љ–µ–љ—М—И–∞—О—В –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –≤ –≥–ї–Є—Ж–Є–љ–µ (—Н—В–∞ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–∞ —Б–ї–∞–±–Њ —Г—Б–≤–∞–Є–≤–∞–µ—В—Б—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ, –њ—А–Є –µ–µ –Ј–∞–Љ–µ–љ–µ —А–∞–Ј–≤–Є—В–Є–µ –≥–Є–њ–µ—А–∞–Љ–Љ–Њ–љ–Є–µ–Љ–Є–Є —Б—В–∞–љ–Њ–≤–Є—В—Б—П –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ). L––Є–Ј–Њ–ї–µ–є—Ж–Є–љ, L––ї–µ–є—Ж–Є–љ –Є L––≤–∞–ї–Є–љ (–љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л —Б —А–∞–Ј–≤–µ—В–≤–ї–µ–љ–љ—Л–Љ–Є –±–Њ–Ї–Њ–≤—Л–Љ–Є —Ж–µ–њ—П–Љ–Є) –њ—А—П–Љ–Њ —Г—Б–≤–∞–Є–≤–∞—О—В—Б—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–Љ–Є —В–Ї–∞–љ—П–Љ–Є (–Є—Е –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –љ–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б—В–µ–њ–µ–љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–µ—З–µ–љ–Є), —Б–љ–Є–ґ–∞—О—В —Г—Б–≤–Њ–µ–љ–Є–µ –Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –≤ –¶–Э–°, —Г–Љ–µ–љ—М—И–∞—П –њ—А–Њ—П–≤–ї–µ–љ–Є—П –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є, –љ–Њ—А–Љ–∞–ї–Є–Ј—Г—О—В —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є–є –Є –∞–Ј–Њ—В–љ—Л–є –±–∞–ї–∞–љ—Б –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ.
–У–µ–њ–∞—Б–Њ–ї®––Э–µ–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Ї–Њ—А—А–Є–≥–Є—А–Њ–≤–∞—В—М –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –∞ —В–∞–Ї–ґ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–ї—Г—З—И–Є—В—М –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –±–µ–ї–Ї–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е —Ж–Є—А—А–Њ–Ј–Њ–Љ –њ–µ—З–µ–љ–Є–Є, –≥–µ–њ–∞—В–Є—В–Њ–Љ –Є —Г–Љ–µ–љ—М—И–Є—В—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є. –Э–µ —Б–Њ–і–µ—А–ґ–Є—В —Г–≥–ї–µ–≤–Њ–і–Њ–≤ –Є —Н–ї–µ–Ї—В—А–Њ–ї–Є—В–Њ–≤.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤—Л—Б–Њ–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –У–µ–њ–∞—Б–Њ–ї–∞®––Э–µ–Њ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П: –≤—Л—Б–Њ–Ї–Є–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ–Љ –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е, —Г—Б–ї–Њ–≤–љ–Њ –Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –Є –Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ —А–∞–Ј–≤–µ—В–≤–ї–µ–љ–љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –≤—Л—А–∞–ґ–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–∞ –њ—А–Њ—Ж–µ—Б—Б—Л –∞–љ–∞–±–Њ–ї–Є–Ј–Љ–∞, –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –∞–Љ–Љ–Є–∞–Ї–∞ –Є —П–≤–ї—П–µ—В—Б—П –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ —Н–љ–µ—А–≥–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –≤ –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є.
–У–µ–њ–∞—Б–Њ–ї®-–Э–µ–Њ –≤–≤–Њ–і–Є—В—Б—П –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ –Ї–∞–њ–µ–ї—М–љ–Њ. –†–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–Њ–≤–Њ–і–Є—В—М –Є–љ—Д—Г–Ј–Є—О —Б–Њ —Б–Ї–Њ—А–Њ—Б—В—М—О 1,0–1,25 –Љ–ї/–Ї–≥ –Љa—Б—Б—Л —Вe–їa/—З (30–35 –Ї–∞–њ./–Љ–Є–љ.), —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В 0,08–0,1 –≥ a–Љ–Є–љo–Ї–Є—Б–їo—В/–Ї–≥ –Љa—Б—Б—Л —Вe–їa/—З. Ma–Ї—Б–Є–Љa–ї—М–љa—П —Б–Їo—Аo—Б—В—М –≤–≤e–іe–љ–Є—П – 1,25 –Љ–ї/–Ї–≥ –Љa—Б—Б—Л —Вe–їa/—З (—Бoo—В–≤e—В—Б—В–≤e–љ–љo 0,1 –≥ a–Љ–Є–љo–Ї–Є—Б–їo—В/–Ї–≥ –Љa—Б—Б—Л —Вe–їa/—З). Ma–Ї—Б–Є–Љa–ї—М–љa—П —Б—Г—Вo—З–љa—П –іo–Јa —Бo—Б—Вa–≤–ї—Пe—В 18,75 –Љ–ї/–Ї–≥ –Љa—Б—Б—Л —Вe–їa (1,5 –≥ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В/–Ї–≥ –Љ–∞—Б—Б—Л —В–µ–ї–∞/—Б—Г—В–Ї–Є), —В.e. 1300 –Љ–ї –і–ї—П –±o–ї—М–љo–≥o –Љ–∞—Б—Б–Њ–є 70 –Ї–≥.
–Р–Љ–Є–љ–Њ—Б–Њ–ї®––Э–µ–Њ – –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П, –Ї–Њ—В–Њ—А—Л–є —Б–Њ–і–µ—А–ґ–Є—В –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л–µ –Є –Ј–∞–Љ–µ–љ–Є–Љ—Л–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л –≤ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–Љ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–Є. –Т—Б–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л –љ–∞—Е–Њ–і—П—В—Б—П –≤ L–—Д–Њ—А–Љ–µ, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Є—Е –њ—А—П–Љ–Њ–≥–Њ —Г—З–∞—Б—В–Є—П –≤ –±–Є–Њ—Б–Є–љ—В–µ–Ј–µ –±–µ–ї–Ї–Њ–≤.
–°–Њ–і–µ—А–ґ–Є—В –≤–Њ—Б–µ–Љ—М –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В (–љ–µ —Б–Є–љ—В–µ–Ј–Є—А—Г–µ–Љ—Л—Е –Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–Љ —З–µ–ї–Њ–≤–µ–Ї–∞): L––Є–Ј–Њ–ї–µ–є—Ж–Є–љ, L––ї–µ–є—Ж–Є–љ, L––ї–Є–Ј–Є–љ, L––Љ–µ—В–Є–Њ–љ–Є–љ, L–—Д–µ–љ–Є–ї–∞–ї–∞–љ–Є–љ, L–—В—А–µ–Њ–љ–Є–љ, L–—В—А–Є–њ—В–Њ—Д–∞–љ –Є L––≤–∞–ї–Є–љ. –£—Б–ї–Њ–≤–љ–Њ –Ј–∞–Љ–µ–љ–Є–Љ—Л–Љ–Є —Б—З–Є—В–∞—О—В—Б—П L––∞—А–≥–Є–љ–Є–љ –Є L––≥–Є—Б—В–Є–і–Є–љ. –Ю–љ–Є —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В—Б—П –Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–Љ, –љ–Њ –њ—А–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е (–љ–∞–њ—А–Є–Љ–µ—А, –њ–Њ—З–µ—З–љ–∞—П –Є –њ–µ—З–µ–љ–Њ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М) –Є —Г –Љ–∞–ї–µ–љ—М–Ї–Є—Е –і–µ—В–µ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Є—Е –љ–µ –і–Њ—Б—В–Є–≥–∞–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П.
L––∞—А–≥–Є–љ–Є–љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–Љ—Г –њ—А–µ–≤—А–∞—Й–µ–љ–Є—О –∞–Љ–Љ–Є–∞–Ї–∞ –≤ –Љ–Њ—З–µ–≤–Є–љ—Г, —Б–≤—П–Ј—Л–≤–∞—П —В–Њ–Ї—Б–Є—З–љ—Л–µ –є–Њ–љ—Л –∞–Љ–Љ–Њ–љ–Є—П, –Ї–Њ—В–Њ—А—Л–µ –Њ–±—А–∞–Ј—Г—О—В—Б—П –њ—А–Є –Ї–∞—В–∞–±–Њ–ї–Є–Ј–Љ–µ –њ—А–Њ—В–µ–Є–љ–Њ–≤ –≤ –њ–µ—З–µ–љ–Є.
L––Є–Ј–Њ–ї–µ–є—Ж–Є–љ, L––ї–µ–є—Ж–Є–љ –Є L––≤–∞–ї–Є–љ – –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л —Б —А–∞–Ј–≤–µ—В–≤–ї–µ–љ–љ—Л–Љ–Є –±–Њ–Ї–Њ–≤—Л–Љ–Є —Ж–µ–њ—П–Љ–Є - —Г–і–Њ–≤–ї–µ—В–≤–Њ—А—П—О—В —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, —З—В–Њ –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ–Њ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ.
–Р–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л, —Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –Ї–Њ–ї—М—Ж–∞, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л L–—Д–µ–љ–Є–ї–∞–ї–∞–љ–Є–љ–Њ–Љ –Є L–—В–Є—А–Њ–Ј–Є–љ–Њ–Љ –≤ –љ–µ–±–Њ–ї—М—И–Њ–Љ –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ, —З—В–Њ –≤—Л–Ј–≤–∞–љ–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О —Ж–µ—А–µ–±—А–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ—А–Є –≤—Л—Б–Њ–Ї–Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—Е. –У–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –Љ–Є–љ–Є–Љ–Є–Ј–∞—Ж–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П–µ—В—Б—П –љ–∞ L–—В–Є—А–Њ–Ј–Є–љ, –Њ–і–љ–Є–Љ –Є–Ј –і–µ—А–Є–≤–∞—В–Њ–≤ –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–ї—П–µ—В—Б—П –Њ–Ї—В–Њ–њ–∞–Љ–Є–љ – –ї–Њ–ґ–љ—Л–є –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—В—В–µ—А, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–є —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ —Ж–µ–љ—В—А–∞–ї—М–љ—Г—О –љ–µ—А–≤–љ—Г—О —Б–Є—Б—В–µ–Љ—Г.
–Р–Љ–Є–љ–Њ—Б–Њ–ї®––Э–µ–Њ –њ—А–Є–Љ–µ–љ—Пe—В—Б—П –≤ –≤–Є–і–µ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є —Зe—Аe–Ј o–і–љ—Г –Є–Ј —Жe–љ—В—Аa–ї—М–љ—Л—Е –≤e–љ. –Фo–Ј–Є—Аo–≤–Їa –Є–љ–і–Є–≤–Є–і—Гa–ї—М–љa—П, —Б —Г—З–µ—В–Њ–Љ —В—П–ґe—Б—В–Є –Љe—Вa–±o–ї–Є—Зe—Б–Їo–≥o –љa—А—Г—Иe–љ–Є—П –Є –њo—В—Аe–±–љo—Б—В–Є o—А–≥a–љ–Є–Ј–Љa –≤ a–Љ–Є–љo–Ї–Є—Б–їo—Вa—Е.
–Т–°–Р–Р – —Н—В–Њ –Њ–±–Њ–Ј–љ–∞—З–µ–љ–Є–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В —Б —А–∞–Ј–≤–µ—В–≤–ї–µ–љ–љ–Њ–є —Ж–µ–њ—М—О, –Т–°–Р–Р –≤—Л–њ—Г—Б–Ї–∞—О—В—Б—П –≤ –≤–Є–і–µ –≥—А–∞–љ—Г–ї, –∞ —В–∞–Ї–ґ–µ —Б–Њ–і–µ—А–ґ–∞—В—Б—П –≤ —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л—Е —А–∞—Б—В–≤–Њ—А–∞—Е —Б –њ—А–Є—Б—В–∞–≤–Ї–Њ–є «–≥–µ–њ–∞». –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Т–°–Р–Р –Њ—Б–љ–Њ–≤–∞–љ–Њ –љ–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Ј–љ–∞–Љ–µ–љ–Є—В–Њ–≥–Њ —Г—З–µ–љ–Њ–≥–Њ –§–Є—И–µ—А–∞, –њ–Њ–Ї–∞–Ј–∞–≤—И–Є—Е, —З—В–Њ –≤ —В–µ—А–∞–њ–Є–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В —Б –∞—А–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є —Ж–µ–њ—М—О –Ї –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–∞–Љ —Б —А–∞–Ј–≤–µ—В–≤–ї–µ–љ–љ–Њ–є —Ж–µ–њ—М—О –і–Њ–ї–ґ–љ–Њ –±—Л—В—М —Г–≤–µ–ї–Є—З–µ–љ–Њ –≤ —Б—В–Њ—А–Њ–љ—Г –Т–°–Р–Р. –≠—В–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –±—Л–ї–Њ –љ–∞–Ј–≤–∞–љ–Њ –Є–љ–і–µ–Ї—Б–Њ–Љ –§–Є—И–µ—А–∞. –Т –љ–Њ—А–Љ–µ –Є–љ–і–µ–Ї—Б –§–Є—И–µ—А–∞ = 3–3,5, –њ—А–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є –Њ–љ —Б–љ–Є–ґ–∞–µ—В—Б—П –і–Њ 1,5 –Є –Љ–µ–љ–µ–µ [4]. –Т–≤–µ–і–µ–љ–Є–µ –Т–°–Р–Р –њ–Њ–Ј–≤–Њ–ї—П–µ—В –∞–Ї—В–Є–≤–Є–Ј–Є—А–Њ–≤–∞—В—М –≥–ї—Г—В–∞–Љ–Є–љ–Њ–≤—Л–є —Ж–Є–Ї–ї –≤ –Љ—Л—И–µ—З–љ–Њ–є —В–Ї–∞–љ–Є –Є —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞—В—М –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ –∞–Љ–Љ–Є–∞–Ї–∞, –Њ–і–љ–∞–Ї–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ–±—А–∞—Й–∞—В—М –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —В–Њ, —З—В–Њ–±—Л –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –≤–≤–Њ–і–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –љ–µ –њ—А–µ–≤—Л—И–∞–ї–Њ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–є —Г—А–Њ–≤–µ–љ—М –і–ї—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є.
–Я—А–Є —А–∞–Ј–≤–Є—В–Є–Є –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Б —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є 1–2 —Б—В–µ–њ–µ–љ–Є –Њ–±—К–µ–Љ –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –њ–Њ–і–і–µ—А–ґ–Ї–Є —А–∞—Б—Б—З–Є—В—Л–≤–∞–µ—В—Б—П –Є–Ј —Б–ї–µ–і—Г—О—Й–Є—Е –і–∞–љ–љ—Л—Е: –љ–µ–±–µ–ї–Ї–Њ–≤—Л—Е –Ї–∞–ї–Њ—А–Є–є 25–35 –Ї–Ї–∞–ї/–Ї–≥/—Б—Г—В., –±–µ–ї–Ї–∞ 1,5 –≥/–Ї–≥/—Б—Г—В., –њ—А–Є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є 3–4 —Б—В–µ–њ–µ–љ–Є –љ–µ–±–µ–ї–Ї–Њ–≤—Л—Е –Ї–∞–ї–Њ—А–Є–є 25–35 –Ї–Ї–∞–ї/–Ї–≥/—Б—Г—В., –±–µ–ї–Ї–∞ 0,5–1,2 –≥/–Ї–≥/—Б—Г—В. –°–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –ґ–Є—А—Л/—Г–≥–ї–µ–≤–Њ–і—Л –њ—А–µ–≤–∞–ї–Є—А—Г–µ—В –≤ —Б—В–Њ—А–Њ–љ—Г —Г–≥–ї–µ–≤–Њ–і–Њ–≤, –Њ–і–љ–∞–Ї–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –ґ–Є—А–Њ–≤—Л—Е —Н–Љ—Г–ї—М—Б–Є–є —В–∞–Ї–ґ–µ –і–Њ–ї–ґ–љ–Њ –њ–Њ—Б—В—Г–њ–∞—В—М [5].
–Ф–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤: –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –і–Њ 1,5–≥/–Ї–≥/—З, –≥–ї—О–Ї–Њ–Ј—Л –і–Њ 6 –≥/–Ї–≥/—З, –ґ–Є—А—Л –і–Њ 1,5 –≥/–Ї–≥/—З [6].
–Т—Л–≤–Њ–і. –Ґ–µ—А–∞–њ–Є—П –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –Њ—Б–љ–Њ–≤—Л–≤–∞–µ—В—Б—П –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –љ–∞ —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Є —В–Њ—З–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ —Н—В–Њ–≥–Њ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Г –Ї–ї–Є–љ–Є—Ж–Є—Б—В–Њ–≤ –њ–Њ—П–≤–Є–ї–Є—Б—М –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —Г–ї—Г—З—И–Є—В—М —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П —Н—В–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е –Ј–∞ —Б—З–µ—В –њ—А–Є–≤–ї–µ—З–µ–љ–Є—П –≤ —Б–≤–Њ–є –∞—А—Б–µ–љ–∞–ї –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є.


–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –†–Њ—Б—Б–Є–є—Б–Ї–Є–є –Ї–Њ–љ–≥—А–µ—Б—Б –њ–Њ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–Љ—Г –Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–Љ—Г –њ–Є—В–∞–љ–Є—О, 2002.
2. –Ґ–∞–Ї—Н–Њ –Ъ. –Я–µ—З–µ–љ–Њ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –Э–Є—В–Є–љ–∞–є—Б–Є 49: 1–33, 1960.
3. –Э–∞–≥–ї—П–і–љ–∞—П –±–Є–Њ—Е–Є–Љ–Є—П, —Н–ї–µ–Ї—В—А–Њ–љ–љ–Њ–µ –њ–Њ—Б–Њ–±–Є–µ. 2002.
4. –Ш–љ—Д–Њ—А–Љ–∞—Ж–Є—П —Д–Є—А–Љ—Л –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В–µ–ї—П – –•–µ–Љ–Њ—Д–∞—А–Љ.
5. –°–Њ–±–Њ—В–Ї–∞ –Ы. –Ю—Б–љ–Њ–≤—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П. 2003.
6. –Ь–µ—В–Њ–і. –њ–Є—Б—М–Љ–Њ. –Ь–µ—В–Њ–і–Њ–ї–Њ–≥–Є—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –Є —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ—Л—Е –±–Њ–ї—М–љ—Л—Е. 2003.








.gif)



