Введение
Крайне важным этапом в диагностике и разработке стратегии лечения злокачественных новообразований является патоморфологическая верификация диагноза. Выбор режимов специального лечения, возможность таргетной и иммунотерапии, необходимость смены линии химиотерапии — вот лишь несколько условий, которые позволяют своевременно выполнить гистологическое исследование.
Существует несколько способов получения материала из опухоли [1]:
открытая биопсия в рамках хирургической операции;
эндоскопическая биопсия (в ходе лапаро- или видеоторакоскопии, эндоскопического исследования полых органов, чрезбронхиальная биопсия объемных образований легких и средостения);
тонкоигольная аспирационная биопсия;
чрескожная трепан-биопсия.
Каждый вид биопсии обладает своими преимуществами и недостатками.
Открытая биопсия выполняется в ходе классического хирургического вмешательства и представляет собой либо забор нескольких участков опухоли при невозможности полной циторедукции, либо тотальное удаление объемного образования или пораженного лимфатического узла с их последующим масштабным гистологическим исследованием. Бесспорным преимуществом данного вида биопсии является получение большого количества опухолевого материала. К недостаткам метода можно отнести необходимость госпитализации пациента, полноценное анестезиологическое сопровождение биопсии, операционную травму и послеоперационные осложнения. На сегодняшний день эксцизионная биопсия в формате циторедуктивной операции является максимально информативным методом одновременно и диагностики, и лечения. Однако существует ряд клинических ситуаций (прогрессирование заболевания и необходимость изучения биологии метастатического очага, прямые противопоказания к циторедукции), в которых предпочтение следует отдавать менее инвазивным методикам.
Эндоскопическая биопсия в различных ее модификациях получила широчайшее распространение и является методом выбора при опухолях желудочно-кишечного тракта, гепатобилиарной зоны, ЛОР-органов, центральном раке легкого [2]. Лапароскопические и торакоскопические видеоассистированные вмешательства также активно внедрены в повседневную клиническую практику и вытесняют эксплоративные лапаротомии и торакотомии, демонстрируя гораздо меньший процент осложнений благодаря снижению объемов операционной травмы. Эндоскопические вмешательства позволяют получить значительный объем материала для патоморфологического исследования и занимают весьма значимое место в арсенале хирургической онкологии. Вместе с тем в случаях метастатического поражения паренхиматозных органов, при технически сложном доступе или высоких анестезиологических рисках данный вид диагностических операций бывает невозможен. Кроме того, не все медицинские учреждения имеют в своем распоряжении специализированные, хорошо оснащенные отделения торакальной или абдоминальной хирургии, что ограничивает выполнение соответствующих видеоассистированных вмешательств.
Тонкоигольная аспирационная биопсия (ТАБ) является самым простым, легко воспроизводимым в амбулаторных условиях методом получения материала для исследования. Наиболее часто, как в случаях выполнения пункций лимфатических узлов или молочной железы, данный вид биопсий осуществляется без сопровождения каким-либо методом медицинской визуализации. Однако же при необходимости всегда возможно применение навигации с помощью ультразвукового сканирования. Основным и самым главным недостатком ТАБ является закономерно незначительное количество получаемого опухолевого материала, что, в свою очередь, позволяет выполнить только цитологическое исследование, указывающее лишь на наличие или отсутствие опухолевых клеток в образце. Подготовка парафинового блока с последующей его нарезкой и окраской, выполнение иммуногистохимического и молекулярно-генетического исследований по результатам ТАБ практически невозможны, что автоматически сводят на нет все преимущества данного метода для онколога.
Наиболее щадящим для пациента и одновременно информативным способом получения опухолевого материала является чрескожная трепан-биопсия (ТБ), которая позволяет получить достаточное количество ткани для иммуногистохимического и молекулярно-генетического анализов. Чрескожные ТБ выполняются под контролем компьютерной томографии (КТ), ультразвукового сканирования (УЗИ), а в последние годы при наличии показаний — под контролем магнитно-резонансной томографии (МРТ). При необходимости, для максимально прицельного планирования и выполнения вмешательства, возможно аппаратное или когнитивное совмещение изображений, полученных различными методами лучевой диагностики, — fusion [3]. ТБ производится в условиях местной анестезии и заключается в проведении специальной иглы к опухолевой массе с последующим забором различного количества столбиков ткани. Вместе с тем ряд организационных трудностей, ограниченная доступность расходных материалов и отсутствие у многих врачей навыков когнитивного таргетинга с совмещением результатов позитронно-эмиссионной компьютерной томографии (ПЭТ-КТ), МРТ и КТ, препятствуют широкому распространению данной методики.
Цель исследования: разработать и внедрить стандартные подходы к выполнению чрескожных биопсий солидных новообразований под контролем различных методов медицинской визуализации.
Материал и методы
В 2016–2018 гг. в онкологической клинике МИБС было выполнено 280 чрескожных ТБ опухолей различной локализации: средостения, легкого, поджелудочной железы, почки, печени, предстательной железы, молочной железы, костных метастазов и внеорганных новообразований. ТБ выполнялись под контролем мультиспиральной компьютерной томографии (МСКТ), УЗИ, МРТ. В 11 случаях использовался когнитивный фьюжн КТ+ПЭТ-КТ и КТ+МРТ. Ведущим методом визуализации, используемым непосредственно в ходе биопсии, являлась МСКТ с толщиной срезов 1,5 мм. При необходимости исследование выполняли с внутривенным контрастным усилением с помощью автоматического инжектора. Первоначально вмешательства проводились на стандартном столе томографа; однако с учетом накопленного клинического опыта укладка пациентов была модифицирована, а процедура стала выполняться на плоском рентгенпрозрачном столе, предназначенном для планирования лучевой терапии. При выявлении технических трудностей доступа (близкое расположение к опухоли магистральных сосудов или полых органов) выполняли 3D-реконструкцию. Все вмешательства производили в диагностическом кабинете (КТ или МРТ, ультразвуковой диагностики) в асептических условиях, с соответствующей обработкой операционного поля и инструментов.
В 11 сложных клинических ситуациях, при недостаточной визуализации опухолевой массы в ходе нативной КТ, выполнялся когнитивный фьюжн — совмещение на рабочей консоли изображений КТ и ПЭТ-КТ или КТ и МРТ. В одном случае биопсия образования печени выполнялась под контролем МРТ, это было обусловлено размерами очага 6,5×6,0 мм и его расположением в VI сегменте.
Все хирургические манипуляции производились по технологии free hand с помощью коаксиальных игл прямого доступа, через которые заводились биопсийные иглы на автоматических пистолетах различных производителей. Исходя из спланированной в ходе первичного КТ-сканирования траектории, иглы проводились в опухолевую массу под различным углом относительно анатомических ориентиров или стола томографа.
Для трансторакальных биопсий органов грудной полости и средостения применялись наборы Tsunami Medical, выбор размера иглы (18 или 20G), как и длины столбика (12 или 25 мм), осуществлялся в каждом случае индивидуально и зависел от расположения очага и его топографических взаимоотношений с другими анатомическими структурами. Для периферических новообразований, с предполагаемой короткой дистанцией прохождения через здоровую ткань легкого, использовались иглы большего диаметра. Для центрально расположенных очагов, с целью минимизации травмы и снижения риска развития тяжелого пневмоторакса, обычно применялись более тонкие иглы 20G.
При чрескожных биопсиях паренхиматозных органов брюшной полости, забрюшинного пространства и внеорганных очаговых образований использовались коаксиальные и биопсийные иглы на автоматическом пистолете Bard Magnum. Наиболее часто применялись комплекты игл C1620 и MN1620. В отдельных случаях, при поверхностном расположении опухолей, вмешательство выполнялось с помощью игл 1420. Длина столбика (15 или 22 мм) также варьировала в зависимости от размеров очага и его взаимоотношений с другими органами.
Для биопсии под контролем МРТ использовали немагнитную титановую иглу прямого доступа 18G и стандартный одноразовый автоматический пистолет в комплекте. Возможность работы данным набором предварительно была проверена в условиях магнитного поля напряженностью 1,5 Т в томографе Siemens Magnetom Aera RT; манипуляция отрабатывалась на фантоме (рис. 1).
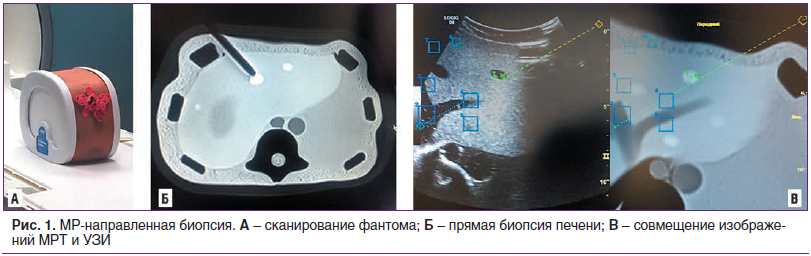
Для исследования использовали специальные дуги фирмы CIVCO, на которых крепилась катушка для тела, тем самым обеспечивался доступ хирурга к пунктируемой зоне. Протокол исследования состоял из адаптированных импульсных последовательностей turbo spin echo и vibe 3d в режиме Dixon. После получения первых сканов хирург вводил иглу, далее выполнялось повторное исследование в режимах Т2/Т1 для оценки положения иглы. С помощью инструментов замеряли оставшееся расстояние от кончика иглы до очага и угол наклона иглы. Последовательная корректировка положения иглы сопровождалась контрольным сканированием.
В случаях биопсии костных метастазов первый этап состоял в прохождении замыкательной пластинки кости и заборе столбика костной иглой 9G с последующим заведением через нее иглы MN1620 на пистолете Bard Magnum и забором мягкотканной части опухолевой массы.
В ходе выполнения биопсии следует выделить ряд этапов (рис. 2).
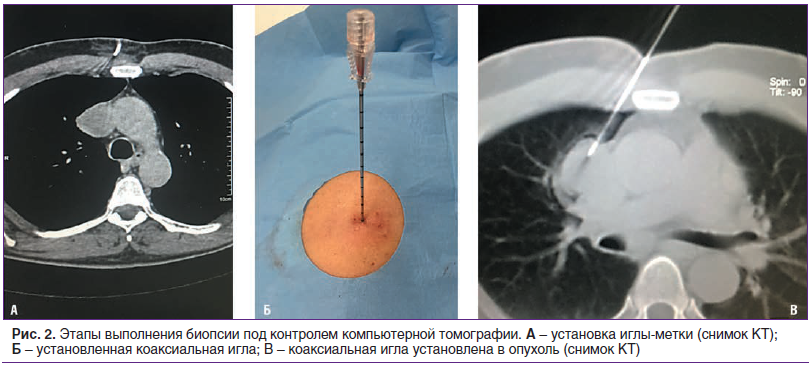
Нативное сканирование и разметка координат входа иглы. При биопсии образований средостения, легких, поджелудочной железы, печени в ряде случаев выполнялось болюсное контрастирование с оценкой васкуляризации предполагаемой зоны интереса.
Установка иглы-метки (обычно использовалась инъекционная игла после местной анестезии лидокаином) для оценки траектории и расчета глубины заведения иглы прямого доступа. Последующее повторное сканирование.
Введение коаксиальной иглы по рассчитанной траектории на необходимую глубину в толщу опухолевой массы и контрольный скан.
Введение биопсийной иглы по коаксиалу и забор необходимого количества столбиков.
Удаление коаксиальной иглы и контрольное сканирование для оценки возможных ранних осложнений, таких как гематома, пневмоторакс, повреждение полых органов.
Контрольное КТ-сканирование спустя минимум час после биопсии.
Для профилактики геморрагических осложнений на завершающем этапе в биопсийный канал вводили гемостатические препараты. При выявлении в ходе контрольной компьютерной томографии признаков продолжающегося кровотечения или формирования клинически значимой гематомы назначали системную гемостатическую терапию.
Результаты исследования
Первичная техническая успешность биопсии, которая заключается в гистологическом подтверждении наличия в парафиновых блоках атипичных клеток, составила 92% (257 биопсий). В 23 случаях потребовалось выполнение повторной биопсии. В связи с тем что проводка материала и его окраска гематоксилин-эозином занимает около 8 ч, повторное вмешательство выполнялось в среднем через сутки после неинформативной биопсии. При заборе материала из костных метастазов, вследствие необходимости предварительной декальцинации препарата, первичный ответ получали в среднем через 6 сут.
Средняя продолжительность биопсии, в зависимости от технической сложности, составила 32 мин (от 25 до 58 мин). Среднее число включений электронно-лучевой трубки компьютерного томографа — 5 (от 4 до 7). Число взятых столбиков ткани составило от 2 до 14 и варьировало в зависимости от типа, размеров и локализации опухоли, а также от сложности доступа. При расположении опухоли рядом с крупными магистральными сосудами (наиболее часто это встречалось в средостении и легком) приходилось ограничиваться двумя столбиками, поскольку риск повреждения полых вен или аорты в ходе вмешательства расценивался как высокий. Аналогичная ситуация, как правило, встречалась при вмешательствах на головке поджелудочной железы. Исходя из анатомии гепатобилиарной зоны, вариабельности расположения и подвижности полых органов брюшной полости, степени васкуляризации брыжеек и сальника, наиболее часто приходилось ограничиваться минимальным размером (длина 15 мм) и количеством образцов ткани. Максимальное количество материала удавалось получить в ходе биопсии метастатических очагов в печени.
В среднем на каждую биопсию использовался один комплект игл: коаксиальная и биопсийная. Исключения составили случаи биопсии объемных образований в костях (3 иглы) и сочетанные вмешательства (одномоментно костная биопсия и забор материала из солидного образования в паренхиматозном органе).
В 95,86% случаев чрескожные ТБ выполняли в условиях дневного стационара. К назначенному времени пациент прибывал в клинику с результатами необходимых анализов; затем производились разметка в томографе и само вмешательство, а спустя 1–2 ч — контрольное сканирование и выписка на амбулаторный этап. Продление госпитализации (перевод в хирургический стационар клиники) требовалось лишь при развитии осложнений и не превышало 1 койко-дня. Осложнения развились у 7 больных (2,5%). У одного пациента (биопсия объемного образования печени) развилось внутрибрюшное кровотечение, потребовавшее лапаротомии. В 2 случаях (биопсия поджелудочной железы и надпочечника) было диагностировано кровотечение: у 1 пациента — с образованием гематомы брыжейки поперечной ободочной кишки объемом 75 мл, у второго пациента — с образованием забрюшинной гематомы объемом 180 мл. В обеих ситуациях не потребовалось какого-либо хирургического вмешательства, кровотечения были остановлены консервативными мероприятиями, местной и системной гемостатической терапией. У 4 пациентов в результате трансторакальных биопсий было отмечено развитие пневмоторакса. Два из них протекали без выраженной клинической симптоматики: частота дыхательных движений в пределах 12–16, Sp02 96–99%. Однако у 2 пациентов объем пневмоторакса составил в среднем 400 мл, в связи с чем им была выполнена пункция плевральной полости с ультразвуковой навигацией (линейным датчиком) во II межреберье на стороне поражения с эвакуацией воздуха шприцем из набора Pleurocan и последующим рентгенологическим контролем спустя 1 и 2 ч соответственно. У одного из этих пациентов для разрешения пневмоторакса потребовалось дренирование плевральной полости и оксигенотерапия в течение суток. Рентгенологических признаков смещения средостения или развития дыхательной недостаточности не было ни у одного из больных.
Обсуждение результатов
В большинстве случаев в нашей стране биопсию рассматривают исключительно как метод верификации впервые выявленного онкологического диагноза. Вместе с тем в зарубежных публикациях в последние десятилетия четко прослеживается новая тенденция — использование биопсии для оценки биологии опухоли и ее патоморфоза в ходе специального лечения, особенно при неэффективности терапии и росте очагов (в т. ч. при местном рецидиве или продолженном росте), а также при появлении вторичных образований (метастазировании) [4].
Вопрос о том, какой специалист должен выполнять биопсию, в настоящее время является дискуссионным. В зарубежной традиции в большинстве случаев биопсию под контролем КТ выполняют врачи-рентгенологи, прошедшие дополнительное обучение по направлению «Интервенционная радиология». В России, в силу сложившихся традиций и образовательной модели, подобные вмешательства чаще выполняются врачами-хирургами с различной дополнительной специализацией. В нашей клинике операционная бригада состоит из врача-хирурга, врача-диагноста и операционной сестры. Исходя из собственного опыта, мы считаем такой подход оправданным. Во-первых, мануальные навыки врача-хирурга при технике free hand имеют далеко не последнее значение. Во-вторых, при развитии интраоперационных осложнений всегда существует вероятность конверсии, т. е. перевода изначально малоинвазивного вмешательства в большую открытую операцию, связанную с необходимостью остановки кровотечения либо ушивания поврежденного полого органа. И организационно (возможность максимально скорой подачи осложненного пациента в операционную или экстренного вмешательства по жизненным показаниям непосредственно на столе томографа), и стратегически (оперирующий хирург полностью владеет информацией о механизме, локализации и характере осложнения) такой подход выглядит логичным и оправданным.
В настоящее время производители оборудования разрабатывают и активно внедряют в клиническую практику различные системы навигации для малоинвазивных вмешательств, включающие в свой состав механические роботизированные устройства, предназначенные для закрепления и позиционирования биопсийной иглы [5]. При ряде локализаций опухоли (молочная или предстательная железа, головной мозг), где возможна жесткая фиксация анатомической области и адекватное устранение влияния дыхательных движений на подвижность мишени, подобные устройства значительно упрощают и стандартизируют технику биопсии [6]. Однако расположение очага в грудной или брюшной полости предполагает, что опухоль обязательно будет смещаться при дыхании пациента с достаточно значимой амплитудой (около 2–3 см). В этих случаях жесткое закрепление иглы в направляющей не обеспечит ее правильного попадания в мишень, а только будет способствовать травматизации окружающих тканей и самого биопсируемого органа. Именно по этим причинам мы в подавляющем числе случаев применяем технику free hand, при которой угол наклона, траектория и глубина введения иглы динамично меняются хирургом в ходе вмешательства, исходя из анализа рентгенологической картины, получаемой на каждом этапе (рис. 3).
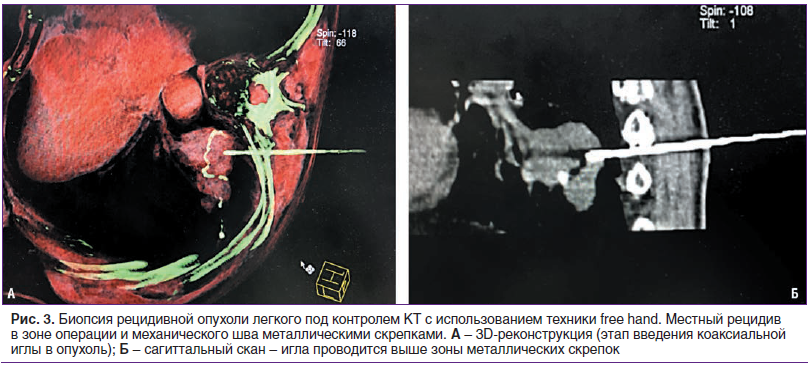
Техника «свободной руки» при необходимости позволяет моментально корректировать положение иглы, менять глубину ее установки, обходить стоящие на ее пути полые органы и крупные сосуды, не повреждая их, что в целом снижает хирургические риски и увеличивает вероятность успешного выполнения биопсии.
При использовании различных методов медицинской визуализации в диагностике злокачественных новообразований, даже в условиях адекватного контрастного усиления, рентгенологи и онкологи нередко сталкиваются со сложностями дифференциации между воспалительными и неопластическими процессами. Типичным примером служит параканкрозная пневмония при раке легкого, когда результаты КТ говорят лишь о наличии ателектаза сочетанного генеза. Невозможно точно и прицельно спланировать биопсию такого смешанного очага, и вероятность получения в материале лишь воспалительных изменений очень высока. В подобных клинических ситуациях мы используем технологию совмещения на одной консоли изображений (fusion), полученных на амбулаторном этапе с помощью ПЭТ-КТ и нативной КТ в ходе биопсии (рис. 4).
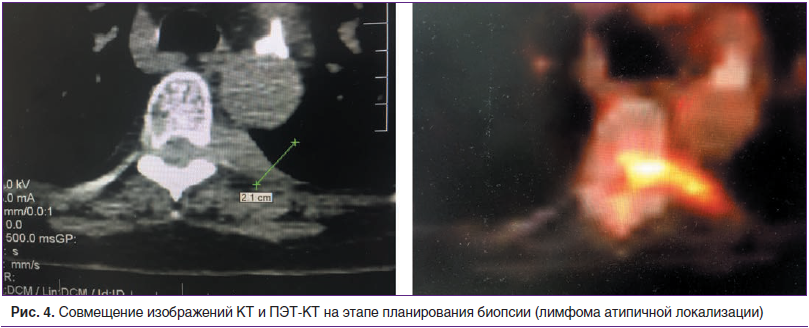
Помимо этого, у пациентов с очаговыми образованиями костного скелета оказалось возможным применение данного подхода, используя предоперационную МРТ с динамическим контрастированием. На практике мы столкнулись с ситуациями, в которых обычная рентгеновская КТ не позволяет визуализировать мягкотканный компонент опухоли, выходящий за пределы костной ткани, тогда как совмещение изображения с данными МРТ дает возможность четко идентифицировать расположение и размеры очага, тем самым упрощая планирование и выполнение биопсии.
Помимо КТ и технологии совмещения изображений, одним из наиболее современных и перспективных методов визуализации в ходе различных инвазивных вмешательств является МРТ. За последнее десятилетие биопсия образований предстательной и молочной желез под контролем МРТ во многих клиниках мира, в т. ч. и в нашей клинике, используется довольно широко [7]. Вместе с тем применение МРТ-навигации в ходе вмешательств на паренхиматозных органах пока ограничено. Существенным преимуществом биопсии печени под контролем МРТ по сравнению с другими диагностическими методами является возможность получить высокую тканевую контрастность патологического очага и окружающей ткани [8]. За счет этого минимальный размер пунктируемой зоны может быть снижен до 5 мм. С другой стороны, смещение внутренних органов, в т. ч. печени, вследствие дыхания пациента является важным фактором, накладывающим ряд требований к визуализации. Однако с появлением новых технологий сканирования его влияние можно устранить.
Внедряя данную методику, нам пришлось решить ряд технических задач.
За одну фазу сканирования (не более 20 с) получить массив данных, удовлетворяющий требованиям визуализации: пространственная разрешающая способность и межтканевая контрастность для определения форм и локализаций очаговых поражений от 5 мм и выше.
Визуализация органов брюшной полости предполагает использование специальной поверхностной катушки, которая накладывается на зону сканирования. В данном случае при сохранении качества визуализации необходимо обеспечить доступ к зоне биопсии для хирурга.
Срезы должны покрывать всю печень при одной задержке дыхания для исключения несовпадения анатомических изображений.
Геометрические искажения (дисторсия), создаваемые иглой, должны быть минимальными.
При настройке импульсных последовательностей оценивали параметры дисторсии от иглы и пространственной разрешающей способности. Результатом адаптации параметров стали 2 последовательности. Первая — t2 turbo spin echo в коронарной плоскости с высоким значением ширины полосы пропускания для снижения эффекта химического сдвига и дисторсии. Она проводилась без задержки дыхания, с триггером, отслеживающим движение диафрагмы. Для снижения динамических артефактов при сканировании на пациентах применялся метод расчета времени повторения импульсов в соответствии с индивидуальным циклом дыхания. Вторая последовательность — t1 vibe 3d в режиме Dixon, позволяющая получить 3 контрастности за один проход с толщиной среза 1,5 мм и покрытием всей печени в фазе, противофазе и в режиме жироподавления. Конструкция из дуг и катушки обеспечивает качественное изображение, полностью удовлетворяющее задачам визуализации. Имея в распоряжении высокоскоростные программы сбора данных, синхронизированные с дыханием пациента, можно добиться точного положения иглы. При этом с учетом толщины среза 3–4 мм минимальный размер очагов-мишеней может составлять 1 см и менее, что в ряде случаев важно и позволяет не ждать прогрессирования заболевания для гистологической верификации.
С точки зрения обеспечения доступа и использования расходных материалов существует 2 принципиально разных подхода. Ряд специалистов применяют только биопсийную иглу и автоматический пистолет, совершая для забора каждого столбика отдельный прокол. На наш взгляд, первичный доступ к очагу с помощью коаксиальной иглы, через которую затем заводится непосредственно биопсийная, обладает рядом преимуществ. Во-первых, в здоровых тканях остается только один биопсийный канал, а не несколько, что, особенно при вмешательстве на паренхиматозных органах (печень, почка), пропорционально снижает риск геморрагических осложнений. При биопсиях легкого наличие всего одного канала также снижает риск пневмоторакса. Во-вторых, забор и перемещение опухолевого материала внутри коаксиальной иглы, а не через здоровые ткани, обеспечивает абластичность и значительно уменьшает вероятность имплантационных метастазов — обсеменения опухолевыми клетками непораженных органов. В-третьих, при правильной установке иглы прямого доступа не требуется перепроверять ее положение при заборе каждого столбика. Простым наклоном данной иглы легко можно добиться получения материала из различных участков очага, что достаточно важно для качества и результата гистологического исследования, поскольку нередко опухоли, особенно метастатические, по своей структуре неоднородны и содержат обширные зоны некроза. Коаксиальная техника незначительно увеличивает себестоимость вмешательства, однако ее преимущества делают ее методом выбора [9].
Отдельным и стратегически важным вопросом является биопсия лимфатических узлов, пораженных метастазами, либо лимфопролиферативными заболеваниями. Как правило, механическое повреждение ткани лимфатического узла приводит к обширным артифициальным реактивным изменениям в столбиках ткани, что значительно снижает информативность патоморфологического исследования. В своей практике мы несколько раз сталкивались с невозможностью точного определения клеточного типа лимфомы даже по результатам иммуногистохимического исследования, в связи с чем в настоящее время, на наш взгляд, позиция, декларируемая в ведущих клинических рекомендациях по диагностике и лечению лимфопролиферативных заболеваний, является абсолютно оправданной, и методом выбора стала эксцизионная биопсия лимфатического узла целиком [10]. Также необходимо отметить, что при распространенной лимфаденопатии, для эксцизии необходимо выбирать максимально активный по результатам ПЭТ-КТ узел.
Выводы
Чрескожная ТБ объемных образований является технически несложным и относительно безопасным методом получения материала для патоморфологического исследования.
Технология совмещения изображений (КТ+ПЭТ-КТ, КТ+МРТ, УЗ+КТ, УЗ+МРТ) дает возможность точно планировать тип и объем вмешательства, траекторию и глубину проникновения биопсийной иглы.
Техника free hand и этапное выполнение биопсии с постоянным КТ-контролем позволяют безопасно выполнять вмешательство даже при малых размерах и сложной анатомической локализации опухоли. Использование коаксиальных игл позволяет минимизировать операционную травму и снизить риск имплантационного метастазирования.












