На 1-ю декаду марта 2016 г. зарегистрировано 8 712 810 человек (5955,0 на 100 тыс. населения) заболевших ОРВИ и 2 177 172 человека (1488,0 на 100 тыс. населения) заболевших гриппом [2]. По результатам мониторинга эпидемический подъем заболеваемости ОРВИ и гриппом начался на 2-й нед. 2016 г., когда превышение порогов по совокупному населению отмечалось в 13 субъектах РФ. В начале декабря 2015 г. на вирус гриппа А(Н1N1)/2009 приходилось 4% всех вирусных находок, выделенных из клинического материала от больных с гриппоподобными симптомами, после 4 января 2016 г. – до 24%, на 2-й нед. января – 35%, а в начале февраля – уже 42%. Эти данные подтверждают тот факт, что именно вирус А(Н1N1)/2009 является ведущим этиологическим агентом гриппа и определяет основную массу случаев заболевания в эпидемический сезон 2015–2016 гг. в РФ [2]. Результаты исследований полногеномного секвенирования, полученные российскими центрами слежения за вирусами гриппа в сезон 2015–2016 гг., свидетельствуют о том, что циркулирующий штамм вируса гриппа А(Н1N1)/2009 не отличается от вакцинного, что, несомненно, способствовало сдерживанию заболеваемости населения [2].
На 01.03.2016 г. превышение недельных эпидемических порогов по совокупному населению отмечалось только в 3-х субъектах РФ (Новосибирская и Сахалинская области, Республика Саха (Якутия) и 4-х крупных городах (Чебоксары, Ульяновск, Салехард, Красноярск).
Среди детей в возрасте 0–2 года превышение недельных порогов заболеваемости отмечено в 3-х субъектах РФ, 3–6 лет – в 4-х субъектах, 7–14 лет – в Сахалинской области и Республике Саха (Якутия), старше 15 лет – в Новосибирской и Сахалинской областях. По результатам вирусологического мониторинга в структуре циркулирующих респираторных вирусов также преобладали вирусы гриппа (до 73,7%) с доминированием вируса гриппа A(H1N1)/2009. Вместе с тем отмечена тенденция к увеличению числа заболевших гриппом типа В [2].
Возникновению последней пандемии гриппа 2009 г. предшествовали достаточно длительный период одномоментной циркуляции разных серотипов и подтипов серотипа вируса гриппа A, а также высокая активность других респираторных вирусов, микоплазм, хламидий и бактерий [3]. На этом фоне появление штамма вируса гриппа А(H1N1)/2009 с высокой восприимчивостью к нему населения привело к быстрому распространению заболеваемости гриппом на территории большинства стран мира. По данным ВОЗ, в ноябре 2009 г. 99% типированных вирусов гриппа относились к пандемичному штамму вируса А(H1N1). Подавляющее большинство выделенных из клинического материала вирусов проявляли чувствительность к препаратам, рекомендованным ВОЗ для лечения гриппа (осельтамивир и занамивир), и устойчивость к адамантанам (амантадин, римантадин) [9].
В соответствии с методическими рекомендациями ВОЗ по лечению и профилактике гриппа [5] и аналогичными российскими документами [4, 6, 7], врач должен назначить прием противовирусных препаратов (ПВП) сразу после появления первых типичных гриппоподобных симптомов, не дожидаясь результатов лабораторного подтверждения этиологии заболевания [5, 7]. Заболевание гриппом может проявляться в виде ряда симптомов – от легкой инфекции верхних дыхательных путей до острого, угрожающего жизни состояния.
Легкое или неосложненное течение гриппа характеризуется такими типичными симптомами, как лихорадка (возникает не у всех больных гриппом), кашель, боль в горле, ринорея, мышечная боль, головная боль, озноб, недомогание, иногда диарея и рвота. Для легкой степени течения гриппа не характерны выраженные обострения хронических состояний [8].
Прогрессирующее заболевание характеризуется типичными симптомами, а также признаками, предполагающими более тяжелое заболевание: болью в груди, плохой оксигенацией (например, одышка, гипоксия, затрудненное дыхание у детей), сердечно-легочной недостаточностью (например, низкое АД), нарушениями со стороны ЦНС (например, спутанность сознания, изменение психического состояния), сильным обезвоживанием, обострением хронических заболеваний: астмы, хронической обструктивной болезни легких, хронической почечной недостаточности, диабета или сердечно-сосудистых заболеваний (ССЗ) [8].
Тяжелое или осложненное заболевание характеризуется признаками заболевания нижних отделов дыхательных путей с рентгенологическим подтверждением (например, гипоксия, требующая оксигенотерапии или искусственной вентиляции легких), нарушений со стороны ЦНС (энцефалит, энцефалопатия), изменений со стороны сердечно-сосудистой системы (миокардит, резкое снижение АД), инфекционно-токсическим шоком, органной недостаточностью, развитием вторичной бактериальной инфекции [8]. Такие состояния требуют незамедлительной госпитализации и оказания высококвалифицированной медицинской помощи.
В группу риска по осложненному течению гриппа входит широкий круг пациентов (дети в возрасте <5 лет, пожилые люди >65 лет, беременные женщины или женщины в первые 2 нед. после родов, пациенты с ожирением при индексе массы тела (ИМТ) ≥40, постояльцы домов престарелых и других учреждений длительного ухода), лица с хроническим течением бронхолегочных заболеваний, ССЗ (за исключением изолированной артериальной гипертонии), хроническими заболеваниями почек и печени, неврологическими, гематологическими заболеваниями, заболеваниями эндокринной системы [14].
Вирусы гриппа относятся к группе высококонтагиозных возбудителей и передаются от человека человеку преимущественно воздушно-капельным путем при кашле, чихании, разговоре. Среди детей вирусы гриппа активно передаются также контактным путем. Инкубационный период длится от 1 до 4 дней (в среднем 2 дня). Выделение вирусов гриппа начинается за 1 день до начала проявления клинических симптомов и продолжается 5–7 дней. Наибольшее количество вирусов выделяется на фоне лихорадки в первые 2–3 дня заболевания, поэтому в рекомендациях ВОЗ инфекционный период при гриппе ограничивается периодом, который начинается за 1 день до начала лихорадки и заканчивается через 24 ч после ее прекращения.
В исследованиях Carrat F., Vergu E. et al. и Sophia N. et al. установлено, что тяжесть клинических проявлений гриппа коррелирует с количеством вирусов, циркулирующих в организме больного (рис. 1). Полученные в этих исследованиях данные подтверждают необходимость как можно более раннего начала приема специфических ПВП.
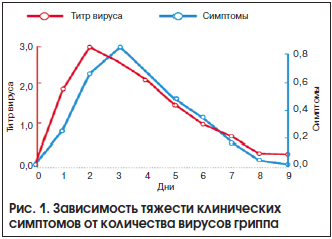
Тяжесть течения гриппа, в первую очередь в группах риска среди населения, значительное число случаев осложненного течения заболевания и повышенная летальность диктуют необходимость точного соблюдения протоколов и стандартов лечения, позволяющих эффективно воздействовать на возбудителя и минимизировать последствия его действия на организм человека.
Изучением эффективности, безопасности и особенностей применения лекарственных средств на популяционном уровне или среди больших групп людей с помощью эпидемиологических методов занимается фармакоэпидемиология. В задачи фармакоэпидемиологических исследований входят: характеристика, контроль и прогноз эффектов фармакотерапии, оценка риска развития нежелательных явлений при приеме лекарственных средств в популяции, изучение величины затрат на фармакотерапию.
При составлении протоколов клинических исследований ПВП лица с тяжелыми хроническими заболеваниями, как правило, попадают под критерии невключения. В то же время обсервационные фармакоэпидемиологические исследования позволяют оценить эффективность и безопасность препарата в условиях реальной клинической практики, в т. ч. у пациентов из групп риска и с отягощенным анамнезом. В этой связи важно анализировать результаты фармакоэпидемиологических исследований и учитывать их при выборе наиболее рациональных с точки зрения соотношения стоимость/эффективность методов лечения [1].
Ниже мы приводим результаты фармакоэпидемиологических исследований, которые проводились в РФ в течение нескольких эпидемических сезонов.
Во время пандемии гриппа 2009–2010 гг. в 9 регионах РФ проводилась оценка фармакотерапии гриппа у пациентов, находящихся в стационарах лечебно-профилактических учреждений (ЛПУ). В ходе исследования был проведен анализ историй болезни 284 пациентов, госпитализированных с диагнозами «грипп» и «ОРВИ». Результаты их изучения показали, что грипп А(H1N1) был лабораторно подтвержден у 250 (98%) пациентов, грипп В – у 2 (0,8%), ОРВИ – у 3 (1,2%). У 94,7% госпитализированных пациентов отмечалось среднетяжелое, у 5,3% – тяжелое течение болезни. Средняя длительность госпитализации составляла 8 дней. На догоспитальном этапе 54% пациентов, включенных в наблюдение, не получали этиотропного и симптоматического лечения гриппа; 27,4% пациентов принимали ПВП. При поступлении в стационар 67,5% пациентов получали монотерапию 1 ПВП, комбинация 2-х ПВП назначалась в 19,4% случаев [11]. У пациентов, начавших прием ПВП для лечения гриппа на догоспитальном этапе в первые 48 ч от момента появления первых симптомов, общая продолжительность заболевания сокращалась в среднем на 4 сут. В группе пациентов, начавших прием ПВП на 3-и сут и позднее, частота осложнений в виде бронхитов и пневмоний была выше, чем в группе пациентов, начавших лечение в первые 48 ч от начала заболевания. При сравнении эффективности препаратов умифеновир и осельтамивир у пациентов со среднетяжелой формой гриппа не было выявлено различий в продолжительности симптомов лихорадки и интоксикации, а также в частоте осложнений. Полученные результаты подтвердили, что вирусы гриппа А(H1N1) поражают преимущественно людей трудоспособного возраста, наибольшая эффективность ПВТ достигается при назначении лечения на ранних этапах заболевания (1–2 сут), установленными предикторами неблагоприятного течения заболевания являются метаболические нарушения и беременность [11].
Фармакоэпидемиологические исследования были продолжены в первом постпандемическом сезоне 2010–2011 гг. Ретроспективный анализ историй болезни 1462 пациентов старше 18 лет был проведен в 26 регионах среди госпитализированных пациентов. В группах больных гриппом и ОРВИ, находившихся в стационарах, чаще оказывались женщины, а также лица, относящиеся к группам повышенного риска заболеваемости: беременные, лица с избыточной массой тела и имеющие соматические хронические заболевания [12]. По результатам лабораторной диагностики 440 (30,2%) пациентам был поставлен диагноз «грипп», 1020 (69,8%) – диагноз «ОРВИ». На догоспитальном этапе ПВТ получали только 225 (17%) пациентов. Большая часть пациентов была госпитализирована позднее 48 ч от начала заболевания. Среднетяжелое течение заболевания было отмечено у 83% пациентов, тяжелое – у 8,9%. Средняя продолжительность госпитализации составила 8 сут. В исследовании проанализированы сроки назначения этиотропных ПВП. Умифеновир назначался на догоспитальном этапе 10,1% заболевших гриппом, на этапе госпитализации – 55,1%; осельтамивир принимали 17,4% заболевших, а кагоцел и имидазолилэтанамид пентандиовой кислоты – 5%; в 11,4% случаев назначались гомеопатические средства и препараты интерферонов [12]. Клиническая эффективность терапии гриппа оценивалась у пациентов, получавших умифеновир или осельтамивир (наиболее часто назначавшиеся препараты). Было достоверно (р<0,05) установлено, что при раннем начале лечения гриппа ПВП общая продолжительность заболевания сокращалась в среднем на 3 сут, длительность лихорадки и интоксикации – на 2 сут, длительность катаральных симптомов – на 3 сут, достоверно снижался риск развития осложнений в сравнении с таковым у больных, не получавших ПВТ [12].
Особенностью эпидемических подъемов ОРВИ и гриппа является более высокая заболеваемость детского населения. Чаще всего эпидемии респираторных вирусных инфекций начинаются именно с подъема заболеваемости среди детей [9, 13]. В течение сезона 2010–2011 гг. в 37 ЛПУ на территории РФ был проведен ретроспективный анализ историй болезни 2044 детей в возрасте до 18 лет, госпитализированных с диагнозами «грипп» и «ОРВИ». Лабораторная диагностика возбудителя проводилась у 794 детей. Среди них вирус гриппа А был обнаружен у 321 (40,4%), штамм А(H1N1) – у 112 (14,1%), вирус гриппа В – у 92 (11,6%), другие респираторные вирусы – у 76 (9,6%) детей. На догоспитальном этапе ПВП получали 24,3% заболевших детей. Из числа госпитализированных большая часть больных (56%) поступила в стационар в ранние сроки (первые 48 ч от развития заболевания), им ПВТ начали проводить своевременно. Средняя продолжительность нахождения в стационаре составляла 7 дней. Среднетяжелое течение заболевания было диагностировано у 94,3% детей, тяжелое – у 5%. Наиболее часто для лечения назначался умифеновир (на догоспитальном этапе – в 10,2% случаев, на госпитальном этапе – в 79,5% случаев), осельтамивир был назначен только 4% больных гриппом [13].
При назначении этиотропной терапии (умифеновир или осельтамивир) в течение первых 48 ч от начала заболевания длительность основных симптомов гриппа и ОРВИ достоверно (р<0,05) сокращалась на 3,3 сут, общая продолжительность болезни – на 3 сут. При назначении для лечения умифеновира заболевания протекали без осложнений в 94,9% случаев. В группе, в которой пациенты не получали ПВТ, осложнения развивались в 57,1% случаев. Различия между группами были статистически значимы (р<0,001) [13].
В эпидемическом сезоне 2014–2015 гг. в 22 городах РФ были проанализированы в ретроспективе 1756 историй болезни взрослых пациентов, перенесших грипп. По результатам лабораторных исследований у 304 (17,3%) пациентов был установлен диагноз «грипп», у 165 (9,4%) – «ОРВИ уточненной этиологии», у 1289 (73,4%) – «ОРВИ неуточненной этиологии». На догоспитальном этапе ПВП (умифеновир, осельтамивир) получали только 50 (2,8%) пациентов. В ЛПУ лечение ПВП (умифеновир, осельтамивир) проводилось 1283 (73%) пациентам. Были проанализированы результаты этиотропной ПВТ. До госпитализации осложнения гриппа и ОРВИ были зафиксированы у 7,1% больных, пневмония – у 4,8%. На госпитальном этапе осложнения развились у 0,7% пациентов, частота развития пневмонии была снижена в 24 раза (p<0,01).
Выводы
1. Корреляция выраженности клинических симптомов гриппа со степенью вирусной нагрузки выдвигает требование раннего (первые 48 ч заболевания) применения специфических ПВП, подавляющих репликацию вируса.2. Своевременное начало ПВТ в пандемический (2009–2010 гг.) период обеспечило сокращение общей длительности заболевания гриппом в среднем на 4 сут (р<0,001), снизило риск развития осложнений в сравнении с таковым в группе, получавшей ПВП в более поздние сроки (р<0,05).
3. В ходе исследований, проведенных в период пандемии гриппа 2009 г. и в постпандемическом периоде, подтверждена клиническая эффективность умифеновира и осельтамивира: назначение данной ПВТ в первые 48 ч сокращало общую продолжительность заболевания гриппом в среднем на 3 сут, длительность лихорадки и интоксикации – на 2 сут, катаральных симптомов – на 3 сут, уменьшался риск развития осложнений.












