–†–µ–±–µ–љ–Њ–Ї –°. (–і–µ–≤–Њ—З–Ї–∞) –Њ—В –њ–µ—А–≤–Њ—А–Њ–і—П—Й–µ–є –Ј–і–Њ—А–Њ–≤–Њ–є –ґ–µ–љ—Й–Є–љ—Л 35 –ї–µ—В. –С–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М 1-—П (–ґ–µ–ї–∞–љ–љ–∞—П, –њ–ї–∞–љ–Є—А—Г–µ–Љ–∞—П), –њ—А–Њ—В–µ–Ї–∞–ї–∞ –≥–ї–∞–і–Ї–Њ. –†–Њ–і—Л 1-–µ, –љ–∞ 38–39 –љ–µ–і., —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–µ. –Ф–µ–≤–Њ—З–Ї–∞ —А–Њ–і–Є–ї–∞—Б—М —Б –Љ–∞—Б—Б–Њ–є 2650 –≥, –і–ї–Є–љ–Њ–є 48 —Б–Љ, –Ј–∞–Ї—А–Є—З–∞–ї–∞ —Б—А–∞–Ј—Г, –Њ—Ж–µ–љ–Ї–∞ –њ–Њ —И–Ї–∞–ї–µ –Р–њ–≥–∞—А 8 –±–∞–ї–ї–Њ–≤. –Ъ –≥—А—Г–і–Є –њ—А–Є–ї–Њ–ґ–µ–љ–∞ –љ–∞ 1-–µ —Б—Г—В, –Њ–і–љ–∞–Ї–Њ –Є–Ј-–Ј–∞ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Љ–Њ–ї–Њ–Ї–∞ —Г –Љ–∞—В–µ—А–Є –і–Њ–Ї–∞—А–Љ–ї–Є–≤–∞–ї–∞—Б—М –∞–і–∞–њ—В–Є—А–Њ–≤–∞–љ–љ–Њ–є —Б–Љ–µ—Б—М—О. –Т —А–∞–љ–љ–Є–є –љ–µ–Њ–љ–∞—В–∞–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –Њ–±–Є–ї—М–љ—Л–µ —Б—А—Л–≥–Є–≤–∞–љ–Є—П. –Я–Њ—В–µ—А—П –Љ–∞—Б—Б—Л —В–µ–ї–∞ –Ј–∞ 6-–µ —Б—Г—В —Б–Њ—Б—В–∞–≤–Є–ї–∞ –і–Њ 300 –≥. –Я—А–Є–≤–Є–≤–Ї–∞ –С–¶–Ц –≤ —А–Њ–і–і–Њ–Љ–µ —Б–і–µ–ї–∞–љ–∞.
–Т—Л–њ–Є—Б–∞–љ–∞ –Є–Ј —А–Њ–і–і–Њ–Љ–∞ –≤ —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є –љ–∞ 6-–µ —Б—Г—В –ґ–Є–Ј–љ–Є. –Ф–Њ–Љ–∞ –њ—А–Њ–і–Њ–ї–ґ–∞–ї–∞ —Б—А—Л–≥–Є–≤–∞—В—М, –Њ—В–Љ–µ—З–∞–ї—Б—П –љ–µ–њ–µ—А–µ–≤–∞—А–µ–љ–љ—Л–є —Б—В—Г–ї. –Ь–∞—В—М –Њ–±—А–∞—Й–∞–ї–∞ –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ –љ–µ–±–Њ–ї—М—И—Г—О –ґ–µ–ї—В—Г—И–љ–Њ—Б—В—М –Ї–Њ–ґ–Є –Є —Б–Ї–ї–µ—А. –Я–Њ—Б—В–µ–њ–µ–љ–љ–Њ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –∞–њ–њ–µ—В–Є—В–∞, —З—В–Њ –±—Л–ї–Њ —А–∞—Б—Ж–µ–љ–µ–љ–Њ –Љ–∞—В–µ—А—М—О –Ї–∞–Ї –љ–µ–ґ–µ–ї–∞–љ–Є–µ —А–µ–±–µ–љ–Ї–∞ –µ—Б—В—М –≥—А—Г–і–љ–Њ–µ –Љ–Њ–ї–Њ–Ї–Њ. –Т —А–∞—Ж–Є–Њ–љ –±—Л–ї –≤–≤–µ–і–µ–љ –∞–і–∞–њ—В–Є—А–Њ–≤–∞–љ–љ—Л–є –Ј–∞–Љ–µ–љ–Є—В–µ–ї—М –≥—А—Г–і–љ–Њ–≥–Њ –Љ–Њ–ї–Њ–Ї–∞, –њ–Њ—Б–ї–µ —З–µ–≥–Њ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М —Б—А—Л–≥–Є–≤–∞–љ–Є–є —Г—Б–Є–ї–Є–ї–∞—Б—М.
–Т 3-–љ–µ–і–µ–ї—М–љ–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ (21-–є –і–µ–љ—М –ґ–Є–Ј–љ–Є) –Њ—В–Љ–µ—З–µ–љ –њ–Њ–і—К–µ–Љ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞ –і–Њ —Б—Г–±—Д–µ–±—А–Є–ї—М–љ—Л—Е —Ж–Є—Д—А, —З—В–Њ –±—Л–ї–Њ —А–∞—Б—Ж–µ–љ–µ–љ–Њ —Г—З–∞—Б—В–Ї–Њ–≤—Л–Љ –≤—А–∞—З–Њ–Љ –Ї–∞–Ї –њ—А–Њ—П–≤–ї–µ–љ–Є–µ –Њ—Б—В—А–Њ–є —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–є –≤–Є—А—Г—Б–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є (–Ю–†–Т–Ш); –±—Л–ї–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–Њ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ. –Ю–і–љ–∞–Ї–Њ –љ–∞–Ј–љ–∞—З–µ–љ–љ—Л–є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї –Є —Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –Њ—Е–ї–∞–ґ–і–µ–љ–Є—П –љ–µ –њ—А–Є–≤–Њ–і–Є–ї–Є –Ї –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞. –Э–∞ 4-–µ —Б—Г—В –ї–Є—Е–Њ—А–∞–і–Ї–Є (24-–є –і–µ–љ—М –ґ–Є–Ј–љ–Є) –њ–Њ—П–≤–Є–ї–Є—Б—М –Њ–і—Л—И–Ї–∞, –±–µ—Б–њ–Њ–Ї–Њ–є—Б—В–≤–Њ, —З—В–Њ —Б–≤—П–Ј—Л–≤–∞–ї–Є —Б –Љ–µ—В–µ–Њ—А–Є–Ј–Љ–Њ–Љ, –Ї–Є—И–µ—З–љ—Л–Љ–Є –Ї–Њ–ї–Є–Ї–∞–Љ–Є –Є –і–Є—Б–њ–µ–њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є. –Э–∞ 9––µ —Б—Г—В –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (30-–є –і–µ–љ—М –ґ–Є–Ј–љ–Є) –±—Л–ї–∞ –љ–∞–њ—А–∞–≤–ї–µ–љ–∞ –љ–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є—О —Б –і–Є–∞–≥–љ–Њ–Ј–Њ–Љ «–Ю–†–Т–Ш, –і–Є—Б–±–∞–Ї—В–µ—А–Є–Њ–Ј –Ї–Є—И–µ—З–љ–Є–Ї–∞».
–Я—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є: t – 37,8o–°, –њ—Г–ї—М—Б – 149/–Љ–Є–љ, —З–∞—Б—В–Њ—В–∞ –і—Л—Е–∞–љ–Є—П – 48/–Љ–Є–љ. –Ь–∞—Б—Б–∞ —В–µ–ї–∞ – 3050 –≥. –°–Њ—Б—В–Њ—П–љ–Є–µ —В—П–ґ–µ–ї–Њ–µ, –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –±–µ—Б–њ–Њ–Ї–Њ–є—Б—В–≤–Њ. –Э–∞ –Њ—Б–Љ–Њ—В—А —А–µ–∞–≥–Є—А—Г–µ—В –љ–µ–≥–∞—В–Є–≤–љ–Њ. –Ь–µ–љ–Є–љ–≥–µ–∞–ї—М–љ—Л–µ –Ј–љ–∞–Ї–Є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–µ. –Ъ–Њ–ґ–∞ –±–ї–µ–і–љ–∞—П, –Њ—В–Љ–µ—З–µ–љ–∞ –ї–µ–≥–Ї–∞—П –ґ–µ–ї—В—Г—И–љ–Њ—Б—В—М. –Ґ—Г—А–≥–Њ—А —В–Ї–∞–љ–µ–є –Є —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В—М –Ї–Њ–ґ–Є —Б–љ–Є–ґ–µ–љ—Л, –њ–Њ–і–Ї–Њ–ґ–љ–Њ-–ґ–Є—А–Њ–≤–Њ–є —Б–ї–Њ–є –Є—Б—В–Њ–љ—З–µ–љ. –Ю—В–Љ–µ—З–∞—О—В—Б—П —Б—А—Л–≥–Є–≤–∞–љ–Є—П, —А–µ–і–Ї–Є–є –Ї–∞—И–µ–ї—М. –£–Љ–µ—А–µ–љ–љ–∞—П –≥–Є–њ–µ—А–µ–Љ–Є—П –љ–µ–±–љ—Л—Е –Љ–Є–љ–і–∞–ї–Є–љ –Є –Ј–∞–і–љ–µ–є —Б—В–µ–љ–Ї–Є –≥–ї–Њ—В–Ї–Є. –Я–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–µ –ї–Є–Љ—Д–∞—В–Є—З–µ—Б–Ї–Є–µ —Г–Ј–ї—Л –і–Њ 1 —Б–Љ, —Н–ї–∞—Б—В–Є—З–љ—Л–µ, –њ–Њ–і–≤–Є–ґ–љ—Л–µ, –±–µ–Ј–±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л–µ, –≤–Њ –≤—Б–µ—Е –≥—А—Г–њ–њ–∞—Е. –Я–µ—А–Ї—Г—В–Њ—А–љ–Њ –љ–∞–і –ї–µ–≥–Ї–Є–Љ–Є – –Ј–≤—Г–Ї –ї–µ–≥–Њ—З–љ—Л–є. –Р—Г—Б–Ї—Г–ї—М—В–∞—В–Є–≤–љ–Њ – –ґ–µ—Б—В–Ї–Њ–µ –і—Л—Е–∞–љ–Є–µ –љ–∞ –≤—Б–µ–Љ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –Њ–±–Њ–Є—Е –ї–µ–≥–Ї–Є—Е, –µ–і–Є–љ–Є—З–љ—Л–µ —Б—Г—Е–Є–µ —Е—А–Є–њ—Л. –°–µ—А–і–µ—З–љ—Л–µ —В–Њ–љ—Л —Г—З–∞—Й–µ–љ—Л, –њ—А–Є–≥–ї—Г—И–µ–љ—Л, —А–Є—В–Љ–Є—З–љ—Л–µ. –Ц–Є–≤–Њ—В —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ –≤–Ј–і—Г—В, –њ–µ—А–Є—Б—В–∞–ї—М—В–Є–Ї–∞ —Г—Б–Є–ї–µ–љ–∞. –°–Є–Љ–њ—В–Њ–Љ «–њ–µ—Б–Њ—З–љ—Л—Е —З–∞—Б–Њ–≤» –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В—Б—П. –Ц–Є–≤–Њ—В –і–Њ—Б—В—Г–њ–µ–љ –≥–ї—Г–±–Њ–Ї–Њ–є –њ–∞–ї—М–њ–∞—Ж–Є–Є, –Љ—П–≥–Ї–Є–є. –Я–µ—З–µ–љ—М +2,5–3 —Б–Љ, —Б–µ–ї–µ–Ј–µ–љ–Ї–∞ – 0,5–1 —Б–Љ. –°—В—Г–ї –ґ–µ–ї—В—Л–є, –љ–µ–њ–µ—А–µ–≤–∞—А–µ–љ–љ—Л–є, —Б –њ—А–Њ–ґ–Є–ї–Ї–∞–Љ–Є —Б–ї–Є–Ј–Є –Є –Ј–µ–ї–µ–љ–Є.
–£—З–Є—В—Л–≤–∞—П —Б–Є–љ–і—А–Њ–Љ —Б—А—Л–≥–Є–≤–∞–љ–Є—П –Є —А–∞–Ј–≤–Є—В–Є–µ –њ–Њ—Б—В–љ–∞—В–∞–ї—М–љ–Њ–є –≥–Є–њ–Њ—В—А–Њ—Д–Є–Є, –њ–Њ cito –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Є—Й–µ–≤–Њ–і–∞, –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є —Б –њ—А–Њ–≤–µ–і–µ–љ–Є–µ–Љ –≤–Њ–і–љ–Њ-—Б–Є—Д–Њ–љ–љ–Њ–є –њ—А–Њ–±—Л – –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ. –Ъ—А–Њ–Љ–µ —Н—В–Њ–≥–Њ, —А–µ–±–µ–љ–Њ–Ї –±—Л–ї –њ—А–Њ–Ї–Њ–љ—Б—Г–ї—М—В–Є—А–Њ–≤–∞–љ —Е–Є—А—Г—А–≥–Њ–Љ – —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –љ–∞ –Љ–Њ–Љ–µ–љ—В –Њ—Б–Љ–Њ—В—А–∞ –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г—З–Є—В—Л–≤–∞—П –і–∞–љ–љ—Л–µ –∞–љ–∞–Љ–љ–µ–Ј–∞ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Ї–∞—А—В–Є–љ—Г –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –±—Л–ї –њ–Њ—Б—В–∞–≤–ї–µ–љ –і–Є–∞–≥–љ–Њ–Ј: «–Ю–†–Т–Ш. –Я–µ—А–Є–љ–∞—В–∞–ї—М–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –¶–Э–° —Б —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –љ–µ—А–≤–љ–Њ-—А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–є –≤–Њ–Ј–±—Г–і–Є–Љ–Њ—Б—В–Є. –§—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –Ц–Ъ–Ґ. –Я–љ–µ–≤–Љ–Њ–љ–Є—П (–∞—Б–њ–Є—А–∞—Ж–Є–Њ–љ–љ–∞—П)?».
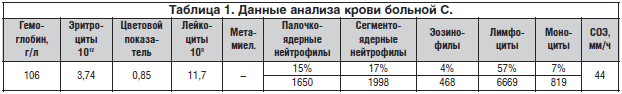
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ –Ї—А–Њ–≤–Є –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –≤—Л—П–≤–ї–µ–љ—Л –ї–µ–≥–Ї–∞—П –љ–Њ—А–Љ–Њ—Е—А–Њ–Љ–љ–∞—П –∞–љ–µ–Љ–Є—П, –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –ї–µ–є–Ї–Њ—Ж–Є—В–∞—А–љ–Њ–є —Д–Њ—А–Љ—Г–ї–µ – –њ—А–Є —Б–Њ—Е—А–∞–љ—П—О—Й–µ–Љ—Б—П –≤–Њ–Ј—А–∞—Б—В–љ–Њ–Љ –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ –Њ—В–Љ–µ—З–µ–љ–Њ «–Њ–Љ–Њ–ї–Њ–ґ–µ–љ–Є–µ» –љ–µ–є—В—А–Њ—Д–Є–ї–Њ–≤, —А–µ–Ј–Ї–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Ї–Њ—А–Њ—Б—В–Є –Њ—Б–µ–і–∞–љ–Є—П —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ (–°–Ю–≠) (—В–∞–±–ї. 1).
–Э–∞ —А–µ–љ—В–≥–µ–љ–Њ–≥—А–∞–Љ–Љ–µ –Њ—А–≥–∞–љ–Њ–≤ –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–Є –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є –Њ—З–∞–≥–Њ–≤—Л—Е –Є–љ—Д–Є–ї—М—В—А–∞—В–Є–≤–љ—Л—Е —В–µ–љ–µ–є –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ, –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г—Б–Є–ї–µ–љ–Є–µ —Б–Њ—Б—Г–і–Є—Б—В–Њ-–Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ–Њ–≥–Њ —А–Є—Б—Г–љ–Ї–∞.
–Т –Ї–Њ–њ—А–Њ–≥—А–∞–Љ–Љ–µ –±—Л–ї–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ—Л —Г–Љ–µ—А–µ–љ–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –љ–µ–є—В—А–∞–ї—М–љ–Њ–≥–Њ –ґ–Є—А–∞, –ґ–Є—А–љ—Л–µ –Ї–Є—Б–ї–Њ—В—Л –Є –Љ—Л–ї–∞.
–Я—А–Є –±–∞–Ї—В–µ—А–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Ї–∞–ї–∞ —Н–љ—В–µ—А–Њ–њ–∞—В–Њ–≥–µ–љ–љ—Л—Е –Љ–Є–Ї—А–Њ–Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–≤ –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ.
–Т –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–Љ –∞–љ–∞–ї–Є–Ј–µ –Ї—А–Њ–≤–Є – –Њ–±—Й–Є–є –±–Є–ї–Є—А—Г–±–Є–љ 41,1 –Љ–Ї–Љ–Њ–ї—М/–ї (–љ–µ–њ—А—П–Љ–Њ–є – 39,2 –Љ–Ї–Љ–Њ–ї—М/–ї, –њ—А—П–Љ–Њ–є – 1,9 –Љ–Ї–Љ–Њ–ї—М/–ї), –≤ –Њ—Б—В–∞–ї—М–љ–Њ–Љ – –±–µ–Ј –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є.
–Т –Њ–±—Й–Є—Е –∞–љ–∞–ї–Є–Ј–∞—Е –Љ–Њ—З–Є – –±–µ–Ј –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –£–Ч–Ш –Њ—А–≥–∞–љ–Њ–≤ –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –Ј–∞–±—А—О—И–Є–љ–љ–Њ–≥–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞, –≠–Ъ–У, –∞ —В–∞–Ї–ґ–µ –љ–µ–є—А–Њ—Б–Њ–љ–Њ–≥—А–∞—Д–Є–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Є –Њ–± –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є.
–Ы–µ—З–µ–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –≤—Л—П–≤–ї–µ–љ–љ—Л–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Є–љ–і—А–Њ–Љ–∞–Љ–Є. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Г–±–µ–і–Є—В–µ–ї—М–љ—Л—Е —А–µ–љ—В–≥–µ–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е –≤ –њ–Њ–ї—М–Ј—Г –њ–љ–µ–≤–Љ–Њ–љ–Є–Є, —А–µ—И–µ–љ–Њ –±—Л–ї–Њ –љ–∞–Ј–љ–∞—З–Є—В—М –∞–љ—В–Є–±–Є–Њ—В–Є–Ї–Є (—Ж–µ—Д–∞–Ј–Њ–ї–Є–љ – –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 4 —Б—Г—В –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є, –∞ –Ј–∞—В–µ–Љ, —Г—З–Є—В—Л–≤–∞—П –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Н—Д—Д–µ–Ї—В–∞, – –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О —Ж–µ—Д–Њ—В–∞–Ї—Б–Є–Љ–∞ —Б –≥–µ–љ—В–∞–Љ–Є—Ж–Є–љ–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і—Г—О—Й–Є—Е 7 —Б—Г—В) –Є –Є–љ—Д—Г–Ј–Є–Њ–љ–љ—Г—О —В–µ—А–∞–њ–Є—О (–≥–ї—О–Ї–Њ–Ј–Њ-—Б–Њ–ї–µ–≤—Л–µ —А–∞—Б—В–≤–Њ—А—Л —Б –і–Њ–±–∞–≤–ї–µ–љ–Є–µ–Љ –≥–µ–њ–∞—А–Є–љ–∞, –Є–љ–Њ–Ј–Є–љ–∞, –∞–Љ–Є–љ–Њ—Д–Є–ї–ї–Є–љ–∞).
–£—З–Є—В—Л–≤–∞—П –≤—Л—А–∞–ґ–µ–љ–љ—Л–є —Б–Є–љ–і—А–Њ–Љ —Б—А—Л–≥–Є–≤–∞–љ–Є—П, –≤ –Ї–∞—З–µ—Б—В–≤–µ –Љ–Њ–ї–Њ—З–љ–Њ–є —Б–Љ–µ—Б–Є –±—Л–ї –≤—Л–±—А–∞–љ —Д—А–Є—Б–Њ–≤–Њ–Љ – –Љ–∞–ї—Л–Љ–Є –њ–Њ—А—Ж–Є—П–Љ–Є –і–Њ 8–10 —А./—Б—Г—В. –Ф–ї—П —Г–Љ–µ–љ—М—И–µ–љ–Є—П –њ—А–Њ—П–≤–ї–µ–љ–Є–є —Б–Є–љ–і—А–Њ–Љ–∞ –љ–∞—А—Г—И–µ–љ–љ–Њ–≥–Њ –Ї–Є—И–µ—З–љ–Њ–≥–Њ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –Є –њ–µ—А–µ–≤–∞—А–Є–≤–∞–љ–Є—П –њ—А–Є–µ–Љ –њ–Є—Й–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї—Б—П –њ—А–Є–µ–Љ–Њ–Љ —Д–µ—А–Љ–µ–љ—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Я–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є –љ–µ–≤—А–Њ–њ–∞—В–Њ–ї–Њ–≥–∞ –±—Л–ї–Є –љ–∞–Ј–љ–∞—З–µ–љ—Л —Б–µ–і–∞—В–Є–≤–љ—Л–µ —Д–Є—В–Њ—Б–±–Њ—А—Л.
–Ю–і–љ–∞–Ї–Њ, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–µ –ї–µ—З–µ–љ–Є–µ, —А–µ–±–µ–љ–Њ–Ї –њ—А–Њ–і–Њ–ї–ґ–∞–ї –ї–Є—Е–Њ—А–∞–і–Є—В—М, —Б–Њ—Е—А–∞–љ—П–ї–Є—Б—М –і–Є—Б–њ–µ–њ—В–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П. –≠—В–Њ –Ј–∞—Б—В–∞–≤–Є–ї–Њ –Ї 11 —Б—Г—В –њ—А–µ–±—Л–≤–∞–љ–Є—П —А–µ–±–µ–љ–Ї–∞ –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ –њ—А–Њ–≤–µ—Б—В–Є —А–µ–≤–Є–Ј–Є—О –і–∞–љ–љ—Л—Е –∞–љ–∞–Љ–љ–µ–Ј–∞, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Ї–ї–Є–љ–Є–Ї–Њ-–ї–∞–±–Њ—А–∞—В–Њ—А–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П.
–£–≥–ї—Г–±–ї–µ–љ–љ–Њ–µ –Є–Ј—Г—З–µ–љ–Є–µ –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –≤—Л—П–≤–Є—В—М —Г –Љ–∞—В–µ—А–Є —Н–њ–Є–Ј–Њ–і –ї–Є—Е–Њ—А–∞–і–Ї–Є —Б –Љ–Њ–љ–Њ–љ—Г–Ї–ї–µ–Њ–Ј–Њ–њ–Њ–і–Њ–±–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –≤ III —В—А–Є–Љ–µ—Б—В—А–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є. –≠—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ—А–Є —Н—В–Њ–Љ –љ–µ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М. –Ъ—А–Њ–Љ–µ —Н—В–Њ–≥–Њ, –њ—А–Є —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ —Г—В–Њ—З–љ–µ–љ–Є–Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Б–Њ—Б—В–Њ—П–љ–Є—П –Ј–і–Њ—А–Њ–≤—М—П —А–µ–±–µ–љ–Ї–∞ –њ—А–Є —А–Њ–ґ–і–µ–љ–Є–Є –±—Л–ї –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ —Б–Є–љ–і—А–Њ–Љ –Ј–∞–і–µ—А–ґ–Ї–Є –≤–љ—Г—В—А–Є—Г—В—А–Њ–±–љ–Њ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П (–Ч–Т–£–†), –љ–∞ –Ї–Њ—В–Њ—А—Л–є —А–∞–љ–µ–µ –љ–µ –Њ–±—А–∞—Й–∞–ї–Є –і–Њ–ї–ґ–љ–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П. –£—З–Є—В—Л–≤–∞—П –≤—Л—П–≤–ї–µ–љ–љ—Л–µ –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є–µ –і–∞–љ–љ—Л–µ, –∞ —В–∞–Ї–ґ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є (—Б–Є–љ–і—А–Њ–Љ –Ч–Т–£–†, –Ј–∞—В—П–ґ–љ–∞—П –ґ–µ–ї—В—Г—Е–∞, –≥–µ–њ–∞—В–Њ—Б–њ–ї–µ–љ–Њ–Љ–µ–≥–∞–ї–Є—П, –љ–∞—А—Г—И–µ–љ–Є—П –Ї–Є—И–µ—З–љ–Њ–≥–Њ –њ–µ—А–µ–≤–∞—А–Є–≤–∞–љ–Є—П –Є –≤—Б–∞—Б—Л–≤–∞–љ–Є—П, –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –љ–µ—А–≤–љ–Њ-—А–µ—Д–ї–µ–Ї—В–Њ—А–љ–∞—П –≤–Њ–Ј–±—Г–і–Є–Љ–Њ—Б—В—М, –љ–Њ—А–Љ–Њ—Е—А–Њ–Љ–љ–∞—П –∞–љ–µ–Љ–Є—П, —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Њ—З–∞–≥–Њ–≤ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є–Є –ї–µ–≥–Њ—З–љ–Њ–є —В–Ї–∞–љ–Є –љ–∞ —А–µ–љ—В–≥–µ–љ–Њ–≥—А–∞–Љ–Љ–µ –Њ—А–≥–∞–љ–Њ–≤ –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–Є, –∞ —В–∞–Ї–ґ–µ –њ–Њ—Б—В–љ–∞—В–∞–ї—М–љ–Њ —А–∞–Ј–≤–Є–≤—И–∞—П—Б—П –≥–Є–њ–Њ—В—А–Њ—Д–Є—П), –±—Л–ї–Њ –≤—Л—Б–Ї–∞–Ј–∞–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ, —З—В–Њ –Є–Љ–µ—О—Й–Є–є—Б—П —Б–Є–љ–і—А–Њ–Љ–Њ–Ї–Њ–Љ–њ–ї–µ–Ї—Б –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –Т–£–Ш. –Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –∞–ї–≥–Њ—А–Є—В–Љ–Њ–Љ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є TORCH-—Б–Є–љ–і—А–Њ–Љ–∞ [1–3] —А–µ–±–µ–љ–Њ–Ї –±—Л–ї –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ –њ—А–Є –њ–Њ–Љ–Њ—Й–Є –Љ–µ—В–Њ–і–∞ –њ–Њ–ї–Є–Љ–µ—А–∞–Ј–љ–Њ–є —Ж–µ–њ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є (–Я–¶–†) –Є —Б–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤ (–Є–Љ–Љ—Г–љ–Њ—Д–µ—А–Љ–µ–љ—В–љ—Л–є –∞–љ–∞–ї–Є–Ј).
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Я–¶–† –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —А–µ–±–µ–љ–Ї–∞ –љ–∞ —Е–ї–∞–Љ–Є–і–Є–Є, –Љ–Є–Ї–Њ–њ–ї–∞–Ј–Љ—Л, —Г—А–µ–∞–њ–ї–∞–Ј–Љ—Л, –≥–µ—А–њ–µ—Б 1-–≥–Њ –Є 2-–≥–Њ —В–Є–њ–∞, –Ї–∞–љ–і–Є–і—Л, —Ж–Є—В–Њ–Љ–µ–≥–∞–ї–Њ–≤–Є—А—Г—Б (–¶–Ь–Т): –≤ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ–±–∞—Е (–Ї—А–Њ–≤—М, –Љ–Њ—З–∞, –Љ–∞–Ј–Ї–Є –Є–Ј –Ј–µ–≤–∞) –≤—Л—П–≤–ї–µ–љ–∞ –Ф–Э–Ъ –¶–Ь–Т (4+).
–†–µ–Ј—Г–ї—М—В–∞—В—Л —Б–µ—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —А–µ–±–µ–љ–Ї–∞: –∞–љ—В–Є-–¶–Ь–Т IgM – 2,069 IU/ml (N –і–Њ 0,6), –∞–љ—В–Є-–¶–Ь–Т IgG – 66 IU/ml (N –і–Њ 15), –Є–љ–і–µ–Ї—Б –∞–≤–Є–і–љ–Њ—Б—В–Є –∞–љ—В–Є-–¶–Ь–Т IgG – 23%.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–∞–ї–Є—З–Є–µ –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е (–ї–Є—Е–Њ—А–∞–і–Ї–∞ —Б –ї–Є–Љ—Д–∞–і–µ–љ–Њ–њ–∞—В–Є–µ–є –≤ III —В—А–Є–Љ–µ—Б—В—А–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є), –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л (–Ч–Т–£–†, –Ј–∞—В—П–ґ–љ–∞—П –ґ–µ–ї—В—Г—Е–∞, –≥–µ–њ–∞—В–Њ—Б–њ–ї–µ–љ–Њ–Љ–µ–≥–∞–ї–Є—П, –∞–љ–µ–Љ–Є—П, –њ–Њ—Б—В–љ–∞—В–∞–ї—М–љ–∞—П –≥–Є–њ–Њ—В—А–Њ—Д–Є—П –Є –і—А.) –Є –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –Љ–∞—А–Ї–µ—А–Њ–≤ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –¶–Ь–Т (–Ф–Э–Ъ –¶–Ь–Т –≤ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –ґ–Є–і–Ї–Њ—Б—В—П—Е, –∞–љ—В–Є-–¶–Ь–Т IgM –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є) –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞—В—М –≤–љ—Г—В—А–Є—Г—В—А–Њ–±–љ—Г—О –¶–Ь–Т-–Є–љ—Д–µ–Ї—Ж–Є—О –≤ –њ–µ—А–Є–Њ–і –Њ—Б—В—А–Њ–≥–Њ —В–µ—З–µ–љ–Є—П. –Т–µ—А–Њ—П—В–љ–Њ, –Є–љ—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Є–µ –њ–ї–Њ–і–∞ –њ—А–Њ–Є–Ј–Њ—И–ї–Њ –≤ –њ–Њ—Б–ї–µ–і–љ–µ–Љ —В—А–Є–Љ–µ—Б—В—А–µ –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є. –Т –њ–Њ–ї—М–Ј—Г —Н—В–Њ–≥–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ—В—Б—Г—В—Б—В–≤–Є–µ –њ–Њ—А–Њ–Ї–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П, –љ–µ–і–Њ–љ–Њ—И–µ–љ–љ–Њ—Б—В–Є, –∞ —В–∞–Ї–ґ–µ –∞—Б—Б–Є–Љ–µ—В—А–Є—З–љ—Л–є —В–Є–њ –Ч–Т–£–† –Є –њ–Њ—Б—В–љ–∞—В–∞–ї—М–љ–∞—П –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є—П –Є–љ—Д–µ–Ї—Ж–Є–Є.
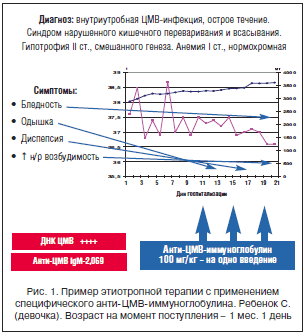
–Т –Ї–∞—З–µ—Б—В–≤–µ —Н—В–Є–Њ—В—А–Њ–њ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±—Л–ї –љ–∞–Ј–љ–∞—З–µ–љ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–є –∞–љ—В–Є-–¶–Ь–Т-–Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ –і–ї—П –≤/–≤ –≤–≤–µ–і–µ–љ–Є—П –≤ –і–Њ–Ј–µ 100 –Љ–ї/–Ї–≥ –Љ–∞—Б—Б—Л —В–µ–ї–∞ –љ–∞ 1 –≤–≤–µ–і–µ–љ–Є–µ —Б –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ 48 —З, —З—В–Њ –њ–Њ–ї–љ–Њ—Б—В—М—О —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –Њ—Д–Є—Ж–Є–∞–ї—М–љ—Л–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ (—А–Є—Б. 1) [5, 6].
–Э–∞ —Д–Њ–љ–µ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–є –∞–љ—В–Є-–¶–Ь–Т-–Є–Љ–Љ—Г–љ–Њ—В–µ—А–∞–њ–Є–Є —Б–Њ—Б—В–Њ—П–љ–Є–µ —Г–ї—Г—З—И–Є–ї–Њ—Б—М. –†–µ—Б–њ–Є—А–∞—В–Њ—А–љ—Л–µ –Є –і–Є—Б–њ–µ–њ—В–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –±—Л–ї–Є –Ї—Г–њ–Є—А–Њ–≤–∞–љ—Л. –Ґ–µ–Љ–њ–µ—А–∞—В—Г—А–∞ —В–µ–ї–∞ –љ–Њ—А–Љ–∞–ї–Є–Ј–Њ–≤–∞–ї–∞—Б—М –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –≤—В–Њ—А–Њ–є –і–Њ–Ј—Л —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ—В–Є-–¶–Ь–Т-–Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–∞ –і–ї—П –≤/–≤ –≤–≤–µ–і–µ–љ–Є—П. –Я—А–Є–±–∞–≤–Ї–∞ –≤ –≤–µ—Б–µ –Ј–∞ 21 –і–µ–љ—М –њ—А–µ–±—Л–≤–∞–љ–Є—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–µ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 510 –≥. –Я—А–Є –≤—Л–њ–Є—Б–Ї–µ —Б–Њ—Е—А–∞–љ—П–ї–Є—Б—М –±–ї–µ–і–љ–Њ—Б—В—М –Ї–Њ–ґ–љ—Л—Е –њ–Њ–Ї—А–Њ–≤–Њ–≤ –Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є –љ–µ—А–≤–љ–Њ-—А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–є –≤–Њ–Ј–±—Г–і–Є–Љ–Њ—Б—В–Є —Б –љ–µ–Ї–Њ—В–Њ—А–Њ–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Њ–є.
–Ъ–∞—В–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Њ–µ –љ–∞–±–ї—О–і–µ–љ–Є–µ –Ј–∞ —А–µ–±–µ–љ–Ї–Њ–Љ – 2 –≥–Њ–і–∞. –§–Є–Ј–Є—З–µ—Б–Ї–Њ–µ, –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–µ –Є —А–µ—З–µ–≤–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –≤–Њ–Ј—А–∞—Б—В–љ—Л–Љ –љ–Њ—А–Љ–∞—В–Є–≤–∞–Љ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–є –њ—А–Є–Љ–µ—А –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г–µ—В, —З—В–Њ –љ–µ–і–Њ–Њ—Ж–µ–љ–Ї–∞ –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –њ–Њ—Б—В–љ–∞—В–∞–ї—М–љ–Њ–є –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є–Є –Т–£–Ш, –Љ–Њ–ґ–µ—В —Б—В–∞—В—М –њ—А–Є—З–Є–љ–Њ–є –њ–Њ–Ј–і–љ–µ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –≤—А–Њ–ґ–і–µ–љ–љ—Л—Е –Є–љ—Д–µ–Ї—Ж–Є–є. –°–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–∞—П –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є—П TORCH-—Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–ґ–µ –љ–∞ —А–∞–љ–љ–Є—Е —Б—А–Њ–Ї–∞—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Н—В–Є–Њ—В—А–Њ–њ–љ—Г—О —В–µ—А–∞–њ–Є—О, —З—В–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–Њ–≤—Л—И–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П.








.gif)



