Наиболее часто при ОА в патологический процесс вовлекаются коленные суставы с развитием гонартроза (ГА). У 25% больных, страдающих ГА, формируются выраженные нарушения функциональной активности, нередко приводящие пациента к утрате трудоспособности [3]. Риск утраты трудоспособности больных ГА сравним с группой больных пожилого возраста, страдающих сердечно–сосудистыми заболеваниями, и выше, чем при других заболеваниях у этой группы пациентов [4,5].
В последние годы отмечается рост заболеваемости ГА. Постоянная боль в суставах, функциональные ограничения значительно снижают качество жизни пациентов. В связи с вышеизложенным, возможность воздействия на течение заболевания имеет большое социальное и экономическое значение [6,7].
Патогенетическое лечение ОА следует начинать в наиболее ранние сроки от момента постановки диагноза, на начальных стадиях патологического процесса, что обеспечит уменьшение выраженности симптомов, снижение темпов прогрессирования структурных изменений в суставах (разрушения суставного хряща, рост остеофитов), а следовательно, и улучшение качества жизни больных [8–10].
Центральное место в лечении ОА (и, в частности, ГА) занимают нестероидные противовоспалительные препараты (НПВП). Однако нельзя не принимать во внимание достаточно большое количество побочных эффектов данной группы лекарственных средств. Важно также учитывать, что некоторые НПВП способны оказывать отрицательное влияние на метаболизм хряща, возможно, способствуя прогрессированию ОА.
Все это послужило предпосылкой для создания лекарственных средств, обладающих не только симптом–модифицирующим эффектом, но и, возможно, сдерживающих прогрессирование патологического процесса в суставе. Наиболее изученными в этом отношении являются глюкозамин (ГА) и хондроитин сульфат (ХС). Оба препарата в виде монотерапии, а также в комбинации способны уменьшать выраженность симптомов ОА [11–17]. Влияние этих лекарственных средств на прогрессирование заболевания еще требует изучения.
В связи с этим целью проведенного исследования явилось изучение влияния длительной терапии Терафлексом (комбинация ХС и ГА) (3–летнее наблюдение), назначенной на ранних стадиях ГА, на клинические симптомы (боль, скованность, нарушение функции) и течение заболевания.
Было обследовано 244 амбулаторных пациента с достоверным диагнозом ГА, давших письменное согласие на участие в исследовании. На момент включения в исследование и в контрольные сроки оценивались клинические показатели, выполнялась артросонография (АСГ), рентгенологическое исследования коленных суставов. Диагностика заболевания осуществлялась на основе критериев ГА Aмериканской коллегии ревматологов [18]. При отсутствии рентгенологических критериев, диагноз устанавливался при сочетании клинических симптомов (боль механического характера, скованность в суставах <30 минут, ограничение функции) и выявленной при АСГ неровности контура суставных поверхностей костей, образующих сустав. Рентгенологическая стадия ГА определялась по классификации Келлгрена–Лоуренса [19].
Критериями включения в исследование были: длительность симптомов ГА не менее 2, но не более 36 месяцев; 0, I, II рентгенологические стадии ГА; первичный ГА; отсутствие других заболеваний суставов. Критерии исключения: применение препаратов симптоматического действия в течение 3 месяцев до момента включения в исследование (в том числе внутрисуставное введение глюкокортикостероидов), применение препаратов с возможным болезнь–модифицирующим эффектом в анамнезе.
Клинические параметры оценивались определением:
• суммарного альго–функционального индекса Лекена (ФИЛ) для ГА в баллах [20];
• выраженности боли в суставах по визуально–аналоговой шкале в покое и при ходьбе (ВАШ) в мм;
• индексов WOMAC (Western Ontario and McMAster Universities Osteorthritis Index) боли, скованности, функции и суммарного глобального в мм по ВАШ [21].
• Потребность в НПВП оценивалась в мг в сутки диклофенака для оценки влияния терапии на течение заболевания.
Высота суставного хряща, толщина синовиальной оболочки, а также наличие выпота в полость сустава на момент включения в исследование и в контрольные сроки определялись АСГ–ки на аппарате «Logiq–400 pro» широкополосным линейным датчиком частотой 5–11 МГц. Оценивались размеры латерального и медиального хряща мыщелков бедренной кости в мм. Толщина синовиальной оболочки в мм измерялась по наиболее гипертрофированному участку при поперечном супрапателлярном сканировании. Наличие экссудата в полости сустава и его объем определялось при продольном супрапателлярном сканировании по средней линии надколенника с оценкой площади супрапателлярной сумки.
Рентгенограммы коленных суставов выполнялись в прямой, боковой и аксиальной проекциях в положении максимального разгибания колена для оценки в динамике высоты рентгеносуставной щели (РСЩ). РСЩ измерялась в наиболее суженном участке медиального отдела тибио–феморальной области (ТФО) с использованием лупы с ценой деления 0,1 мм. Степень сужения РСЩ определялась полуколичественным методом в баллах: 0 – отсутствие сужения РСЩ; 1 балл – РСЩ 4,5–5 мм; 2 балла – РСЩ 4–4,5 мм; 3 балла – РСЩ < 4 мм.
Пациенты с ГА были разделены на основную и контрольную группы. В основную группу вошли 104 пациента, которым с момента включения в исследование была начата терапия Терафлексом (Т): 83 (79,7%) женщины и 21 (20,3%) мужчина со средним возрастом 47,4±11,6 лет и средней длительностью ГА 11,5±6,7 месяцев. В соответствии с классификацией Келлгрена–Лоуренса 0 стадия ГА имела место у 22 (20,8%) больных, I – у 51 (49,4%), II – у 31 (29,8%) исследованного. Двухсторонний ГА был диагностирован у 71 (68,5%) пациента. Синовит (определялся клинически и по данным АСГ) был выявлен у 31 (29,5%) больного основной группы.
Т назначался по 1 капсуле 3 раза в сутки на протяжении 1 месяца, далее по 1 капсуле 2 раза в сутки в течение последующих 5 месяцев. Повторные курсы лечения Т в дозе 2 капсулы препарата в сутки в течение 2 месяцев повторяли с интервалом 1 месяц. Общая длительность приема Т на момент окончания исследования составила 3 года. При усилении болей в суставах больным разрешался прием диклофенака в суточной дозе 100 мг.
Контрольную группу составили 140 пациентов с ГА, 107 (76,4%) женщин и 33 (23,6%) мужчины со средним возрастом 46,7±10,4 лет и средней длительностью ГА 11,7±5,9 месяцев. В соответствии с классификацией Келлгрена–Лоуренса 0 стадия ГА имела место у 29 (20,7%) больных, I – у 67 (47,9%), II – у 44 (31,4%) исследованных. Двухсторонний ГА был диагностирован у 89 (63,8%) пациентов. Синовит выявлен у 36 (25,7%) больных контрольной группы. Пациентам контрольной группы с момента включения в исследование был рекомендован прием 100 мг диклофенака в сутки в сочетании с различными видами физиолечения. При достижении положительного эффекта лечения диклофенак принимался лишь при усилении болей в суставах в суточной дозе 100 мг.
На момент включения в исследование основная и контрольная группы были сопоставимы по параметрам суставного синдрома.
Статистическую обработку полученных данных проводили с помощью статистического пакета STATISTICA. Для описания характера распределения количественных признаков определялись средние величины, стандартное отклонение. Характер распределения количественных признаков оценивали по Колмогорову–Смирнову. Достоверность различий оценивалась с использованием t–критерия Стьюдента при нормальном распределении признака и с помощью U–критерия Манна–Уитни при ненормальном распределении. Различия считались достоверными при р<0,05.
При длительном приеме Т оказал положительное влияние на симптомы ГА. Уже через 6 месяцев ежедневного приема Т была отмечена положительная динамика всех клинических показателей. Так, выраженность боли по ВАШ в покое и при ходьбе снизилась по сравнению с исходными значениями с 31,44±7,12 и 52,82±12,48 мм до 20,89±7,44 и 30,65±12,42 мм соответственно (p<0,01). Достоверно отличались от исходных и значения ФИЛ (исходно 10,12±2,98 баллов), всех шкал индекса WOMAC (боли, скованности, функции, глобальный: исходно 172,48±47,54 мм, 48,91±12,75 мм, 554,75±158,97 мм, 785,65±160,51 мм), составив 5,20±2,42 баллов, 98,65±40,32 мм, 25,26±12,69 мм, 376,86±131,34 мм, 528,91±145,21 мм соответственно (р<0,01) через 6 месяцев непрерывного приема Т.
Далее, в соответствии с протоколом исследования, больные принимали Т повторными курсами по 2 месяца с интервалами 1 месяц. Положительная динамика всех клинических показателей сохранялась в течение всего срока наблюдения за больными основной группы.
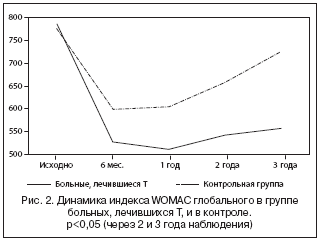
Достоверность различий выраженности боли по ВАШ, ФИЛ, индекса WOMAC с исходными значениями сохранялась через 1, 2 и 3 года наблюдения. Так, ФИЛ составил 5,72±2,16, 6,08±2,75, 6,27±2,81 баллов через 1, 2 и 3 года лечения Т соответственно (р<0,05), а индекс WOMAC глобальный – 513,18±156,71, 544,20±151,78, 558,61±153,12 мм в вышеназванные сроки наблюдения соответственно (р<0,05).
На фоне лечения Т значительно снизилась потребность пациентов в НПВП, которая достоверно отличалась от исходной во все сроки наблюдения за больными. После 6 месяцев лечения 22% пациентов смогли полностью отказаться от приема НПВП, через 1 год – 26,4%, через 2 года – 27,5%, через 3 года – 27,7% совсем не принимали НПВП.
В контрольной группе также наблюдалась положительная динамика всех клинических показателей через 6 месяцев, 1, 2 года наблюдения. Однако уже через 2 года лечения достоверность различий с исходным значением сохранялась лишь для выраженности боли по ВАШ. Через 3 года наблюдения значения всех клинических показателей приблизились к исходным.
Достоверность различий в значениях клинических показателей в группе пациентов, лечившихся Т, и в контрольной отсутствовали через 6 месяцев и 1 год наблюдения. Однако через 2 и 3 года лечения все клинические показатели (за исключением выраженности боли по ВАШ в покое исследуемой группы) были достоверно ниже, чем в контрольной. При сравнении основной и контрольной групп выявлены достоверные различия выраженности боли по ВАШ при ходьбе через 3 года наблюдения (37,96±12,84 и 51,25±13,01 мм, р<0,05), ФИЛ – через 2 и 3 года (6,08±2,75 и 8,90±3,54 баллов через 2 года, 6,27±2,81 и 9,45±3,20 баллов через 3 года соответственно, р<0,05) и индекса WOMAC глобального – через 2 и 3 года (544,20±151,78 и 658,24±172,30 мм через 2 года, 558,61±153,12 и 725,27±178,75 мм через 3 года соответственно, р<0,05) (рис. 1 и 2).
Как уже было сказано выше, эпицентром патологического процесса при ОА является суставной гиалиновый хрящ. В ходе проведенного исследования АСГ–ки были исследованы 175 суставов больных основной и 229 – больных контрольной группы, пораженных ГА, на момент включения и в контрольные сроки наблюдения (через 6 месяцев, 1, 2 и 3 года лечения).
На фоне лечения Т отмечена стабилизация размеров суставного хряща латерального и медиального мыщелков бедренной кости у больных основной группы (статистически значимые различия с исходными значениями отсутствовали во все сроки наблюдения).
В контрольной группе снижение высоты хряща было выявлено уже через 1 год наблюдения, которое, тем не менее, не было статистически достоверным. Однако в этой группе больных статистически достоверное снижение высоты хряща по сравнению с исходными значениями наблюдалось через 3 года лечения. Данные динамики высоты хряща мыщелков бедренной кости в основной и контрольной группах по данным АСГ представлены на рисунке 3.
Синовит той или иной степени выраженности сопровождает течение ОА на всех стадиях развития заболевания, в том числе и на самых ранних. Локальный воспалительный процесс утяжеляет симптомы ОА, способствует его прогрессированию.
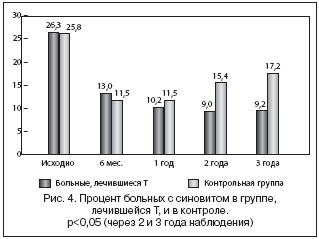
Положительное влияние длительной терапии Т на локальный воспалительный процесс было отмечено уже через 6 месяцев терапии. Процент больных с синовитом по данным АСГ был достоверно более низким на фоне лечения Т по сравнению с контрольной группой во все сроки наблюдения (рис. 4). Толщина синовиальной оболочки больных основной группы колебалась в пределах 1,7±0,3–2,2±0,4 мм.
Прогрессирование структурных изменений в коленных суставах ведет к нарастанию клинических проявлений заболевания – усиливается боль, выраженность функциональных расстройств. Для оценки влияния терапии на рентгенологическое прогрессирование ГА используется определение в динамике размеров РСЩ.
Через 1 год лечения Т отрицательная динамика высоты РСЩ в медиальном отделе ТФО практически отсутствовала. Через 2 и 3 года наблюдения различия в высоте РСЩ с исходными значениями не достигли статистической достоверности.
В контрольной группе через 1 год наблюдения отрицательная динамика данного рентгенологического показателя также отсутствовала. Через 2 года отрицательная динамика высоты РСЩ не достигла статистической достоверности различий с исходными значениями. Однако уже через 3 года лечения имело место статистически достоверное уменьшение размеров РСЩ (р<0,05) в данной группе больных. Динамика высоты РСЩ в медиальном отделе ТФО в группе больных, лечившихся Т, и в контрольной группе представлена на рисунке 5.
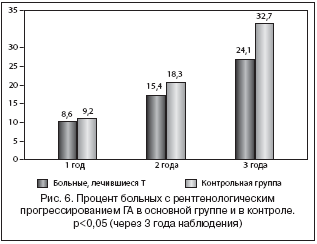
Рентгенологическое прогрессирование по Келлгрену–Лоуренсу на ≥1 рентгенологическую стадию на фоне терапии Т было констатировано у 9 (8,6%) пациентов через 1 год, у 15 (15,4%) – через 2 года, у 25 (24,1%) – через 3 года наблюдения. В контрольной группе утяжеление рентгенологической стадии ГА было выявлено через 1 год – у 13 (9,2%) пациентов, у 26 (18,3%) – через 2 года, у 46 (32,7 %) – через 3 года лечения (рис. 6).
Необходимо отметить, что Т при длительном приеме хорошо переносился пациентами. Лишь у трех больных развились побочные эффекты лечения в виде дискомфорта в эпигастральной области или запоров, не потребовавшие отмены препарата.
Таким образом, Т является эффективным средством длительного лечения ГА. Назначенная на ранних стадиях заболевания терапия Т оказала положительное влияние на симптомы заболевания, сохранявшееся на всех сроках наблюдения за пациентами. По данным АСГ выявлено сдерживающее влияние повторных курсов Т на темпы деградации суставного хряща. Препарат оказал положительное воздействие на воспалительный процесс в коленных суставах, было отмечено снижение частоты выявления синовита при АСГ. На фоне терапии Т констатировано замедление темпов рентгенологического прогрессирования ГА.



Литература
1. Алексеева Л.И. Факторы риска при остеоартрозе // Научно–практич. ревматология. – 2000. – № 2. – C. 36–45.
2. Насонова В.А. Проблема остеоартроза в начале XXI века // CONSILIUM MEDICUM. – 2000. – том 2. – № 6. – C. 61–64.
3. Насонова В.А. Остеоартроз коленного сустава: причины развития, диагностика и профилактика // CONSILIUM MEDICUM. – 2003. – том 5. – № 2. – C. 46–51.
4. Цурко В.В. Остеоартроз: гериартрическая проблема // РМЖ. – 2005. – том 13. – № 24. – C. 1627–1631.
5. Brandt K.D. Animal models of osteoarthritis. In: Reginster J.–Y., Peletier J.–P., Martel–Pelleter I., Heniotin Y. (eds). Osteoarthritis. Clinical and experimental aspects / Springer, 1999.
6. Felson D.T. Epidemiology of hip and knee osteoarthritis // Epidemical. Rev. – 1988. – № 10. – P. 1–28.
7. Felson D.T. Osteoarthritis of the knee // Clinical Practis. – 2006. – № 354. – P. 841–848.
8. Алексеева Л.И. Современные представления о диагностике, лечении и профилактике остеоартроза // РМЖ. – 2000. – том 8. – № 9. – С. 377–382.
9. Артемьева Н.А., Жарская Ф.С. К особенностям лечения остеоартроза // Научно–практич. ревматология. – 2001. – № 3. – C. 9.
10. Бадокин В.В. Современная терапия остеоартроза // Леч. врач. – 2001. – № 8. – C. 55–56.
11. Зоткин Е.Г. Рациональная терапия остеоартроза // Научно–практич. ревматология. – 2005. – № 5. – C. 48–51.
12. Лила А.М. Современная фармакотерапия остеоартроза // Terra Medica. – 2005. – том 1. – № 37. – C. 3–9.
13. Biggee B.A. Glucosamine for osteoarthritis // Evidence–Based Healthcare & Pablic Health. – 2005. – № 9. – P. 322–331.
14. Bruyere O., Pavelka K., Rovati L.C. et al. Glucosamine sulphate reduces osteoarhritis progression in postmenopausal with knee osteoarthritis: evidence from two 3–year studies // Menopause. – 2004. – vol. 11. – № 2. – P. 138–143.
15. Clegg D.O. Reda D. J., Harris C.L. et al. Glucosamine, chondroitin sulfate and the two in combination for painful knee osteoarthritis // NEJM. – 2006. – № 354. – P. 795–808.
16. Pavelka K., Gatterova J., Olejarova M. et al. Glucosamine sulphate use and delay of progression of knee osteoarthritis // JAMA and archives journals. – 2002. – № 14. – P. 2113–2123.
17. Pavelka K., Gatterova J., Giacovelli G. et al. Glucosamine sulphate prevents total joint replacement in the long–term follow–up of knee osteoarthritis patients // Arthritis Rheum. – 2004. – № 49. – P. 251.
18. Altman R., Asch E., Bloch D. et al. Development of criteria for the classification and reporting of osteoarthritis. Classification of the arthritis of the knee // Arthritis Rheum. – 1986. – № 29. – P. 1039–1049.
19. Kellgren J.H., Lawrence J.S. Radiographic assessment of osteoarthritis // Ann. Rheum. Dis. – 1957. – № 16. – P. 494–501.
20. Lequesne M., Samson M., Gerard P., Mery C. Pain–function indices for the follow–up of osteoarthritis of the hip and the knee // Rev. Rheum. Mal. Osteoartic. – 1990. – № 57(9pt2). – P. 32–36.
21. Bellamy N., Buchanan W.W., Goldsmith C.H. et al. Validation study of WOMAC: a health status instrument for measuring clinically important patient relevant outcomes to antirheumatic drug therapy in patients with osteoarthritis of the hip or knee // J. Rheumatol. – 1998. – № 15. – P. 1833–1840.












