–Т–≤–µ–і–µ–љ–Є–µ
–Т —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —В—А—Г–і–љ–Њ –≤—Б—В—А–µ—В–Є—В—М –њ–∞—Ж–Є–µ–љ—В–∞ —Б –Ї–∞–Ї–Є–Љ-–ї–Є–±–Њ –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ. –І–∞—Й–µ –≤—Б–µ–≥–Њ –Є–Љ–µ–µ—В –Љ–µ—Б—В–Њ —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В—М –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є, –Ї–Њ—В–Њ—А—Л–µ —Г—Б—Г–≥—Г–±–ї—П—О—В —В–µ—З–µ–љ–Є–µ –і—А—Г–≥ –і—А—Г–≥–∞. –Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –і–µ—Б—П—В–Є–ї–µ—В–Є–µ —И–Є—А–Њ–Ї–Њ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є–µ –њ–Њ–ї—Г—З–Є–ї–Њ –њ–Њ–љ—П—В–Є–µ –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В–Є, —З—В–Њ —В–∞–Ї–ґ–µ –љ–∞—И–ї–Њ —Б–≤–Њ–µ –Њ—В—А–∞–ґ–µ–љ–Є–µ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є. –Ґ–∞–Ї, –њ–∞—Ж–Є–µ–љ—В—Л —Б –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –Є–Љ–µ—О—В –≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є (–°–°–Ч) –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–∞—Б–µ–ї–µ–љ–Є–µ–Љ –≤ —Ж–µ–ї–Њ–Љ [1]. –Э–∞–Ї–Њ–њ–ї–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –њ—А–Є —В–∞–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е, –Ї–∞–Ї –њ–Њ–і–∞–≥—А–∞, –≤–∞—Б–Ї—Г–ї–Є—В, —Б–Є—Б—В–µ–Љ–љ–∞—П —Б–Ї–ї–µ—А–Њ–і–µ—А–Љ–Є—П, –Љ–Є–Њ–Ј–Є—В, —Б–Љ–µ—И–∞–љ–љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, —Б–Є–љ–і—А–Њ–Љ –®–µ–≥—А–µ–љ–∞, —Б–Є—Б—В–µ–Љ–љ–∞—П –Ї—А–∞—Б–љ–∞—П –≤–Њ–ї—З–∞–љ–Ї–∞ –Є –∞–љ—В–Є—Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ—Л–є —Б–Є–љ–і—А–Њ–Љ [2вАУ8]. –Я—А–Є —Н—В–Њ–Љ –і–∞–љ–љ—Л–є —Д–∞–Ї—В –љ–µ–ї—М–Ј—П –њ—А–Њ—Б—В–Њ –Њ–±—К—П—Б–љ–Є—В—М —А–∞–Ј–ї–Є—З–Є—П–Љ–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –°–°–Ч. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ —П–≤–ї—П–µ—В—Б—П –Ї–ї—О—З–µ–≤—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ –≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –°–°–Ч –њ—А–Є —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Ф–ї—П –ї–µ—З–µ–љ–Є—П —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —З–µ—В–Ї–Њ–µ –њ–Њ–љ–Є–Љ–∞–љ–Є–µ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–µ–є –Љ–µ–ґ–і—Г –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ, –Є–Љ–Љ—Г–љ–Є—В–µ—В–Њ–Љ –Є –Ї–∞—А–і–Є–Њ–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є.
–Ю–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є —П–≤–ї—П–µ—В—Б—П –њ–Њ–і–∞–≥—А–∞. –Я–Њ —Б–∞–Љ—Л–Љ —Б–Ї—А–Њ–Љ–љ—Л–Љ –њ–Њ–і—Б—З–µ—В–∞–Љ, –µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –љ–∞ —В–µ—А—А–Є—В–Њ—А–Є–Є –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є –і–Њ—Б—В–Є–≥–∞–µ—В 0,3% –≤–Ј—А–Њ—Б–ї–Њ–≥–Њ –љ–∞—Б–µ–ї–µ–љ–Є—П [9]. –Я—А–Є —Н—В–Њ–Љ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ —Н—В–Є–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ —Б—В—А–∞–і–∞—О—В –ї–Є—Ж–∞ –Љ—Г–ґ—Б–Ї–Њ–≥–Њ –њ–Њ–ї–∞ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –∞ —Г—З–Є—В—Л–≤–∞—П —Г—А–±–∞–љ–Є–Ј–∞—Ж–Є—О –љ–∞—Б–µ–ї–µ–љ–Є—П, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й—Г—О—Б—П —А–µ–Ј–Ї–Є–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –∞–ї–Є–Љ–µ–љ—В–∞—А–љ–Њ–≥–Њ –Њ–ґ–Є—А–µ–љ–Є—П –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –њ–Є–Ї –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –≤ –љ–∞—Б—В–Њ—П—Й–Є–є –Љ–Њ–Љ–µ–љ—В –њ—А–Є—Е–Њ–і–Є—В—Б—П –љ–∞ –ї–Є—Ж –≤ –≤–Њ–Ј—А–∞—Б—В–µ 30вАУ40 –ї–µ—В. –Ю–і–љ–∞–Ї–Њ –і–∞–љ–љ—Л–є –њ–Њ—А—В—А–µ—В —Е–∞—А–∞–Ї—В–µ—А–µ–љ –љ–µ —В–Њ–ї—М–Ї–Њ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б—В—А–∞–і–∞—О—Й–Є—Е —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, –љ–Њ –Є –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–°–Ч (–Є—И–µ–Љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М —Б–µ—А–і—Ж–∞ (–Ш–С–°), –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П (–Р–У) –Є —В. –і.), —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ, –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є–µ–є, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –њ–Њ—З–µ–Ї. –°–Њ–≥–ї–∞—Б–љ–Њ –Њ—Д–Є—Ж–Є–∞–ї—М–љ–Њ–є —Б—В–∞—В–Є—Б—В–Є–Ї–µ —Б–Љ–µ—А—В–љ–Њ—Б—В—М –≤ –†–Њ—Б—Б–Є–є—Б–Ї–Њ–є –§–µ–і–µ—А–∞—Ж–Є–Є –Њ—В –°–°–Ч –≤ 2020 –≥. —Б–Њ—Б—В–∞–≤–Є–ї–∞ 167,9 –љ–∞ 100 000 –љ–∞—Б–µ–ї–µ–љ–Є—П (–ї–Є—Ж–∞ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ –Њ–±–Њ–Є—Е –њ–Њ–ї–Њ–≤). –Я–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ–Љ –і–∞–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Љ–Њ–ґ–µ—В –±—Л—В—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ NHANES I (the National Health –Рnd Nutrition Examination Survey), –≤ –Ї–Њ—В–Њ—А–Њ–Љ –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –≥–Є–њ–µ—А—Г—А–Є–Ї–µ–Љ–Є–µ–є –Є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Љ–µ—А—В–љ–Њ—Б—В—М—О. –Ґ–∞–Ї, –љ–∞ —Д–Њ–љ–µ –њ–Њ–≤—Л—И–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Љ–Њ—З–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (–Ь–Ъ) –≤ –Ї—А–Њ–≤–Є –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є –Њ—В –Ш–С–° –љ–∞ 77% —Г –Љ—Г–ґ—З–Є–љ –Є –љ–∞ 300% —Г –ґ–µ–љ—Й–Є–љ [10].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–Њ–ґ–љ–Њ –≥–Њ–≤–Њ—А–Є—В—М –Њ –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –і–∞–љ–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ—Л –љ–µ —В–Њ–ї—М–Ї–Њ –і–ї—П —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Њ–≤, –љ–Њ –Є –і–ї—П —В–µ—А–∞–њ–µ–≤—В–Њ–≤ (–Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤, —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Њ–≤, –љ–µ—Д—А–Њ–ї–Њ–≥–Њ–≤). –†–∞–Ј—А–∞–±–Њ—В–Ї–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є —В–Њ–ї—М–Ї–Њ –њ–Њ –Ї–∞–Ї–Њ–є-–ї–Є–±–Њ —Г–Ј–Ї–Њ–є —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ—Б—В–Є –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ —Б–Њ–≤—Б–µ–Љ –∞–Ї—В—Г–∞–ї—М–љ–∞. –Т —Б–≤–µ—В–µ –≤—Л—И–µ–Є–Ј–ї–Њ–ґ–µ–љ–љ–Њ–≥–Њ —И–Є—А–Њ–Ї–Њ –≤–Њ—Б—В—А–µ–±–Њ–≤–∞–љ—Л –і–∞–љ–љ—Л–µ —А–µ–≥–Є—Б—В—А–Њ–≤ —Б —Г—З–µ—В–Њ–Љ –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –∞ —В–∞–Ї–ґ–µ –љ–∞—Г—З–љ—Л–µ –њ—Г–±–ї–Є–Ї–∞—Ж–Є–Є –љ–∞ —Б—В—Л–Ї–µ —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ—Б—В–µ–є, –љ–∞–њ—А–Є–Љ–µ—А —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є, –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Є–Є, —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є–Є.
–°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –Р—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Њ–≤ –†–Њ—Б—Б–Є–Є (2018 –≥.) —Г—А–∞—В—Б–љ–Є–ґ–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П –Є–љ–Є—Ж–Є–Є—А—Г–µ—В—Б—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –і–µ–±—О—В–Њ–Љ –њ–Њ–і–∞–≥—А—Л –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Љ–ї–∞–і—И–µ 40 –ї–µ—В –њ—А–Є –љ–∞–ї–Є—З–Є–Є –њ–Њ—З–µ—З–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –Ї–Њ–Љ–Њ—А–±–Є–і–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б—А–∞–Ј—Г –њ–Њ—Б–ї–µ –њ–µ—А–≤–Њ–≥–Њ –њ—А–Є—Б—В—Г–њ–∞ –∞—А—В—А–Є—В–∞. –Я–∞—Ж–Є–µ–љ—В–∞–Љ —Б—В–∞—А—И–µ 40 –ї–µ—В –±–µ–Ј –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В–Є –њ—А–µ–і–њ–Є—Б–∞–љ–Њ –љ–∞–Ј–љ–∞—З–∞—В—М —Г—А–∞—В—Б–љ–Є–ґ–∞—О—Й—Г—О —В–µ—А–∞–њ–Є—О —Б–Њ —Б—В–Њ–є–Ї–Њ–є –≥–Є–њ–µ—А—Г—А–Є–Ї–µ–Љ–Є–µ–є –Є –Њ—Б—В—А—Л–Љ–Є –∞—В–∞–Ї–∞–Љ–Є –∞—А—В—А–Є—В–∞ (—Б —З–∞—Б—В–Њ—В–Њ–є –њ—А–Є—Б—В—Г–њ–∞ вЙ•2 –≤ –≥–Њ–і), —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –∞—А—В—А–Є—В–Њ–Љ, –љ–∞–ї–Є—З–Є–µ–Љ —В–Њ—Д—Г—Б–Њ–≤. –Э–∞–Љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П, —З—В–Њ —В–∞–Ї–Њ–є –њ–Њ–і—Е–Њ–і —П–≤–ї—П–µ—В—Б—П –љ–µ —Б–Њ–≤—Б–µ–Љ —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ—Л–Љ (–Ј–∞–њ–∞–Ј–і—Л–≤–∞—О—Й–Є–Љ), —В–∞–Ї –Ї–∞–Ї –Ј–∞—З–∞—Б—В—Г—О –њ–∞—Ж–Є–µ–љ—В –Є–Љ–µ–µ—В –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –і–ї–Є—В–µ–ї—М–љ–Њ —Б—Г—Й–µ—Б—В–≤—Г—О—Й–µ–є –≥–Є–њ–µ—А—Г—А–Є–Ї–µ–Љ–Є–Є –≤ –≤–Є–і–µ –≤–Њ–≤–ї–µ—З–µ–љ–Є—П –≤ –њ—А–Њ—Ж–µ—Б—Б –њ–Њ—З–µ–Ї, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –њ–Њ–і–∞–≥—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є, —Г—А–∞—В–љ–Њ–≥–Њ –љ–µ—Д—А–Њ–ї–Є—В–Є–∞–Ј–∞. –Я—А–Њ–±–ї–µ–Љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ–Њ–є –≥–Є–њ–µ—А—Г—А–Є–Ї–µ–Љ–Є–Є –∞–Ї—В–Є–≤–љ–Њ –Њ–±—Б—Г–ґ–і–∞–µ—В—Б—П —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є —Б–Њ–Њ–±—Й–µ—Б—В–≤–∞–Љ–Є –Љ–Є—А–∞, –Њ–і–љ–∞–Ї–Њ –≤ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е —Н—В–Є –њ–Њ–ї–Њ–ґ–µ–љ–Є—П –і–Њ —Б–Є—Е –њ–Њ—А –љ–µ –Ј–∞–Ї—А–µ–њ–ї–µ–љ—Л –Ј–∞–Ї–Њ–љ–Њ–і–∞—В–µ–ї—М–љ–Њ.
–°–Њ–≥–ї–∞—Б–љ–Њ –Ї–Њ–љ—Б–µ–љ—Б—Г—Б—Г –њ–Њ –≤–µ–і–µ–љ–Є—О –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≥–Є–њ–µ—А—Г—А–Є–Ї–µ–Љ–Є–µ–є –Є –≤—Л—Б–Њ–Ї–Є–Љ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —А–Є—Б–Ї–Њ–Љ, —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ–Њ–Љ—Г –њ–Њ–і —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ –∞–Ї–∞–і–µ–Љ–Є–Ї–∞ –Ш.–Х. –І–∞–Ј–Њ–≤–Њ–є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Б—З–Є—В–∞—В—М –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–µ–љ—М –Ь–Ъ –±–Њ–ї–µ–µ 360 –Љ–Ї–Љ–Њ–ї—М/–ї, –∞ —В–∞–Ї–ґ–µ –Њ—Ж–µ–љ–Є–≤–∞—В—М –љ–∞–ї–Є—З–Є–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –°–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –≤ —Н—В–Њ–є –≥—А—Г–њ–њ–µ —Б–ї–µ–і—Г–µ—В —Б—З–Є—В–∞—В—М —Ж–µ–ї–µ–≤—Л–Љ —Г—А–Њ–≤–µ–љ—М –Ь–Ъ –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є –љ–Є–ґ–µ 300 –Љ–Ї–Љ–Њ–ї—М/–ї [11].
–°–Њ–≥–ї–∞—Б–љ–Њ –Њ–±—К–µ–і–Є–љ–µ–љ–љ—Л–Љ –і–∞–љ–љ—Л–Љ III —Д–∞–Ј—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є (–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Р–†–Х–•, –†–Р–°–Ґ –Є –°–ЮNFIR–Ь–Е) —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ–і–∞–≥—А–Њ–є —З–∞—Б—В–Њ—В–∞ –љ–∞—А—Г—И–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л —Б–Њ—Б—В–∞–≤–Є–ї–∞ 0,7 –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –∞–ї–ї–Њ–њ—Г—А–Є–љ–Њ–ї, –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б —З–∞—Б—В–Њ—В–Њ–є 0,6 —Б–ї—Г—З–∞—П –љ–∞ 100 –њ–∞—Ж–Є–µ–љ—В–Њ-–ї–µ—В –≤ –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Д–µ–±—Г–Ї—Б–Њ—Б—В–∞—В.
–Т –њ–Њ—Б—В—А–µ–≥–Є—Б—В—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –°–РR–Х–Е [12] —З–∞—Б—В–Њ—В–∞ —Б–µ—А—М–µ–Ј–љ—Л—Е —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є –±—Л–ї–∞ —Б—Е–Њ–і–љ–Њ–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е —Д–µ–±—Г–Ї—Б–Њ—Б—В–∞—В, –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –∞–ї–ї–Њ–њ—Г—А–Є–љ–Њ–ї, –љ–Њ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞ —Б–ї—Г—З–∞–µ–≤ —Б–Љ–µ—А—В–Є –њ–Њ –њ—А–Є—З–Є–љ–∞–Љ, —Б–≤—П–Ј–∞–љ–љ—Л–Љ —Б —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є (4,3% –њ—А–Њ—В–Є–≤ 3,2%, p=0,03). –≠—В–Њ —Б—В–∞–ї–Њ –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –≤–љ–µ—Б–µ–љ–Є—П —Б–µ—А—М–µ–Ј–љ—Л—Е –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–є –≤ –Є–љ—Б—В—А—Г–Ї—Ж–Є—О –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О —Д–µ–±—Г–Ї—Б–Њ—Б—В–∞—В–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–°–Ч.
–Т 2022 –≥. —Б–≤–µ—В —Г–≤–Є–і–µ–ї–Є —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є EULAR –њ–Њ —Г–њ—А–∞–≤–ї–µ–љ–Є—О —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є —А–Є—Б–Ї–∞–Љ–Є –њ—А–Є —А–µ–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –Њ–њ–Њ—А–љ–Њ-–і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞, –≤–Ї–ї—О—З–∞—П —Б–Є—Б—В–µ–Љ–љ—Г—О –Ї—А–∞—Б–љ—Г—О –≤–Њ–ї—З–∞–љ–Ї—Г –Є –∞–љ—В–Є—Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ—Л–є —Б–Є–љ–і—А–Њ–Љ [13], –Ї–Њ—В–Њ—А—Л–µ –Є–Ј–Љ–µ–љ–Є–ї–Є –Њ—В–љ–Њ—И–µ–љ–Є–µ –Ї –≥–Є–њ–Њ—Г—А–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —А–Є—Б–Ї–Њ–Љ. –Т —Н—В–Њ–Љ –і–Њ–Ї—Г–Љ–µ–љ—В–µ –Ї—А–Є—В–Є—З–µ—Б–Ї–Є –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л –Є –њ–µ—А–µ—Б–Љ–Њ—В—А–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П CARES, –∞ —В–∞–Ї–ґ–µ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ, —З—В–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ FAST [14] –њ–Њ–Ї–∞–Ј–∞–ї–Њ –±–Њ–ї–µ–µ –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–µ –і–∞–љ–љ—Л–µ. –Ш—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є –њ—А–Є—И–ї–Є –Ї –≤—Л–≤–Њ–і—Г, —З—В–Њ –∞–ї–ї–Њ–њ—Г—А–Є–љ–Њ–ї –љ–µ –Є–Љ–µ–µ—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –≤ –њ–µ—А–≤–Є—З–љ–Њ–Љ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –њ–µ—А–µ–і —Д–µ–±—Г–Ї—Б–Њ—Б—В–∞—В–Њ–Љ —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–≥–Њ —А–Є—Б–Ї–∞. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ FAST –љ–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ —А–∞–Ј–ї–Є—З–Є–є –≤ —З–∞—Б—В–Њ—В–µ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ–Њ–є –і–Њ–Ј—Л –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Љ–µ–ґ–і—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–Љ–Є –∞–ї–ї–Њ–њ—Г—А–Є–љ–Њ–ї –Є–ї–Є —Д–µ–±—Г–Ї—Б–Њ—Б—В–∞—В. –≠—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В –Є –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л–µ –≤ 2019 –≥. —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П FREED [15], –≤ –Ї–Њ—В–Њ—А–Њ–Љ –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М —З–∞—Б—В–Њ—В–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л—Е, —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Є –њ–Њ—З–µ—З–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ 65 –ї–µ—В, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Д–µ–±—Г–Ї—Б–Њ—Б—В–∞—В, –∞–ї–ї–Њ–њ—Г—А–Є–љ–Њ–ї, –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—А—А–µ–Ї—В–Є—А–Њ–≤–∞–≤—И–Є—Е –≥–Є–њ–µ—А—Г—А–Є–Ї–µ–Љ–Є—О –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–µ–є –Њ–±—А–∞–Ј–∞ –ґ–Є–Ј–љ–Є.
–Т –Њ–Ї–Њ–љ—З–∞—В–µ–ї—М–љ–Њ–Љ –ґ–µ –≤—Л–≤–Њ–і–µ –Є–Ј–ї–Њ–ґ–µ–љ–Њ, —З—В–Њ –љ–∞ –і–∞–љ–љ—Л–є –Љ–Њ–Љ–µ–љ—В –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ–і–∞–≥—А–Њ–є –≤ –њ–ї–∞–љ–µ —В–µ—А–∞–њ–Є–Є –љ–µ—В –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є—П –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–Љ—Г —Г—А–∞—В—Б–љ–Є–ґ–∞—О—Й–µ–Љ—Г –њ—А–µ–њ–∞—А–∞—В—Г —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є 1b) [12].
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Њ—Ж–µ–љ–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –§–µ–±—Г–Ї—Б–Њ—Б—В–∞—В-–°–Ч —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ–і–∞–≥—А–Њ–є –Є –≤—Л—Б–Њ–Ї–Є–Љ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —А–Є—Б–Ї–Њ–Љ.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Я—А–Њ–≤–µ–і–µ–љ–Њ –Њ–і–љ–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Љ—Г–ґ—Б–Ї–Њ–≥–Њ –њ–Њ–ї–∞ —Б –њ–Њ–і–∞–≥—А–Њ–є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Р–У. –Т—Б–µ–≥–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 50 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ—Л–Љ –і–Є–∞–≥–љ–Њ–Ј–Њ–Љ –њ–Њ–і–∞–≥—А—Л –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Њ–љ–љ—Л–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є ACR/EULAR (2015 –≥.) [16]. –Я–∞—Ж–Є–µ–љ—В—Л –њ–Њ–і–њ–Є—Б—Л–≤–∞–ї–Є –і–Њ–±—А–Њ–≤–Њ–ї—М–љ–Њ–µ –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ —Б–Њ–≥–ї–∞—Б–Є–µ. –Ф–Є–∞–≥–љ–Њ–Ј –Р–У –≤—Л—Б—В–∞–≤–ї—П–ї—Б—П –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —А–Њ—Б—Б–Є–є—Б–Ї–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є [17]. –Э–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В—Л –љ–µ –њ–Њ–ї—Г—З–∞–ї–Є –ї–µ—З–µ–љ–Є–µ –њ–Њ –њ–Њ–≤–Њ–і—Г –њ–Њ–і–∞–≥—А—Л –Є–ї–Є –њ–Њ–ї—Г—З–∞–ї–Є –∞–ї–ї–Њ–њ—Г—А–Є–љ–Њ–ї –≤ —В–µ—З–µ–љ–Є–µ 3 –Љ–µ—Б. вАФ 2 –ї–µ—В, –љ–Њ –љ–µ –і–Њ—Б—В–Є–≥–ї–Є —Ж–µ–ї–µ–≤–Њ–≥–Њ —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Ь–Ъ (<360 –Љ–Ї–Љ–Њ–ї—М/–ї; –і–ї—П –±–Њ–ї—М–љ—Л—Е —Б —В—П–ґ–µ–ї–Њ–є —В–Њ—Д—Г—Б–љ–Њ–є –њ–Њ–і–∞–≥—А–Њ–є –Є–ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ —А–Є—Б–Ї–Њ–Љ вАФ <300 –Љ–Ї–Љ–Њ–ї—М/–ї). –£ –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–Њ–Ј–∞ –∞–ї–ї–Њ–њ—Г—А–Є–љ–Њ–ї–∞ —В–Є—В—А–Њ–≤–∞–ї–∞—Б—М —Б–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –і–Њ 300 –Љ–≥/—Б—Г—В. –°–Ї–Њ—А–Њ—Б—В—М –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є (–°–Ъ–§), —А–∞—Б—Б—З–Є—В–∞–љ–љ–∞—П –њ–Њ —Д–Њ—А–Љ—Г–ї–µ CKD-EPI, —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ >30 –Љ–ї/–Љ–Є–љ/1,73 –Љ2. –Э–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Г—А–∞—В—Б–љ–Є–ґ–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –∞–љ–∞–Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є –Є –Ј–∞–Ї–ї—О—З–∞–ї–∞—Б—М –≤ –љ–µ–і–Њ—Б—В–Є–ґ–µ–љ–Є–Є —Ж–µ–ї–µ–≤—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ь–Ъ, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –љ–∞ —Д–Њ–љ–µ –љ–µ–ґ–µ–ї–∞–љ–Є—П –і–∞–ї–µ–µ –њ—А–Є–љ–Є–Љ–∞—В—М –∞–ї–ї–Њ–њ—Г—А–Є–љ–Њ–ї. –†–µ—И–µ–љ–Є–µ –Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Д–µ–±—Г–Ї—Б–Њ—Б—В–∞—В–∞ –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –∞–љ–∞–Љ–љ–µ–Ј–∞ –њ–Њ –њ—А–Є–µ–Љ—Г –∞–ї–ї–Њ–њ—Г—А–Є–љ–Њ–ї–∞ –њ—А–Є–љ–Є–Љ–∞–ї–Њ—Б—М –њ—А–Є –љ–∞–ї–Є—З–Є–Є —В–Њ—Д—Г—Б–љ–Њ–є –њ–Њ–і–∞–≥—А—Л –Є/–Є–ї–Є —Б–љ–Є–ґ–µ–љ–Є—П –°–Ъ–§ –љ–Є–ґ–µ 60 –Љ–ї/–Љ–Є–љ/1,73 –Љ2. –° —Ж–µ–ї—М—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –њ—А–Є—Б—В—Г–њ–Њ–≤ –Њ—Б—В—А–Њ–≥–Њ –∞—А—В—А–Є—В–∞ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б—В–∞–љ–і–∞—А—В–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–∞—П –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –љ–∞–њ—А–Њ–Ї—Б–µ–љ 100 –Љ–≥ (—Г—В—А–Њ–Љ –њ–Њ—Б–ї–µ –Ј–∞–≤—В—А–∞–Ї–∞ 1 –Љ–µ—Б.) [18вАУ20]. –Т—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –§–µ–±—Г–Ї—Б–Њ—Б—В–∞—В-–°–Ч 80 –Љ–≥ –≤–љ–µ –њ–Њ–і–∞–≥—А–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В—А–Є—В–∞ (—З–µ—А–µ–Ј 2 –љ–µ–і. –њ–Њ—Б–ї–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –Њ—Б—В—А–Њ–≥–Њ –∞—А—В—А–Є—В–∞).
–Я—А–Є –≤–Є–Ј–Є—В–∞—Е –≤ –њ–µ—А–≤—Л–є –і–µ–љ—М –Є —З–µ—А–µ–Ј –њ–Њ–ї–≥–Њ–і–∞ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Б—В–∞—В—Г—Б, –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–є –њ—А–Њ—Д–Є–ї—М (–Њ–±—Й–Є–є –∞–љ–∞–ї–Є–Ј –Ї—А–Њ–≤–Є, –Љ–Њ—З–Є, –ї–Є–њ–Є–і–љ—Л–є —Б–њ–µ–Ї—В—А, —Г—А–Њ–≤–µ–љ—М –≥–ї—О–Ї–Њ–Ј—Л –Ї—А–Њ–≤–Є, –Ї—А–µ–∞—В–Є–љ–Є–љ–∞, –Ь–Ъ, —В—А–∞–љ—Б–∞–Љ–Є–љ–∞–Ј), –°–Ъ–§, –≤—Л–њ–Њ–ї–љ—П–ї–Є –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (—Н–ї–µ–Ї—В—А–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞—Д–Є—П, —Н—Е–Њ–Ї–∞—А–і–Є–Њ–≥—А–∞—Д–Є—П, —Б—Г—В–Њ—З–љ–Њ–µ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є–µ –≠–Ъ–У –Є –Р–Ф –њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ, –£–Ч–Ш –±—А—О—И–љ–Њ–є –њ–Њ–ї–Њ—Б—В–Є –Є –њ–Њ—З–µ–Ї).
–Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –Ј–∞–њ–Њ–ї–љ—П–ї–Є —А–Њ—Б—Б–Є–є—Б–Ї–Є–є –Њ–њ—А–Њ—Б–љ–Є–Ї –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—О –Ъ–Ю–Я-25 [21]. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –Њ—В–Њ–±—А–∞–ґ–∞—О—В—Б—П –≤ –њ—А–Њ—Ж–µ–љ—В–∞—Е, –≥–і–µ –Ј–љ–∞—З–µ–љ–Є—П –љ–Є–ґ–µ 50% —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В –љ–Є–Ј–Ї—Г—О –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В—М, 50вАУ75% вАФ —Б—А–µ–і–љ—О—О, –∞ –±–Њ–ї–µ–µ 75% вАФ –≤—Л—Б–Њ–Ї—Г—О. –Ф–Є–љ–∞–Љ–Є–Ї—Г —Б–Њ—Б—В–Њ—П–љ–Є—П –Ј–і–Њ—А–Њ–≤—М—П –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ SF-36, –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ вАФ –њ–Њ –≤–Є–Ј—Г–∞–ї—М–љ–Њ-–∞–љ–∞–ї–Њ–≥–Њ–≤–Њ–є —И–Ї–∞–ї–µ (–Т–Р–®).
–Р–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є —Н–њ–Є–Ј–Њ–і—Л –Њ—Б—В—А–Њ–≥–Њ –њ–Њ–і–∞–≥—А–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В—А–Є—В–∞ –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –§–µ–±—Г–Ї—Б–Њ—Б—В–∞—В-–°–Ч, –∞ —В–∞–Ї–ґ–µ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–µ —Б–Њ–±—Л—В–Є—П (–≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є—П –њ–Њ –њ—А–Є—З–Є–љ–µ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–∞—П —Б–Љ–µ—А—В—М, –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є—П –Р–У, –Ш–С–°, —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –љ–µ —В—А–µ–±—Г—О—Й–∞—П –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–Є), –љ–∞–ї–Є—З–Є–µ –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є.
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї—Г—О –Њ–±—А–∞–±–Њ—В–Ї—Г –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О –њ–∞–Ї–µ—В–∞ –њ—А–Њ–≥—А–∞–Љ–Љ IBM SPSS Statistics, Version 10.0 (IBM, –°–®–Р). –Ю—Ж–µ–љ–Ї—Г –љ–Њ—А–Љ–∞–ї—М–љ–Њ—Б—В–Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О W-–Ї—А–Є—В–µ—А–Є—П –®–∞–њ–Є—А–Њ вАФ –£–Є–ї–Ї–∞. –Ъ–∞—В–µ–≥–Њ—А–Є–∞–ї—М–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –∞–±—Б–Њ–ї—О—В–љ—Л–Љ–Є –Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–Љ–Є (–≤ %) —З–∞—Б—В–Њ—В–∞–Љ–Є, –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Њ–њ–Є—Б—Л–≤–∞–ї–Є –Љ–µ–і–Є–∞–љ–∞–Љ–Є –Є –Љ–µ–ґ–Ї–≤–∞—А—В–Є–ї—М–љ—Л–Љ–Є –Є–љ—В–µ—А–≤–∞–ї–∞–Љ–Є (–Ь–µ [LQ; HQ]). –Ч–љ–∞—З–Є–Љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–Є–є –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ —Б–≤—П–Ј–∞–љ–љ—Л—Е –≤—Л–±–Њ—А–Ї–∞—Е –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О –Ї—А–Є—В–µ—А–Є—П –Т–Є–ї–Ї–Њ–Ї—Б–Њ–љ–∞. –Ф–ї—П –њ—А–Њ–≤–µ—А–Ї–Є –≥–Є–њ–Њ—В–µ–Ј –Њ —А–∞–≤–µ–љ—Б—В–≤–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Ї—А–Є—В–µ—А–Є–є –Ь–∞–љ–љ–∞ вАФ –£–Є—В–љ–Є. –Я–Њ—А–Њ–≥–Њ–≤—Л–є —Г—А–Њ–≤–µ–љ—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –≤—Л–≤–Њ–і–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П–ї —А<0,05.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Т–Њ–Ј—А–∞—Б—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, —Б–Њ—Б—В–∞–≤–Є–ї 58 [49; 63] –ї–µ—В, —Б—В–∞–ґ –њ–Њ–і–∞–≥—А—Л вАФ 2 [2; 10] –≥–Њ–і–∞. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 1.

–Р–љ–∞–ї–Є–Ј –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Ј–∞ 6 –Љ–µ—Б. –љ–∞–±–ї—О–і–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–Њ–і–∞–≥—А—Л. –Ґ–∞–Ї, –≤ –≥—А—Г–њ–њ–µ –љ–∞–±–ї—О–і–µ–љ–Є—П –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б—В–Њ–є–Ї–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Ь–Ъ –і–Њ 270,6 [233; 306] –Љ–Ї–Љ–Њ–ї—М/–ї (—А<0,0001) (—В–∞–±–ї. 2). –£—А–Њ–≤–µ–љ—М –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б–Њ—Б—В–∞–≤–Є–ї 100% –≤ –≥—А—Г–њ–њ–µ –≤—Л—Б–Њ–Ї–Њ–≥–Њ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —А–Є—Б–Ї–∞ –Є 82% –њ—А–Є –љ–∞–ї–Є—З–Є–Є —В–Њ—Д—Г—Б–Њ–≤. –£—А–∞—В—Б–љ–Є–ґ–∞—О—Й–Є–є —Н—Д—Д–µ–Ї—В –≤–∞—А—М–Є—А–Њ–≤–∞–ї –Њ—В 190 –Љ–Ї–Љ–Њ–ї—М/–ї –і–Њ 400 –Љ–Ї–Љ–Њ–ї—М/–ї, —Б–Њ—Б—В–∞–≤–Є–≤ –≤ —Б—А–µ–і–љ–µ–Љ 260,9 –Љ–Ї–Љ–Њ–ї—М/–ї. –£ –Њ–і–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –±—Л–ї –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ –Њ—Б—В—А—Л–є –њ–Њ–і–∞–≥—А–Є—З–µ—Б–Ї–Є–є –∞—А—В—А–Є—В, —З—В–Њ –њ–Њ—В—А–µ–±–Њ–≤–∞–ї–Њ –≤–Њ–Ј–Њ–±–љ–Њ–≤–ї–µ–љ–Є—П –њ—А–Є–µ–Љ–∞ –љ–∞–њ—А–Њ–Ї—Б–µ–љ–∞. –Ф–Є–љ–∞–Љ–Є–Ї–∞ —Г—А–Њ–≤–љ—П –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –њ–Њ–Ї–∞–Ј–∞–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –Я—А–Є —Н—В–Њ–Љ —Г—А–Њ–≤–µ–љ—М –°–Ъ–§ –≤ –і–Є–љ–∞–Љ–Є–Ї–µ –љ–µ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є (—Б–Љ. —В–∞–±–ї. 2). –°–Њ–≥–ї–∞—Б–љ–Њ –ґ–µ –і–∞–љ–љ—Л–Љ –Ь.–°. –Х–ї–Є—Б–µ–µ–≤–∞ –Є —Б–Њ–∞–≤—В. [22] –њ—А–Є—А–Њ—Б—В –°–Ъ–§ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–Њ–і–∞–≥—А–Њ–є —Б–Њ—Б—В–∞–≤–Є–ї –њ–Њ—А—П–і–Ї–∞ 1 –Љ–ї/–Љ–Є–љ/1,73 –Љ2 (—Б 63,98 –Љ–ї/–Љ–Є–љ/1,73 –Љ2 –і–Њ 64,74 –Љ–ї/–Љ–Є–љ/1,73 –Љ2).
![–Ґ–∞–±–ї–Є—Ж–∞ 2. –Ч–љ–∞—З–µ–љ–Є—П –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ –і–Є–љ–∞–Љ–Є–Ї–µ –љ–∞–±–ї—О–і–µ–љ–Є—П (Me [LQ; HQ]) –Ґ–∞–±–ї–Є—Ж–∞ 2. –Ч–љ–∞—З–µ–љ–Є—П –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ –і–Є–љ–∞–Љ–Є–Ї–µ –љ–∞–±–ї—О–і–µ–љ–Є—П (Me [LQ; HQ])](/upload/medialibrary/287/62-2.png)
–Ч–∞ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л–є –њ–µ—А–Є–Њ–і —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–µ –±—Л–ї–Њ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ –Ї–∞–Ї–Є—Е-–ї–Є–±–Њ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є. –Т —Ж–µ–ї–Њ–Љ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б—В–∞–±–Є–ї—М–љ–Њ–µ —В–µ—З–µ–љ–Є–µ –≤—Б–µ—Е —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є (–Ш–С–°, –Р–У, –•–°–Э). –Э–µ–Њ—В–ї–Њ–ґ–љ—Л—Е –Є –њ–ї–∞–љ–Њ–≤—Л—Е –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є, –∞ —В–µ–Љ –±–Њ–ї–µ–µ –ї–µ—В–∞–ї—М–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–Њ –љ–µ –±—Л–ї–Њ. –Ф–∞–љ–љ—Л–є —Д–∞–Ї—В —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –§–µ–±—Г–Ї—Б–Њ—Б—В–∞—В-–°–Ч —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–°–Ч. –Ю–і–љ–∞–Ї–Њ —Б —Г—З–µ—В–Њ–Љ –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –њ—А–Њ–Љ–µ–ґ—Г—В–Ї–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П –і–∞–љ–љ—Л–є –≤—Л–≤–Њ–і —П–≤–ї—П–µ—В—Б—П –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ—Л–Љ –Є —В—А–µ–±—Г–µ—В –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–∞–±–ї—О–і–µ–љ–Є—П. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –љ–∞–Љ–Є –і–∞–љ–љ—Л–µ —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П CONFIRMS [23].
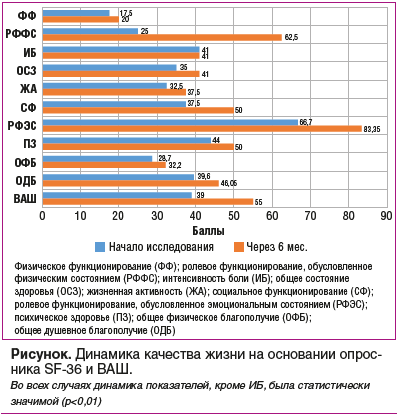
–Ю—Ж–µ–љ–Ї–∞ –і–Є–љ–∞–Љ–Є–Ї–Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ SF-36 (–Њ–і–Є–љ –Є–Ј –љ–µ–Љ–∞–ї–Њ–≤–∞–ґ–љ—Л—Е –∞—Б–њ–µ–Ї—В–Њ–≤ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤) –њ–Њ–Ї–∞–Ј–∞–ї–∞ —Е–Њ—А–Њ—И–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л. –Т—Л—П–≤–ї–µ–љ–∞ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ (—А<0,01) –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ –≤—Б–µ–Љ –∞—Б–њ–µ–Ї—В–∞–Љ –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ SF-36, –Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–Є (—Б–Љ. —А–Є—Б—Г–љ–Њ–Ї). –Ф–∞–љ–љ—Л–є —Д–∞–Ї—В —П–≤–ї—П–µ—В—Б—П –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ—Л–Љ, —В–∞–Ї –Ї–∞–Ї –Є–Ј—Г—З–∞–µ–Љ—Л–є –њ—А–µ–њ–∞—А–∞—В –љ–µ –Њ–±–ї–∞–і–∞–µ—В –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ. –Я–Њ–ї—Г—З–µ–љ–љ—Л–є —А–µ–Ј—Г–ї—М—В–∞—В –Љ—Л —Б—З–Є—В–∞–µ–Љ –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л–Љ, —В–∞–Ї –Ї–∞–Ї –і–ї—П –њ–∞—Ж–Є–µ–љ—В–∞ —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –µ–≥–Њ –ґ–Є–Ј–љ–Є —П–≤–ї—П–µ—В—Б—П –њ—А–Є–Њ—А–Є—В–µ—В–љ—Л–Љ –Є –≥–Њ–≤–Њ—А–Є—В –Њ–± —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–ї—Г—З—И–Є—В—М –µ–≥–Њ –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –Є —В–µ–Љ —Б–∞–Љ—Л–Љ —Б–љ–Є–Ј–Є—В—М –љ–∞–≥—А—Г–Ј–Ї—Г –љ–∞ —Б–Є—Б—В–µ–Љ—Г –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П.
–Ю–і–љ–Є–Љ –Є–Ј –Ї–ї—О—З–µ–≤—Л—Е –≤–Њ–њ—А–Њ—Б–Њ–≤ –≤ –≤–µ–і–µ–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є —П–≤–ї—П–µ—В—Б—П –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є. –°—А–µ–і–Є –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –≤—Л–і–µ–ї—П–µ–Љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –љ–Є–Ј–Ї–Њ–є –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є—О –≤—А–∞—З–µ–±–љ—Л—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –≤—Л–і–µ–ї—П—О—В –љ–Є–Ј–Ї–Є–є —Г—А–Њ–≤–µ–љ—М –і–Њ—Б—В–∞—В–Ї–∞, –Ј–∞–±—Л–≤—З–Є–≤–Њ—Б—В—М, –Љ–Њ–ї–Њ–і–Њ–є –Є —Б—В–∞—А—З–µ—Б–Ї–Є–є –≤–Њ–Ј—А–∞—Б—В, –Љ—Г–ґ—Б–Ї–Њ–є –њ–Њ–ї, –Ї—Г—А–µ–љ–Є–µ, –љ–µ–і–Њ–≤–µ—А–Є–µ –Ї –≤—А–∞—З–∞–Љ, –љ–µ–≤–µ—А–Є–µ –≤ —Г—Б–њ–µ—И–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –Є –і—А. [24]. –Р–љ–∞–ї–Є–Ј –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –і–∞–љ–љ—Л—Е –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ъ–Ю–Я-25 –≤—Л—П–≤–Є–ї –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г. –Ґ–∞–Ї, –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Н–њ–Є–Ј–Њ–і–Њ–≤ –Њ—Б—В—А–Њ–≥–Њ –њ–Њ–і–∞–≥—А–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—А—В—А–Є—В–∞, —Б—В–Њ–є–Ї–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Ь–Ъ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Є –њ–Њ–≤—Л—И–µ–љ–Є—О –і–Њ–≤–µ—А–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –Ї –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–Љ—Г –њ–µ—А—Б–Њ–љ–∞–ї—Г, –Є –Ї –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Я—А–Є—З–µ–Љ –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ (—А<0,0005) –њ–Њ –≤—Б–µ–Љ –∞—Б–њ–µ–Ї—В–∞–Љ –Њ–њ—А–Њ—Б–љ–Є–Ї–∞, –љ–∞—З–Є–љ–∞—П –Њ—В –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–Љ—Г —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–µ–љ–Є—О –Є –Ј–∞–Ї–∞–љ—З–Є–≤–∞—П –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–µ–є –Њ–±—А–∞–Ј–∞ –ґ–Є–Ј–љ–Є (—В–∞–±–ї. 3).
![–Ґ–∞–±–ї–Є—Ж–∞ 3. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–≤ %) –њ–Њ –і–∞–љ–љ—Л–Љ –Ъ–Ю–Я-25 (Me [LQ; HQ]) –Ґ–∞–±–ї–Є—Ж–∞ 3. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –њ—А–Є–≤–µ—А–ґ–µ–љ–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–≤ %) –њ–Њ –і–∞–љ–љ—Л–Љ –Ъ–Ю–Я-25 (Me [LQ; HQ])](/upload/medialibrary/75b/62-3.png)
–Ч–∞–Ї–ї—О—З–µ–љ–Є–µ
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –§–µ–±—Г–Ї—Б–Њ—Б—В–∞—В-–°–Ч —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є —А–Є—Б–Ї–∞–Љ–Є, —Б–Њ–≥–ї–∞—Б–љ–Њ –Њ–±–љ–Њ–≤–ї–µ–љ–љ—Л–Љ –Ї—А–Є—В–µ—А–Є—П–Љ EULAR (2022 –≥.), –њ—А–Є –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ —Г—А–∞—В—Б–љ–Є–ґ–∞—О—Й–µ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ–Є —А–Є—Б–Ї–∞–Љ–Є. –≠—В–Њ—В –∞—Б–њ–µ–Ї—В –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–Љ –љ–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ. –†–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞—П –і–Њ—Б—В—Г–њ–љ–∞—П —Г—А–∞—В—Б–љ–Є–ґ–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –§–µ–±—Г–Ї—Б–Њ—Б—В–∞—В-–°–Ч –њ–Њ–Ј–≤–Њ–ї—П–µ—В –і–Њ—Б—В–Є–≥–∞—В—М —Ж–µ–ї–µ–є –ї–µ—З–µ–љ–Є—П –≤ –±–Њ–ї—М—И–Њ–Љ –њ—А–Њ—Ж–µ–љ—В–µ —Б–ї—Г—З–∞–µ–≤ –±–µ–Ј —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —А–Є—Б–Ї–Њ–≤.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ—А–Є –њ–Њ–і–і–µ—А–ґ–Ї–µ –Э–Р–Ю ¬Ђ–°–µ–≤–µ—А–љ–∞—П –Ј–≤–µ–Ј–і–∞¬ї.












