Для цитирования. Бирюкова Е.В., Соловьева И.В. Терапия остеоартроза при сопутствующих метаболических нарушениях // РМЖ. 2015. No 25. С. 1504–1506.
Учитывая высокую распространенность сахарного диабета (СД), не удивляет, что с данной проблемой приходится сталкиваться не только эндокринологам, но и специалистам разного профиля. По экспертной оценке Международной федерации диабета, в 2014 г. число больных СД во всем мире достигло 387 млн, причем 90% случаев приходится на долю СД 2-го типа [7]. При CД вследствие развивающихся метаболических расстройств происходят изменения практически во всех тканях организма. Так, поражение сетчатки, нервной системы, сосудов нижних конечностей, почек, сердца достаточно хорошо изучены, однако состоянию опорно-двигательного аппарата у пациентов с СД уделено не так много внимания.В эпидемиологических исследованиях показано частое сочетание остеоартроза (ОА) с ожирением, метаболическим синдромом и СД 2-го типа [2, 10, 23]. В первую очередь это относится к ОА коленных суставов, при котором выявлена четкая зависимость между величиной индекса массы тела (ИМТ) и риском этой патологии [2, 11, 13]. При ОА, как правило, быстрее поражаются так называемые нагрузочные суставы, особенно суставы нижних конечностей (коленный и тазобедренный), что значительно ухудшает качество жизни больных, сопровождается гиподинамией и может приводить к развитию инвалидности. В исследовании F.M. Cicuttini et al. показано, что прибавка массы тела всего на 1 кг увеличивает риск ОА коленного сустава и карпометокарпальных суставов на 9–11%. Кроме того, симптоматический или бессимптомный ОА нижних конечностей был обнаружен у тех, кто был лишь на 3–5 кг тяжелее своего близнеца-брата или сестры [10]. У лиц с ИМТ>30 кг/м2 риск развития ОА коленных суставов в 4 раза выше, чем при ИМТ 25 кг/м2 [20]. Исследование Hart et al. [16], включившее 1000 женщин, выявило, что относительный риск развития одностороннего и двустороннего ОА коленных суставов, по данным рентгенологического исследования, составил 6,2 для ИМТ<23,4 кг/м2 и для ИМТ>26,4 кг/м2. Ожирение оказывает влияние и на прогноз ОА [18]. Описаны 27% и 69% случаев артропластики соответственно бедра и колена у женщин среднего возраста с ожирением в Великобритании [2]. Повышенная масса тела способствует прогрессии рентгенологических проявлений ОА коленных суставов, при этом влияние высокого ИМТ на заболеваемость ОА выше, чем на прогрессирование ОА [10, 11]. Итак, ожирение является одной из важных причин развития ОА и его прогрессирования.
Сложность патогенеза ОА связана с особым строением хрящевой ткани. Ее основная функция сводится к адаптации сустава к механической нагрузке (сжатие при нагрузке и восстановление при ее снятии) и обеспечению движения в суставе без трения суставных поверхностей [2, 11]. При этом компоненты внутрисуставной жидкости обеспечивают механические характеристики суставов. Напомним, что суставной хрящ на 98% состоит из соединительнотканного матрикса, основными компонентами которого являются коллагеновые волокна, в основном II типа. Все остальное пространство заполнено гиалуроновой кислотой и сульфатированными протеогликанами. При недостатке глюкозамина ухудшается качество синовиальной жидкости, может появляться хруст в суставах. Ключевая роль в поддержании равновесия между анаболическими и катаболическими процессами отводится клеточным элементам хряща – хондроцитам [8].
Существует несколько точек зрения в отношении механизмов, при помощи которых ожирение способствует развитию ОА [20]. Несомненно, что при лишнем весе происходит повышенная механическая нагрузка на различные суставы. Интересно, что на поверхности хондроцитов обнаружены механорецепторы, чувствительные к давлению и связанные с внеклеточным матриксом сигнальным каскадом. Вероятно, что ожирение может индуцировать повреждение хряща через активацию этих рецепторов [22].
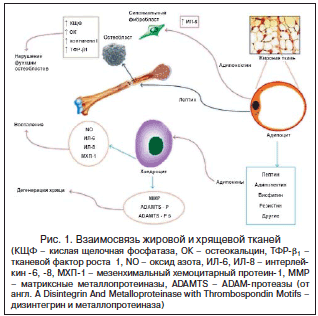
Вместе с тем существуют и другие механизмы, связанные с ожирением, способные изменить метаболизм хрящевой, костной ткани и привести к развитию ОА (рис. 1). В научной литературе представлены многочисленные данные о взаимосвязи ОА с метаболическими нарушениями, связанными с инсулинорезистентностью (ИР) [2, 14, 19]. Жировая ткань является эндокринным органом и секретирует большое количество цитокинов, хемокинов и пептидов, осуществляющих важные физиологические функции в организме. Имея паракринный, аутокринный и эндокринный механизмы действия, адипоцитокины влияют на метаболизм углеводов, жиров, процессы воспаления, свертывания, иммунитета, ангиогенеза, жизнедеятельности костной, хрящевой ткани и многое другое [20, 28].
Нарушение регуляции синтеза и секреции сигнальных веществ жировой тканью может служить связующим звеном, посредством которого ожирение и ИР становятся факторами риска заболеваний опорно-двигательного аппарата, поскольку активизируют дегенеративно-воспалительные процессы в суставных структурах. Известно, что накопление жира в организме не всегда является равномерным. Причем риск развития сопутствующих ожирению патологических состояний в значительной степени определяется особенностями отложения жировой ткани в организме [29]. Более опасно абдоминальное отложение жира, о котором свидетельствует увеличение окружности талии (у мужчин – более 94 см, у женщин – более 80 см). Особенность абдоминального жира заключается в том, что в нем очень активно протекают метаболические процессы. Адипоциты висцерального (в отличие от подкожного) жира имеют высокую плотность и чувствительность β-адренорецепторов (особенно β3-типа), рецепторов кортизола и андрогенов, но при этом низкую плотность и чувствительность инсулиновых рецепторов и α-адренорецепторов. Незначительное влияние инсулина в абдоминальной жировой ткани способствует повышенной продукции свободных жирных кислот. ИР представляет собой снижение биологических эффектов инсулина в различных органах и тканях. При этом возникает необходимость в увеличении количества инсулина для компенсации состояния ИР. Развивающаяся компенсаторная гиперинсулинемия (ГИ) усиливает поглощение глюкозы периферическими тканями, а также уменьшает гепатическую продукцию глюкозы печенью, что определенное время поддерживает нормальное содержание глюкозы крови. ГИ, с одной стороны, необходима для преодоления ИР, а с другой – является патологическим процессом, способствующим возникновению и развитию метаболических, гемодинамических и системных нарушений. Нарушение метаболизма инсулина при ожирении также способствует ухудшению анаболических процессов в хондроцитах, учитывая их чувствительность к инсулину [21].
В настоящее время ожирение рассматривается как состояние хронического системного воспаления, что связано с увеличением синтеза провоспалительных цитокинов как адипоцитами, так и макрофагами жировой ткани (например, ИЛ-1b, ИЛ-6, С-реактивного протеина, ФНО-a). При этом количество макрофагов, мигрирующих в жировую ткань (особенно в висцеральную), тем больше, чем выраженнее состояние ИР [27]. Это вносит весомый вклад в развитие ОА, патофизиологические механизмы развития которого включают и еще одно существенное нарушение – сопутствующее хроническое воспаление, ведущее к разрушению гиалинового хряща (основной компонент сустава) [11, 31].
Воспаление усиливает разрушение хряща. Провоспалительные цитокины способствуют высвобождению хондроцитами ферментов, прежде всего матриксных металлопротеиназ, активаторов плазминогена, повреждающих коллаген и протеогликаны хрящевой ткани [26]. Повреждение хондроцита связано с активацией специфических рецепторов на мембране (рецепторы к ИЛ-1, лептину, фибронектину f), запускающих активацию синтеза провоспалительных и деструктивных медиаторов, опосредованную белками ядерного фактора транскрипции-kB (NF-kB). К тому же значение имеет увеличение продукции цитокинов, которые стимулируют синтез протеаз, активатора плазминогена, простагландина Е и способствуют, с одной стороны, пролиферации синовиальных клеток, с другой – подавляют хондроцитами синтез коллагена и протеогликанов [8, 15, 20]. ОА сопровождается гиперпродукцией хондроцитами циклооксигеназы-2, фермента, индуцирующего синтез простагландинов, принимающих участие в развитии воспаления и индуцибельной формы оксида азота, оказывающего токсическое действие на хрящ и индуцирующего апоптоз хондроцитов [16, 20, 31]. Обмен в хрящевой ткани изменяется в сторону преобладания катаболических процессов при несостоятельности анаболических. Характерным признаком деструкции хряща является потеря матриксом гликозаминогликанов (гиалуроновая кислота, хондроитинсульфат), как следствие, сопротивление хрящевого матрикса воздействию физической нагрузки уменьшается, и поверхность хряща становится чувствительной к повреждению. Следует учитывать, что последствия ОА – боль и нарушение функции сустава вынуждают больного сократить или ограничить физическую активность, что в свою очередь увеличивает прибавку массы тела, ухудшает чувствительность тканей к инсулину и затрудняет терапию СД 2-го типа и ожирения [5].
Для проведения патогенетической терапии ОА существует несколько групп препаратов. Одной из них является группа SYSADOA (Symptomatic Slow Acting Drugs for Osteoarthritis) – симптоматические препараты замедленного действия, принадлежащие к разным по химической структуре соединениям и представляющие собой биологически активные (хондромодулирующие, хондропротективные) субстанции, состоящие из компонентов хрящевой ткани, необходимых для построения и обновления суставного хряща [4, 5, 17]. Эффект этого класса препаратов проявляется более медленно по сравнению с симптоматическими средствами, но при этом длится после окончания их применения. Эти средства обладают противовоспалительным и обезболивающим действием, что позволяет уменьшить дозировки применяемых НПВП, и, соответственно, снизить риск нежелательных эффектов этого класса лекарственных средств.
В настоящее время накоплена достаточная доказательная база, свидетельствующая об эффективности SYSADOA в качестве моно- и комбинированной терапии и необходимости их применения для долгосрочного лечения и профилактики развития ОА [4, 6, 12]. Особенностями применения препаратов этой группы являются постепенное наступление эффекта – спустя 2–8 нед. от начала терапии и его сохранение в течение 2 мес. и более после окончания лечения [3, 4].
Одним из современных и наиболее изученных хондропротекторов можно считать препараты на основе хондроитин сульфата натрия (ХСН) и глюкозамина (ГА). Эффективность применения ХСН и ГА при ОА определяется их способностью активно влиять на метаболизм костной и хрящевой ткани, стимулировать синтез соединительной ткани, как следствие, способствовать регенерации и предотвращению процессов разрушения хряща [12].
Оба лекарственных средства показаны к применению при ОА, а эффективность значительно увеличивается при их совместном применении [3, 4]. Оба препарата оказывают анаболическое действие на структуру хряща, стимулируя синтез протеогликанов. Напомним, что ГА усиливает выработку хрящевого матрикса и обеспечивает неспецифическую защиту хряща от химического повреждения, снижает провоспалительное, деструктивное действие цитокинов, препятствует образованию супероксидных радикалов. ГА используется хондроцитами для синтеза протеогликанов, глюкозаминогликанов и гиалуроновой кислоты. ХСН стимулирует образование гиалуроновой кислоты, а также синтез протеогликанов и коллагена типа II. Подавляя активность гиалуронидазы, ХСН защищает гиалуроновую кислоту от ферментативного расщепления; стимулирует механизмы репарации хряща и угнетает активность ферментов, которые расщепляют хрящевую ткань. Кроме того, сохраняя воду в толще хряща, ХСН повышает прочность соединительной ткани [17].
Отличительными особенностями ХСН и ГА являются собственный умеренный обезболивающий эффект и противовоспалительное действие. Поэтому при лечении ОА сочетание ХСН и ГА не только облегчает клинические симптомы заболевания, но и уменьшает потребность в HПВС [3, 12]. Лечение ХСН и ГА хорошо переносится пациентами.
Необходимость длительной, по существу, пожизненной, терапии ОА обосновывает особые требования к безопасности лекарственных средств. Учитывая клинический профиль пациента с ОА, который, как правило, включает избыточную массу тела / ожирение – ведущий фактор риска развития СД 2-го типа (не говоря о пациентах с СД 2-го типа), крайне важно быть уверенным в метаболической безопасности терапии ОА в отношении как показателей углеводного обмена, так и чувствительности к инсулину. Очень важно, чтобы медикаментозные вмешательства не способствовали прогрессированию метаболических расстройств у пациентов с ожирением и ухудшению гликемического контроля при СД 2-го типа.
Некоторое время назад появилась информация о повышении уровня глюкозы натощак и ухудшении чувствительности тканей к инсулину на фоне терапии ХСН и ГА. Эти экспериментальные исследования были выполнены на животных моделях, и, хотя применялись большие дозы указанных препаратов и чаще парентеральный путь введения, их результаты послужили поводом для дискуссий о возможном диабетогенном риске применения препаратов ХСН и ГА [24].
Вместе с тем в последние годы проведено много рандомизированных клинических исследований (КИ) с ХСН и ГА [6, 25, 26, 30]. Так, в двойном слепом плацебо-контролируемом КИ приняли участие пациенты с ОА и СД 2-го типа (с удовлетворительным контролем гликемии); общая продолжительность исследования составила 90 дней [25]. В ходе КИ не выявлено различий по лабораторным показателям углеводного обмена между группой плацебо и группой ХСН (1200 мг/сут) и ГА (1500 мг/сут). В частности, применение ХСН и ГА никак не отразилось на уровне HbA1c. Изучив состояние углеводного обмена у пациентов с СД 2-го типа, страдающих ОА, авторы пришли к выводу, что применение ХСН и ГА не ухудшает показатели углеводного обмена.
В целом изучению гликемического контроля у пациентов с СД 2-го типа, получающих по поводу ОА ХСН и ГА, были посвящены КИ различной длительности. Наиболее исчерпывающая информация о влиянии применения ХСН (1200 мг/сут) и ГА (1500 мг/сут) на гомеостаз глюкозы представлена в недавно опубликованном R.R. Simon et al. обзоре [ 26]. Авторы провели анализ многочисленных КИ (период наблюдения – от 4 нед. до 3 лет) с применением ХСН и ГА для оценки их влияния на метаболизм глюкозы у лиц с нормальной толерантностью к глюкозе и с различными нарушениями гликемии, включая больных с нарушенной толерантностью к глюкозе (НТГ) и больных СД 2–го типа. В целом не было обнаружено существенного влияния ХС и ГА на уровень HbA1c, концентрацию глюкозы натощак и после глюкозотолерантного теста как у пациентов с нормальной толерантностью к глюкозе, так и у пациентов с НТГ и СД. Кроме того, терапия ХСН и ГА не приводила к существенным изменениям чувствительности периферических тканей к инсулину при изучении метаболизма глюкозы с помощью гипергликемического клэмпа. Более того, долгосрочные КИ показали, что терапия ХСН и ГА не ассоциируется с увеличением частоты новых случаев СД 2-го типа.
На сегодняшний день одним из эффективных направлений лечения ОА является комбинированная фармакотерапия. Наиболее удобны официальные комбинированные препараты для перорального приема. Их преимущество заключается в сочетании 2 активных ингредиентов: ХСН и ГА гидрохлорида в эффективных дозировках (ХСН 1200 мг/сут и ГА 1500 мг/сут), что, несомненно, улучшает приверженность пациента к длительному лечению [3, 4]. Доказан синергизм в действии ХСН и ГА, что проявляется значительным увеличением продукции протеогликанов хондроцитами при совместном применении этих веществ по сравнению с монотерапией каждым из данных препаратов [12]. Комбинация ХСН и ГА в одном лекарственном средстве не только стимулирует регенерацию хрящевой ткани, но и уменьшает потребность в НПВП, что становится важным при лечении ОА у пациентов с коморбидностью.
Патогенетически обоснованным при болевой симптоматике ОА считается назначение комбинации ХСН, ГА и малых доз НПВП [3–5]. Существует другая лекарственная форма: в 1 капсуле содержится ХСН 200 мг, ГА гидрохлорид 250 мг и ибупрофен 100 мг, который оказывает быстрое противовоспалительное и обезболивающее действие и является более безопасным по сравнению с другими НПВС. При назначении хондропротективной терапии в период болевого эпизода предпочтение отдается комбинированному препарату ( ХСН, ГА и ибупрофен). После купирования болевого синдрома рационально перейти на прием пероральных форм ХСН и ГА (1 капс. 2–3 р./сут) курсом 3–6 мес. и более. Такая последовательная схема назначения препаратов улучшает приверженность пациентов лечению.
Лечение ОА представляет собой непростую задачу, а эффективность его в повседневной практике порой далека от желаемой. Сбалансированный состав современных комбинированных форм хондропротекторов, объединяющих ХСН, ГА, хорошая переносимость позволяют достичь оптимального терапевтического результата и избежать неблагоприятных метаболических сдвигов у пациентов с нормальной толерантностью к глюкозе и с различными нарушениями гликемии при длительном применении.












