Остеоартроз (ОА) – хроническое мультифакториальное заболевание суставов, являющееся основной причиной боли и нарушения трудоспособности у населения во многих странах мира. В 25% случаев обращение пациента к врачу первичного звена связано с ОА [1]. По частоте поражения гонартроз занимает одну из лидирующих позиций. Высокая распространенность данной патологии определяет ее социальную значимость и необходимость совершенствования подходов к лечению. Современный арсенал лекарственных средств c различной эффективностью, стремление повысить приверженность больного к лечению ставят перед врачом нелегкую клиническую задачу по выбору оптимального способа терапии.
В развитии ОА ключевую роль играют нарушения метаболизма хряща, воспаление и изменения субхондральной кости. Воспалительный процесс затрагивает практически все структуры сустава с формированием хондрита, синовита и остеита. Хронический воспалительный процесс в синовиальной оболочке способствует изменению метаболизма хондроцитов и нарушению баланса между анаболическими и катаболическими процессами с преобладанием последних. В основе нарушения метаболизма хряща лежат количественные и качественные изменения протеогликанов – белково-полисахаридных комплексов, обеспечивающих стабильность структуры коллагеновой сети, которая является основой хрящевого матрикса. В настоящее время активно дискутируются и вопросы первичности изменений субхондральной кости и ее роли в патогенезе ОА.
Ранняя стадия ОА характеризуется набуханием и разволокнением коллагенового каркаса. Далее в хряще нарастают процессы деградации с разрушением протеогликанов протеазами, что приводит к истончению и размягчению хряща в местах максимальной нагрузки. На поздних стадиях происходит фрагментация хряща. Растрескивание хряща приводит к его изъязвлению с обнажением подлежащей субхондральной кости и отделением фрагментов, которые поступают в полость сустава в виде детрита. При истонченном хрящевом покрове распределение давления между суставными поверхностями становится неравномерным. Это ведет к локальным перегрузкам, появлению участков остеосклероза, субхондральных кист и возникновению остеофитов.
Традиционно терапия ОА применяется с целью механической разгрузки пораженных суставов, купирования воспаления и предотвращения прогрессирования заболевания. Комплексное лечение ОА на современном этапе требует комбинированного использования нефармакологических, фармакологических и, при необходимости, хирургических методов. Фармакотерапия включает применение симптом-модифицирующих препаратов быстрого действия (парацетамола, нестероидных противовоспалительных препаратов (НПВП)) и симптом-модифицирующих препаратов замедленного действия. Для лечения ОА активно используют локальные (топические) средства, содержащие НПВП, капсаицин. Аппликационная терапия подразумевает применение лекарственных веществ с созданием в месте нанесения терапевтической концентрации препарата в тканях, обусловливающей противовоспалительный и обезболивающий эффекты. При развитии реактивного синовита используется внутрисуставное введение глюкокортикоидов. Симптом-модифицирующие препараты замедленного действия (хондроитин, глюкозамин (ГА), экстракты сои и авокадо, диацереин, гиалуроновая кислота) оказывают влияние на боль, воспаление, улучшая метаболизм хрящевой ткани.
За последние 10 лет во всем мире проведено около 100 исследований, результаты которых подтверждают эффективность и безопасность применения глюкозамина сульфата (ГС) в лечении ОА. ГА является моноаминосахаридом, в организме он синтезируется из глюкозы посредством гексозаминного биосинтетического пути. Фармацевтическая промышленность выпускает ГА в виде ГС и глюкозамина гидрохлорида (ГГ). Прием препаратов восполняет эндогенный дефицит ГА, стимулирует синтез протеогликанов и гиалуроновой кислоты. После перорального приема ГС подвергается диссоциации в желудке с последующим поступлением свободного ГА в кишечник. Биодоступность ГС при приеме внутрь составляет 26%. В экспериментах на крысах было показано, что эффект «первого прохождения» не наблюдался только при интраперитонеальном введении. ГА, по-видимому, начинает разрушаться уже в тонком кишечнике. Системно доступный ГС распределяется в органах и тканях, в наибольших концентрациях обнаруживается в печени, почках и суставном хряще [2, 3].
Особый интерес в последнее время приобретает аппликационная терапия ОА с использованием ГА. В ряде работ подчеркиваются преимущества трансдермального способа введения лекарственного средства над пероральным, позволяющего избежать эффекта «первого прохождения» ГА в ЖКТ, снизить вероятность колебаний пиковых концентраций лекарственного вещества в сыворотке крови, повысить комплаентность пациента [4]. Для повышения биодоступности лекарственных средств при трансдермальном пути введения используются вещества-проводники и нанотехнологии [5]. Высокая клиническая эффективность и безопасность крема, содержащего ГС, в лечении ОА продемонстрированы в работе N.G. Guat Hua et al. Авторы пришли к выводу, что трансдермальная форма ГС при 4-недельном приеме способствует уменьшению боли и улучшению функции суставов [5].
С учетом необходимости применения длительной терапии ОА, потребности в максимальном продлении функциональной активности пациента и контроля болевого синдрома на фоне тяжелой коморбидности подавляющего числа больных повышение безопасности проводимого лечения является актуальным.
На базе городской клинической больницы № 1 им. Н.И. Пирогова (кафедра факультетской терапии им. акад. А.И. Нестерова) (г. Москва), городской клинической больницы № 15 им. О.М. Филатова (г. Москва), городской клинической больницы № 5 г. Нижнего Новгорода проведено открытое сравнительное рандомизированное клиническое исследование по оценке эффективности, безопасности и переносимости препарата Хондроксид® Максимум – крема для наружного применения 8% (производитель – «Лихт Фар Ист (С) Пте Лтд», Сингапур) и диклофенака – геля для наружного применения у пациентов с ОА коленного сустава.
Материалы и методы
В клиническое исследование были включены 80 пациентов (68 женщин и 12 мужчин) от 40 до 80 лет с ОА коленного сустава I–III стадий по Келлгрену и интенсивностью болевого синдрома при ходьбе по визуально-аналоговой шкале (ВАШ) ≥40 мм на протяжении последних 2 нед., подписавшие информированное согласие и прошедшие рандомизацию. ОА диагностировался в соответствии с критериями ACR 1991 г. Пациенты, получавшие локальную или системную терапию с использованием препаратов, содержащих симптом-модифицирующие средства замедленного действия в течение предыдущих 2 мес., а также НПВП перорально, парентерально или локально в течение предыдущих 2 нед. до скрининга, не включались в исследование. На протяжении настоящего исследования пациенты не принимали системные симптом-модифицирующие препараты короткого и замедленного действия.
Клиническое исследование было проведено в соответствии с Хельсинкской декларацией Всемирной медицинской ассоциации, правилами надлежащей клинической практики. Проведение клинического исследования было одобрено Советом по этике при Минздраве РФ.
Продолжительность терапии исследуемыми препаратами составляла 4 нед. Период наблюдения после завершения лечения составлял 4 нед. Исследование проводилось с учетом составленного графика визитов (визит 0 – период скринингового обследования (0–5 дней), визит 1 – рандомизация, начало терапии (1-й день), визит 2 – 7-й день; визит 3 – 28-й день; визит 4 – 56-й день.
После скринингового периода пациенты были рандомизированы в соотношении 1:1 в 2 лечебные группы: пациентам 1-й группы был назначен препарат Хондроксид® Максимум крем для наружного применения 8% (нанесение препарата на область пораженного сустава полоской в 2–3 см 3 р./сут); пациентам 2-й группы – диклофенак гель для наружного применения (нанесение препарата на область пораженного сустава полоской в 2–3 см 3 р./сут). В качестве анальгетика пациенты обеих групп могли использовать парацетамол (таблетки 500 мг, покрытые пленочной оболочкой) – 1–2 таблетки до 4 р./сут. Пациентам был выдан дневник для фиксации времени нанесения и дозирования исследуемых препаратов.
Оценка эффективности терапии проводилась по динамике изучаемых показателей в целевом коленном суставе. Первичной конечной точкой исследования явилось изменение индекса WOMAC (боль, скованность, двигательная функция) за период лечения по сравнению с исходным моментом, вторичной – через 4 нед. после окончания терапии по сравнению с моментом окончания терапии. Кроме того, оценивались интенсивность боли при пальпации (ВАШ, мм), окружность сустава (см). Общая оценка врачом ответа на лечение проводилась на основании следующих критериев: «хороший эффект» – уменьшение значения WOMAC (по шкале боли) на 20% и более; «удовлетворительный эффект» – уменьшение значения WOMAC (по шкале боли) менее 20%; «неудовлетворительный эффект» – отсутствие уменьшения значения WOMAC (по шкале боли). Эффективность терапии по мнению пациента определялась на основании субъективных ощущений: «хороший эффект», «удовлетворительный», «неудовлетворительный». Оценивалась также потребность в пероральном приеме парацетамола.
Профиль безопасности исследуемых препаратов изучался на основании переносимости и регистрации нежелательных явлений (НЯ). При возникновении НЯ оценивались его выраженность (легкая, средняя, выраженная), связь с приемом препарата: «нет», «маловероятна», «возможна», «вероятна», «определена», «неизвестна». Лабораторный мониторинг безопасности терапии включал: общий анализ крови (гемоглобин, эритроциты, лейкоциты, лейкоцитарная формула, тромбоциты, СОЭ); биохимический анализ крови (общий белок, мочевина, креатинин, аланинаминотрансфераза, аспартатаминотрансфераза, общий билирубин, глюкоза); общий анализ мочи (относительная плотность, рН, белок, глюкоза, эритроциты, лейкоциты). Кроме того, пациентам проводилась регистрация электрокардиограммы до и после лечения.
Статистическая обработка данных выполнялась c использованием программы Statistica 6.0. Качественные показатели, представленные в форме встречаемости и процентов, сравнивались с использованием критерия хи-квадрата / точного критерия Фишера. Все данные, собранные по числовой или одинарной шкале, суммировались с определением среднего значения, среднеквадратичного отклонения, медианы и диапазона. Разности средних значений непрерывных величин между группами исследовались с применением критерия независимых выборок Стьюдента.
Результаты и обсуждение
Все пациенты завершили исследование в соответствии с протоколом. Группы статистически не различались по возрасту, росту и весу, систолическому и диастолическому АД, клинической оценке суставного синдрома (WOMAC, боль в суставе при пальпации, окружность сустава). В обеих группах преобладали пациенты со II рентгенологической стадией гонартроза. Сопутствующие заболевания имелись у 65 (81%) пациентов, 37 (46%) больных имели более одного заболевания. Наиболее часто встречающимися сопутствующими заболеваниями были ишемическая болезнь сердца (29% в основной группе и 33% – в контрольной, p=0,695) и артериальная гипертензия (66% в основной группе и 41% – в контрольной, p=0,026).
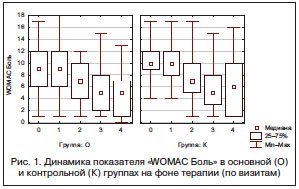
Согласно полученным результатам, в обеих группах больных наблюдалась статистически значимая положительная динамика по показателю «WOMAC Боль» со 2-го визита исследования, сохраняющаяся до окончания лечения (табл. 1, рис. 1).
По критерию «уменьшение более чем на 20% по «WOMAC Боль» на 2-м и 3-м визитах статистически значимых различий между группами выявлено не было. Достижение первичной конечной точки отмечалось у 34 (85%) и 30 (75%) больных основной и контрольной групп соответственно. На последнем (4-м) визите число больных, достигших уменьшения боли по WOMAC более чем на 20%, составило 31 (80%) и 25 (63%) соответственно (табл. 2).
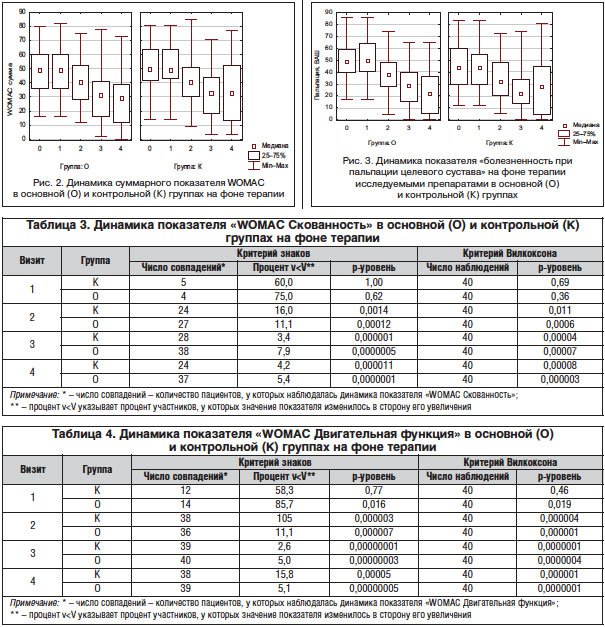
Значения показателей скованности и двигательной функции по WOMAC претерпевали статистически значимую положительную динамику, начиная со 2-го визита в обеих группах больных (табл. 3, 4).
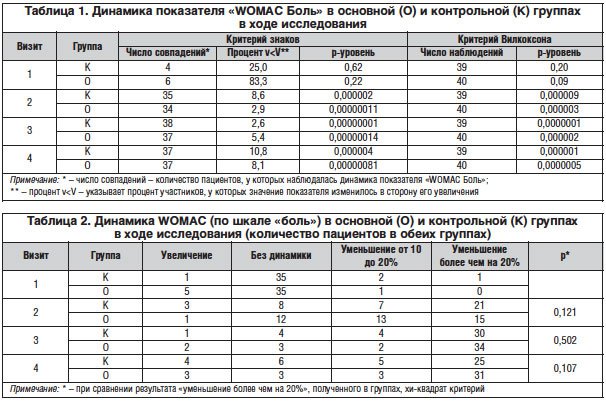
При оценке суммарного показателя шкалы WOMAC основная и контрольная группы статистически не отличались друг от друга (рис. 2).
В ходе терапии в обеих группах были достигнуты статистически значимые изменения суммарного показателя WOMAC (табл. 5).
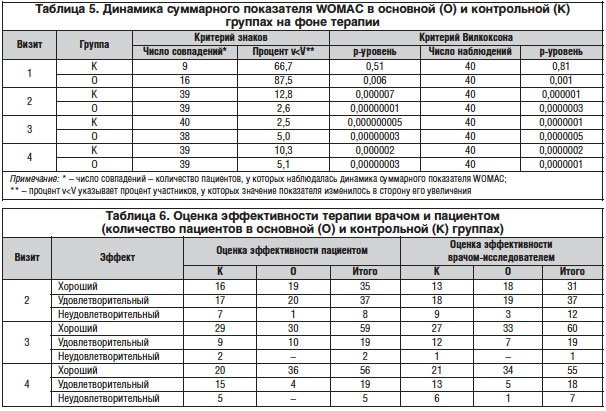
При оценке эффективности терапии число «хороших эффектов» на 2-м и 3-м визитах сопоставимо в обеих группах лечения; на 4-м визите отмечалось их статистически значимое преобладание в основной группе как по мнению пациента (р=0,0002), так и по мнению врача-исследователя (р=0,0017) (табл. 6).
Выраженность болезненности при пальпации целевого сустава, оцениваемая по ВАШ (мм), уменьшалась у всех больных ко 2-му визиту. Положительная динамика сохранялась в обеих группах до 4-го визита (рис. 3).
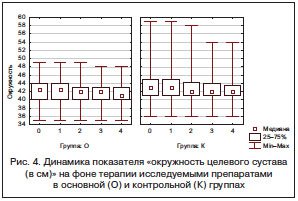
Окружность целевого сустава в обеих группах уменьшилась к 3-му и 4-му визитам. Положительная динамика данного показателя сохранялась и в течение 4 нед. после отмены исследуемых препаратов в основной и контрольной группах (рис. 4).
У всех больных оценивали потребность в пероральном приеме парацетамола. Статистически значимых различий между группами в ходе лечения не выявлено. Назначение препаратов Хондроксид® Максимум крем и диклофенак гель позволило отказаться от перорального приема парацетамола к концу терапии в 40 и 45% случаев соответственно.
В ходе исследования зарегистрированы 11 (13,7%) НЯ легкой степени выраженности, среди которых 2 (по одному в каждой группе) были связаны с приемом препарата, не требовали сопутствующего лечения и завершились выздоровлением/разрешением. Статистически значимых отклонений в лабораторных показателях, данных электрокардиографии между группами получено не было.
Принимая во внимание полученные в ходе клинического исследования данные по оценке эффективности и безопасности исследуемого препарата Хондроксид® Максимум, можно сделать вывод о его сходном с препаратом сравнения профиле эффективности и безопасности. Достижение уменьшения боли по шкале WOMAC более чем на 20% отмечено у подавляющего числа больных в основной и контрольной группах (85 и 75% соответственно). Число «хороших результатов» через 4 нед. после окончания использования препаратов было статистически значимо выше в основной группе как по мнению пациента (р=0,0002), так и по мнению врача-исследователя (р=0,0017). Таким образом, Хондроксид® Максимум со статистически значимыми различиями превосходит препарат сравнения по длительности последействия. В ходе исследования серьезных и непредвиденных НЯ не зарегистрировано. У всех пациентов показатели жизненно важных функций не имели клинически значимых отклонений на всем протяжении исследования.
Заключение
ОА, являясь наиболее распространенным заболеванием суставов, представляет собой актуальную медицинскую проблему не только из-за высокой распространенности, но и в связи с трудностью выбора оптимального подхода к лечению. Неотъемлемым компонентом терапии ОА является назначение симптоматических препаратов замедленного действия. Проведенное исследование позволяет положительно оценить применение крема для наружного применения, содержащего ГС 8% (Хондроксид® Максимум), у больных ОА коленного сустава, обладающего высокой клинической эффективностью и безопасностью. Крем Хондроксид® Максимум имеет отчетливый симптом-модифицирующий эффект и способствует уменьшению степени функциональной недостаточности суставов, обладает выраженным последействием, что делает актуальным его использование в лечении гонартроза.












