–Т–≤–µ–і–µ–љ–Є–µ
–Т–Њ–Ј—А–∞—Б—В–љ–∞—П –Љ–∞–Ї—Г–ї—П—А–љ–∞—П –і–µ–≥–µ–љ–µ—А–∞—Ж–Є—П (–Т–Ь–Ф) вАФ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–µ –Љ—Г–ї—М—В–Є—Д–∞–Ї—В–Њ—А–Є–∞–ї—М–љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й–µ–µ—Б—П –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –Ј–Њ–љ—Л –≥–ї–∞–Ј–љ–Њ–≥–Њ –і–љ–∞ (–Љ–∞–Ї—Г–ї—Л), –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ —Б—В—А–∞–і–∞—О—В —Б–µ—В—З–∞—В–Ї–∞, –њ–Є–≥–Љ–µ–љ—В–љ—Л–є —Н–њ–Є—В–µ–ї–Є–є –Є —Е–Њ—А–Є–Њ–Ї–∞–њ–Є–ї–ї—П—А—Л, —П–≤–ї—П—О—Й–µ–µ—Б—П –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –њ–Њ—В–µ—А–Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –Ј—А–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ 50 –ї–µ—В. –Т–Ь–Ф —П–≤–ї—П–µ—В—Б—П –≤—В–Њ—А—Л–Љ –њ–Њ –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ –≤ –Љ–Є—А–µ, –њ—А–Є–≤–Њ–і—П—Й–Є–Љ –Ї –љ–∞—А—Г—И–µ–љ–Є—О –Ј—А–µ–љ–Є—П –Є —Б–ї–µ–њ–Њ—В–µ [1вАУ4]. –І–∞—Б—В–Њ—В–∞ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є —А–∞–љ–љ–Є—Е —Д–Њ—А–Љ –Т–Ь–Ф —Г –ї–Є—Ж –≤ –≤–Њ–Ј—А–∞—Б—В–µ 65вАУ74 –≥–Њ–і–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 15%, —Б—В–∞—А—И–µ 85 –ї–µ—В вАФ 30%; —З–∞—Б—В–Њ—В–∞ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –њ–Њ–Ј–і–љ–Є—Е —Д–Њ—А–Љ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –Њ—В 1% —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –≤–Њ–Ј—А–∞—Б—В–µ 65вАУ74 –≥–Њ–і–∞ –і–Њ 13% —Г –ї–Є—Ж 85 –ї–µ—В –Є —Б—В–∞—А—И–µ [5].–Я—А–Є—З–Є–љ—Л —А–∞–Ј–≤–Є—В–Є—П –Т–Ь–Ф –Њ—Б—В–∞—О—В—Б—П –љ–µ–≤—Л—П—Б–љ–µ–љ–љ—Л–Љ–Є, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –њ–Њ—Б—В–Њ—П–љ–љ–Њ –≤–µ–і—Г—Й–Є–µ—Б—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ —Н—В–Њ–є –Њ–±–ї–∞—Б—В–Є [7вАУ10]. –Э–∞–Є–±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ —Б—З–Є—В–∞—О—В—Б—П –≤–Њ–Ј—А–∞—Б—В, –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ—Л–є —Б—В—А–µ—Б—Б –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П —Б–≤–µ—В–∞, –≥–Є–њ–µ—А—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є—П, —Г–і–∞–ї–µ–љ–Є–µ –Ї–∞—В–∞—А–∞–Ї—В—Л –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ, –љ–∞—Б–ї–µ–і—Б—В–≤–µ–љ–љ–Њ—Б—В—М, –Ї—Г—А–µ–љ–Є–µ, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј –Є –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –і–Є–µ—В—Л [12, 13].
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є –≤—Л–і–µ–ї—П—О—В ¬Ђ—Б—Г—Е—Г—О¬ї –Є ¬Ђ–≤–ї–∞–ґ–љ—Г—О¬ї —Д–Њ—А–Љ—Л –Т–Ь–Ф. –†–∞–љ–љ—П—П —Д–Њ—А–Љ–∞ (¬Ђ—Б—Г—Е–∞—П¬ї) –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –і—А—Г–Ј–∞–Љ–Є; –≤ —В–Њ–Љ —Б–ї—Г—З–∞–µ, –Ї–Њ–≥–і–∞ –Є–Љ–µ–µ—В—Б—П —А–∞—Б–њ–∞–і –њ–Є–≥–Љ–µ–љ—В–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П, —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –њ–Њ–Ј–і–љ—П—П ¬Ђ—Б—Г—Е–∞—П¬ї —Д–Њ—А–Љ–∞ –Т–Ь–Ф. –Х—Б–ї–Є –њ—А–µ–Њ–±–ї–∞–і–∞—О—В —Н–Ї—Б—Б—Г–і–∞—В–Є–≤–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л, —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –њ–Њ–Ј–і–љ—П—П ¬Ђ–≤–ї–∞–ґ–љ–∞—П¬ї —Д–Њ—А–Љ–∞, –Ї–Њ—В–Њ—А–∞—П —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –±–Њ–ї–µ–µ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–Њ–є.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Љ—Г–ї—М—В–Є—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П AREDS (Age Related Eye Disease Study) –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –њ—А–Є–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є —Д–Њ—А–Љ—Г–ї—Л AREDS –≤ —В–µ—З–µ–љ–Є–µ 10 –ї–µ—В (–≤–Є—В–∞–Љ–Є–љ –° 500 –Љ–≥, –≤–Є—В–∞–Љ–Є–љ –Х 400 –Ь–Х, ќ≤-–Ї–∞—А–Њ—В–Є–љ 15 –Љ–≥, –Њ–Ї—Б–Є–і —Ж–Є–љ–Ї–∞ 80 –Љ–≥, –Њ–Ї—Б–Є–і –Љ–µ–і–Є 2 –Љ–≥) —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–їc—П 25% —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–Ј–і–љ–µ–є —Б—В–∞–і–Є–Є –Т–Ь–Ф [11]. –†–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (AREDS 2) –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ—А–Є –Т–Ь–Ф –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Њ–Љ–µ–≥–∞-3 –њ–Њ–ї–Є–љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л—Е –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В. –Я—А–Є–µ–Љ –ї—О—В–µ–Є–љ–∞/–Ј–µ–∞–Ї—Б–∞–љ—В–Є–љ–∞ –њ—А–Є–≤–Њ–і–Є–ї –Ї —Б–љ–Є–ґ–µ–љ–Є—О —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–Ј–і–љ–Є—Е —Б—В–∞–і–Є–є –Т–Ь–Ф –љ–∞ 10%, –љ–µ–Њ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є вАФ –љ–∞ 11%, –≤–µ—А–Њ—П—В–љ–Њ—Б—В–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Т–Ь–Ф вАФ –љ–∞ 20%. –Ч–∞–Љ–µ–љ–∞ ќ≤-–Ї–∞—А–Њ—В–Є–љ–∞ –≤ —Д–Њ—А–Љ—Г–ї–µ AREDS –љ–∞ –ї—О—В–µ–Є–љ + –Ј–µ–∞–Ї—Б–∞–љ—В–Є–љ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–∞–ї–∞ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–Ј–і–љ–Є—Е —Б—В–∞–і–Є–є –Т–Ь–Ф —Б 34 –і–Њ 30% [16]. –Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —Д–Њ—А–Љ—Г–ї–∞ AREDS 2 —Б –ї—О—В–µ–Є–љ–Њ–Љ –Є –Ј–µ–∞–Ї—Б–∞–љ—В–Є–љ–Њ–Љ –±—Л–ї–∞ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–∞ –Ї —И–Є—А–Њ–Ї–Њ–Љ—Г –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ—Г –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –њ—А–Є –њ—А–Њ–Љ–µ–ґ—Г—В–Њ—З–љ–Њ–є —Б—В–∞–і–Є–Є –Т–Ь–Ф –Є–ї–Є –ї—О–±–Њ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –љ–∞ –ї—Г—З—И–µ–Љ –≥–ї–∞–Ј—Г –њ—А–Є –љ–∞–ї–Є—З–Є–Є –і–∞–ї–µ–Ї–Њ –Ј–∞—И–µ–і—И–µ–є –Т–Ь–Ф –љ–∞ –њ–∞—А–љ–Њ–Љ –≥–ї–∞–Ј—Г. –£—Б–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞–љ–љ–∞—П —Д–Њ—А–Љ—Г–ї–∞ AREDS 2 –≤–Ї–ї—О—З–∞–ї–∞ –≤ —Б–µ–±—П –≤–Є—В–∞–Љ–Є–љ –° 500 –Љ–≥, –≤–Є—В–∞–Љ–Є–љ –Х 400 –Ь–Х (268 –Љ–≥), –ї—О—В–µ–Є–љ 10 –Љ–≥, –Ј–µ–∞–Ї—Б–∞–љ—В–Є–љ 2 –Љ–≥, –Њ–Ї—Б–Є–і —Ж–Є–љ–Ї–∞ 25 –Љ–≥, –Њ–Ї—Б–Є–і –Љ–µ–і–Є 2 –Љ–≥.
–Т —А—П–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –і–Њ–Ї–∞–Ј–∞–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б–µ–ї–µ–љ–∞ –і–ї—П —Г–ї—Г—З—И–µ–љ–Є—П —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤ —Б–µ—В—З–∞—В–Ї–Є, –њ–Њ–Ї–∞–Ј–∞–љ–∞ –µ–≥–Њ —А–Њ–ї—М –≤ –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є–Є —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ [14, 15]. –°–µ–ї–µ–љ –њ—А–µ–і–Њ—Е—А–∞–љ—П–µ—В –Њ—В –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є –љ—Г–Ї–ї–µ–Є–љ–Њ–≤—Л–µ –Ї–Є—Б–ї–Њ—В—Л –Є –Њ–±–ї–∞–і–∞–µ—В —Б–Є–љ–µ—А–≥–Є–Ј–Љ–Њ–Љ —Б –≤–Є—В–∞–Љ–Є–љ–∞–Љ–Є –Х –Є –°, –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞—П –њ—А–Њ—Ж–µ—Б—Б—Л –Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П.
–Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —Г—Б–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞–љ–љ–Њ–є —Д–Њ—А–Љ—Г–ї—Л AREDS 2 –±—Л–ї —А–∞–Ј—А–∞–±–Њ—В–∞–љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б –†–µ—В–Є–љ–Њ—А–Љ, –≤–Ї–ї—О—З–∞—О—Й–Є–є –≤–Є—В–∞–Љ–Є–љ –° 500 –Љ–≥, –≤–Є—В–∞–Љ–Є–љ –Х 150 –Љ–≥, –ї—О—В–µ–Є–љ 10 –Љ–≥, –Ј–µ–∞–Ї—Б–∞–љ—В–Є–љ 2 –Љ–≥, —Ж–Є–љ–Ї 25 –Љ–≥, –Љ–µ–і—М 2 –Љ–≥ –Є –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ 0,100 –Љ–≥ —Б–µ–ї–µ–љ–∞.
–†–∞–љ–љ—П—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –љ–∞—З–∞–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ —Б–µ—В—З–∞—В–Ї–µ –і–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ —А–∞–љ—М—И–µ –љ–∞—З–∞—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є c —Д–Њ—А–Љ—Г–ї–Њ–є AREDS 2.
–Ю–њ—В–Є—З–µ—Б–Ї–∞—П –Ї–Њ–≥–µ—А–µ–љ—В–љ–∞—П —В–Њ–Љ–Њ–≥—А–∞—Д–Є—П (–Ю–Ъ–Ґ) –њ–Њ–Ј–≤–Њ–ї—П–µ—В –њ–Њ–ї—Г—З–∞—В—М –≤—Л—Б–Њ–Ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –≤–љ—Г—В—А–µ–љ–љ–µ–є –Љ–Є–Ї—А–Њ—Б—В—А—Г–Ї—В—Г—А—Л —Б–µ—В—З–∞—В–Ї–Є. –Ю–Ъ–Ґ-–∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—П –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –∞–љ–∞–ї–Є–Ј –љ–µ —В–Њ–ї—М–Ї–Њ —Б—В—А—Г–Ї—В—Г—А—Л, –љ–Њ –Є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ —А—Г—Б–ї–∞ —Б–µ—В—З–∞—В–Ї–Є, –і–Є—Б–Ї–∞ –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞, –Њ—Ж–µ–љ–Ї—Г —Б–Њ—Б—В–Њ—П–љ–Є—П —Е–Њ—А–Є–Њ–Є–і–µ–Є –Є –≤—Л—П–≤–ї–µ–љ–Є–µ –Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –љ–∞ —А–∞–љ–љ–µ–є —Б—В–∞–і–Є–Є –±—Л—Б—В—А–Њ, –љ–µ–Є–љ–≤–∞–Ј–Є–≤–љ–Њ –Є –±–µ–Ј –Ї–Њ–љ—В—А–∞—Б—В–Є—А–Њ–≤–∞–љ–Є—П.
–Я—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Ю–Ъ–Ґ-–∞–љ–≥–Є–Њ–≥—А–∞—Д–Є–Є –љ–∞ –∞–њ–њ–∞—А–∞—В–µ Cirrus HD-OCT 5000 AngioPlex (Carl Zeiss Meditec AG, –У–µ—А–Љ–∞–љ–Є—П) –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Њ—Б–љ–Њ–≤–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Њ—Ж–µ–љ–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–µ—В—З–∞—В–Ї–Є: –њ–ї–Њ—В–љ–Њ—Б—В—М —Б–Њ—Б—Г–і–Њ–≤ (–Њ–±—Й–∞—П –і–ї–Є–љ–∞ –Ї—А–Њ–≤–µ–љ–Њ—Б–љ–Њ–≥–Њ —Б–Њ—Б—Г–і–∞ –љ–∞ –µ–і–Є–љ–Є—Ж—Г –њ–ї–Њ—Й–∞–і–Є), –њ–ї–Њ—В–љ–Њ—Б—В—М –њ–µ—А—Д—Г–Ј–Є–Є (–Є–Ј–Љ–µ—А–µ–љ–Є–µ –Њ–±—Й–µ–є –њ–ї–Њ—Й–∞–і–Є, –њ–Њ–Ї—А—Л—В–Њ–є –Ї—А–Њ–≤–µ–љ–Њ—Б–љ—Л–Љ–Є —Б–Њ—Б—Г–і–∞–Љ–Є, –љ–∞ –µ–і–Є–љ–Є—Ж—Г –њ–ї–Њ—Й–∞–і–Є), –њ–µ—А–Є–Љ–µ—В—А –Є –њ–ї–Њ—Й–∞–і—М –∞–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –Ј–Њ–љ—Л. –Я—А–Њ–≥—А–∞–Љ–Љ–љ–Њ–µ –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ –∞–≤—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є —А–∞—Б—Б—З–Є—В—Л–≤–∞–µ—В –Ј–љ–∞—З–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Њ–≤ (–Я–°, –Љ–Љ-1) –Є –њ–ї–Њ—В–љ–Њ—Б—В–Є –њ–µ—А—Д—Г–Ј–Є–Є (–Я–Я, –±–µ–Ј –µ–і. –Є–Ј–Љ–µ—А–µ–љ–Є—П) –і–ї—П —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –Ј–Њ–љ—Л, –Ј–Њ–љ –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ –Є –≤–љ–µ—И–љ–µ–≥–Њ –Ї–Њ–ї—М—Ж–∞, –∞ —В–∞–Ї–ґ–µ –Њ–±—Й–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є (–±–µ–Ј –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П). –°—А–∞–≤–љ–µ–љ–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–є –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е —Б –њ–Њ–Љ–Њ—Й—М—О AngioPlex MetrixвДҐ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞—В—М —В–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–Ј–љ–Є –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П.
–Ь—Г–ї—М—В–Є—Д–Њ–Ї–∞–ї—М–љ–∞—П —Н–ї–µ–Ї—В—А–Њ—А–µ—В–Є–љ–Њ–≥—А–∞—Д–Є—П (–Љ—Д-–≠–†–У) вАФ –Љ–µ—В–Њ–і —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є –ї–Њ–Ї–∞–ї—М–љ—Л—Е –±–Є–Њ—Н–ї–µ–Ї—В—А–Є—З–µ—Б–Ї–Є—Е –Њ—В–≤–µ—В–Њ–≤ —Б –Ї–∞–ґ–і–Њ–≥–Њ –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ —Г—З–∞—Б—В–Ї–∞ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є —Б–µ—В—З–∞—В–Ї–Є. –Ь—Д-–≠–†–У –Њ—В—А–∞–ґ–∞–µ—В —Д—Г–љ–Ї—Ж–Є—О –≤—Б–µ—Е –љ–µ–є—А–Њ–љ–Њ–≤ —Б–µ—В—З–∞—В–Ї–Є –Є —В–Њ–њ–Њ–≥—А–∞—Д–Є—О –±–Є–Њ—Н–ї–µ–Ї—В—А–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–∞–Ї—Г–ї—П—А–љ–Њ–є –Њ–±–ї–∞—Б—В–Є, —В. –Ї. –µ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–∞–±–ї—О–і–∞—О—В—Б—П –њ—А–Є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є –њ—А–Њ—Ж–µ—Б—Б–∞ –Њ—В —Е–Њ—А–Є–Њ–Є–і–µ–Є –і–Њ –≥–∞–љ–≥–ї–Є–Њ–Ј–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –Я–Њ–ї—Г—З–∞–µ–Љ–∞—П –Ї—А–Є–≤–∞—П —Н–ї–µ–Ї—В—А–Њ—А–µ—В–Є–љ–Њ–≥—А–∞—Д–Є–Є –≤ –Ї–∞–ґ–і–Њ–Љ –≥–µ–Ї—Б–∞–≥–Њ–љ–µ —Б–Њ—Б—В–Њ–Є—В –Є–Ј –љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П N1, —Б–ї–µ–і—Г—О—Й–µ–≥–Њ –Ј–∞ –љ–Є–Љ –њ–Њ–Ј–Є—В–Є–≤–љ–Њ–≥–Њ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П –†1 –Є –≤—В–Њ—А–Њ–≥–Њ –љ–µ–≥–∞—В–Є–≤–љ–Њ–≥–Њ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П N2. –Э–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —Б—В—А–Њ–Є—В—Б—П —В—А–µ—Е–Љ–µ—А–љ–Њ–µ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є–µ —Н–ї–µ–Ї—В—А–Њ—А–µ—В–Є–љ–Њ–≥—А–∞–Љ–Љ—Л, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –≤—Л–і–µ–ї—П—О—В –њ—П—В—М —В–Њ–њ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –Ї–Њ–ї–µ—Ж. R1 —В–Њ–њ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–∞ –Њ–±–ї–∞—Б—В–Є —Д–Њ–≤–µ–∞, R2 вАФ –њ–∞—А–∞—Д–Њ–≤–µ–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є –Є R3 вАФ –њ–µ—А–Є—Д–Њ–≤–µ–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є. –Я—А–Є –њ–Њ—П–≤–ї–µ–љ–Є–Є —Н–Ї—Б—В—А–∞—Ж–µ–ї–ї—О–ї—П—А–љ–Њ–≥–Њ –Њ—В–µ–Ї–∞ –Є–ї–Є –Є—И–µ–Љ–Є–Є –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≥–Є–њ–µ—А–Њ—В–≤–µ—В (—А–µ–∞–Ї—Ж–Є—П —Д–Њ—В–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –љ–∞ –≥–Є–±–µ–ї—М –Љ—О–ї–ї–µ—А–Њ–≤—Б–Ї–Є—Е –Ї–ї–µ—В–Њ–Ї).
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –Њ—Ж–µ–љ–Є—В—М —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –†–µ—В–Є–љ–Њ—А–Љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б ¬Ђ—Б—Г—Е–Њ–є¬ї —Д–Њ—А–Љ–Њ–є –Т–Ь–Ф –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –і–∞–љ–љ—Л—Е –Ю–Ъ–Ґ –Є –Љ—Д-–≠–†–У.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Њ 40 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (66 –≥–ї–∞–Ј) –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 45 –і–Њ 65 –ї–µ—В —Б ¬Ђ—Б—Г—Е–Њ–є¬ї —Д–Њ—А–Љ–Њ–є –Т–Ь–Ф (–і—А—Г–Ј—Л), –Є–Ј –љ–Є—Е 26 (65%) вАФ –ґ–µ–љ—Й–Є–љ—Л, 14 (35%) вАФ –Љ—Г–ґ—З–Є–љ—Л. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–µ –≤–Ї–ї—О—З–∞–ї–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є–Љ–µ—О—Й–Є—Е —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–µ—В—З–∞—В–Ї–Є –Є –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–µ—А–≤–∞ (–Љ–Є–Њ–њ–Є—П –≤—Л—Б–Њ–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є, –≥–ї–∞—Г–Ї–Њ–Љ–∞, –і—А—Г–≥–Є–µ —Д–Њ—А–Љ—Л –Т–Ь–Ф –Є –і—А.). –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ–Њ–ї—Г—З–∞–µ–Љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –≤—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –±—Л–ї–Є –Њ–±—К–µ–і–Є–љ–µ–љ—Л –≤ –і–≤–µ –≥—А—Г–њ–њ—Л. –У—А—Г–њ–њ—Г 1 —Б–Њ—Б—В–∞–≤–Є–ї–Є 20 –±–Њ–ї—М–љ—Л—Е (34 –≥–ї–∞–Ј–∞), –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –†–µ—В–Є–љ–Њ—А–Љ –њ–Њ 1 –Ї–∞–њ—Б—Г–ї–µ 3 —А./—Б—Г—В –≤–Њ –≤—А–µ–Љ—П –µ–і—Л –≤ —В–µ—З–µ–љ–Є–µ 16 –љ–µ–і. –Т –≥—А—Г–њ–њ—Г 2 –±—Л–ї–Є –Њ–±—К–µ–і–Є–љ–µ–љ—Л 20 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (32 –≥–ї–∞–Ј–∞), –њ–Њ–ї—Г—З–∞–≤—И–Є–µ —Б—В–∞–љ–і–∞—А—В–љ—Г—О –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О (–Љ–µ–ї—М–і–Њ–љ–Є–є –њ–Њ 0,25 –≥ 3 —А./—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 2-—Е –Љ–µ—Б.) –±–µ–Ј –њ—А–Є–µ–Љ–∞ –Ї–∞—А–Њ—В–Є–љ–Њ–Є–і–Њ–≤, –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –°, –Х, –≤–µ—Й–µ—Б—В–≤ —Б –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О –≤ —В–µ—З–µ–љ–Є–µ 16 –љ–µ–і. –њ—А–Є–µ–Љ–∞ (4 –Љ–µ—Б.).
–Т—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Є —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –≤–Ї–ї—О—З–∞–≤—И–µ–µ —Б—В–∞—В–Є—З–µ—Б–Ї—Г—О –њ–µ—А–Є–Љ–µ—В—А–Є—О (–њ—А–Є –њ–Њ–Љ–Њ—Й–Є Oculus twinfield-2, –У–µ—А–Љ–∞–љ–Є—П). –Ю–Ъ–Ґ —Б–µ—В—З–∞—В–Ї–Є –њ—А–Њ–≤–Њ–і–Є–ї–Є –љ–∞ –∞–њ–њ–∞—А–∞—В–µ Cirrus HD-OCT 5000 AngioPlex (Carl Zeiss Meditec AG, –У–µ—А–Љ–∞–љ–Є—П) —Б –Њ—Ж–µ–љ–Ї–Њ–є —Б–ї–µ–і—Г—О—Й–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є: –њ–µ—А–Є–Љ–µ—В—А (–† –∞–≤.), –њ–ї–Њ—Й–∞–і—М (S –∞–≤.) –Є –Њ–Ї—А—Г–≥–ї–Њ—Б—В—М (–Ю–Ї—А –∞–≤.) —Д–Њ–≤–µ–∞–ї—М–љ–Њ–є –∞–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –Ј–Њ–љ—Л, –њ–ї–Њ—В–љ–Њ—Б—В—М —Б–Њ—Б—Г–і–Њ–≤ (–Я–°) –Є –њ–ї–Њ—В–љ–Њ—Б—В—М –њ–µ—А—Д—Г–Ј–Є–Є (–Я–Я). –Ю–њ—А–µ–і–µ–ї—П–ї–Є—Б—М –Я–° –і–ї—П —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –Ј–Њ–љ—Л (–Я–° —Ж–µ–љ—В—А), –Ј–Њ–љ –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ (–Я–° –≤–љ—Г—В—А) –Є –≤–љ–µ—И–љ–µ–≥–Њ –Ї–Њ–ї—М—Ж–∞ (–Я–° –≤–љ–µ—И), –∞ —В–∞–Ї–ґ–µ –Њ–±—Й–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П (–Я–° –±/–Њ). –Я–Я –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –і–ї—П —Н—В–Є—Е –ґ–µ —Б–µ–Ї—В–Њ—А–Њ–≤. –Т—Б–µ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Љ—Д-–≠–†–У
–љ–∞ –∞–њ–њ–∞—А–∞—В–µ Retiscan (Roland Consult, –У–µ—А–Љ–∞–љ–Є—П) –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ–Є ISCEV –њ–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–Љ—Г –њ—А–Њ—В–Њ–Ї–Њ–ї—Г —Б 61 –≥–µ–Ї—Б–∞–≥–Њ–љ–∞–ї—М–љ—Л–Љ —Б–µ–≥–Љ–µ–љ—В–Њ–Љ.
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є –ї–µ—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О –њ–∞–Ї–µ—В–∞ –њ—А–Є–Ї–ї–∞–і–љ—Л—Е –њ—А–Њ–≥—А–∞–Љ–Љ Statistica 6.0. –Я—А–Є–Љ–µ–љ—П–ї–Є –Љ–µ—В–Њ–і—Л —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞: –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Б—А–µ–і–љ–µ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П, –Њ—И–Є–±–Ї–Є —Б—А–µ–і–љ–µ–≥–Њ, –і–Њ–≤–µ—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –Є–љ—В–µ—А–≤–∞–ї–∞, —Б—В–∞–љ–і–∞—А—В–љ–Њ–≥–Њ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є—П. –Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Е–∞—А–∞–Ї—В–µ—А–∞ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –і–∞–љ–љ—Л—Е –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О –≥—А–∞—Д–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –Є –Љ–µ—В–Њ–і–∞ –®–∞–њ–Є—А–Њ вАФ –£–Є–ї–Ї–∞. –С—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–µ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –і–∞–љ–љ—Л—Е. –Ч–љ–∞—З–Є–Љ–Њ—Б—В—М —А–∞–Ј–ї–Є—З–Є—П —Б—А–µ–і–љ–Є—Е –≤–µ–ї–Є—З–Є–љ –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–≥–Њ t-–Ї—А–Є—В–µ—А–Є—П –°—В—М—О–і–µ–љ—В–∞ (p<0,05).
–†–µ–Ј—Г–ї—М—В–∞—В—Л
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –≤ –Њ–±–ї–∞—Б—В–Є —Д–Њ–≤–µ–∞ –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л –і—А—Г–Ј—Л —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞: –Љ–µ–ї–Ї–Є–µ —В–≤–µ—А–і—Л–µ, –Ї—А—Г–њ–љ—Л–µ —В–≤–µ—А–і—Л–µ –Є–ї–Є —Б–ї–Є–≤–љ—Л–µ.–Я—А–Њ–≤–µ–і–µ–љ–Њ –Є–Ј—Г—З–µ–љ–Є–µ –і–Є–љ–∞–Љ–Є–Ї–Є –Њ–±—Й–µ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є –њ–µ—А—Д—Г–Ј–Є–Є –≤ —Д–Њ–≤–µ–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1 –Є 2 –≥—А—Г–њ–њ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б. –Т –≥—А—Г–њ–њ–µ 1 –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Љ–µ–ї–Ї–Є—Е —В–≤–µ—А–і—Л—Е –і—А—Г–Ј –Њ–±—Й–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –Я–Я —Б–Њ—Б—В–∞–≤–Є–ї–Њ 0,308¬±0,03, –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –њ–Њ–≤—Л—Б–Є–ї–Њ—Б—М –і–Њ 0,386¬±0,04. –Я—А–Є –љ–∞–ї–Є—З–Є–Є –Ї—А—Г–њ–љ—Л—Е —В–≤–µ—А–і—Л—Е –і—А—Г–Ј –Я–Я —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ 0,295¬±0,07 –і–Њ –ї–µ—З–µ–љ–Є—П –Є 0,278¬±0,06 –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ—П—П—Б—М. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б–ї–Є–≤–љ—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є –Я–Я —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 0,161¬±0,04 –Є —В–∞–Ї–ґ–µ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Љ–µ–љ—П–ї–∞—Б—М –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П.
–Т –≥—А—Г–њ–њ–µ 2 –Њ–±—Й–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –Я–Я —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–µ–ї–Ї–Є–Љ–Є —В–≤–µ—А–і—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є —Б–Њ—Б—В–∞–≤–ї—П–ї–Њ 0,319¬±0,05, —Б –Ї—А—Г–њ–љ—Л–Љ–Є —В–≤–µ—А–і—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є вАФ 0,287¬±0,08, —Б–Њ —Б–ї–Є–≤–љ—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є вАФ 0,154¬±0,07. –Ф–∞–љ–љ—Л–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М —В–∞–Ї–ґ–µ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Љ–µ–љ—П–ї—Б—П –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б.
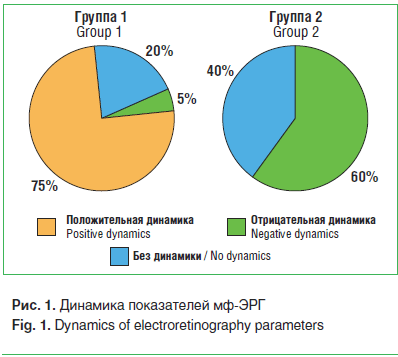
–Р–љ–∞–ї–Є–Ј —Н–ї–µ–Ї—В—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л –њ–Є–Ї–∞ –†1 (–≤ –µ–і–Є–љ–Є—З–љ—Л—Е —Б–ї—Г—З–∞—П—Е вАФ –≥–Є–њ–µ—А—Н—А–≥–Є—З–µ—Б–Ї–Є–є –Њ—В–≤–µ—В) –≤ –±–Њ–ї—М—И–µ–є —З–∞—Б—В–Є –Є–ї–Є –≤–Њ –≤—Б–µ—Е –≥–µ–Ї—Б–∞–≥–Њ–љ–∞—Е, —З—В–Њ –≥—А–∞—Д–Є—З–µ—Б–Ї–Є –≤—Л—А–∞–ґ–∞–ї–Њ—Б—М –≤ –≤–Є–і–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–љ—Д–Є–≥—Г—А–∞—Ж–Є–Є —В—А–µ—Е–Љ–µ—А–љ–Њ–≥–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –і–∞–љ–љ—Л—Е –Љ—Д-–≠–†–У. –Я–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –Љ—Д-–≠–†–У –Ј–∞–Ї–ї—О—З–∞–ї–∞—Б—М –≤ —Г–ї—Г—З—И–µ–љ–Є–Є –µ–µ –Ї–Њ–љ—Д–Є–≥—Г—А–∞—Ж–Є–Є, —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –∞–Љ–њ–ї–Є—В—Г–і—Л –њ–Є–Ї–∞ –†1 (–Є–ї–Є —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –≤ —Б–ї—Г—З–∞–µ –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ–≥–Њ –≥–Є–њ–µ—А—Н—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–≤–µ—В–∞) –Є –њ—А–Є–±–ї–Є–ґ–µ–љ–Є–Є –µ–µ –Ї –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ –Ј–љ–∞—З–µ–љ–Є—П–Љ. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Љ—Д-–≠–†–У –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 1.
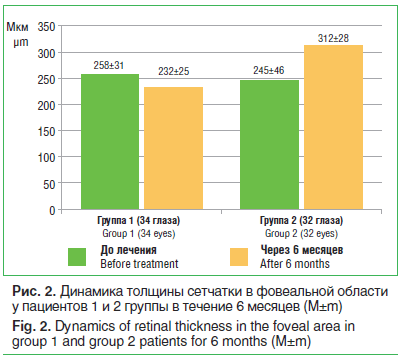
–Р–љ–∞–ї–Є–Ј –і–∞–љ–љ—Л—Е –Ю–Ъ–Ґ –≤—Л—П–≤–Є–ї, —З—В–Њ —В–Њ–ї—Й–Є–љ–∞ —Б–µ—В—З–∞—В–Ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л 1 —Б–Њ—Б—В–∞–≤–Є–ї–∞ 258¬±31 –Љ–Ї–Љ –і–Њ –ї–µ—З–µ–љ–Є—П –Є –Ј–љ–∞—З–Є–Љ–Њ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–∞—Б—М –Ј–∞ –≤—А–µ–Љ—П –ї–µ—З–µ–љ–Є—П. –Т –≥—А—Г–њ–њ–µ 2 —В–Њ–ї—Й–Є–љ–∞ —Б–µ—В—З–∞—В–Ї–Є –≤ —Д–Њ–≤–µ–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ 245¬±46 –Љ–Ї–Љ –і–Њ –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є 312¬±28 –Љ–Ї–Љ вАФ —З–µ—А–µ–Ј 6 –Љ–µ—Б. –Т –≥—А—Г–њ–њ–µ 2 –Њ—В–Љ–µ—З–∞–ї–∞—Б—М —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Г—В–Њ–ї—Й–µ–љ–Є—О —Б–µ—В—З–∞—В–Ї–Є, –љ–Њ —Н—В–Є –Ј–љ–∞—З–µ–љ–Є—П –љ–µ –і–Њ—Б—В–Є–≥–ї–Є —Г—А–Њ–≤–љ—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В–Є (—А–Є—Б. 2).
–£ 5% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –≥—А—Г–њ–њ–µ 1 –Є —Г 15% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –≥—А—Г–њ–њ–µ 2 –љ–∞–±–ї—О–і–∞–ї—Б—П –њ–µ—А–µ—Е–Њ–і –Т–Ь–Ф –≤–Њ ¬Ђ–≤–ї–∞–ґ–љ—Г—О¬ї —Д–Њ—А–Љ—Г. –£ 10% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л 1 –Є 30% –≥—А—Г–њ–њ—Л 2 –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ –≤ –≤–Є–і–µ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —В–≤–µ—А–і—Л—Е –і—А—Г–Ј, –њ–Њ—П–≤–ї–µ–љ–Є—П –Є–ї–Є —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Б–ї–Є–≤–љ—Л—Е –і—А—Г–Ј –ї–Є–±–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Є—Е —А–∞–Ј–Љ–µ—А–∞ (—А–Є—Б. 3).
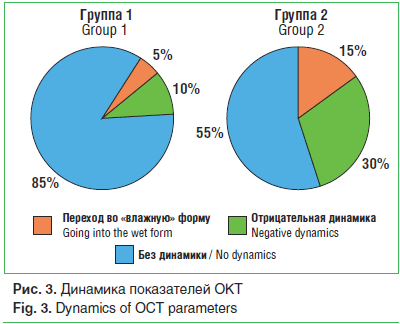
–Ю—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≥—А—Г–њ–њ—Л 1 –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–∞—Б—М –Ј–∞ –≤—А–µ–Љ—П –ї–µ—З–µ–љ–Є—П: 0,7¬±0,15 –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –Є 0,7¬±0,2 —З–µ—А–µ–Ј 6 –Љ–µ—Б. –Т –≥—А—Г–њ–њ–µ 2 –Њ—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ 0,9¬±0,15 –Є 0,8¬±0,1 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –Є –љ–∞–±–ї—О–і–∞–ї–∞—Б—М —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Њ—Б—В—А–Њ—В—Л –Ј—А–µ–љ–Є—П, –љ–µ –і–Њ—Б—В–Є–≥–∞—О—Й–∞—П —Г—А–Њ–≤–љ—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є.
–°—Г–±—К–µ–Ї—В–Є–≤–љ—Л–µ –Њ—Й—Г—Й–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ–Њ –ґ–∞–ї–Њ–±–∞–Љ –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ –Ј—А–µ–љ–Є—П, –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В –њ—А–Є —А–∞–±–Њ—В–µ –љ–∞ –±–ї–Є–Ј–Ї–Њ–Љ —А–∞—Б—Б—В–Њ—П–љ–Є–Є, —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М –≥–ї–∞–Ј –Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –±–Њ–ї–µ–µ —П—А–Ї–Њ–≥–Њ, —З–µ–Љ –Њ–±—Л—З–љ–Њ, –Њ—Б–≤–µ—Й–µ–љ–Є—П. –Ю—Ж–µ–љ–Ї–∞ —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 4.
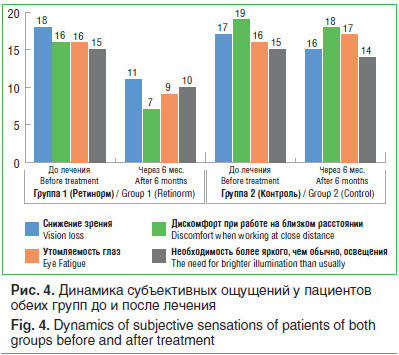
–Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј —А–Є—Б—Г–љ–Ї–∞ 4, —Г–ї—Г—З—И–µ–љ–Є–µ —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –ґ–∞–ї–Њ–± –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –≤ –≥—А—Г–њ–њ–µ 1, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –≥—А—Г–њ–њ–µ 2 –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –±–Њ–ї—М–љ—Л—Е, –њ—А–µ–і—К—П–≤–ї—П–≤—И–Є—Е –ґ–∞–ї–Њ–±—Л, –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Њ—Б—М.
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≥—А—Г–њ–њ—Л, –≤ –Ї–Њ—В–Њ—А—Г—О –Њ–љ–Є –±—Л–ї–Є –Њ–±—К–µ–і–Є–љ–µ–љ—Л) –≤ –Њ–±–ї–∞—Б—В–Є —Д–Њ–≤–µ–∞ –Є–Љ–µ–ї–Є—Б—М —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ –і–ї—П –Т–Ь–Ф –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –≤–Є–і–µ –і—А—Г–Ј —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞. –С—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л –њ–∞—Ж–Є–µ–љ—В—Л —Б –Љ–µ–ї–Ї–Є–Љ–Є —В–≤–µ—А–і—Л–Љ–Є, –Ї—А—Г–њ–љ—Л–Љ–Є —В–≤–µ—А–і—Л–Љ–Є –Є–ї–Є —Б–ї–Є–≤–љ—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є –≤ —Д–Њ–≤–µ–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є. –Ъ–Њ–љ—В—А–Њ–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є –њ–∞—А–љ—Л–µ –≥–ї–∞–Ј–∞ –±–µ–Ј –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Т–Ь–Ф (22 –≥–ї–∞–Ј–∞). –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Е–∞—А–∞–Ї—В–µ—А–∞ –Є–Љ–µ—О—Й–Є—Е—Б—П –і—А—Г–Ј –Њ–њ—А–µ–і–µ–ї—П–ї–Є—Б—М —А–∞–Ј–ї–Є—З–љ—Л–µ –Ј–љ–∞—З–µ–љ–Є—П –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Д–Њ–≤–µ–∞–ї—М–љ–Њ–є –Њ–±–ї–∞—Б—В–Є (—В–∞–±–ї. 1).
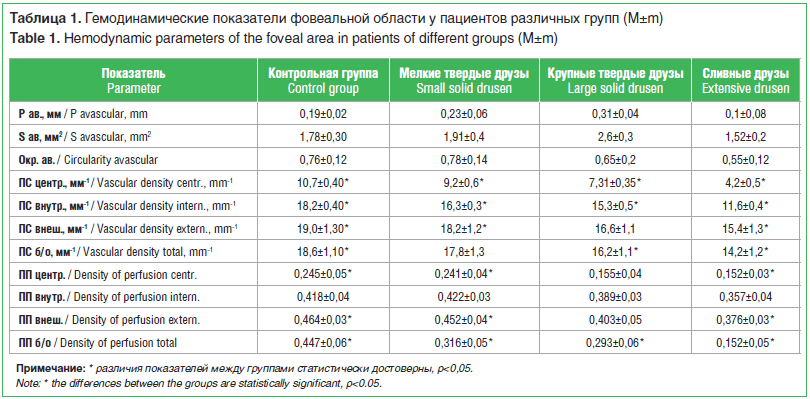
–Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј —В–∞–±–ї–Є—Ж—Л 1, –љ–∞–±–ї—О–і–∞–µ—В—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–ї–Њ—В–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Њ–≤ –≤ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –Ј–Њ–љ–µ –Є –Ј–Њ–љ–µ –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ –Ї–Њ–ї—М—Ж–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї—А—Г–њ–љ—Л–Љ–Є —В–≤–µ—А–і—Л–Љ–Є –Є —Б–ї–Є–≤–љ—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–∞–Ї–Њ–≤–Њ–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–µ–ї–Ї–Є–Љ–Є —В–≤–µ—А–і—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є –Є –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ.
–Ґ–∞–Ї–ґ–µ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–ї–Њ—В–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Њ–≤ –≤ –Ј–Њ–љ–µ –≤–љ–µ—И–љ–µ–≥–Њ –Ї–Њ–ї—М—Ж–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б–ї–Є–≤–љ—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–∞–Ї–Њ–≤–Њ–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–µ–ї–Ї–Є–Љ–Є —В–≤–µ—А–і—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є –Є –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї—А—Г–њ–љ—Л–Љ–Є —В–≤–µ—А–і—Л–Љ–Є –Є —Б–ї–Є–≤–љ—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є –Њ–±—Й–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –њ–ї–Њ—В–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Њ–≤ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–µ–љ–Њ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–∞–Ї–Њ–≤—Л–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л.
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б–ї–Є–≤–љ—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–ї–Њ—В–љ–Њ—Б—В–Є –њ–µ—А—Д—Г–Ј–Є–Є –≤ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –Ј–Њ–љ–µ –Є –≤ –Ј–Њ–љ–µ –≤–љ–µ—И–љ–µ–≥–Њ –Ї–Њ–ї—М—Ж–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В–∞–Ї–Њ–≤—Л–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Љ–µ–ї–Ї–Є–Љ–Є —В–≤–µ—А–і—Л–Љ–Є –і—А—Г–Ј–∞–Љ–Є –Є –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ. –С—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ –Њ—В–ї–Є—З–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –Њ–±—Й–µ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є –њ–µ—А—Д—Г–Ј–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –≤–Є–і–∞–Љ–Є –і—А—Г–Ј.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –њ—А–Є–Љ–µ—А
–С–Њ–ї—М–љ–∞—П –Р., 60 –ї–µ—В, –њ–Њ—Б—В—Г–њ–Є–ї–∞ –≤ –Ї–ї–Є–љ–Є–Ї—Г –≥–ї–∞–Ј–љ—Л—Е –±–Њ–ї–µ–Ј–љ–µ–є —Б –і–Є–∞–≥–љ–Њ–Ј–Њ–Љ –Т–Ь–Ф OD (¬Ђ—Б—Г—Е–∞—П¬ї —Д–Њ—А–Љ–∞), –љ–∞—З–∞–ї—М–љ–∞—П –≤–Њ–Ј—А–∞—Б—В–љ–∞—П –Ї–∞—В–∞—А–∞–Ї—В–∞ –Њ–±–Њ–Є—Е –≥–ї–∞–Ј.–Ш–Ј –∞–љ–∞–Љ–љ–µ–Ј–∞ –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В–Ї–∞ —Б—В—А–∞–і–∞–µ—В –Т–Ь–Ф –Њ–Ї–Њ–ї–Њ 2 –ї–µ—В, –Ї–∞–Ї–Њ–µ-–ї–Є–±–Њ –ї–µ—З–µ–љ–Є–µ —А–µ–≥—Г–ї—П—А–љ–Њ –љ–µ –њ–Њ–ї—Г—З–∞–µ—В.
–Я—А–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ–±–Њ–Є—Е –≥–ї–∞–Ј –≤—Л—П–≤–ї—П–ї–Є—Б—М –њ–Њ–Љ—Г—В–љ–µ–љ–Є—П –≤ –Ї–Њ—А–Ї–Њ–≤—Л—Е —Б–ї–Њ—П—Е —Е—А—Г—Б—В–∞–ї–Є–Ї–∞, —Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤ —Б–µ—В—З–∞—В–Ї–Є. –Т –њ—А–∞–≤–Њ–Љ –≥–ї–∞–Ј—Г –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ (–±–Њ–ї—М—И–µ 20) –Љ–µ–ї–Ї–Є—Е —В–≤–µ—А–і—Л—Е –і—А—Г–Ј –≤ –Њ–±–ї–∞—Б—В–Є —Д–Њ–≤–µ–∞, –≤ –ї–µ–≤–Њ–Љ –≥–ї–∞–Ј—Г вАФ –µ–і–Є–љ—Б—В–≤–µ–љ–љ–∞—П –Љ–µ–ї–Ї–∞—П —В–≤–µ—А–і–∞—П –і—А—Г–Ј–∞ –њ–∞—А–∞—Д–Њ–≤–µ–Њ–ї—П—А–љ–Њ. –Ю—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П –њ—А–∞–≤–Њ–≥–Њ –≥–ї–∞–Ј–∞ —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ 0,6, –ї–µ–≤–Њ–≥–Њ вАФ 0,8.
–Я–∞—Ж–Є–µ–љ—В–Ї–∞ –±—Л–ї–∞ –≤–Ї–ї—О—З–µ–љ–∞ –≤ –≥—А—Г–њ–њ—Г 1, –њ–Њ–ї—Г—З–∞–≤—И—Г—О –†–µ—В–Є–љ–Њ—А–Љ –њ–Њ 1 –Ї–∞–њ—Б—Г–ї–µ 3 —А./—Б—Г—В –≤ —В–µ—З–µ–љ–Є–µ 16 –љ–µ–і. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б. –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 2.
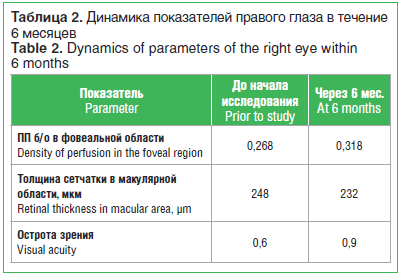
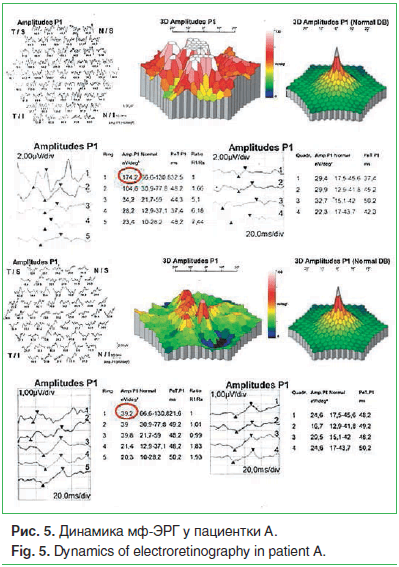
–Т —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б. –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ–ї–Њ—В–љ–Њ—Б—В–Є –њ–µ—А—Д—Г–Ј–Є–Є —Б 0,268 –і–Њ 0,318. –£ –і–∞–љ–љ–Њ–є –њ–∞—Ж–Є–µ–љ—В–Ї–Є –љ–∞–±–ї—О–і–∞–ї—Б—П –≥–Є–њ–µ—А—Н—А–≥–Є—З–µ—Б–Ї–Є–є –Њ—В–≤–µ—В –≤–Њ –≤—Б–µ—Е –≥–µ–Ї—Б–∞–≥–Њ–љ–∞—Е, —З—В–Њ –≥—А–∞—Д–Є—З–µ—Б–Ї–Є –≤—Л—А–∞–ґ–∞–ї–Њ—Б—М –≤ –≤–Є–і–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤—Б–µ–є –Ї–Њ–љ—Д–Є–≥—Г—А–∞—Ж–Є–Є —В—А–µ—Е–Љ–µ—А–љ–Њ–≥–Њ –Є–Ј–Њ–±—А–∞–ґ–µ–љ–Є—П –і–∞–љ–љ—Л—Е –Љ—Д-–≠–†–У. –І–µ—А–µ–Ј 6 –Љ–µ—Б. –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–Њ–љ—Д–Є–≥—Г—А–∞—Ж–Є–Є –Љ—Д-–≠–†–У, —Б–љ–Є–ґ–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л –†1 –Є –њ—А–Є–±–ї–Є–ґ–µ–љ–Є–µ –µ–µ –Ї –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ –Ј–љ–∞—З–µ–љ–Є—П–Љ (—А–Є—Б. 5).
–°—Г–±—К–µ–Ї—В–Є–≤–љ–Њ –њ–∞—Ж–Є–µ–љ—В–Ї–∞ –Њ—В–Љ–µ—В–Є–ї–∞ —Г–ї—Г—З—И–µ–љ–Є–µ –Њ–±—Й–µ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П, —Г–ї—Г—З—И–µ–љ–Є–µ –Ј—А–µ–љ–Є—П –≤–±–ї–Є–Ј–Є, —Б–љ–Є–ґ–µ–љ–Є–µ —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В–Є –≥–ї–∞–Ј –њ—А–Є —А–∞–±–Њ—В–µ –≤–±–ї–Є–Ј–Є.
–Т—Л–≤–Њ–і—Л
–Э–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –†–µ—В–Є–љ–Њ—А–Љ –њ—А–Є —А–∞–љ–љ–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є—П—Е –Т–Ь–Ф (–і—А—Г–Ј—Л) –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–Њ—В–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –њ—А–Є —Б—В–∞–±–Є–ї—М–љ–Њ–є —В–Њ–ї—Й–Є–љ–µ —Б–µ—В—З–∞—В–Ї–Є —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤.–†–µ—В–Є–љ–Њ—А–Љ –Ї–∞–Ї —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–є –Є—Б—В–Њ—З–љ–Є–Ї –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л—Е –і–ї—П —Б–µ—В—З–∞—В–Ї–Є –≤–µ—Й–µ—Б—В–≤ –Љ–Њ–ґ–µ—В –њ—А–Є–Љ–µ–љ—П—В—М—Б—П –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б ¬Ђ—Б—Г—Е–Њ–є¬ї —Д–Њ—А–Љ–Њ–є –Т–Ь–Ф.












