–í–≤–µ–¥–µ–Ω–∏–µ
–ë—Ä–æ–Ω—Ö–∏–∞–ª—å–Ω–∞—è –∞—Å—Ç–º–∞ (–ë–ê) –∏ —Ö—Ä–æ–Ω–∏—á–µ—Å–∫–∞—è –æ–±—Å—Ç—Ä—É–∫—Ç–∏–≤–Ω–∞—è –±–æ–ª–µ–∑–Ω—å –ª–µ–≥–∫–∏—Ö (–•–û–ë–õ) ‚Äì –¥–≤–∞ —Å–∞–º–æ—Å—Ç–æ—è—Ç–µ–ª—å–Ω—ã—Ö, –Ω–∞–∏–±–æ–ª–µ–µ —á–∞—Å—Ç–æ –≤—Å—Ç—Ä–µ—á–∞—é—â–∏—Ö—Å—è –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è —Ä–µ—Å–ø–∏—Ä–∞—Ç–æ—Ä–Ω–æ–π —Å–∏—Å—Ç–µ–º—ã. –ü–æ –¥–∞–Ω–Ω—ã–º –í–û–ó, –•–û–ë–õ —Å—Ç—Ä–∞–¥–∞—é—Ç 230 –º–ª–Ω —á–µ–ª–æ–≤–µ–∫ –≤ –º–∏—Ä–µ. –ï–∂–µ–≥–æ–¥–Ω–æ –æ—Ç –¥–∞–Ω–Ω–æ–≥–æ –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è —É–º–∏—Ä–∞—é—Ç 2,74 –º–ª–Ω, –∏ –∫ 2020 –≥. –•–û–ë–õ –≤—ã–π–¥–µ—Ç –Ω–∞ 3-–µ –º–µ—Å—Ç–æ —Å—Ä–µ–¥–∏ –ø—Ä–∏—á–∏–Ω —Å–º–µ—Ä—Ç–∏ [1]. –í —Ç–µ—á–µ–Ω–∏–µ –¥–ª–∏—Ç–µ–ª—å–Ω–æ–≥–æ –≤—Ä–µ–º–µ–Ω–∏ –•–û–ë–õ –¥–∏–∞–≥–Ω–æ—Å—Ç–∏—Ä–æ–≤–∞–ª–∞—Å—å –ø—Ä–µ–∏–º—É—â–µ—Å—Ç–≤–µ–Ω–Ω–æ —É –º—É–∂—á–∏–Ω, –æ–¥–Ω–∞–∫–æ –≤ –Ω–∞—Å—Ç–æ—è—â–µ–µ –≤—Ä–µ–º—è –≤–æ –≤—Å–µ–º –º–∏—Ä–µ –≤–æ–∑—Ä–æ—Å–ª–æ –ø–æ—Ç—Ä–µ–±–ª–µ–Ω–∏–µ —Ç–∞–±–∞–∫–∞ –∂–µ–Ω—â–∏–Ω–∞–º–∏, —á—Ç–æ –ø—Ä–∏–≤–µ–ª–æ –∫ —Ä–æ—Ŭ≠—Ç—É –∑–∞–±–æ–ª–µ–≤–∞–µ–º–æ—Å—Ç–∏ –•–û–ë–õ –≤ –∂–µ–Ω—Å–∫–æ–π –ø–æ–ø—É–ª—è—Ü–∏–∏.–í –º–∏—Ä–µ –æ–∫–æ–ª–æ 300 –º–ª–Ω —á–µ–ª–æ–≤–µ–∫ —Å—Ç—Ä–∞–¥–∞—é—Ç –ë–ê ‚Äì –∫–∞–∂–¥—ã–π 20-–π –∂–∏—Ç–µ–ª—å –ø–ª–∞–Ω–µ—Ç—ã. –Ý–∞—Å–ø—Ä–æ—Å—Ç—Ä–∞–Ω–µ–Ω–Ω–æ—Å—Ç—å —ç—Ç–æ–≥–æ –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è –≤ —Ä–∞–∑–Ω—ã—Ö —Å—Ç—Ä–∞–Ω–∞—Ö –º–∏—Ä–∞ –∫–æ–ª–µ–±–ª–µ—Ç—Å—è –æ—Ç 1 –¥–æ 18%. –ü–æ –¥–∞–Ω–Ω—ã–º –í–û–ó, –ª–µ—Ç–∞–ª—å–Ω–æ—Å—Ç—å –æ—Ç –∞—Å—Ç–º—ã —Å–æ—Å—Ç–∞–≤–ª—è–µ—Ç 250 —Ç—ã—Å. —á–µ–ª–æ–≤–µ–∫ –≤ –≥–æ–¥. –ò—Å—Ö–æ–¥—è –∏–∑ —Ä–µ–∑—É–ª—å—Ç–∞—Ç–æ–≤ –∞–Ω–∞–ª–∏—Ç–∏–∫–æ-–ø—Ä–æ–≥–Ω–æ—Å—Ç–∏—á–µ—Å–∫–∏—Ö –∏—Å—Å–ª–µ–¥–æ–≤–∞–Ω–∏–π –Ω–µ –∏—Å–∫–ª—é—á–µ–Ω–æ, —á—Ç–æ –ø—Ä–∏ —Å—Ç—Ä–µ–º–∏—Ç–µ–ª—å–Ω—ã—Ö —Ç–µ–º–ø–∞—Ö —É—Ä–±–∞–Ω–∏–∑–∞—Ü–∏–∏ –∫ 2025 –≥. –ë–ê —Ä–∞–∑–æ–≤—å–µ—Ç—Å—è –¥–æ–ø–æ–ª–Ω–∏—Ç–µ–ª—å–Ω–æ —É 100‚Äì150 –º–ª–Ω —á–µ–ª–æ–≤–µ–∫ [2, 3].
–°–æ—Ü–∏–∞–ª—å–Ω–∞—è –∏ —ç–∫–æ–Ω–æ–º–∏—á–µ—Å–∫–∞—è –∑–Ω–∞—á–∏–º–æ—Å—Ç—å –•–û–ë–õ –∏ –ë–ê –æ–ø—Ä–µ–¥–µ–ª—è—é—Ç –Ω–µ–æ–±—Ö–æ–¥–∏–º–æ—Å—Ç—å –≥–ª—É–±–æ–∫–æ–≥–æ –∏–∑—É—á–µ–Ω–∏—è –∏—Ö —Å–æ—á–µ—Ç–∞–Ω–∏—è —É –æ–¥–Ω–æ–≥–æ –ø–∞—Ü–∏–µ–Ω—Ç–∞. –ù–µ—Å–º–æ—Ç—Ä—è –Ω–∞ —á–µ—Ç–∫–∏–µ –¥–∏–∞–≥–Ω–æ—Å—Ç–∏—á–µ—Å–∫–∏–µ –∫—Ä–∏—Ç–µ—Ä–∏–∏, –≤ —Ä—è–¥–µ —Å–ª—É—á–∞–µ–≤ —Ç—Ä—É–¥–Ω–æ –ø—Ä–æ–≤–µ—Å—Ç–∏ –≥—Ä–∞–Ω–∏—Ü—É –º–µ–∂–¥—É —ç—Ç–∏–º–∏ –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è–º–∏ [4]. –í 2014 –≥. –≤–ø–µ—Ä–≤—ã–µ –≤—ã–¥–µ–ª–µ–Ω —Å–∏–Ω–¥—Ä–æ–º –ø–µ—Ä–µ–∫—Ä–µ—Å—Ç–∞ –ë–ê –∏ –•–û–ë–õ, –∏–ª–∏ ACOS-—Å–∏–Ω–¥—Ä–æ–º, –∫–æ—Ç–æ—Ä—ã–π —Å–æ—á–µ—Ç–∞–µ—Ç –≤ —Å–µ–±–µ –ø—Ä–∏–∑–Ω–∞–∫–∏ –æ–±–µ–∏—Ö –Ω–æ–∑–æ–ª–æ–≥–∏–π [5]. –ß–∞—Å—Ç–æ—Ç–∞ —Å–æ—á–µ—Ç–∞–Ω–∏—è –ë–ê –∏ –•–û–ë–õ –∫–æ–ª–µ–±–ª–µ—Ç—Å—è –æ—Ç 12,1 –¥–æ 55,2% —Å—Ä–µ–¥–∏ –±–æ–ª—å–Ω—ã—Ö –•–û–ë–õ –∏ –æ—Ç 13,3 –¥–æ 61,0% —Å—Ä–µ–¥–∏ –±–æ–ª—å–Ω—ã—Ö –ë–ê [6].
–ú–æ—Ä—Ñ–æ–ª–æ–≥–∏—á–µ—Å–∫–æ–π –æ—Å–Ω–æ–≤–æ–π –æ–±–æ–∏—Ö –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏–π —è–≤–ª—è–µ—Ç—Å—è —Ö—Ä–æ–Ω–∏—á–µ—Å–∫–æ–µ –≤–æ—Å–ø–∞–ª–µ–Ω–∏–µ –≤ –±—Ä–æ–Ω—Ö–∏–∞–ª—å–Ω–æ–º –¥–µ—Ä–µ–≤–µ, –Ω–∞—Ä—É—à–∞—é—â–µ–µ —Ü–µ–ª–æ—Å—Ç–Ω–æ—Å—Ç—å —ç–ø–∏—Ç–µ–ª–∏–∞–ª—å–Ω–æ–≥–æ —Å–ª–æ—è, –æ–±—É—Å–ª–æ–≤–ª–∏–≤–∞—é—â–µ–µ –∑–∞–ø—É—Å–∫ –±—Ä–æ–Ω—Ö–æ–∫–æ–Ω—Å—Ç—Ä–∏–∫—Ç–æ—Ä–Ω—ã—Ö —Ä–µ–∞–∫—Ü–∏–π, –ø—Ä–∏–≤–æ–¥—è—â–∏—Ö –∫ –±—Ä–æ–Ω—Ö–∏–∞–ª—å–Ω–æ–π –æ–±—Å—Ç—Ä—É–∫—Ü–∏–∏ [7, 8]. –ò–∑–≤–µ—Å—Ç–Ω–æ, —á—Ç–æ —Ç–∞–±–∞–∫–æ–∫—É—Ä–µ–Ω–∏–µ —Å–ø–æ—Å–æ–±—Å—Ç–≤—É–µ—Ç –¥–∏—Å–±–∞–ª–∞–Ω—Å—É –ø—Ä–æ—Ç–µ–∞–∑ –∏ –∞–Ω—Ç–∏–ø—Ä–æ—Ç–µ–∞–∑ –≤ –ª–µ–≥–æ—á–Ω–æ–π —Ç–∫–∞–Ω–∏ –∏ —Ä–∞–∑–≤–∏—Ç–∏—é —Å–∏—Å—Ç–µ–º–Ω–æ–≥–æ –æ–∫–∏—Å–ª–∏—Ç–µ–ª—å–Ω–æ–≥–æ —Å—Ç—Ä–µ—Å—Å–∞, —É—Å–∏–ª–∏–≤–∞—é—â–µ–≥–æ –≤–æ—Å–ø–∞–ª–µ–Ω–∏–µ [9, 10]. –ù–µ–æ–±—Ö–æ–¥–∏–º–æ –æ—Ç–º–µ—Ç–∏—Ç—å, —á—Ç–æ —Ä–∏—Å–∫ —Ä–∞–∑–≤–∏—Ç–∏—è –•–û–ë–õ —É –∫—É—Ä—è—â–µ–≥–æ –∞—Å—Ç–º–∞—Ç–∏–∫–∞ –∑–Ω–∞—á–∏—Ç–µ–ª—å–Ω–æ –≤—ã—à–µ, —á–µ–º —É –Ω–µ–∫—É—Ä—è—â–µ–≥–æ, —Ö–æ—Ç—è —Å—É–º–º–∞—Ä–Ω–∞—è –∏–Ω—Ç–µ–Ω—Å–∏–≤–Ω–æ—Å—Ç—å –∫—É—Ä–µ–Ω–∏—è –Ω–∏–∂–µ –ø–æ —Å—Ä–∞–≤–Ω–µ–Ω–∏—é —Å –ª—é–¥—å–º–∏, —Å—Ç—Ä–∞–¥–∞—é—â–∏–º–∏ —Ç–æ–ª—å–∫–æ –•–û–ë–õ [11]. –ü—Ä–∏ —ç—Ç–æ–º —Ö–∞—Ä–∞–∫—Ç–µ—Ä –≤–æ—Å–ø–∞–ª–µ–Ω–∏—è –ø—Ä–∏ –ë–ê –∏ –•–û–ë–õ –∏–º–µ–µ—Ç –ø—Ä–∏–Ω—Ü–∏–ø–∏–∞–ª—å–Ω—ã–µ —Ä–∞–∑–ª–∏—á–∏—è.
Согласно определению, «ACOS-синдром характеризуется персистирующим ограничением воздушного потока, рядом признаков, ассоциированных с астмой, и рядом признаков, ассоциированных с ХОБЛ» [12]. В настоящий момент сочетание БА и ХОБЛ может быть диагностировано при наличии 3-х признаков характерных для БА и 3-х признаков характерных для ХОБЛ [9].
–ü—Ä–∏–∑–Ω–∞–∫–∏ —Ö–∞—Ä–∞–∫—Ç–µ—Ä–Ω—ã–µ –¥–ª—è –ë–ê
–í–æ–∑—Ä–∞—Å—Ç –¥–µ–±—é—Ç–∞ –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è –¥–æ 20 –ª–µ—Ç.–ü—Ä–æ—è–≤–ª–µ–Ω–∏—è –≥–∏–ø–µ—Ä—Ä–µ–∞–∫—Ç–∏–≤–Ω–æ—Å—Ç–∏ (—Å–∏–º–ø—Ç–æ–º—ã –≤–∞—Ä—å–∏—Ä—É—é—Ç –ø–æ –º–∏–Ω—É—Ç–∞–º, —á–∞—Å–∞–º –∏ –¥–Ω—è–º).
–£—Ö—É–¥—à–µ–Ω–∏–µ –Ω–æ—á—å—é –∏–ª–∏ –≤ —Ä–∞–Ω–Ω–∏–µ —É—Ç—Ä–µ–Ω–Ω–∏–µ —á–∞—Å—ã.
–°–∏–º–ø—Ç–æ–º—ã –ø–æ—è–≤–ª—è—é—Ç—Å—è –≤–æ –≤—Ä–µ–º—è –Ω–∞–≥—Ä—É–∑–∫–∏, —ç–º–æ—Ü–∏–π, –∫–æ–Ω—Ç–∞–∫—Ç–∞ —Å –∞–ª–ª–µ—Ä–≥–µ–Ω–æ–º.
–í–∞—Ä–∏–∞–±–µ–ª—å–Ω—ã–µ –æ–≥—Ä–∞–Ω–∏—á–µ–Ω–∏—è –≤–æ–∑–¥—É—à–Ω–æ–≥–æ –ø–æ—Ç–æ–∫–∞.
–ù–æ—Ä–º–∞–ª—å–Ω–∞—è —Ñ—É–Ω–∫—Ü–∏—è –ª–µ–≥–∫–∏—Ö –º–µ–∂–¥—É —Å–∏–º–ø—Ç–æ–º–∞–º–∏.
–Ý–∞–Ω–µ–µ –¥–∏–∞–≥–Ω–æ—Å—Ç–∏—Ä–æ–≤–∞–ª–∞—Å—å –∞—Å—Ç–º–∞.
–ù–∞–ª–∏—á–∏–µ –æ—Ç—è–≥–æ—â–µ–Ω–Ω–æ–π –Ω–∞—Å–ª–µ–¥—Å—Ç–≤–µ–Ω–Ω–æ—Å—Ç–∏ –ø–æ –ë–ê –∏–ª–∏ –¥—Ä—É–≥–∏–º –∞—Ç–æ–ø–∏—á–µ—Å–∫–∏–º –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è–º.
–¢–µ—á–µ–Ω–∏–µ –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è —Ö–∞—Ä–∞–∫—Ç–µ—Ä–∏–∑—É–µ—Ç—Å—è –æ—Ç—Å—É—Ç—Å—Ç–≤–∏–µ–º –ø—Ä–æ–≥—Ä–µ—Å—Å–∏—Ä–æ–≤–∞–Ω–∏—è —Å–∏–º–ø—Ç–æ–º–æ–≤ –∏–ª–∏ –Ω–∞–ª–∏—á–∏–µ–º —Å–µ–∑–æ–Ω–Ω–æ–π –≤–∞—Ä–∏–∞–±–µ–ª—å–Ω–æ—Å—Ç–∏.
–í–æ–∑–º–æ–∂–Ω–æ —Å–ø–æ–Ω—Ç–∞–Ω–Ω–æ–µ —É–ª—É—á—à–µ–Ω–∏–µ –∏–ª–∏ –±—ã—Å—Ç—Ä—ã–π —ç—Ñ—Ñ–µ–∫—Ç –ø—Ä–∏ –ª–µ—á–µ–Ω–∏–∏ –±—Ä–æ–Ω—Ö–æ–ª–∏—Ç–∏–∫–∞–º–∏ –∏–ª–∏ –≤ —Ç–µ—á–µ–Ω–∏–µ –Ω–µ—Å–∫–æ–ª—å–∫–∏—Ö –Ω–µ–¥–µ–ª—å –≤ –æ—Ç–≤–µ—Ç –Ω–∞ –∏–Ω–≥–∞–ª—è—Ü–∏–æ–Ω–Ω—ã–µ –≥–ª—é–∫–æ–∫–æ—Ä—Ç–∏–∫–æ—Å—Ç–µ—Ä–æ–∏–¥—ã (–ò–ì–ö–°).
–ù–æ—Ä–º–∞–ª—å–Ω–∞—è —Ä–µ–Ω—Ç–≥–µ–Ω–æ–ª–æ–≥–∏—á–µ—Å–∫–∞—è –∫–∞—Ä—Ç–∏–Ω–∞.
–ü—Ä–∏–∑–Ω–∞–∫–∏ —Ö–∞—Ä–∞–∫—Ç–µ—Ä–Ω—ã–µ –¥–ª—è –•–û–ë–õ
–í–æ–∑—Ä–∞—Å—Ç –¥–µ–±—é—Ç–∞ –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è –ø–æ—Å–ª–µ 40 –ª–µ—Ç.–°–∏–º–ø—Ç–æ–º—ã –ø–µ—Ä—Å–∏—Å—Ç–∏—Ä—É—é—Ç, –Ω–µ—Å–º–æ—Ç—Ä—è –Ω–∞ –ª–µ—á–µ–Ω–∏–µ.
Наличие «хороших» и «плохих» дней, но симптомы ежедневные.
–•—Ä–æ–Ω–∏—á–µ—Å–∫–∏–π –∫–∞—à–µ–ª—å –∏ –ø—Ä–æ–¥—É–∫—Ü–∏—è –º–æ–∫—Ä–æ—Ç—ã –æ–±—ã—á–Ω–æ –ø—Ä–µ–¥—à–µ—Å—Ç–≤—É—é—Ç –æ–¥—ã—à–∫–µ –∏ –Ω–µ —Å–≤—è–∑–∞–Ω—ã —Å —Ç—Ä–∏–≥–≥–µ—Ä–∞–º–∏.
–ü–µ—Ä—Å–∏—Å—Ç–∏—Ä—É—é—â–µ–µ –æ–≥—Ä–∞–Ω–∏—á–µ–Ω–∏–µ –≤–æ–∑–¥—É—à–Ω–æ–≥–æ –ø–æ—Ç–æ–∫–∞.
–°–Ω–∏–∂–µ–Ω–Ω–∞—è —Ñ—É–Ω–∫—Ü–∏—è –ª–µ–≥–∫–∏—Ö –º–µ–∂–¥—É —Å–∏–º–ø—Ç–æ–º–∞–º–∏.
–Ý–∞–Ω–µ–µ –¥–∏–∞–≥–Ω–æ—Å—Ç–∏—Ä–æ–≤–∞–ª–∞—Å—å –•–û–ë–õ.
–ò–Ω—Ç–µ–Ω—Å–∏–≤–Ω–æ–µ –≤–æ–∑–¥–µ–π—Å—Ç–≤–∏–µ —Ñ–∞–∫—Ç–æ—Ä–æ–≤ —Ä–∏—Å–∫–∞ (–∫—É—Ä–µ–Ω–∏–µ, –æ—Ä–≥–∞–Ω–∏—á–µ—Å–∫–æ–µ —Ç–æ–ø–ª–∏–≤–æ).
–¢–µ—á–µ–Ω–∏–µ –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è —Ö–∞—Ä–∞–∫—Ç–µ—Ä–∏–∑—É–µ—Ç—Å—è —Ç–µ–º, —á—Ç–æ —Å–∏–º–ø—Ç–æ–º—ã –º–µ–¥–ª–µ–Ω–Ω–æ –ø—Ä–æ–≥—Ä–µ—Å—Å–∏—Ä—É—é—Ç (–ø—Ä–æ–≥—Ä–µ—Å—Å–∏—Ä–æ–≤–∞–Ω–∏–µ –≥–æ–¥ –æ—Ç –≥–æ–¥–∞).
–ö–æ—Ä–æ—Ç–∫–æ–¥–µ–π—Å—Ç–≤—É—é—â–∏–µ –±—Ä–æ–Ω—Ö–æ–ª–∏—Ç–∏–∫–∏ –ø—Ä–∏–Ω–æ—Å—è—Ç –≤—Ä–µ–º–µ–Ω–Ω–æ–µ –æ–±–ª–µ–≥—á–µ–Ω–∏–µ.
–Ý–µ–Ω—Ç–≥–µ–Ω–æ–ª–æ–≥–∏—á–µ—Å–∫–∞—è –∫–∞—Ä—Ç–∏–Ω–∞: –≥–∏–ø–µ—Ä–∏–Ω—Ñ–ª—è—Ü–∏—è.
Прогрессирующее ухудшение легочной функции при сочетании БА и ХОБЛ обусловливает выраженность клинической симптоматики, наряду с которой отмечается снижение качества и продолжительности жизни у данной категории больных [13]. Именно поэтому пациенты с перекрестом БА и ХОБЛ нуждаются в интенсивном использовании ресурсов здравоохранения и требуют назначения персонифицированной фармакотерапии [14]. Комплексное изучение респираторных показателей во взаимосвязи с клиническими особенностями будет способствовать пониманию патофизио­логических изменений дыхательной системы и позволит упростить дифференциальную диагностику бронхообструктивных заболеваний [15, 16].
–¶–µ–ª—å –∏—Å—Å–ª–µ–¥–æ–≤–∞–Ω–∏—è: –∏–∑—É—á–∏—Ç—å –∫–ª–∏–Ω–∏–∫–æ-—Ñ—É–Ω–∫—Ü–∏–æ–Ω–∞–ª—å–Ω—ã–µ –ø–∞—Ä–∞–º–µ—Ç—Ä—ã, —Å–æ–¥–µ—Ä–∂–∞–Ω–∏–µ –æ–∫—Å–∏–¥–∞ –∞–∑–æ—Ç–∞ –≤ –≤—ã–¥—ã—Ö–∞–µ–º–æ–º –≤–æ–∑–¥—É—Ö–µ –∏ –æ—Å–æ–±–µ–Ω–Ω–æ—Å—Ç–∏ –∫–ª–µ—Ç–æ—á–Ω–æ–≥–æ —Å–æ—Å—Ç–∞–≤–∞ –∏–Ω–¥—É—Ü–∏—Ä–æ–≤–∞–Ω–Ω–æ–π –º–æ–∫—Ä–æ—Ç—ã –ø—Ä–∏ —Å–æ—á–µ—Ç–∞–Ω–∏–∏ –ë–ê –∏ –•–û–ë–õ.
–ó–∞–¥–∞—á–∏ –∏—Å—Å–ª–µ–¥–æ–≤–∞–Ω–∏—è
1. –û—Ü–µ–Ω–∏—Ç—å –∫–ª–∏–Ω–∏–∫–æ-—Ñ—É–Ω–∫—Ü–∏–æ–Ω–∞–ª—å–Ω—ã–µ –æ—Å–æ–±–µ–Ω–Ω–æ—Å—Ç–∏ —É –±–æ–ª—å–Ω—ã—Ö —Å–æ—á–µ—Ç–∞–Ω–Ω–æ–π –ø–∞—Ç–æ–ª–æ–≥–∏–µ–π –≤ —Å—Ä–∞–≤–Ω–µ–Ω–∏–∏ —Å –ø–∞—Ü–∏–µ–Ω—Ç–∞–º–∏ —Å –•–û–ë–õ –∏ –ø–∞—Ü–∏–µ–Ω—Ç–∞–º–∏ —Å –ë–ê.2. –ò–∑—É—á–∏—Ç—å –æ—Å–æ–±–µ–Ω–Ω–æ—Å—Ç–∏ –∫–ª–µ—Ç–æ—á–Ω–æ–≥–æ —Å–æ—Å—Ç–∞–≤–∞ –∏–Ω–¥—É—Ü–∏—Ä–æ–≤–∞–Ω–Ω–æ–π –º–æ–∫—Ä–æ—Ç—ã —É –±–æ–ª—å–Ω—ã—Ö –ë–ê, –•–û–ë–õ –∏ –∏—Ö —Å–æ—á–µ—Ç–∞–Ω–∏–µ–º.
3. –ò–∑—É—á–∏—Ç—å —Å–æ–¥–µ—Ä–∂–∞–Ω–∏–µ –æ–∫—Å–∏–¥–∞ –∞–∑–æ—Ç–∞ –≤ –≤—ã–¥—ã—Ö–∞–µ–º–æ–º –≤–æ–∑–¥—É—Ö–µ –ø—Ä–∏ –ë–ê –∏ –•–û–ë–õ –∏ –∏—Ö —Å–æ—á–µ—Ç–∞–Ω–∏–∏.
4. –í—ã—è–≤–∏—Ç—å –≤–æ–∑–º–æ–∂–Ω—ã–µ –≤–∑–∞–∏–º–æ—Å–≤—è–∑–∏ –º–µ–∂–¥—É –ø–æ–∫–∞–∑–∞—Ç–µ–ª—è–º–∏ –±—Ä–æ–Ω—Ö–∏–∞–ª—å–Ω–æ–π –ø—Ä–æ—Ö–æ–¥–∏–º–æ—Å—Ç–∏, —É—Ä–æ–≤–Ω–µ–º –æ–∫—Å–∏–¥–∞ –∞–∑–æ—Ç–∞ –≤ –≤—ã–¥—ã—Ö–∞–µ–º–æ–º –≤–æ–∑–¥—É—Ö–µ –∏ –ø–æ–∫–∞–∑–∞—Ç–µ–ª—è–º–∏ –∏–Ω–¥—É—Ü–∏—Ä–æ–≤–∞–Ω–Ω–æ–π –º–æ–∫—Ä–æ—Ç—ã –ø—Ä–∏ –±—Ä–æ–Ω—Ö–æ–æ–±—Å—Ç—Ä—É–∫—Ç–∏–≤–Ω—ã—Ö –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è—Ö –ª–µ–≥–∫–∏—Ö.
–ú–∞—Ç–µ—Ä–∏–∞–ª –∏ –º–µ—Ç–æ–¥—ã
–í—Å–µ–≥–æ –∏—Å—Å–ª–µ–¥–æ–≤–∞–Ω–æ 57 —Ä–µ—Å–ø–æ–Ω–¥–µ–Ω—Ç–æ–≤, –∫–æ—Ç–æ—Ä—ã–µ –±—ã–ª–∏ —Ä–∞–∑–¥–µ–ª–µ–Ω—ã –Ω–∞ 3 –≥—Ä—É–ø–ø—ã.–ö—Ä–∏—Ç–µ—Ä–∏–∏ –≤–∫–ª—é—á–µ–Ω–∏—è –≤ –∏—Å—Å–ª–µ–¥–æ–≤–∞–Ω–∏–µ: –≤–æ–∑—Ä–∞—Å—Ç –æ—Ç 40 –¥–æ 75 –ª–µ—Ç; –ø–æ–ª—É—á–µ–Ω–∏–µ –∏–Ω—Ñ–æ—Ä–º–∏—Ä–æ–≤–∞–Ω–Ω–æ–≥–æ —Å–æ–≥–ª–∞—Å–∏—è –Ω–∞ —É—á–∞—Å—Ç–∏–µ –≤ –∏—Å—Å–ª–µ–¥–æ–≤–∞–Ω–∏–∏.
–ö—Ä–∏—Ç–µ—Ä–∏–∏ –∏—Å–∫–ª—é—á–µ–Ω–∏—è: –Ω–∞–ª–∏—á–∏–µ –≤ –∞–Ω–∞–º–Ω–µ–∑–µ —Ö—Ä–æ–Ω–∏—á–µ—Å–∫–∏—Ö –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏–π –ª–µ–≥–∫–∏—Ö, –∫—Ä–æ–º–µ –ë–ê –∏ –•–û–ë–õ; —Å–∞—Ö–∞—Ä–Ω—ã–π –¥–∏–∞–±–µ—Ç; —Ü–µ—Ä–µ–±—Ä–æ–≤–∞—Å–∫—É–ª—è—Ä–Ω—ã–µ –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è (–∏–Ω—Å—É–ª—å—Ç, —Ç—Ä–∞–Ω–∑–∏—Ç–æ—Ä–Ω—ã–µ –∏—à–µ–º–∏—á–µ—Å–∫–∏–µ –∞—Ç–∞–∫–∏), –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è —Å–µ—Ä–¥—Ü–∞ (–∏–Ω—Ñ–∞—Ä–∫—Ç –º–∏–æ–∫–∞—Ä–¥–∞ –≤ —Ç–µ—á–µ–Ω–∏–µ –≥–æ–¥–∞ –¥–æ –º–æ–º–µ–Ω—Ç–∞ –≤–∫–ª—é—á–µ–Ω–∏—è, –∫–æ—Ä–æ–Ω–∞—Ä–Ω–∞—è —Ä–µ–≤–∞—Å–∫—É–ª—è—Ä–∏–∑–∞—Ü–∏—è, —Ö—Ä–æ–Ω–∏—á–µ—Å–∫–∞—è —Å–µ—Ä–¥–µ—á–Ω–∞—è –Ω–µ–¥–æ—Å—Ç–∞—Ç–æ—á–Ω–æ—Å—Ç—å II –∏ III —Å—Ç–∞–¥–∏–∏); –∑–ª–æ–∫–∞—á–µ—Å—Ç–≤–µ–Ω–Ω—ã–µ –Ω–æ–≤–æ–æ–±—Ä–∞–∑–æ–≤–∞–Ω–∏—è; —Ç—è–∂–µ–ª–∞—è –ø–æ—á–µ—á–Ω–∞—è –∏ –ø–µ—á–µ–Ω–æ—á–Ω–∞—è –Ω–µ–¥–æ—Å—Ç–∞—Ç–æ—á–Ω–æ—Å—Ç—å; –±–µ—Ä–µ–º–µ–Ω–Ω—ã–µ –∏ –∫–æ—Ä–º—è—â–∏–µ –∂–µ–Ω—â–∏–Ω—ã.
В 1-ю группу вошли 20 больных БА, во 2-ю группу – 19 с сочетанием БА и ХОБЛ, в 3-ю группу – 18 больных с ХОБЛ (табл. 1). Все пациенты находились на стационарном лечении в легочно-аллергологическом центре ККБ. Во 2-й и 3-й группах преобладали мужчины (68,4% и 83,3%, при р=0,039 и р=0,003 соответственно), тогда как среди больных БА больше было женщин. Возраст пациентов с БА составил 51 (46; 59) год, что существенно меньше, чем у пациентов 2-й и 3-й группы (р=0,019, р=0,004 соответственно).
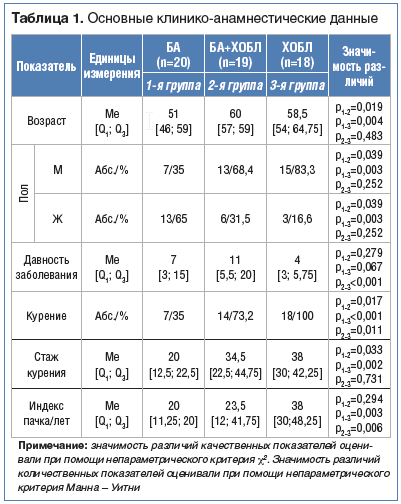
–î–∏–∞–≥–Ω–æ–∑ –ë–ê –±—ã–ª –≤–µ—Ä–∏—Ñ–∏—Ü–∏—Ä–æ–≤–∞–Ω —É –±–æ–ª—å–Ω—ã—Ö, –∏–º–µ—é—â–∏—Ö –º–µ–Ω–µ–µ 3-—Ö –ø—Ä–∏–∑–Ω–∞–∫–æ–≤ –•–û–ë–õ.
–í—Å–µ–º –ø–∞—Ü–∏–µ–Ω—Ç–∞–º –ø—Ä–æ–≤–æ–¥–∏–ª–æ—Å—å –∫–ª–∏–Ω–∏—á–µ—Å–∫–æ–µ –æ–±—Å–ª–µ–¥–æ–≤–∞–Ω–∏–µ, –≤–∫–ª—é—á–∞—é—â–µ–µ —Å–±–æ—Ä –∞–Ω–∞–º–Ω–µ–∑–∞, —Ñ–∏–∑–∏–∫–∞–ª—å–Ω—ã–π –æ—Å–º–æ—Ç—Ä, –æ—Ü–µ–Ω–∫—É —Å–∏–º–ø—Ç–æ–º–æ–≤ –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è –∏ –æ–¥—ã—à–∫–∏ –ø–æ —à–∫–∞–ª–µ MRS.
–ò—Å—Å–ª–µ–¥–æ–≤–∞–Ω–∏–µ —Ñ—É–Ω–∫—Ü–∏–∏ –≤–Ω–µ—à–Ω–µ–≥–æ –¥—ã—Ö–∞–Ω–∏—è (–§–í–î) –≤–∫–ª—é—á–∞–ª–æ –ø—Ä–æ–≤–µ–¥–µ–Ω–∏–µ: –æ–±—â–µ–π –±–æ–¥–∏–ø–ª–µ—Ç–∏–∑–º–æ–≥—Ä–∞—Ñ–∏–∏ (–∏–∑–º–µ—Ä–µ–Ω–∏–µ —Ñ—É–Ω–∫—Ü–∏–æ–Ω–∞–ª—å–Ω–æ–π –æ—Å—Ç–∞—Ç–æ—á–Ω–æ–π –µ–º–∫–æ—Å—Ç–∏ –ª–µ–≥–∫–∏—Ö (–§–û–ï), –æ–ø—Ä–µ–¥–µ–ª–µ–Ω–∏–µ –æ–±—â–µ–π –µ–º–∫–æ—Å—Ç–∏ –ª–µ–≥–∫–∏—Ö (–û–ï–õ), –æ—Å—Ç–∞—Ç–æ—á–Ω–æ–≥–æ –æ–±—ä–µ–º–∞ –ª–µ–≥–∫–∏—Ö (–û–û–õ) –∏ –∏—Ö –æ—Ç–Ω–æ—à–µ–Ω–∏—è (–û–û–õ/–û–ï–õ), —Å–æ–ø—Ä–æ—Ç–∏–≤–ª–µ–Ω–∏–µ –¥—ã—Ö–∞—Ç–µ–ª—å–Ω—ã—Ö –ø—É—Ç–µ–π –Ω–∞ –≤–¥–æ—Ö–µ (–°–î–ü –≤–¥.) –∏ –Ω–∞ –≤—ã–¥–æ—Ö–µ (–°–î–ü –≤—ã–¥.) –∏ —Å–ø–∏—Ä–æ–º–µ—Ç—Ä–∏–∏ —Å –±—Ä–æ–Ω—Ö–æ–¥–∏–ª–∞—Ç–∞—Ü–∏–æ–Ω–Ω—ã–º —Ç–µ—Å—Ç–æ–º (400 –º–∫–≥ —Å–∞–ª—å–±—É—Ç–∞–º–æ–ª–∞) (–∏–∑–º–µ—Ä–µ–Ω–∏–µ –∂–∏–∑–Ω–µ–Ω–Ω–æ–π –µ–º–∫–æ—Å—Ç–∏ –ª–µ–≥–∫–∏—Ö (–ñ–ï–õ), —Ñ–æ—Ä—Å–∏—Ä–æ–≤–∞–Ω–Ω–æ–π –∂–∏–∑–Ω–µ–Ω–Ω–æ–π –µ–º–∫–æ—Å—Ç–∏ –ª–µ–≥–∫–∏—Ö (–§–ñ–ï–õ), –æ–±—ä–µ–º–∞ —Ñ–æ—Ä—Å–∏—Ä–æ–≤–∞–Ω–Ω–æ–≥–æ –≤—ã–¥–æ—Ö–∞ –∑–∞ 1 —Å (–û–§–í1), –∏–Ω–¥–µ–∫—Å–∞ –ì–µ–Ω—Å–ª–µ—Ä–∞ (–û–§–í1/–§–ñ–ï–õ)).
–ò—Å—Å–ª–µ–¥–æ–≤–∞–Ω–∏–µ –∏–Ω–¥—É—Ü–∏—Ä–æ–≤–∞–Ω–Ω–æ–π –º–æ–∫—Ä–æ—Ç—ã –ø—Ä–æ–≤–æ–¥–∏–ª–æ—Å—å –ø—É—Ç–µ–º –ø–æ—Å–ª–µ–¥–æ–≤–∞—Ç–µ–ª—å–Ω–æ–π –∏–Ω–≥–∞–ª—è—Ü–∏–∏ 3%, 4% –∏ 5% —Ä–∞—Å—Ç–≤–æ—Ä–∞ —Ö–ª–æ—Ä–∏–¥–∞ –Ω–∞—Ç—Ä–∏—è —á–µ—Ä–µ–∑ —É–ª—å—Ç—Ä–∞–∑–≤—É–∫–æ–≤–æ–π –Ω–µ–±—É–ª–∞–π–∑–µ—Ä (OMRON, –Ø–ø–æ–Ω–∏—è) —Å–µ–∞–Ω—Å–∞–º–∏ –ø–æ 5 –º–∏–Ω –ø–æ–¥ –∫–æ–Ω—Ç—Ä–æ–ª–µ–º –§–í–î, —Å –ø–æ—Å–ª–µ–¥—É—é—â–∏–º –ø–æ–¥—Å—á–µ—Ç–æ–º –Ω–µ –º–µ–Ω–µ–µ 400 –∫–ª–µ—Ç–æ–∫ –≤ 100 –ø–æ–ª—è—Ö –∑—Ä–µ–Ω–∏—è. –ü–æ–ª—É—á–∏–≤—à–µ–µ—Å—è –∫–æ–ª–∏—á–µ—Å—Ç–≤–æ –∫–ª–µ—Ç–æ–∫ –≤—ã—Ä–∞–∂–∞–ª–∏ –≤ –ø—Ä–æ—Ü–µ–Ω—Ç–∞—Ö [10].
–ò—Å—Å–ª–µ–¥–æ–≤–∞–Ω–∏–µ –æ–∫—Å–∏–¥–∞ –∞–∑–æ—Ç–∞ –≤ –∫–æ–Ω–¥–µ–Ω—Å–∞—Ç–µ –≤—ã–¥—ã—Ö–∞–µ–º–æ–≥–æ –≤–æ–∑–¥—É—Ö–∞ –ø—Ä–æ–≤–æ–¥–∏–ª–æ—Å—å —Å –ø–æ–º–æ—â—å—é –∞–ø–ø–∞—Ä–∞—Ç–∞ N–ûBre–∞th (ppb).
–°—Ç–∞—Ç–∏—Å—Ç–∏—á–µ—Å–∫–∞—è –æ–±—Ä–∞–±–æ—Ç–∫–∞ –ø–æ–ª—É—á–µ–Ω–Ω—ã—Ö –¥–∞–Ω–Ω—ã—Ö –≤—ã–ø–æ–ª–Ω—è–ª–∞—Å—å –ø—Ä–∏ –ø–æ–º–æ—â–∏ –ø—Ä–æ–≥—Ä–∞–º–º—ã Statistica –≤–µ—Ä—Å–∏–∏ 7,0. –ö–æ–ª–∏—á–µ—Å—Ç–≤–µ–Ω–Ω—ã–µ –∑–Ω–∞—á–µ–Ω–∏—è –ø—Ä–µ–¥—Å—Ç–∞–≤–ª–µ–Ω—ã –≤ –≤–∏–¥–µ –º–µ–¥–∏–∞–Ω—ã (–ú–µ) –∏ –∏–Ω—Ç–µ—Ä–∫–≤–∞—Ä—Ç–∏–ª—å–Ω–æ–≥–æ –∏–Ω—Ç–µ—Ä–≤–∞–ª–∞ (Q1 –∏ Q3), –≥–¥–µ Q1 ‚Äî 25-–π –ø—Ä–æ—Ü–µ–Ω—Ç–∏–ª—å, Q3 ‚Äî 75-–π –ø—Ä–æ—Ü–µ–Ω—Ç–∏–ª—å. –ö–∞—á–µ—Å—Ç–≤–µ–Ω–Ω—ã–µ –ø–µ—Ä–µ–º–µ–Ω–Ω—ã–µ –æ–ø–∏—Å–∞–Ω—ã –∞–±—Å–æ–ª—é—Ç–Ω—ã–º–∏ –∏ –æ—Ç–Ω–æ—Å–∏—Ç–µ–ª—å–Ω—ã–º–∏ —á–∞—Å—Ç–æ—Ç–∞–º–∏ (–ø—Ä–æ—Ü–µ–Ω—Ç–∞–º–∏). –ü—Ä–∏ —Å—Ä–∞–≤–Ω–∏—Ç–µ–ª—å–Ω–æ–º –∞–Ω–∞–ª–∏–∑–µ –≥—Ä—É–ø–ø –ø–æ –∫–æ–ª–∏—á–µ—Å—Ç–≤–µ–Ω–Ω—ã–º –ø—Ä–∏–∑–Ω–∞–∫–∞–º –∏—Å–ø–æ–ª—å–∑–æ–≤–∞–ª–∏ –Ω–µ–ø–∞—Ä–∞–º–µ—Ǭ≠—Ä–∏—á–µ—Å–∫–∏–π U-–∫—Ä–∏—Ç–µ—Ä–∏–π –ú–∞–Ω–Ω–∞ ‚Äì –£–∏—Ç–Ω–∏ (–Ω–µ –∑–∞—Ñ–∏–∫—Å–∏—Ä–æ–≤–∞–Ω–æ –Ω–æ—Ä–º–∞–ª—å–Ω–æ–µ —Ä–∞—Å–ø—Ä–µ–¥–µ–ª–µ–Ω–∏–µ –≤—ã–±–æ—Ä–æ–∫, –æ–ø—Ä–µ–¥–µ–ª—è–µ–º–æ–µ –ø–æ –º–µ—Ç–æ–¥—É –ö–æ–ª–º–æ–≥–æ—Ä–æ–≤–∞ ‚Äì –°–º–∏—Ä–Ω–æ–≤–∞ –∏ –∫—Ä–∏—Ç–µ—Ä–∏—é –®–∞–ø–∏—Ä–æ ‚Äì –£–∏–ª–∫–∞). –î–ª—è –æ—Ü–µ–Ω–∫–∏ —Å–≤—è–∑–∏ –ø—Ä–∏–∑–Ω–∞–∫–æ–≤ –ø—Ä–∏–º–µ–Ω—è–ª–∏ –∫–æ—Ä—Ä–µ–ª—è—Ü–∏–æ–Ω–Ω—ã–π –∞–Ω–∞–ª–∏–∑ —Å —Ä–∞—Å—á–µ—Ç–æ–º –∫–æ—Ä—Ä–µ–ª—è—Ü–∏–∏ –ø–æ –º–µ—Ç–æ–¥—É –°–ø–∏—Ä–º–µ–Ω–∞. –Ý–∞–∑–ª–∏—á–∏—è —Å—á–∏—Ç–∞–ª–∏—Å—å —Å—Ç–∞—Ç–∏—Å—Ç–∏—á–µ—Å–∫–∏ –∑–Ω–∞—á–∏–º—ã–º–∏ –ø—Ä–∏ p<0,05.
–Ý–µ–∑—É–ª—å—Ç–∞—Ç—ã –∏ –æ–±—Å—É–∂–¥–µ–Ω–∏–µ
–ù–∞–∏–±–æ–ª–µ–µ –∑–Ω–∞—á–∏–º–∞—è –¥–ª–∏—Ç–µ–ª—å–Ω–æ—Å—Ç—å –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è —Ä–µ–≥–∏—Å—Ç—Ä–∏—Ä–æ–≤–∞–ª–∞—Å—å —É –ø–∞—Ü–∏–µ–Ω—Ç–æ–≤ —Å —Å–æ—á–µ—Ç–∞–Ω–∏–µ–º –ë–ê –∏ –•–û–ë–õ –∏ —Å–æ—Å—Ç–∞–≤–∏–ª–∞ 11 (5,5; 20) –ª–µ—Ç. –°–ª–µ–¥—É–µ—Ç –ø–æ–¥—á–µ—Ä–∫–Ω—É—Ç—å, —á—Ç–æ –•–û–ë–õ —É –±–æ–ª—å–Ω—ã—Ö —Å —Å–æ—á–µ—Ç–∞–Ω–Ω–æ–π –ø–∞—Ç–æ–ª–æ–≥–∏–µ–π, –≤–∫–ª—é—á–µ–Ω–Ω—ã—Ö –≤ –∏—Å—Å–ª–µ–¥–æ–≤–∞–Ω–∏–µ, —Å—Ñ–æ—Ä–º–∏—Ä–æ–≤–∞–ª–∞—Å—å –Ω–∞ —Ñ–æ–Ω–µ –¥–ª–∏—Ç–µ–ª—å–Ω–æ–≥–æ —Ç–µ—á–µ–Ω–∏—è –ë–ê. –ë–æ–ª–µ–µ —Ç–æ–≥–æ, —É –ø–∞—Ü–∏–µ–Ω—Ç–æ–≤ 3-–π –≥—Ä—É–ø–ø—ã –ø–æ–∫–∞–∑–∞—Ç–µ–ª—å –¥–∞–≤–Ω–æ—Å—Ç–∏ –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è –æ–∫–∞–∑–∞–ª—Å—è –Ω–∞–∏–º–µ–Ω—å—à–∏–º –∏ —Å–æ—Å—Ç–∞–≤–∏–ª 4 (3; 5,75) –≥–æ–¥–∞, —á—Ç–æ –º–æ–∂–µ—Ç –±—ã—Ç—å —Å–≤—è–∑–∞–Ω–æ —Å –Ω–µ—Å–≤–æ–µ–≤—Ä–µ–º–µ–Ω–Ω–æ–π –¥–∏–∞–≥–Ω–æ—Å—Ç–∏–∫–æ–π –∏ –ø–æ–∑–¥–Ω–µ–π –æ–±—Ä–∞—â–∞–µ–º–æ—Å—Ç—å—é –ø–∞—Ü–∏–µ–Ω—Ç–æ–≤.–°–æ–≥–ª–∞—Å–Ω–æ –ø–æ–ª—É—á–µ–Ω–Ω—ã–º –¥–∞–Ω–Ω—ã–º, —Ç–∞–±–∞–∫–æ–∫—É—Ä–µ–Ω–∏–µ –∫–∞–∫ —Ñ–∞–∫—Ç–æ—Ä —Ä–∏—Å–∫–∞ –•–û–ë–õ —Ä–µ–≥–∏—Å—Ç—Ä–∏—Ä–æ–≤–∞–ª–æ—Å—å –≤ 100% —Å–ª—É—á–∞–µ–≤ –≤ 3-–π –≥—Ä—É–ø–ø–µ. –ë–æ–ª–µ–µ —Ç–æ–≥–æ, –∏–Ω—Ç–µ–Ω—Å–∏–≤–Ω–æ—Å—Ç—å –∫—É—Ä–µ–Ω–∏—è, –∫–æ—Ç–æ—Ä–∞—è –æ—Ü–µ–Ω–∏–≤–∞–ª–∞—Å—å —Å –ø–æ–º–æ—â—å—é –∏–Ω–¥–µ–∫—Å–∞ –ø–∞—á–∫–∞/–ª–µ—Ç, –±—ã–ª–∞ —Å—É—â–µ—Å—Ç–≤–µ–Ω–Ω–æ –≤—ã—à–µ —É –±–æ–ª—å–Ω—ã—Ö –•–û–ë–õ –≤ —Å—Ä–∞–≤–Ω–µ–Ω–∏–∏ —Å –ø–æ–∫–∞–∑–∞—Ç–µ–ª—è–º–∏ –≤ 1-–π –∏ 2-–π –≥—Ä—É–ø–ø–µ (—Ä=0,003, —Ä=0,006 —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤–µ–Ω–Ω–æ). –í–º–µ—Å—Ç–µ —Å —Ç–µ–º, –Ω–∞–∏–º–µ–Ω—å—à–µ–µ —á–∏—Å–ª–æ –∫—É—Ä—è—â–∏—Ö –ø–∞—Ü–∏–µ–Ω—Ç–æ–≤ –æ—Ç–º–µ—á–∞–ª–æ—Å—å –≤ –≥—Ä—É–ø–ø–µ –±–æ–ª—å–Ω—ã—Ö –ë–ê –∏ —Å–æ—Å—Ç–∞–≤–∏–ª–æ 35%, —á—Ç–æ —Å—É—â–µ—Å—Ç–≤–µ–Ω–Ω–æ –º–µ–Ω—å—à–µ, —á–µ–º –≤–æ 2-–π –∏ 3-–π –≥—Ä—É–ø–ø–µ (—Ä=0,017, —Ä<0,001 —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤–µ–Ω–Ω–æ).
–ü—Ä–∏ –æ—Ü–µ–Ω–∫–µ –∫–ª–∏–Ω–∏—á–µ—Å–∫–∏—Ö —Å–∏–º–ø—Ç–æ–º–æ–≤ —É—Å—Ç–∞–Ω–æ–≤–ª–µ–Ω–æ, —á—Ç–æ —É –ø–∞—Ü–∏–µ–Ω—Ç–æ–≤ —Å —Å–æ—á–µ—Ç–∞–Ω–∏–µ–º –ë–ê –∏ –•–û–ë–õ –∫–æ–ª–∏—á–µ—Å—Ç–≤–æ –ø—Ä–∏—Å—Ç—É–ø–æ–≤ —É–¥—É—à—å—è –≤ —Ç–µ—á–µ–Ω–∏–µ —Å—É—Ç–æ–∫ —Å–æ—Å—Ç–∞–≤–∏–ª–æ 6 (3,5; 8), —á—Ç–æ —Å—É—â–µ—Å—Ç–≤–µ–Ω–Ω–æ –≤—ã—à–µ –≤ —Å—Ä–∞–≤–Ω–µ–Ω–∏–∏ —Å –±–æ–ª—å–Ω—ã–º–∏ 1-–π –≥—Ä—É–ø–ø—ã
(р=0,031) и 2-й группы (р=0,029): 3 (2; 5) и 2 (1; 2,75) соответственно. Наибольшая потребность в короткодействующих β2-агонистах (КДБА) также была зафиксирована при сочетании БА и ХОБЛ (р<0,001). Кроме того, в этой группе отмечена тенденция более частого использования высоких доз ИГКС, которая регистрировалась у 63,2% пациентов в сравнении с больными БА и ХОБЛ (15%, р=0,004 и 42,1%, р=0,046 соответственно) [17].
Одним из признаков, характеризующих тяжесть забо­левания, является количество обострений и госпитализаций в течение года. Согласно полученным результатам, у пациентов с сочетанной патологией отмечается наибольшее количество обострений, требующих госпитализации, которое составило 2 (1,5; 3), тогда как при БА данный показатель равен 1,5 (1; 3,25) (р=0,279) и при ХОБЛ – 2 (1; 2) (р=0,031).
По данным спирометрии, во всех группах регистрировалось нарушение бронхиальной проходимости. Наиболее значимые изменения выявлены у больных ХОБЛ (р<0,05), наименее выраженные – у больных БА. Скоростные показатели среди пациентов с сочетанной патологией принимали промежуточные значения (табл. 2).

Согласно результатам исследования, по данным спирометрии, в группе больных ХОБЛ изменения скоростных показателей ассоциированы с интенсивностью курения, что подтверждено отрицательной корреляционной связью между стажем курения, параметрами ОФВ1 (r=–0,50, р=0,041) и ФЖЕЛ (r=–0,57, р=0,016), а также между индексом пачка/лет, величиной ОФВ1 (r=–0,49, р=0,038) и ОФВ1/ФЖЕЛ (r=–0,48, р=0,039). Кроме того, снижение ОФВ1 сопряжено с нарастанием показателя MRS (r=–0,68, р=0,014).
По данным бодиплетизмографии установлено, чтово всех группах регистрировалось повышение сопротивления дыхательных путей как на вдохе, так и на выдохе (табл. 3), наибольшие показатели регистрировались у больных ХОБЛ, а наименьшие – у больных БА (р<0,05). Высокие показатели ФОЕ и внутригрудного объема (ВГО) при ХОБЛ и сочетании ХОБЛ и БА свидетельствуют о наличии гипер­инфляции легочной ткани [18].

–í –≥—Ä—É–ø–ø–µ –±–æ–ª—å–Ω—ã—Ö –•–û–ë–õ –ø–æ–≤—ã—à–µ–Ω–∏–µ –±—Ä–æ–Ω—Ö–∏–∞–ª—å–Ω–æ–≥–æ —Å–æ–ø—Ä–æ—Ç–∏–≤–ª–µ–Ω–∏—è, –ø–æ –¥–∞–Ω–Ω—ã–º –±–æ–¥–∏–ø–ª–µ—Ç–∏–∑–º–æ–≥—Ä–∞—Ñ–∏–∏, –∞—Å—Å–æ—Ü–∏–∏—Ä–æ–≤–∞–Ω–æ —Å –≤—ã—Ä–∞–∂–µ–Ω–Ω–æ—Å—Ç—å—é –∫–ª–∏–Ω–∏—á–µ—Å–∫–∏—Ö –ø—Ä–æ—è–≤–ª–µ–Ω–∏–π, –æ —á–µ–º —Å–≤–∏–¥–µ—Ç–µ–ª—å—Å—Ç–≤—É–µ—Ç –ø—Ä—è–º–∞—è –∫–æ—Ä—Ä–µ–ª—è—Ü–∏–æ–Ω–Ω–∞—è –≤–∑–∞–∏–º–æ—Å–≤—è–∑—å –º–µ–∂–¥—É –±—Ä–æ–Ω—Ö–∏–∞–ª—å–Ω—ã–º —Å–æ–ø—Ä–æ—Ç–∏–≤–ª–µ–Ω–∏–µ–º –≤—ã–¥–æ—Ö–∞ –∏ —Å—É—Ç–æ—á–Ω–æ–π –ø–æ—Ç—Ä–µ–±–Ω–æ—Å—Ç—å—é –≤ –ö–î–ë–ê (r=0,58; p=0,018). –ö—Ä–æ–º–µ —Ç–æ–≥–æ, –Ω–∞–ª–∏—á–∏–µ –≥–∏–ø–µ—Ä–≤–æ–∑–¥—É—à–Ω–æ—Å—Ç–∏ –ª–µ–≥–æ—á–Ω–æ–π —Ç–∫–∞–Ω–∏ –≤–∑–∞–∏–º–æ—Å–≤—è–∑–∞–Ω–æ —Å –¥–ª–∏—Ç–µ–ª—å–Ω–æ—Å—Ç—å—é –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è, —á—Ç–æ –ø–æ–¥—Ç–≤–µ—Ä–∂–¥–∞–µ—Ç—Å—è –ø—Ä—è–º—ã–º–∏ –∫–æ—Ä—Ä–µ–ª—è—Ü–∏–æ–Ω–Ω—ã–º–∏ –≤–∑–∞–∏–º–æ—Å–≤—è–∑—è–º–∏ —Å –û–û–õ/–û–ï–õ, –û–û–õ (r=0,59, p=0,015; r=0,8, p<0,001 —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤–µ–Ω–Ω–æ). –£ –ø–∞—Ü–∏–µ–Ω—Ç–æ–≤ —Å —Å–æ—á–µ—Ç–∞–Ω–∏–µ–º –ë–ê –∏ –•–û–ë–õ –≤—ã—Ä–∞–∂–µ–Ω–Ω–æ—Å—Ç—å –ª–µ–≥–æ—á–Ω–æ–π –≥–∏–ø–µ—Ä–∏–Ω—Ñ–ª—è—Ü–∏–∏ —Å–æ–ø—Ä—è–∂–µ–Ω–∞ —Å –±–æ–ª–µ–µ —á–∞—Å—Ç–æ–π –ø–æ—Ç—Ä–µ–±–Ω–æ—Å—Ç—å—é –≤ –ø—Ä–µ–ø–∞—Ä–∞—Ç–∞—Ö –Ω–µ–æ—Ç–ª–æ–∂–Ω–æ–π –ø–æ–º–æ—â–∏ (r=0,81, p=0,039). –í –≥—Ä—É–ø–ø–µ –±–æ–ª—å–Ω—ã—Ö –ë–ê —É–≤–µ–ª–∏—á–µ–Ω–∏–µ –∫–æ–ª–∏—á–µ—Å—Ç–≤–∞ –ø—Ä–∏—Å—Ç—É–ø–æ–≤ —É–¥—É—à—å—è –∏ –ø–æ—Ç—Ä–µ–±–Ω–æ—Å—Ç–∏ –≤ –ö–î–ë–ê –≤–∑–∞–∏–º–æ—Å–≤—è–∑–∞–Ω–æ —Å –ø–æ–∫–∞–∑–∞—Ç–µ–ª—è–º–∏ –û–û–õ (r=0,90, —Ä=0,037 –∏ r=0,97, —Ä=0,004 —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤–µ–Ω–Ω–æ).
–°—Ä–µ–¥–∏ –º–∞—Ä–∫–µ—Ä–æ–≤ –≤–æ—Å–ø–∞–ª–µ–Ω–∏—è –¥—ã—Ö–∞—Ç–µ–ª—å–Ω—ã—Ö –ø—É—Ç–µ–π –ø—Ä–∏ –ë–ê –±–æ–ª—å—à–æ–µ –≤–Ω–∏–º–∞–Ω–∏–µ —É–¥–µ–ª—è–µ—Ç—Å—è –æ–ø—Ä–µ–¥–µ–ª–µ–Ω–∏—é –æ–∫—Å–∏–¥–∞ –∞–∑–æ—Ç–∞ –≤ –≤—ã–¥—ã—Ö–∞–µ–º–æ–º –≤–æ–∑–¥—É—Ö–µ, –ø–æ–≤—ã—à–µ–Ω–Ω–æ–µ —Å–æ–¥–µ—Ä–∂–∞–Ω–∏–µ –∫–æ—Ç–æ—Ä–æ–≥–æ —Å—á–∏—Ç–∞—é—Ç –Ω–∞–∏–±–æ–ª–µ–µ —Ä–∞–Ω–Ω–∏–º –∏ –¥–æ—Å—Ç–æ–≤–µ—Ä–Ω—ã–º –º–∞—Ä–∫–µ—Ä–æ–º –∞–ª–ª–µ—Ä–≥–∏—á–µ—Å–∫–æ–≥–æ –≤–æ—Å–ø–∞–ª–µ–Ω–∏—è –¥—ã—Ö–∞—Ç–µ–ª—å–Ω—ã—Ö –ø—É—Ç–µ–π [12, 19]. –ü—Ä–∏ –•–û–ë–õ –µ–¥–∏–Ω–∏—á–Ω—ã–µ –¥–∞–Ω–Ω—ã–µ –ø—Ä–æ—Ç–∏–≤–æ—Ä–µ—á–∏–≤—ã–µ, –∞ –ø—Ä–∏ —Å–æ—á–µ—Ç–∞–Ω–∏–∏ –ë–ê –∏ –•–û–ë–õ –∏ –≤–æ–≤—Å–µ –æ—Ç—Å—É—Ç—Å—Ç–≤—É—é—Ç.
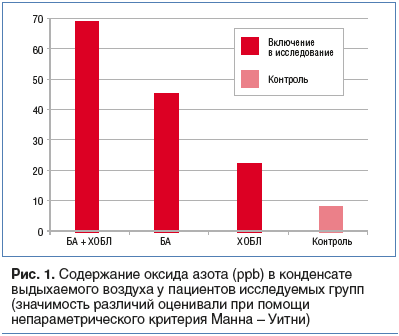
–°–æ–≥–ª–∞—Å–Ω–æ –ø–æ–ª—É—á–µ–Ω–Ω—ã–º –¥–∞–Ω–Ω—ã–º, —É—Ä–æ–≤–µ–Ω—å –æ–∫—Å–∏–¥–∞ –∞–∑–æ—Ç–∞ –≤ –≤—ã–¥—ã—Ö–∞–µ–º–æ–º –≤–æ–∑–¥—É—Ö–µ —Å—É—â–µ—Å—Ç–≤–µ–Ω–Ω–æ –≤—ã—à–µ –ø—Ä–∏ —Å–æ—á–µ—Ç–∞–Ω–Ω–æ–π –ø–∞—Ç–æ–ª–æ–≥–∏–∏ –≤ —Å—Ä–∞–≤–Ω–µ–Ω–∏–∏ —Å –ë–ê –∏ –•–û–ë–õ –≤–∑—è—Ç—ã—Ö –≤ –æ—Ç–¥–µ–ª—å–Ω–æ—Å—Ç–∏ (—Ä<0,001 –∏ —Ä=0,003 —Å–æ–æ—Ç–≤–µ—Ç—Å—Ç–≤–µ–Ω–Ω–æ) (—Ä–∏—Å. 1) –∏ –∞—Å—Å–æ—Ü–∏–∏—Ä–æ–≤–∞–Ω–æ —Å –∫–æ–ª–∏—á–µ—Å—Ç–≤–æ–º –æ–±–æ—Å—Ç—Ä–µ–Ω–∏–π –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è (r=0,60, —Ä=0,022) [12], —á—Ç–æ —Å–≤–∏–¥–µ—Ç–µ–ª—å—Å—Ç–≤—É–µ—Ç –æ–± —ç–æ–∑–∏–Ω–æ—Ñ–∏–ª—å–Ω–æ–º —Ö–∞—Ä–∞–∫—Ç–µ—Ä–µ –≤–æ—Å–ø–∞–ª–µ–Ω–∏—è –≤ –¥—ã—Ö–∞—Ç–µ–ª—å–Ω—ã—Ö –ø—É—Ç—è—Ö.
Отклонения клеточного состава индуцированной мокроты от нормы могут характеризовать тип воспаления, который определяют по содержанию в мокроте эффекторных воспалительных клеток — эозинофилов, нейтрофилов, лимфоцитов, макрофагов. Их количество зависит от активности процесса, т. к. именно они первыми реагируют на патогенный агент и запускают воспаление [20]. Одним из основных методов исследования является подсчет клеток мокроты и формирование цитограммы, в которой указывается процентное содержание каждого типа клеток. В результате многочисленных исследований выделили 4 клеточных фенотипа: 1) эозинофильный (≥2% эозинофилов); 2) нейтрофильный (≥61% нейтрофилов); 3) смешанный; 4) неэозинофильный (эозинофилов <2%) и ненейтрофильный (нейтрофилов <61%) [21].
–¢–∞–∫, –≤ —Ö–æ–¥–µ –∞–Ω–∞–ª–∏–∑–∞ —Ü–∏—Ç–æ–≥—Ä–∞–º–º—ã –∏–Ω–¥—É—Ü–∏—Ä–æ–≤–∞–Ω–Ω–æ–π –º–æ–∫—Ä–æ—Ç—ã –Ω–∞–∏–±–æ–ª—å—à–µ–µ —Å–æ–¥–µ—Ä–∂–∞–Ω–∏–µ —ç–æ–∑–∏–Ω–æ—Ñ–∏–ª–æ–≤ –æ—Ç–º–µ—á–∞–ª–æ—Å—å –ø—Ä–∏ –ë–ê –∏ –ø—Ä–∏ —Å–æ—á–µ—Ç–∞–Ω–Ω–æ–π –ø–∞—Ç–æ–ª–æ–≥–∏–∏ (—Ç–∞–±–ª. 4), —á—Ç–æ —Å–≤–∏–¥–µ—Ç–µ–ª—å—Å—Ç–≤—É–µ—Ç –æ–± —ç–æ–∑–∏–Ω–æ—Ñ–∏–ª—å–Ω–æ–º —Ç–∏–ø–µ –≤–æ—Å–ø–∞–ª–µ–Ω–∏—è [21].
–ù–µ–π—Ç—Ä–æ—Ñ–∏–ª—ã —Ä–∞—Å—Å–º–∞—Ç—Ä–∏–≤–∞—é—Ç—Å—è –Ω–µ —Ç–æ–ª—å–∫–æ –∫–∞–∫ –∫–ª–µ—Ç–∫–∏, –≤—ã–ø–æ–ª–Ω—è—é—â–∏–µ —Ñ—É–Ω–∫—Ü–∏—é —Ñ–∞–≥–æ—Ü–∏—Ç–æ–∑–∞ –∏ –ø—Ä–æ–¥—É—Ü–∏—Ä—É—é—â–∏–µ —Ü–∏—Ç–æ—Ç–æ–∫—Å–∏—á–µ—Å–∫–∏–µ –≤–µ—â–µ—Å—Ç–≤–∞ –ø—Ä–∏ –≤–æ—Å–ø–∞–ª–µ–Ω–∏–∏ [19]. –û–Ω–∏ —Å–µ–∫—Ä–µ—Ç–∏—Ä—É—é—Ç –Ω–µ—Å–∫–æ–ª—å–∫–æ –ø—Ä–æ—Ç–µ–∏–Ω–∞–∑, —Ç–∞–∫–∏—Ö, –∫–∞–∫ –Ω–µ–π—Ç—Ä–æ—Ñ–∏–ª—å–Ω–∞—è –ø—Ä–æ—Ç–µ–∏–Ω–∞–∑–∞, —ç–ª–∞—Å—Ç–∞–∑–∞, –Ω–µ–π—Ç—Ä–æ—Ñ–∏–ª—å–Ω—ã–π –∫–∞—Ç–µ–ø—Å–∏–Ω G –∏ –¥—Ä., –∫–æ—Ç–æ—Ä—ã–µ –≤—ã–∑—ã–≤–∞—é—Ç –¥–µ—Å—Ç—Ä—É–∫—Ü–∏—é –ø–∞—Ä–µ–Ω—Ö–∏–º—ã, —É—á–∞—Å—Ç–≤—É—é—Ç –≤ –¥–µ–≥—Ä–∞–¥–∞—Ü–∏–∏ —ç–ª–∞—Å—Ç–∏–Ω–∞ –∏ —Ç–µ–º —Å–∞–º—ã–º –ø—Ä–∏–≤–æ–¥—è—Ç –∫ —Ä–∞–∑–≤–∏—Ç–∏—é —ç–º—Ñ–∏–∑–µ–º—ã [22]. –ü–æ –¥–∞–Ω–Ω—ã–º –ì.–ë. –§–µ–¥–æ—Å–µ–µ–≤–∞ –∏ —Å–æ–∞–≤—Ç., –ø—Ä–∏ —Å–æ—á–µ—Ç–∞–Ω–∏–∏ –ë–ê –∏ –•–û–ë–õ –Ω–µ–π—Ç—Ä–æ—Ñ–∏–ª—å–Ω—ã–π —Ñ–µ–Ω–æ—Ç–∏–ø –º–æ–∫—Ä–æ—Ç—ã –≤—Å—Ç—Ä–µ—á–∞–µ—Ç—Å—è —Å —á–∞—Å—Ç–æ—Ç–æ–π 59% [22] –∏ –º–æ–∂–µ—Ç —è–≤–ª—è—Ç—å—Å—è –∏–Ω–¥–∏–∫–∞—Ç–æ—Ä–æ–º —Ç—è–∂–µ–ª–æ–≥–æ —Ç–µ—á–µ–Ω–∏—è –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è. –î–ª—è —Ç–∞–∫–∏—Ö –±–æ–ª—å–Ω—ã—Ö —Ö–∞—Ä–∞–∫—Ç–µ—Ä–Ω–∞ –Ω–∏–∑–∫–∞—è —ç—Ñ—Ñ–µ–∫—Ç–∏–≤–Ω–æ—Å—Ç—å –ª–µ—á–µ–Ω–∏—è –ò–ì–ö–° [23]. –°–æ–≥–ª–∞—Å–Ω–æ –ø–æ–ª—É—á–µ–Ω–Ω—ã–º –¥–∞–Ω–Ω—ã–º, –≤—ã—Å–æ–∫–æ–µ —Å–æ–¥–µ—Ä–∂–∞–Ω–∏–µ –Ω–µ–π—Ç—Ä–æ—Ñ–∏–ª—å–Ω—ã—Ö –∫–ª–µ—Ç–æ–∫ –æ—Ç–º–µ—á–∞–µ—Ç—Å—è —É –±–æ–ª—å–Ω—ã—Ö –•–û–ë–õ –∏ —É –ø–∞—Ü–∏–µ–Ω—Ç–æ–≤ —Å —Å–æ—á–µ—Ç–∞–Ω–∏–µ–º –ë–ê –∏ –•–û–ë–õ (—Å–º. —Ç–∞–±–ª. 4). –ë–æ–ª–µ–µ —Ç–æ–≥–æ, –≤–æ 2-–π –≥—Ä—É–ø–ø–µ —Å–æ–¥–µ—Ä–∂–∞–Ω–∏–µ –Ω–µ–π—Ç—Ä–æ—Ñ–∏–ª–æ–≤ –≤ –∏–Ω–¥—É—Ü–∏—Ä–æ–≤–∞–Ω–Ω–æ–π –º–æ–∫—Ä–æ—Ç–µ –∞—Å—Å–æ—Ü–∏–∏—Ä–æ–≤–∞–Ω–æ —Å –ø–æ–≤—ã—à–µ–Ω–∏–µ–º –æ–±—ä–µ–º–∞ –±–∞–∑–∏—Å–Ω–æ–π —Ç–µ—Ä–∞–ø–∏–∏, —á—Ç–æ –ø–æ–¥—Ç–≤–µ—Ä–∂–¥–µ–Ω–æ –ø—Ä—è–º–æ–π –∫–æ—Ä—Ä–µ–ª—è—Ü–∏–æ–Ω–Ω–æ–π —Å–≤—è–∑—å—é –º–µ–∂–¥—É –∫–æ–ª–∏—á–µ—Å—Ç–≤–æ–º –¥–∞–Ω–Ω—ã—Ö –∫–ª–µ—Ç–æ–∫ –∏ –¥–æ–∑–æ–π –ò–ì–ö–° (r=0,70, —Ä=0,021).

–¢–∞–∫–∏–º –æ–±—Ä–∞–∑–æ–º, –∫–ª–µ—Ç–æ—á–Ω—ã–π —Å–æ—Å—Ç–∞–≤ –∏–Ω–¥—É—Ü–∏—Ä–æ–≤–∞–Ω–Ω–æ–π –º–æ–∫—Ä–æ—Ç—ã –º–µ–Ω—è–µ—Ç—Å—è –≤ –∑–∞–≤–∏—Å–∏–º–æ—Å—Ç–∏ –æ—Ç –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è. –ù–∞–∏–±–æ–ª—å—à–∏–µ –∏–∑–º–µ–Ω–µ–Ω–∏—è –≤ —Ü–∏—Ç–æ–≥—Ä–∞–º–º–µ –ø—Ä–µ—Ç–µ—Ä–ø–µ–≤–∞–µ—Ç —Å–æ–¥–µ—Ä–∂–∞–Ω–∏–µ —ç–æ–∑–∏–Ω–æ—Ñ–∏–ª–æ–≤ –∏ –Ω–µ–π—Ç—Ä–æ—Ñ–∏–ª–æ–≤. –ù–∞–ª–∏—á–∏–µ —Ä–∞–∑–Ω–æ–æ–±—Ä–∞–∑–Ω–æ–≥–æ —Å–ø–µ–∫—Ç—Ä–∞ —ç—Ñ—Ñ–µ–∫—Ç–æ—Ä–Ω—ã—Ö –∫–ª–µ—Ç–æ–∫ –ø—Ä–∏ —Å–æ—á–µ—Ç–∞–Ω–∏–∏ –ë–ê –∏ –•–û–ë–õ, –≤–∫–ª—é—á–∞—è —ç–æ–∑–∏–Ω–æ—Ñ–∏–ª—ã –∏ –Ω–µ–π—Ç—Ä–æ—Ñ–∏–ª—ã, —Å–≤–∏–¥–µ—Ç–µ–ª—å—Å—Ç–≤—É–µ—Ç –æ —Å–º–µ—à–∞–Ω–Ω–æ–º –ø–∞—Ç—Ç–µ—Ä–Ω–µ –≤–æ—Å–ø–∞–ª–µ–Ω–∏—è.
–í—ã–≤–æ–¥—ã
–°—Ä–∞–≤–Ω–∏—Ç–µ–ª—å–Ω—ã–π –∞–Ω–∞–ª–∏–∑ –ø–æ–∫–∞–∑–∞–ª, —á—Ç–æ –ø—Ä–∏ —Å–æ—á–µ—Ç–∞–Ω–∏–∏ –ë–ê –∏ –•–û–ë–õ –æ—Ç–º–µ—á–∞–µ—Ç—Å—è –±–æ–ª–µ–µ –≤—ã—Ä–∞–∂–µ–Ω–Ω–∞—è –≥–∏–ø–µ—Ä–≤–æ–∑–¥—É—à–Ω–æ—Å—Ç—å, –ø—Ä–æ—è–≤–ª—è—é—â–∞—è—Å—è –ø–æ–≤—ã—à–µ–Ω–∏–µ–º —Ñ—É–Ω–∫—Ü–∏–æ–Ω–∞–ª—å–Ω–æ–π –æ—Å—Ç–∞—Ç–æ—á–Ω–æ–π –µ–º–∫–æ—Å—Ç–∏ –ª–µ–≥–∫–∏—Ö –∏ –≤–Ω—É—Ç—Ä–∏–≥—Ä—É–¥–Ω–æ–≥–æ –æ–±—ä–µ–º–∞, —á—Ç–æ –º–æ–∂–µ—Ç —Å–≤–∏–¥–µ—Ç–µ–ª—å—Å—Ç–≤–æ–≤–∞—Ç—å –æ –ø–æ—Ä–∞–∂–µ–Ω–∏–∏ –¥–∏—Å—Ç–∞–ª—å–Ω—ã—Ö –±—Ä–æ–Ω—Ö–æ–≤ –∏ —Ä–∞–∑–≤–∏—Ç–∏–∏ –ª–µ–≥–æ—á–Ω–æ–π –≥–∏–ø–µ—Ä–∏–Ω—Ñ–ª—è—Ü–∏–∏.–ü—Ä–∏ —Å–æ—á–µ—Ç–∞–Ω–Ω–æ–π –ø–∞—Ç–æ–ª–æ–≥–∏–∏ –æ—Ç–º–µ—á–∞–µ—Ç—Å—è –ø–æ–≤—ã—à–µ–Ω–∏–µ —É—Ä–æ–≤–Ω—è –æ–∫—Å–∏–¥–∞ –∞–∑–æ—Ç–∞ –≤ –≤—ã–¥—ã—Ö–∞–µ–º–æ–º –≤–æ–∑–¥—É—Ö–µ, –∫–æ—Ç–æ—Ä–æ–µ –≤–∑–∞–∏–º–æ—Å–≤—è–∑–∞–Ω–æ —Å –∫–æ–ª–∏—á–µ—Å—Ç–≤–æ–º –æ–±–æ—Å—Ç—Ä–µ–Ω–∏–π –∑–∞–±–æ–ª–µ–≤–∞–Ω–∏—è.
–•—Ä–æ–Ω–∏—á–µ—Å–∫–∏–π –≤–æ—Å–ø–∞–ª–∏—Ç–µ–ª—å–Ω—ã–π –ø—Ä–æ—Ü–µ—Å—Å –±—Ä–æ–Ω—Ö–æ–ª–µ–≥–æ—á–Ω–æ–π —Å–∏—Å—Ç–µ–º—ã –ø—Ä–∏ —Å–æ—á–µ—Ç–∞–Ω–∏–∏ –ë–ê –∏ –•–û–ë–õ —Ö–∞—Ä–∞–∫—Ç–µ—Ä–∏–∑—É–µ—Ç—Å—è –Ω–∞—Ä—É—à–µ–Ω–∏–µ–º —Ñ–∏–∑–∏–æ–ª–æ–≥–∏—á–µ—Å–∫–∏—Ö —Å–æ–æ—Ç–Ω–æ—à–µ–Ω–∏–π –æ—Ç–¥–µ–ª—å–Ω—ã—Ö –∫–ª–µ—Ç–æ—á–Ω—ã—Ö –ø–æ–ø—É–ª—è—Ü–∏–π –≤ –∏–Ω–¥—É—Ü–∏—Ä–æ–≤–∞–Ω–Ω–æ–π –º–æ–∫—Ä–æ—Ç–µ –≤ —Å—Ç–æ—Ä–æ–Ω—É —É–≤–µ–ª–∏—á–µ–Ω–∏—è –∫–æ–ª–∏—á–µ—Å—Ç–≤–∞ —ç–æ–∑–∏–Ω–æ—Ñ–∏–ª–æ–≤ –∏ –Ω–µ–π—Ç—Ä–æ—Ñ–∏–ª–æ–≤, —á—Ç–æ –≤–∑–∞–∏–º–æ—Å–≤—è–∑–∞–Ω–æ —Å —É–≤–µ–ª–∏—á–µ–Ω–∏–µ–º –æ–±—ä–µ–º–∞ –±–∞–∑–∏—Å–Ω–æ–π —Ç–µ—Ä–∞–ø–∏–∏.








.gif)



