–С–Њ–ї—М –≤ –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є —Б–њ–Є–љ—Л вАУ –Њ–і–љ–∞ –Є–Ј —Б–∞–Љ—Л—Е —З–∞—Б—В—Л—Е –њ—А–Є—З–Є–љ –Њ–±—А–∞—Й–µ–љ–Є—П –Ј–∞ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ–Њ–Љ–Њ—Й—М—О. –≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є –≤—Л—Б–Њ–Ї—Г—О —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–Є –≤ –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є —Б–њ–Є–љ—Л, –Ї–Њ—В–Њ—А–∞—П –і–Њ—Б—В–Є–≥–∞–µ—В 40вАУ80%, –∞ –µ–ґ–µ–≥–Њ–і–љ–∞—П –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М —Б–Њ—Б—В–∞–≤–ї—П–µ—В 5%. –Ч–∞—В—А–∞—В—Л –љ–∞ –ї–µ—З–µ–љ–Є–µ –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ –≤ 3 —А–∞–Ј–∞ –њ—А–µ–≤—Л—И–∞—О—В –Ј–∞—В—А–∞—В—Л –љ–∞ –ї–µ—З–µ–љ–Є–µ –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є [1].
–Ъ–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–Њ-–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –≤ —Б–≤–Њ–µ–є –Њ—Б–љ–Њ–≤–µ –Љ–Њ–≥—Г—В –Є–Љ–µ—В—М —Б–∞–Љ—Л–µ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –њ—А–Є—З–Є–љ—Л: —Н—В–Њ –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ-–і–Є—Б—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –њ—А–Њ—В—А—Г–Ј–Є–Є –Є —Н–Ї—Б—В—А—Г–Ј–Є–Є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –і–Є—Б–Ї–Њ–≤, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –Њ–±—К–µ–Љ–љ—Л–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ [2, 3]. –†–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ –≤—Л—И–µ–љ–∞–Ј–≤–∞–љ–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —П–≤–ї—П–µ—В—Б—П —Б—Г–ґ–µ–љ–Є–µ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П –Є —Б–і–∞–≤–ї–µ–љ–Є–µ –Ї–Њ—А–µ—И–Ї–Њ–≤—Л—Е –≤–µ–љ —Б —П–≤–ї–µ–љ–Є—П–Љ–Є –≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ –Ј–∞—Б—В–Њ—П. –Т–Њ–Ј–љ–Є–Ї–∞—О—В –Љ–µ—Б—В–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є —Б –Њ—В–µ–Ї–Њ–Љ –Њ–Ї—А—Г–ґ–∞—О—Й–Є—Е —В–Ї–∞–љ–µ–є, –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ —А–∞–Ј–≤–Є—В–Є–µ–Љ –ї–Њ–Ї–∞–ї—М–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є –Є—И–µ–Љ–Є–µ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ-–љ–µ—А–≤–љ–Њ–≥–Њ –њ—Г—З–Ї–∞ [4, 5]. –Т—Л—И–µ–Њ–њ–Є—Б–∞–љ–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л –≤—Л–Ј—Л–≤–∞—О—В –Є –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—В –њ—А–Њ—Ж–µ—Б—Б –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є–Є, –∞ –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –Є –±–Њ–ї–µ–µ –≥—А—Г–±–Њ–µ –∞–Ї—Б–Њ–љ–∞–ї—М–љ–Њ–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ –Ї–Њ—А–µ—И–Ї–Њ–≤, —З—В–Њ –≤ –Ї–ї–Є–љ–Є–Ї–µ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є, –љ–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Њ–±—А–∞—В–Є–Љ–Њ–є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є [3]. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П —Б—В–Њ–є–Ї–Є–Љ –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–Љ –±–Њ–ї–µ–≤—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –≤—Л–њ–∞–і–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–≥–Њ –Ї–Њ—А–µ—И–Ї–∞. –Ф–ї—П –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –і–Є–∞–≥–љ–Њ–Ј–∞ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П —В–∞–Ї–Є–µ –Љ–µ—В–Њ–і—Л, –Ї–∞–Ї –Љ–∞–≥–љ–Є—В–љ–Њ-—А–µ–Ј–Њ–љ–∞–љ—Б–љ–∞—П —В–Њ–Љ–Њ–≥—А–∞—Д–Є—П, —Б—В–Є–Љ—Г–ї—П—Ж–Є–Њ–љ–љ–∞—П –Є –Є–≥–Њ–ї—М—З–∞—В–∞—П —Н–ї–µ–Ї—В—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є—П.
–Т –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–Њ-–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П–Љ–Є –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П —И–Є—А–Њ–Ї–Є–є —Б–њ–µ–Ї—В—А –њ—А–µ–њ–∞—А–∞—В–Њ–≤: –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Э–Я–Т–Я), –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞, –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В—Л, –∞–љ—В–Є–Ї–Њ–љ–≤—Г–ї—М—Б–∞–љ—В—Л, —Е–Њ–љ–і—А–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А—Л, –і–Є—Г—А–µ—В–Є–Ї–Є [6, 7]. –Т—Б–µ –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ –Њ–Ї–∞–Ј—Л–≤–∞—О—В –љ–µ–њ—А—П–Љ–Њ–µ –њ—А–Њ—В–Є–≤–Њ–Њ—В–µ—З–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —Г–Љ–µ–љ—М—И–∞—О—В –Њ—В–µ–Ї –±–µ–Ј –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ —Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б—В–µ–љ–Ї—Г. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –і–ї—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –≤–∞–Ј–Њ–≥–µ–љ–љ–Њ–≥–Њ –Њ—В–µ–Ї–∞, –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –Є —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –љ–Є–Љ–Є –±–Њ–ї–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л –њ—А–µ–њ–∞—А–∞—В—Л —Б –њ—А—П–Љ—Л–Љ –њ—А–Њ—В–Є–≤–Њ–Њ—В–µ—З–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, –Ї–Њ—В–Њ—А—Л–µ —Г–Љ–µ–љ—М—И–∞—О—В –Њ—В–µ–Ї –њ—Г—В–µ–Љ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ —Б—В–µ–љ–Ї—Г –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤.
–Я—А–µ–њ–∞—А–∞—В–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ—А—П–Љ–Њ–µ –њ—А–Њ—В–Є–≤–Њ–Њ—В–µ—З–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ, —П–≤–ї—П–µ—В—Б—П L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В вАУ –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ—Л–є –∞–љ–≥–Є–Њ–њ—А–Њ—В–µ–Ї—В–Њ—А –і–ї—П –ї–µ—З–µ–љ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Њ—В–µ–Ї–Њ–≤ –ї—О–±–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є, –≤ —В. —З. –њ—А–Є –і–Њ—А—Б–∞–ї–≥–Є—П—Е.
L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В вАУ —Н—В–Њ –≤–Њ–і–Њ—А–∞—Б—В–≤–Њ—А–Є–Љ–∞—П —Б–Њ–ї—М –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л –ї–Є–Ј–Є–љ–∞ –Є —Б–∞–њ–Њ–љ–Є–љ–∞ –Ї–∞—И—В–∞–љ–∞ –Ї–Њ–љ—Б–Ї–Њ–≥–Њ —Н—Б—Ж–Є–љ–∞. –Я–Њ —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —Б–≤–Њ–є—Б—В–≤–∞–Љ –њ—А–µ–њ–∞—А–∞—В –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Ї–∞–њ–Є–ї–ї—П—А–Њ—Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—Й–Є–Љ —Б—А–µ–і—Б—В–≤–∞–Љ. –Ю—Б–љ–Њ–≤–љ—Л–Љ –і–µ–є—Б—В–≤—Г—О—Й–Є–Љ –≤–µ—Й–µ—Б—В–≤–Њ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ —П–≤–ї—П–µ—В—Б—П —Н—Б—Ж–Є–љ. LвАУ–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В —Б–љ–Є–ґ–∞–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–Є–Ј–Њ—Б–Њ–Љ–∞–ї—М–љ—Л—Е –≥–Є–і—А–Њ–ї–∞–Ј, –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞–µ—В —А–∞—Б—Й–µ–њ–ї–µ–љ–Є–µ –Љ—Г–Ї–Њ–њ–Њ–ї–Є—Б–∞—Е–∞—А–Є–і–Њ–≤ –≤ —Б—В–µ–љ–Ї–∞—Е –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤ –Є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –љ–Њ—А–Љ–∞–ї–Є–Ј—Г–µ—В –њ–Њ–≤—Л—И–µ–љ–љ—Г—О –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є [8]. –≠—Б—Ж–Є–љ –Є–љ–≥–Є–±–Є—А—Г–µ—В –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Д–Њ—Б—Д–Њ–ї–Є–њ–∞–Ј—Л –Р2, —А–∞–Ј—А—Г—И–∞—О—Й–µ–є —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і—Л –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ –Є –Ј–∞–њ—Г—Б–Ї–∞—О—Й–µ–є –Ї–∞—Б–Ї–∞–і –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П [9]. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Г–ї—Г—З—И–∞–µ—В—Б—П –∞—А—В–µ—А–Є–∞–ї—М–љ—Л–є –Є –≤–µ–љ–Њ–Ј–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –≤ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–Љ —А—Г—Б–ї–µ, —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –≤–µ–љ–Њ–Ј–љ—Л–є –Ј–∞—Б—В–Њ–є. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –Ї—Г–њ–Є—А—Г–µ—В —Г–ґ–µ –≤–Њ–Ј–љ–Є–Ї—И–Є–є –Њ—В–µ–Ї, –љ–Њ –Є –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞–µ—В –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –љ–Њ–≤–Њ–≥–Њ [10]. –†—П–і–Њ–Љ –∞–≤—В–Њ—А–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, —З–µ—А–µ–њ–љ–Њ-–Љ–Њ–Ј–≥–Њ–≤—Л—Е —В—А–∞–≤–Љ–∞—Е [10вАУ15].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В —П–≤–ї—П–µ—В—Б—П —Б—А–µ–і—Б—В–≤–Њ–Љ —Б —Г–љ–Є–≤–µ—А—Б–∞–ї—М–љ—Л–Љ –њ—А–Њ—В–Є–≤–Њ–Њ—В–µ—З–љ—Л–Љ, –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ –Є –∞–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –µ–≥–Њ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ—Б—В—А—Л—Е –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–Њ-–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–є.
–¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П вАУ –Є–Ј—Г—З–Є—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М LвАУ–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ—Б—В—А—Л—Е –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–Њ-–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е –і–Є—Б—В—А–Њ—Д–Є—З–µ—Б–Ї–Є–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –і–Є—Б–Ї–∞.
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –љ–∞ –±–∞–Ј–µ –У–Њ—Б—Г–і–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–≥–Њ —Г—З—А–µ–ґ–і–µ–љ–Є—П –Ј–і—А–∞–≤–Њ–Њ—Е—А–∞–љ–µ–љ–Є—П ¬Ђ–†–µ—Б–њ—Г–±–ї–Є–Ї–∞–љ—Б–Ї–Є–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Ж–µ–љ—В—А¬ї (–У–Р–£–Ч –†–Ъ–Э–¶) –≤ –њ–µ—А–Є–Њ–і —Б 2012 –њ–Њ 2014 –≥. –Ъ—А–Є—В–µ—А–Є—П–Љ–Є –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —П–≤–Є–ї–Є—Б—М: –љ–∞–ї–Є—З–Є–µ –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–Њ-–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є L5, S1 –≤—Б–ї–µ–і—Б—В–≤–Є–µ –і–Є—Б—В—А–Њ—Д–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –і–Є—Б–Ї–Њ–≤, –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–є –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ —Б –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М—О –љ–µ –Љ–µ–љ–µ–µ 30 –±–∞–ї–ї–Њ–≤ –Є–Ј 100 –њ–Њ –≤–Є–Ј—Г–∞–ї—М–љ–Њ–є –∞–љ–∞–ї–Њ–≥–Њ–≤–Њ–є —И–Ї–∞–ї–µ (–Т–Р–®). –Ъ—А–Є—В–µ—А–Є—П–Љ–Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Є: –≤–Њ–Ј—А–∞—Б—В –Љ–Њ–ї–Њ–ґ–µ 18 –ї–µ—В, –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М, –ї–∞–Ї—В–∞—Ж–Є—П, —В—П–ґ–µ–ї–∞—П —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–∞—П –њ–∞—В–Њ–ї–Њ–≥–Є—П (—П–Ј–≤–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є –≤ —Б—В–∞–і–Є–Є –Њ–±–Њ—Б—В—А–µ–љ–Є—П —А–µ–∞–Ї—Ж–Є–Є, –љ–∞—А—Г—И–µ–љ–Є—П —Б–Є—Б—В–µ–Љ—Л –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–Є—Б—В–µ–Љ—Л –Ї—А–Њ–≤–µ—В–≤–Њ—А–µ–љ–Є—П, —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В, —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –љ–µ–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–∞—П –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П, –љ–∞—А—Г—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ–Ї, —Б–Є—Б—В–µ–Љ–љ—Л–µ –Ї–Њ–ї–ї–∞–≥–µ–љ–Њ–Ј—Л, –Њ–љ–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П), –∞ —В–∞–Ї–ґ–µ —А–µ–∞–Ї—Ж–Є—П –≥–Є–њ–µ—А—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ї –Э–Я–Т–Я –Є L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В—Г.
–Я–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –љ–∞—Е–Њ–і–Є–ї–Є—Б—М 180 (72 (40%) –ґ–µ–љ—Й–Є–љ—Л –Є 108 (60%) –Љ—Г–ґ—З–Є–љ) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 30 –і–Њ 65 –ї–µ—В (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 46,6¬±3,3 –≥–Њ–і–∞). –Ь–µ—В–Њ–і–Њ–Љ —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є –±—Л–ї–Є –≤—Л–і–µ–ї–µ–љ—Л 2 –≥—А—Г–њ–њ—Л –њ–Њ 90 —З–µ–ї–Њ–≤–µ–Ї, —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л—Е –њ–Њ –≤–Њ–Ј—А–∞—Б—В—Г, –њ–Њ–ї—Г, –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, —Б—В–µ–њ–µ–љ–Є –љ–∞—А—Г—И–µ–љ–Є—П –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д—Г–љ–Ї—Ж–Є–є.
–Я–∞—Ж–Є–µ–љ—В–∞–Љ –±—Л–ї–Є –њ—А–Њ–≤–µ–і–µ–љ—Л –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є –љ–µ–є—А–Њ–Њ—А—В–Њ–њ–µ–і–Є—З–µ—Б–Ї–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –Ї–Њ–љ—В—А–Њ–ї—М –Њ–±—Й–µ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –∞–љ–∞–ї–Є–Ј–Њ–≤, –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї—А–Њ–≤–Є. –Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Б—В–∞—В—Г—Б –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –њ—А–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–Є, –љ–∞ 3-–є –Є 10-–є –і–µ–љ—М –ї–µ—З–µ–љ–Є—П. –£ –≤—Б–µ—Е –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –і–Є–∞–≥–љ–Њ–Ј —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї –Ь–Ъ–С-10 –Є –±—Л–ї –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ –і–∞–љ–љ—Л–Љ–Є –љ–µ–є—А–Њ–≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є–Є, —Б—В–Є–Љ—Г–ї—П—Ж–Є–Њ–љ–љ–Њ–є –Є –Є–≥–Њ–ї—М—З–∞—В–Њ–є —Н–ї–µ–Ї—В—А–Њ–љ–µ–є—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є–Є.
–Я–∞—Ж–Є–µ–љ—В—Л –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –њ–Њ–ї—Г—З–∞–ї–Є –±–∞–Ј–Є—Б–љ—Г—О —В–µ—А–∞–њ–Є—О —Б–Њ–≥–ї–∞—Б–љ–Њ —Б—В–∞–љ–і–∞—А—В–∞–Љ –ї–µ—З–µ–љ–Є—П, –њ—А–Є–љ—П—В—Л–Љ –Є —Г—В–≤–µ—А–ґ–і–µ–љ–љ—Л–Љ –Ь–Ч –†–§, –Ї–Њ—В–Њ—А—Л–µ –≤–Ї–ї—О—З–∞—О—В –≤ —Б–µ–±—П –Э–Я–Т–Я, –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Є, –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В—Л, –≤–Є—В–∞–Љ–Є–љ—Л –≥—А—Г–њ–њ—Л –Т, –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є—О —В—А–Є–≥–≥–µ—А–љ—Л—Е –Ј–Њ–љ –Љ–µ—Б—В–љ—Л–Љ–Є –∞–љ–µ—Б—В–µ—В–Є–Ї–∞–Љ–Є, —Д–Є–Ј–Є–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—Ж–µ–і—Г—А—Л, —А–µ—Д–ї–µ–Ї—Б–Њ—В–µ—А–∞–њ–Є—О, –Ї—Г—А—Б –ї–µ—З–µ–±–љ–Њ–є –≥–Є–Љ–љ–∞—Б—В–Є–Ї–Є. –Я–∞—Ж–Є–µ–љ—В—Л 1-–є –≥—А—Г–њ–њ—Л –љ–∞—А—П–і—Г —Б –±–∞–Ј–Є—Б–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є –њ–Њ–ї—Г—З–∞–ї–Є —В–µ—А–∞–њ–Є—О L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–Њ–Љ: 5 –Љ–ї L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ —А–∞–Ј–≤–Њ–і–Є–ї–Є –≤ 200 –Љ–ї 0,9% —А–∞—Б—В–≤–Њ—А–∞ –љ–∞—В—А–Є—П —Е–ї–Њ—А–Є–і–∞ –Є –≤–≤–Њ–і–Є–ї–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ –Ї–∞–њ–µ–ї—М–љ–Њ 1 —А./—Б—Г—В, –Ї—Г—А—Б —Б–Њ—Б—В–∞–≤–Є–ї 10 –і–љ–µ–є. –Ъ—Г—А—Б —В–µ—А–∞–њ–Є–Є –±—Л–ї –Ј–∞–≤–µ—А—И–µ–љ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е. –°–ї—Г—З–∞–µ–≤ –Њ—В–Ї–∞–Ј–∞ –Њ—В —В–µ—А–∞–њ–Є–Є, –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П –ї–µ—З–µ–љ–Є—П –≤ —Б–≤—П–Ј–Є —Б –њ–Њ–±–Њ—З–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є, –њ–ї–Њ—Е–Њ–є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М—О –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ –љ–µ –±—Л–ї–Њ.
–Ф–ї—П –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М —Б–ї–µ–і—Г—О—Й–Є–µ –Ї—А–Є—В–µ—А–Є–Є:
1. –Ъ–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Т–Р–® —Б –Є–Ј–Љ–µ—А–µ–љ–Є–µ–Љ —А–µ–Ј—Г–ї—М—В–∞—В–∞ –Њ—В 0 –і–Њ 10, –±–Њ–ї–µ–≤–Њ–≥–Њ –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ь–∞–Ї-–У–Є–ї–ї–∞, –Ї–Њ—В–Њ—А—Л–є —В–∞–Ї–ґ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ—Ж–µ–љ–Є—В—М –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –±–Њ–ї—М–љ—Л—Е.
2. –Ю—Ж–µ–љ–Ї–∞ –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є –≥—А—Г–і–љ–Њ–≥–Њ –Є –њ–Њ—П—Б–љ–Є—З–љ–Њ–≥–Њ –Њ—В–і–µ–ї–Њ–≤ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞: –Є–Ј—Г—З–∞–ї–∞—Б—М –і–Є–љ–∞–Љ–Є–Ї–∞ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ю—В—В–∞ –Є –®–Њ–±–µ—А–∞.
3. –Ю—Ж–µ–љ–Ї–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є —Б–Є–Љ–њ—В–Њ–Љ–∞ –Ы–∞—Б–µ–≥–∞ (–≤—Л—А–∞–ґ–µ–љ–љ—Л–є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ вАУ –і–Њ 30¬∞, —Г–Љ–µ—А–µ–љ–љ–Њ вАУ –Њ—В 30 –і–Њ 45¬∞, —Б–ї–∞–±–Њ вАУ –±–Њ–ї–µ–µ 45¬∞).
4. –Ю—Ж–µ–љ–Ї–∞ –∞–Љ–њ–ї–Є—В—Г–і—Л –Ь-–Њ—В–≤–µ—В–∞ –Ї–Њ—А–Њ—В–Ї–Њ–≥–Њ —А–∞–Ј–≥–Є–±–∞—В–µ–ї—П –њ–∞–ї—М—Ж–µ–≤ –Є –Љ—Л—И—Ж—Л, –Њ—В–≤–Њ–і—П—Й–µ–є –±–Њ–ї—М—И–Њ–є –њ–∞–ї–µ—Ж —Б—В–Њ–њ—Л, –Љ–Є–љ–Є–Љ–∞–ї—М–љ–∞—П –ї–∞—В–µ–љ—В–љ–Њ—Б—В—М –Є —З–∞—Б—В–Њ—В–∞ —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є FвАУ–≤–Њ–ї–љ –њ—А–Є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –Љ–∞–ї–Њ–±–µ—А—Ж–Њ–≤–Њ–≥–Њ –Є –±–Њ–ї—М—И–µ–±–µ—А—Ж–Њ–≤–Њ–≥–Њ –љ–µ—А–≤–Њ–≤.
–Р–љ–∞–ї–Є–Ј –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —Б –њ–Њ–Љ–Њ—Й—М—О –Т–Р–® –њ—А–Њ–Є–Ј–≤–Њ–і–Є–ї—Б—П —Б–ї–µ–і—Г—О—Й–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ. –Я–∞—Ж–Є–µ–љ—В –≤—Л–њ–Њ–ї–љ—П–ї –і–≤–Є–ґ–µ–љ–Є–µ, –Ї–Њ—В–Њ—А–Њ–µ –≤—Л–Ј—Л–≤–∞–µ—В –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Г—О –±–Њ–ї—М –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ (–љ–∞–њ—А–Є–Љ–µ—А, –љ–∞–Ї–ї–Њ–љ —В—Г–ї–Њ–≤–Є—Й–∞ –≤–њ–µ—А–µ–і), –Є –Њ—Ж–µ–љ–Є–≤–∞–ї –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –±–Њ–ї–Є –њ–Њ –Т–Р–®, –њ–µ—А–µ—З–µ—А–Ї–Є–≤–∞—П –Њ–і–љ–Њ–є –ї–Є–љ–Є–µ–є —И–Ї–∞–ї—Г –≤ –Љ–µ—Б—В–µ, –Ї–Њ—В–Њ—А–Њ–µ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –µ–≥–Њ –Њ—Й—Г—Й–µ–љ–Є—О –±–Њ–ї–Є. –Ш–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є–Ј–Љ–µ—А—П–ї–∞—Б—М –≤–Њ –≤—Б–µ—Е —Б–ї—Г—З–∞—П—Е –Њ–і–љ–Њ–є –Є —В–Њ–є –ґ–µ –ї–Є–љ–µ–є–Ї–Њ–є —Б–ї–µ–≤–∞ –љ–∞–њ—А–∞–≤–Њ —Б —В–Њ—З–љ–Њ—Б—В—М—О –і–Њ 1 –Љ–Љ (0 –Љ–Љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г–µ—В –Њ—В—Б—Г—В—Б—В–≤–Є—О –±–Њ–ї–Є, 100 –Љ–Љ вАУ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ–≥–і–∞-–ї–Є–±–Њ –Є—Б–њ—Л—В—Л–≤–∞–µ–Љ–Њ–є –њ–∞—Ж–Є–µ–љ—В–Њ–Љ –±–Њ–ї–Є). –У—А–∞–і–∞—Ж–Є—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ –Т–Р–®: –Њ—В—Б—Г—В—Б—В–≤–Є–µ –±–Њ–ї–Є вАУ 0,0вАУ10,0 –Љ–Љ, –Љ–Є–љ–Є–Љ–∞–ї—М–љ–∞—П –±–Њ–ї—М вАУ 10вАУ30 –Љ–Љ, —Г–Љ–µ—А–µ–љ–љ–∞—П –±–Њ–ї—М вАУ 30вАУ50 –Љ–Љ, —Б–Є–ї—М–љ–∞—П –±–Њ–ї—М вАУ 50вАУ70 –Љ–Љ, –Њ—З–µ–љ—М —Б–Є–ї—М–љ–∞—П –±–Њ–ї—М вАУ 70вАУ90 –Љ–Љ, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –±–Њ–ї—М вАУ 90вАУ100 –Љ–Љ.
–Ю–њ—А–Њ—Б–љ–Є–Ї –±–Њ–ї–Є –Ь–∞–Ї-–У–Є–ї–ї–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤—Л—П—Б–љ–Є—В—М —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–µ –≤–Њ—Б–њ—А–Є—П—В–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–Љ —Е–∞—А–∞–Ї—В–µ—А–∞ –±–Њ–ї–Є, –Њ—Ж–µ–љ–Є—В—М –µ–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М, –∞ —В–∞–Ї–ґ–µ —Б–µ–љ—Б–Њ—А–љ—Л–є –Є –∞—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л. –Я–Њ—Б–ї–µ –Ј–∞–њ–Њ–ї–љ–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–Љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–≥–Њ –±–ї–∞–љ–Ї–∞ —А–∞—Б—Б—З–Є—В—Л–≤–∞–ї–Є—Б—М —В—А–Є –±–∞–ї–ї–∞: ¬Ђ—Б–µ–љ—Б–Њ—А–љ—Л–є¬ї –±–∞–ї–ї (—Б—Г–Љ–Љ–∞ –њ–Њ –њ—Г–љ–Ї—В–∞–Љ 1вАУ11), ¬Ђ–∞—Д—Д–µ–Ї—В–Є–≤–љ—Л–є¬ї –±–∞–ї–ї (—Б—Г–Љ–Љ–∞ –њ–Њ –њ—Г–љ–Ї—В–∞–Љ 12вАУ15) –Є –Њ–±—Й–Є–є –±–∞–ї–ї (—Б—Г–Љ–Љ–∞ –њ–Њ –≤—Б–µ–Љ 15 –њ—Г–љ–Ї—В–∞–Љ).
–°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј –і–∞–љ–љ—Л—Е –њ—А–Њ–≤–Њ–і–Є–ї—Б—П –≤ –њ—А–Њ–≥—А–∞–Љ–Љ–µ StatSoft Statistica 7.0 Excel –Є–Ј –њ–∞–Ї–µ—В–∞ MS Offi—Бe 2003; –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ –Є –љ–µ–њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —В–Є–њ–∞ –∞–љ–∞–ї–Є–Ј–Є—А—Г–µ–Љ–Њ–≥–Њ –њ—А–Є–Ј–љ–∞–Ї–∞ –≤ –≤—Л–±–Њ—А–Ї–µ.
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Є—Е –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
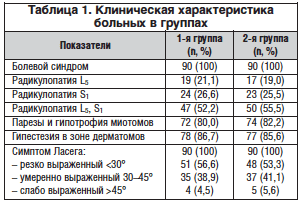
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ—А–Є–љ—П–ї–Є —Г—З–∞—Б—В–Є–µ 180 —З–µ–ї–Њ–≤–µ–Ї, –Є–Ј –љ–Є—Е 72 (40%) –ґ–µ–љ—Й–Є–љ—Л –Є 108 (60%) –Љ—Г–ґ—З–Є–љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 30 –і–Њ 65 –ї–µ—В (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 46,6¬±3,3 –ї–µ—В). –Т 1-—О –≥—А—Г–њ–њ—Г –≤–Њ—И–ї–Є 90 –њ–∞—Ж–Є–µ–љ—В–Њ–≤: 37 (41,1%) –ґ–µ–љ—Й–Є–љ –Є 53 (58,9%) –Љ—Г–ґ—З–Є–љ—Л; –≤–Њ 2-—О –≥—А—Г–њ–њ—Г вАУ 35 (38,9%) –ґ–µ–љ—Й–Є–љ –Є 55 (61,1%) –Љ—Г–ґ—З–Є–љ. –Т —Ж–µ–ї–Њ–Љ –Њ–±–µ –≥—А—Г–њ–њ—Л –±—Л–ї–Є –њ–Њ–ї–љ–Њ—Б—В—М—О —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л –і—А—Г–≥ —Б –і—А—Г–≥–Њ–Љ –њ–Њ –Њ—Б–љ–Њ–≤–љ—Л–Љ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞–Љ (—Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П –Њ—В—Б—Г—В—Б—В–≤–Њ–≤–∞–ї–Є). –Т –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –і–Њ–Љ–Є–љ–Є—А–Њ–≤–∞–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л –Љ—Г–ґ—Б–Ї–Њ–≥–Њ –њ–Њ–ї–∞, —З—В–Њ, –≤–µ—А–Њ—П—В–љ–Њ, —Б–≤—П–Ј–∞–љ–Њ —Б –±–Њ–ї—М—И–Є–Љ–Є —Д–Є–Ј–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞–≥—А—Г–Ј–Ї–∞–Љ–Є. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –±–Њ–ї—М–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 1.
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –њ—А–µ–Њ–±–ї–∞–і–∞–ї–Њ —Б–Њ—З–µ—В–∞–љ–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Ї–Њ—А–µ—И–Ї–Њ–≤ L5 –Є S1, –љ–∞ –≤—В–Њ—А–Њ–Љ –Љ–µ—Б—В–µ –њ–Њ —З–∞—Б—В–Њ—В–µ –≤—Б—В—А–µ—З–∞–µ–Љ–Њ—Б—В–Є –±—Л–ї–∞ –Љ–Њ–љ–Њ—А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П –Ї–Њ—А–µ—И–Ї–∞ S1. –Я–∞—А–µ–Ј—Л, –≥–Є–њ–Њ—В—А–Њ—Д–Є—П –Љ–Є–Њ—В–Њ–Љ–Њ–≤, –∞ —В–∞–Ї–ґ–µ –≥–Є–њ–µ—Б—В–µ–Ј–Є—П –і–µ—А–Љ–∞—В–Њ–Љ–Њ–≤ –≤—Б—В—А–µ—З–∞–ї–Є—Б—М —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –°–Є–Љ–њ—В–Њ–Љ –Ы–∞—Б–µ–≥–∞ –≤—Л—П–≤–ї–µ–љ –≤ 100% —Б–ї—Г—З–∞–µ–≤, —З–∞—Й–µ –Њ—В–Љ–µ—З–∞–ї—Б—П —А–µ–Ј–Ї–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–є –≤–∞—А–Є–∞–љ—В (56,6% –Є 53,3% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ).
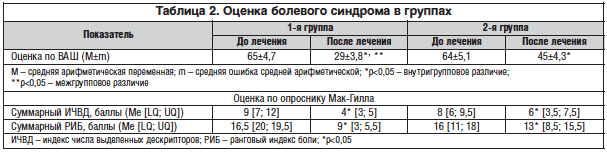
–Я–∞—Ж–Є–µ–љ—В—Л –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –љ–∞ —Д–Њ–љ–µ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–Њ–Ї–∞–Ј–∞–ї–Є –Њ–і–Є–љ–∞–Ї–Њ–≤—Г—О –і–Њ—Б—В–Њ–≤–µ—А–љ—Г—О –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Ї–∞–Ї –≤–љ—Г—В—А–Є, —В–∞–Ї –Є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є (—А<0,05). –°—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В, –Љ–Є–љ–Є–Љ–∞–ї—М–љ–∞—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є–ї–Є –µ–≥–Њ –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ, —Б–Њ–≥–ї–∞—Б–љ–Њ –Т–Р–®, –љ–∞ 10-–є –і–µ–љ—М –љ–∞ —Д–Њ–љ–µ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —Г 83 (92,2%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Б—А–µ–і–Є –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –і–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В вАУ —В–Њ–ї—М–Ї–Њ —Г 58 (64,4%) –±–Њ–ї—М–љ—Л—Е (—А<0,05). –Ю—Ж–µ–љ–Ї–∞ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ –Њ–њ—А–Њ—Б–љ–Є–Ї—Г –Ь–∞–Ї-–У–Є–ї–ї–∞ —В–∞–Ї–ґ–µ –њ–Њ–Ї–∞–Ј–∞–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ—Г—О –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е 1-–є –≥—А—Г–њ–њ—Л –Њ—В–Љ–µ—З–∞–ї—Б—П –±–Њ–ї–µ–µ –±—Л—Б—В—А—Л–є –Є —Б—В–Њ–є–Ї–Є–є —А–µ–≥—А–µ—Б—Б –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –Њ—Б–Њ–±–µ–љ–љ–Њ —Н—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –±–Њ–ї–µ–є –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є –њ–Њ–Ї–Њ—П –Є –љ–Њ—З–љ—Л—Е –±–Њ–ї–µ–є. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 2.
–Ю–і–љ–Є–Љ –Є–Ј –Ї—А–Є—В–µ—А–Є–µ–≤ –Њ—Ж–µ–љ–Ї–Є –і–Є–љ–∞–Љ–Є–Ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е —Б –Њ—Б—В—А—Л–Љ–Є –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–Њ-–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П–Љ–Є —П–≤–ї—П–µ—В—Б—П –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞. –° —Н—В–Њ–є —Ж–µ–ї—М—О –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –Њ—Ж–µ–љ–Ї–∞ –і–Є–љ–∞–Љ–Є–Ї–Є —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ю—В—В–∞ –Є –®–Њ–±–µ—А–∞ –і–Њ –Є –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П (—В–∞–±–ї. 3).
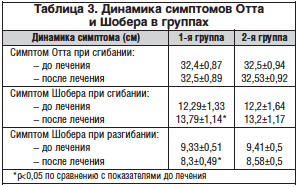
–Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј —В–∞–±–ї–Є—Ж—Л 3, –њ–∞—Ж–Є–µ–љ—В—Л, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –љ–∞—А—П–і—Г —Б–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В, –Є–Љ–µ–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Њ–±—К–µ–Љ–∞ –і–≤–Є–ґ–µ–љ–Є–є –≤ –њ–Њ—П—Б–љ–Є—З–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –і–Њ –ї–µ—З–µ–љ–Є—П, –Њ–і–љ–∞–Ї–Њ –Љ–µ–ґ–≥—А—Г–њ–њ–Њ–≤—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ.
–°—А–∞–≤–љ–Є—В–µ–ї—М–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1-–є –Є 2-–є –≥—А—Г–њ–њ –њ–Њ–Ї–∞–Ј–∞–ї–∞, —З—В–Њ —Г–ґ–µ –љ–∞ 3-–є –і–µ–љ—М –Њ—В –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –≤ –≥—А—Г–њ–њ–µ, –њ–Њ–ї—Г—З–∞–≤—И–µ–є L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В, –Њ—В–Љ–µ—З–∞–µ—В—Б—П –±–Њ–ї–µ–µ –±—Л—Б—В—А—Л–є —А–µ–≥—А–µ—Б—Б —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –љ–∞—В—П–ґ–µ–љ–Є—П. –Ґ–∞–Ї–∞—П –ґ–µ —В–µ–љ–і–µ–љ—Ж–Є—П –њ—А–Њ—Б–ї–µ–ґ–Є–≤–∞–µ—В—Б—П –Є –Ї 10-–Љ—Г –і–љ—О –ї–µ—З–µ–љ–Є—П: –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤ —В–µ—А–∞–њ–Є–Є –Ї–Њ—В–Њ—А—Л—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В, —Б–Є–Љ–њ—В–Њ–Љ—Л –љ–∞—В—П–ґ–µ–љ–Є—П –Ї—Г–њ–Є—А–Њ–≤–∞–ї–Є—Б—М —Г 79 (87,8%) —З–µ–ї–Њ–≤–µ–Ї, –≤ 11 (12,2%) —Б–ї—Г—З–∞—П—Е –≤—Л—П–≤–ї—П–ї–∞—Б—М —Г–Љ–µ—А–µ–љ–љ–∞—П –Є–ї–Є —Б–ї–∞–±–∞—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –љ–∞—В—П–ґ–µ–љ–Є—П (—А<0,05). –Т –≥—А—Г–њ–њ–µ –±–Њ–ї—М–љ—Л—Е, –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–µ—З–µ–љ–Є—П L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–Њ–Љ, –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Б–Њ—Б—В–∞–≤–Є–ї–Є 53 (58,9 %) –Є 37 (41,1%) —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –≤—Л—П–≤–ї–µ–љ—Л —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–µ –≤–љ—Г—В—А–Є–≥—А—Г–њ–њ–Њ–≤—Л–µ –Є –Љ–µ–ґ–≥—А—Г–њ–њ–Њ–≤—Л–µ —А–∞–Ј–ї–Є—З–Є—П (—А<0,05). –Ф–∞–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 4.
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –њ—А–Њ—Б–ї–µ–ґ–Є–≤–∞–ї—Б—П –љ–µ–Ї–Њ—В–Њ—А—Л–є —А–µ–≥—А–µ—Б—Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –≥–Є–њ–µ—Б—В–µ–Ј–Є–Є, –≥–Є–њ–Њ—В–Њ–љ–Є–Є –Є —Б–ї–∞–±–Њ—Б—В–Є –њ–Њ—А–∞–ґ–µ–љ–љ—Л—Е –Љ–Є–Њ—В–Њ–Љ–Њ–≤, –љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ.
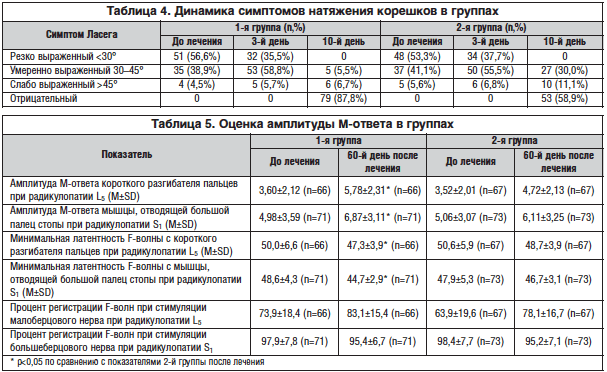
–≠–ї–µ–Ї—В—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ (–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є –Љ–Њ—В–Њ—А–љ—Л—Е –Є —Б–µ–љ—Б–Њ—А–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –Љ–∞–ї–Њ–±–µ—А—Ж–Њ–≤–Њ–≥–Њ –Є –±–Њ–ї—М—И–µ–±–µ—А—Ж–Њ–≤–Њ–≥–Њ –љ–µ—А–≤–Њ–≤) –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –і–ї—П –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є —Б –љ–µ–є—А–Њ–њ–∞—В–Є—П–Љ–Є –і–∞–љ–љ—Л—Е –љ–µ—А–≤–Њ–≤ (–і–ї—П –Є—Б–Ї–ї—О—З–µ–љ–Є—П –Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П). –Ґ–∞–Ї–ґ–µ –±—Л–ї–∞ –Њ—Ж–µ–љ–µ–љ–∞ –і–Є–љ–∞–Љ–Є–Ї–∞ –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Ь-–Њ—В–≤–µ—В–∞ –Є F-–≤–Њ–ї–љ –і–ї—П –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –Є –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ –Ї 60-–Љ—Г –і–љ—О –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П. –†–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 5. –Т –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –ї–µ—З–µ–љ–Є–µ —Б –≤–Ї–ї—О—З–µ–љ–Є–µ–Љ L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞, –Є–Љ–µ–ї–Њ—Б—М –±–Њ–ї—М—И–µ–µ –љ–∞—А–∞—Б—В–∞–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л –Ь-–Њ—В–≤–µ—В–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –≥—А—Г–њ–њ–Њ–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ. –Ґ–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є–є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –ї–∞—В–µ–љ—В–љ–Њ—Б—В–Є F-–≤–Њ–ї–љ—Л –њ—А–Є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –Ї–∞–Ї –Љ–∞–ї–Њ–±–µ—А—Ж–Њ–≤–Њ–≥–Њ, —В–∞–Ї –Є –±–Њ–ї—М—И–µ–±–µ—А—Ж–Њ–≤–Њ–≥–Њ –љ–µ—А–≤–Њ–≤. –Я—А–Є —Н—В–Њ–Љ –њ—А–Њ—Ж–µ–љ—В —А–µ–≥–Є—Б—В—А–∞—Ж–Є–Є F-–≤–Њ–ї–љ –љ–µ –Њ—В–ї–Є—З–∞–ї—Б—П –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є. –Ф–∞–љ–љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –ї—Г—З—И–µ–Љ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Є –∞–Ї—Б–Њ–љ–Њ–≤ –Є –Љ–Є–µ–ї–Є–љ–∞ –Ї–Њ—А–µ—И–Ї–Њ–≤ L5 –Є S1 –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–Њ–Љ (—В–∞–±–ї. 5).
–Т—Л–≤–Њ–і—Л
–Я—А–µ–њ–∞—А–∞—В L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В –њ—А–µ–і–љ–∞–Ј–љ–∞—З–µ–љ –і–ї—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є –Є –Њ—В–µ—З–љ–Њ-–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –њ—А–Є —В–∞–Ї–Њ–є —В—П–ґ–µ–ї–Њ–є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –Ї–∞–Ї –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–Њ-–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є. –Я—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–µ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –≤ —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Ї–Њ–Љ–њ—А–µ—Б—Б–Є–Њ–љ–љ–Њ-–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П–Љ–Є. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В –Љ–Њ–ґ–µ—В –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—В—М –±–Њ–ї–µ–µ –±—Л—Б—В—А—Г—О –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г –љ–µ —В–Њ–ї—М–Ї–Њ —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є, –љ–Њ –Є –Њ–±—К–µ–Ї—В–Є–≤–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (—Б–Є–Љ–њ—В–Њ–Љ—Л –љ–∞—В—П–ґ–µ–љ–Є—П –Ї–Њ—А–µ—И–Ї–Њ–≤, –љ–∞—А–∞—Б—В–∞–љ–Є–µ –Њ–±—К–µ–Љ–∞ –і–≤–Є–ґ–µ–љ–Є–є –≤ –њ–Њ—А–∞–ґ–µ–љ–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –і–∞–љ–љ—Л—Е —Н–ї–µ–Ї—В—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є–Є), —З—В–Њ, –љ–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, —Г–ї—Г—З—И–∞–µ—В –Ї–∞—З–µ—Б—В–≤–Њ –Є—Е –ґ–Є–Ј–љ–Є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ L-–ї–Є–Ј–Є–љ–∞ —Н—Б—Ж–Є–љ–∞—В–∞ –љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –Є —Е–Њ—А–Њ—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –њ–Њ–Ј–≤–Њ–ї—П—О—В —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –µ–≥–Њ –і–ї—П —И–Є—А–Њ–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –≤ –∞–Љ–±—Г–ї–∞—В–Њ—А–љ–Њ–є –Є —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ.












