
Введение
Современное понимание патогенетических основ развития хронического риносинусита (ХРС) позволяет на сегодняшний день отнести эту патологию к гетерогенной группе заболеваний носа и околоносовых пазух, которые характеризуются воспалением и ремоделированием тканей.В соответствии с европейской классификацией ХРС подразделяется на хронический риносинусит с полипами и хронический риносинусит без полипов [1]. Диагноз ХРС устанавливается при наличии по крайней мере 2-х симптомов из следующих: заложенность носа, носовая секреция и/или постназальный синдром, головные и/или лицевые боли, снижение обоняния в течение более чем 12 нед. за последний год. Согласно последним данным, различные формы ХРС отличаются также процессом ремоделирования верхних дыхательных путей. Гистологически ХРС без полипов характеризуется фиброзом слизистой оболочки и базальной мембраны, в то время как полипозный риносинусит (ПРС) сопровождается выраженным отеком с отложением альбумина и развитием псевдокист.
Процесс ремоделирования слизистой оболочки полости носа и околоносовых пазух при хроническом воспалении создает условия для ослабления защитных механизмов и в большинстве случаев делает ее более восприимчивой к воздействию различных видов микроорганизмов [2].
При хронических синуситах микробная флора отличается большим разнообразием и спектр возбудителей несколько смещается в пользу анаэробной флоры. Так, по данным ряда авторов, в 52% случаев выделяются аэробы (различные стрептококки – 21%, гемофильная палочка – 16%, синегнойная палочка – 15%, золотистый стафилококк и моракселла − по 10%). Анаэробным возбудителям принадлежит 48% случаев (Prevotella – 31%, анаэробные стрептококки – 22%, Fusobacterium − 15% и др.). Выделение энтеробактерий при синуситах может быть объяснено кишечным дисбактериозом, который рассматривается в настоящее время как побочное действие антибиотикотерапии. По причине дефицита бифидобактерий и молочнокислых бактерий происходит беспрепятственное заселение условно-патогенной микрофлорой не только кишечника, но и других сообщающихся с внешней средой полостей организма. Этим же обстоятельством объясняется выявление грибов рода Candida [3].
Т.Н. Леонтьева и соавт. (1988) при обследовании 200 больных ПРС выявили стафилококковую обсемененность слизистой оболочки полости носа у 70,7% больных ПРС и у 81,5% больных полипозно-гнойным риносинуситом (ПГРС). При ПРС выявлялись в основном условно-патогенные штаммы. В 13,7% определялась стрептококковая флора, представленная в большей степени зеленящим стрептококком и встречающаяся одинаково часто как при ПРС, так и при ПГРС. E. сoli высевалась из отделяемого полости носа в 10,5% случаев. По результатам исследования авторы приходят к выводу, что S. aureus способствует более тяжелому течению заболевания с частыми рецидивами. Флора околоносовых пазух (ОНП) как сапрофитирующая, так и патогенная крайне разнообразна, причем микробный пейзаж варьирует в зависимости от тяжести и продолжительности заболевания.
Для возникновения инфекционного процесса ведущее значение, наряду с вирулентностью возбудителя, имеет состояние макроорганизма. Оно определяется сложным комплексом факторов и механизмов, тесно связанных между собой, а также чувствительностью и резистентностью к инфекции. Наиболее значимыми факторами являются неблагоприятный аллергический фон, частые полипотомии полости носа, нерациональное назначение антибактериальных препаратов, как в виде местной терапии, так и в виде общей антибиотикотерапии.
Особое внимание в последнее время уделяется способности микроорганизмов собираться в сообщества, т. е. формировать биопленки. Доказано, что биопленки оказывают серьезное влияние на свойства и потенциальные возможности образующих их патогенов. В первую очередь речь идет о защитном матриксе, своеобразной среде внутри микроколоний, способности микроорганизмов к элементарным видам взаимодействия между собой. В биопленке бактерия способна продуцировать такие факторы устойчивости, которые не продуцируют планктонные микроорганизмы, не говоря о лабораторных штаммах, а матрикс, окружающий микроколонии, служит защитным барьером, благодаря которому бактерии в биопленке более устойчивы к внешнесредовым влияниям и действию защитных факторов организма. Биопленкообразование широко изучено на золотистом стафилококке. Продемонстрировано, что S. aureus может не только обсеменять слизистую полости носа, но и формировать биопленку на слизистой оболочке, в особенности у пациентов с полипами.
Недавние исследования были посвящены изучению роли биопленок в персистенции S. aureus: биопленки выступают в качестве резервуара для микроорганизмов и позволяют им быстро внедряться в слизистую оболочку [4]. Используя флуоресцентную гибридизацию in situ пептидно-нуклеиновых кислот, было продемонстрировано наличие внутриклеточно расположенного S. aureus в ткани полипов от пациентов с аспирин-индуцированными заболеваниями дыхательной системы [5]. Также было выявлено, что данный микроорганизм располагается интраэпителиально в слизистой полипов, но не присутствует в назальном эпителии пациентов с хроническим риносинуситом без полипоза и у здоровых добровольцев. S. aureus не только выживает, но и размножается внутри эпителиальных клеток назальных полипов [6]. Данные исследований подчеркивают способность S. aureus к персистенции в условиях нарушенного механизма защиты слизистой оболочки. Как известно, Th2 сдвиг воспалительной реакции поддерживает программирование так называемых М2 макрофагов в ткани полипов, у которых, как было показано, снижена способность к фагоцитированию и внутриклеточному лизису S. aureus [7].
Кроме того, предполагается, что S. aureus высвобождает энтеротоксин в ткань полипа лишь в небольшом количестве, что приводит к постоянной стимуляции местной иммунной системы и изменению как врожденного [6], так и адаптивного иммунитета [8]. Все это позволяет бактерии в течение длительного времени выживать в пораженных дыхательных путях. Нами было проведено собственное исследованиею
Цель исследования: повысить эффективность лечения ПРС с учетом изученного влияния персистирующей стафилококковой инфекции на возникновение и течение этого заболевания.
Материал и методы
В исследование включено 105 пациентов с ПРС в возрасте от 20 до 65 лет: 65 (62%) женщин и 40 (38%) мужчин. В общем количестве пациентов с ПРС 49 (47%) имели астматическую триаду (ПРС + бронхиальная астма (БА) + непереносимость НПВС), у 32 (38%) пациентов диагностирован только ПРС, у 16 (15%) − ПРС и БА.Всем пациентам проведено стандартное клиническое обследование, а также обследование, соответствующее заболеванию: оториноларингологический осмотр (передняя и задняя риноскопия, фарингоскопия и т. д.), эндоскопическое исследование полости носа и носоглотки эндоскопами, рентгенологическое исследование − КТ ОНП. Проведено микробиологическое исследование посевов со слизистой оболочки полости носа. Особое внимание, учитывая природу полипозного процесса, мы уделили иммунологическому и аллергологическому исследованиям, которые проводили по стандартной методике, разработанной НИАЛ АМН СССР. Сенсибилизацию к золотистому стафилококку исследовали по уровню специфического IgE крови к стафилококковым энтеротоксинам А, В, TSST.
Для оценки эффективности лечения выполняли указанное комплексное обследование многократно: перед операцией и на контрольных визитах через 6 мес., далее через 1 год после операции или по показаниям.
Всем пациентам выполнена функциональная эндоскопическая риносинусхирургия по поводу ПРС. В послеоперационном периоде все пациенты получали антибактериальную терапию согласно одной из 2-х используемых в данном исследовании терапевтических схем:
1) топические глюкокортикостероиды (ГКС), антигистаминные препараты; через 6 мес. повторный курс лечения в той же дозировке;
2) 1-я схема + антибиотик; через 6 мес. повторный курс лечения в той же дозировке.
Результаты и обсуждение
В результате проведенного исследования выявлена высокая распространенность среди пациентов ПРС персистирующей стафилококковой инфекции, которая составляет 71%, и высокая частота встречаемости пациентов, сенсибилизированных к антигенам Staph. aureus, – 55,2%. Установлено, что ПРС, ассоциированный с носительством золотистого стафилококка, сопровождается в 1,5 раза более тяжелым клиническим течением, нежели ПРС без носительства (6±0,64 балла и 4±0,84 соответственно) и большей частотой обострений гнойного воспаления ОНП за год (2,7±0,79 и 1,8±0,67 соответственно).Описанная закономерность объективно объясняется более выраженным эозинофильным воспалением при ПРС, ассоциированным с колонизацией Staph. аureus, чем при ПРС, ассоциированным с инфицированием прочими микроорганизмами (Str. pneumoniae, Str. viridans, Staph. epidermidis, E. coli, K. pneumoniae, H. influenzae, P. аeruginosa), что выражается повышенным количеством эозинофилов в крови (7,98±2,86 и 5,98±3,20 соответственно), в мазках со слизистой оболочки полости носа (13,3±6,20 и 7,87±5,22 соответственно) и средним уровнем эозинофильного катионного протеина (17,5±5,10 и 11,3±6,07 мкг/мл соответственно). Сенсибилизация к Staph. аureus также приводит к увеличению выраженности эозинофильного воспаления при полипозном синусите по сравнению с несенсибилизированными пациентами: повышение количества эозинофилов в крови (8,26±2,97 и 4,32±1,59 соответственно), в мазках со слизистой оболочки полости носа (13,3±5,54 и 4,8±3,89 соответственно) и повышение среднего уровня эозинофильного катионного протеина (17,6±4,66 и 8,0±6,64 мкг/мл соответственно).
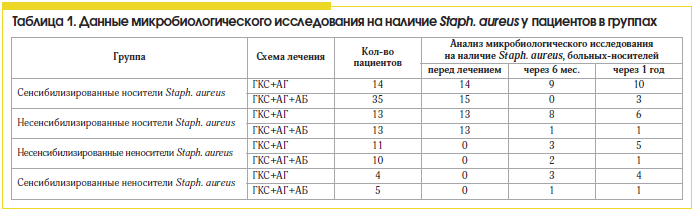
В группах, получавших лечение без антибиотика, положительная эрадикация микрофлоры была достигнута только в 28,5% у сенсибилизированных носителей и в 54% случаев – у несенсибилизированных носителей, что можно расценивать как спонтанную эрадикацию возбудителя на фоне нормализации носового дыхания и аэрации в ОНП, при условии отсутствия сенсибилизации (табл. 1). Обращает на себя внимание тот факт, что у всех пациентов, сенсибилизированных к стафилококку, не получавших антибактериальную терапию и не являвшихся носителями, через год был выявлен рост микрооганизма в значимой концентрации (>104). Это свидетельствует о необходимости проведения бактериологического мониторинга у всех сенсибилизированных к стафилококку пациентов.
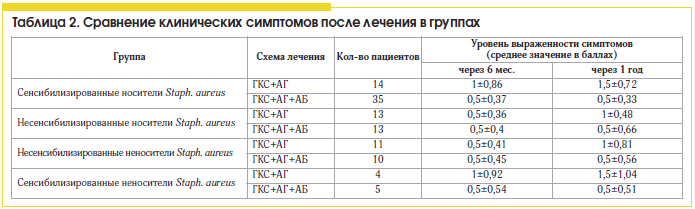
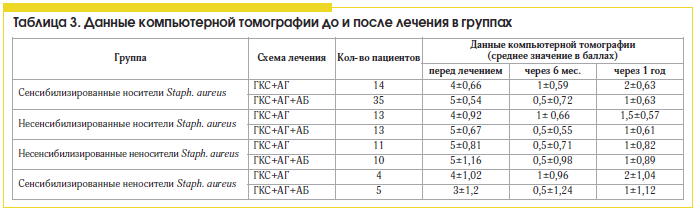
Сравнивая различные схемы лечения ПРС, мы установили, что больные полипозным синуситом, сенсибилизированные к антигенам Staph. aureus, более резистентны к стандартной противорецидивной терапии (табл. 2 и 3) топическими стероидами и антигистаминными препаратами, чем несенсибилизированные пациенты, и требуют проведения антибактериальной терапии.
Как известно, выбор антибиотика зависит от определенных факторов: срока последнего обострения (менее 6 мес.); результатов микробиологического исследования; тяжести течения заболевания; наличия осложнений. Все пациенты с хроническим синуситом в несколько раз чаще применяют антибактериальные препараты, что значительно повышает риск встречи с резистентной флорой. Уже этот фактор служит показанием к назначению антибиотиков, резистентность к которым минимальна.
В этом аспекте понятен повышенный интерес оториноларингологов к респираторным фторхинолонам, в частности к левофлоксацину – высокоэффективному в отношении респираторной флоры, с практическим отсутствием резистентных штаммов в России, который, к тому же в терапевтических концентрациях способствует ингибированию синтеза биопленки.
Заключение
В нашем исследовании применение антибиотиков в составе комплексной терапии ПРС, ассоциированного с персистирующей стафилококковой инфекцией, приводит к статистически достоверному (в 2 раза) уменьшению выраженности эозинофильного воспаления и улучшению клинических показателей заболевания (клинических симптомов, картины компьютерной томографии околоносовых пазух) и снижению частоты гнойных осложнений по сравнению со стандартной противорецидивной терапией.Фторхинолоны − это полностью синтетические препараты, которые не имеют природного аналога. Одной из последних разработок препаратов данной группы является левофлоксацин. Левофлоксацин обладает быстрым бактерицидным действием, поскольку проникает внутрь микробной клетки и подавляет, так же как и фторхинолоны первого поколения, ДНК-гиразу (топоизомеразу II) бактерий, что нарушает процесс образования бактериальной ДНК. Ферменты клеток человека не чувствительны к фторхинолонам, и последние не оказывают токсического действия на клетки макроорганизма. В отличие от препаратов прежнего поколения новые фторхинолоны ингибируют не только ДНК-гиразу, но и второй фермент, ответственный за синтез ДНК, − топоизомеразу IV, выделенную у некоторых микроорганизмов, прежде всего грамположительных. Считается, что именно воздействием на этот фермент объясняется высокая антипневмококковая и антистафилококковая активность новых фторхинолонов.
Левофлоксацин обладает клинически значимым дозозависимым постантибиотическим эффектом, достоверно более длительным по сравнению с ципрофлоксацином, а также длительным (2−3 ч) субингибирующим действием [9].
Под действием левофлоксацина отмечено повышение функции полиморфноядерных лимфоцитов у здоровых добровольцев и ВИЧ-инфицированных пациентов. Показано его иммуномодулирующее воздействие на тонзиллярные лимфоциты у больных хроническим тонзиллитом. Полученные данные позволяют говорить не только об антибактериальной активности, но и о синергическом противовоспалительном и антиаллергическом действии левофлоксацина. Левофлоксацин характеризуется широким антимикробным спектром, включающим грамположительные и грамотрицательные микроорганизмы, в т. ч. внутриклеточные возбудители [10]. При сравнении эффективности различных антибактериальных препаратов в отношении возбудителей респираторных инфекций было выявлено, что по противомикробной активности левофлоксацин превосходит остальные препараты. К нему оказались чувствительны все штаммы пневмококка, в т. ч. пенициллин-резистентные, при сравнительно более низкой чувствительности пневмококков к препаратам сравнения: офлоксацин − 92%, ципрофлоксацин − 82%, кларитромицин − 96%, азитромицин − 94%, амоксициллин/клавуланат − 96%, цефуроксим − 80%. К левофлоксацину оказались также чувствительны все штаммы моракселлы катаралис, гемофильной палочки и метициллин-чувствительного золотистого стафилококка, 95% штаммов клебсиеллы пневмонии [11]. Важным преимуществом левофлоксацина, наряду с хорошей переносимостью, является возможность однократного приема в течение суток.
Перечисленные характеристики препарата обусловливают чрезвычайно важное в практическом отношении свойство левофлоксацина – высокую комплаентность. Сокращение кратности приема и длительности лечения играют ключевую роль в формировании лучшей приверженности протоколам антибиотикотерапии.
Таким образом, левофлоксацин высокоактивен относительно основных возбудителей бактериального синусита. Как показали исследования, чувствительность пневмококка, гемофильной палочки, моракселлы к левофлоксацину превышает 99%. Отмечается также низкий уровень устойчивости золотистого стафилококка (его метициллин-резистентных штаммов) и других возбудителей синусита.












