Введение
Табачные изделия содержат никотин — вещество, которое вызывает развитие зависимости. При курении табака никотин попадает в легкие с табачным дымом, быстро проникает в кровеносную систему через альвеолярно-капиллярную мембрану, преодолевает гематоэнцефалический барьер и попадает в головной мозг. В среднем достаточно 7 с после вдыхания табачного дыма, чтобы никотин достиг головного мозга. В результате взаимодействия никотина с никотиновыми ацетилхолиновыми рецепторами происходит высвобождение дофамина и других нейромедиаторов, что является положительным подкреплением для развития никотиновой зависимости. При прекращении такого взаимодействия развивается синдром отмены, связанный с нарушением работы центральной нервной системы. J.R. Hughes провел анализ 120 исследований, посвященных последствиям отказа от употребления табака, и выявил, что основными и наиболее распространенными симптомами отмены являются тревога, депрессия, снижение концентрации внимания, нетерпение, бессонница и беспокойство [1]. Симптомы развиваются сразу после прекращения потребления табака, максимально проявляются в течение 1-й нед. и в целом длятся 2–4 нед. Кроме того, после отказа от табака могут развиваться такие симптомы отмены, как запор, кашель, головокружение, интенсивные сновидения, язвы во рту.
S.B. Morissette et al. провели анализ исследований по изучению взаимосвязи тревожности, тревожных расстройств, с одной стороны, и употребления табака и никотиновой зависимости — с другой и сделали вывод, что употребление табака повышает риск позднего развития некоторых тревожных расстройств, а у курильщиков, страдающих тревожными расстройствами, развиваются более тяжелые симптомы отмены во время прекращения курения, чем у курильщиков без тревожных расстройств [2]. Авторы также показали, что курение табака широко распространено среди лиц, страдающих тревожными расстройствами различного происхождения.
A.M. Leventhal et al. провели исследование взаимосвязи эмоциональной психопатологии и курения сигарет [3]. Авторы сделали заключение, что ярко выраженным коморбидным состоянием при никотиновой зависимости являются симптомы и синдромы тревоги и депрессии, среди которых выделяются: ангедония (снижение или утрата способности получать удовольствие), повышение тревожной чувствительности и снижение толерантности к дистрессу. Это приводит к повышенному ожиданию удовольствия от курения табака, усиливает анксиолитический эффект никотина, но усиливает и симптомы отмены при прекращении курения. В совокупности у лиц с эмоциональной психопатологией эти процессы приводят к усилению стимулирующих эффектов курения табака, прогрессированию и поддержанию курения, отказу от прекращения курения и рецидивам. N.L. Watson et al. в своем исследовании выявили, что среди людей с повышенной социальной тревожностью распространенность курения табака выше в 2 раза про сравнению с общей популяцией [4]. Для этой категории лиц также характерны более низкие показатели отказа от употребления табака и более частые рецидивы курения. Таким образом, тревожные состояния являются наиболее распространенным коморбидным состоянием при курении табака. С одной стороны, лица с тревожными расстройствами часто употребляют табак с целью подавления тревоги и беспокойства, с другой стороны, тревожные состояния являются наиболее распространенными проявлениями синдрома отмены. Поэтому при лечении никотиновой зависимости применение фармакологических средств, снимающих тревогу и страх, может существенно повысить эффективность лечения.
Безусловно, наиболее приемлемыми для лечения никотиновой зависимости, учитывая ее длительность, являются селективные анксиолитики, т. к. они обладают противотревожным действием, не вызывают привыкания, синдрома отмены и не обладают негативными побочными действиями антидепрессантов.
Исследования применения анксиолитиков при отказе от табака показали, что они способствуют прекращению курения, ослабляя синдром отмены и заменяя эффекты действия никотина. Несмотря на то, что данные по использованию анксиолитиков для отказа от курения ограничены, данные метаанализа, опубликованного в библиотеке Кохрейновского общества, свидетельствуют об их возможной эффективности, в т. ч. для пациентов с выраженными тревожными расстройствами [5].
Фабомотизол — анксиолитик нового поколения
Фабомотизол — селективный анксиолитик, не относящийся к классу агонистов бензодиазепиновых рецепторов [6–8]. Действуя на сигма-1-рецепторы в нервных клетках головного мозга, фабомотизол стабилизирует рецепторы гамма-аминомасляной кислоты и ГАМК-бензодиазепиновый рецептор и восстанавливает их чувствительность к эндогенным медиаторам торможения. Фабомотизол также повышает биоэнергетический потенциал нейронов и оказывает нейропротективное действие: восстанавливает и защищает нервные клетки. Препарат не оказывает миорелаксирующего действия, не нарушает память и внимание. При его применении не формируется лекарственная зависимость и не развивается синдром отмены.
Действие препарата реализуется преимущественно в виде сочетания анксиолитического (противотревожного) и легкого стимулирующего (активизирующего) эффектов. Селективный анксиолитик фабомотизол, восстанавливая естественные процессы торможения в центральной нервной системе, уменьшает и устраняет чувство тревоги (озабоченность, плохие предчувствия, опасения), раздражительность, напряженность (пугливость, плаксивость, чувство беспокойства, неспособность расслабиться, бессонница, страх), депрессивное настроение, соматические проявления тревоги (мышечные, сенсорные, сердечно-сосудистые, дыхательные, желудочно-кишечные расстройства), вегетативные нарушения (сухость во рту, потливость, головокружение), когнитивные (сниженная концентрация внимания, ослабленная память), в т. ч. возникающие при стрессорных расстройствах (расстройствах адаптации). Применение препарата особенно показано пациентам, неустойчивым к стрессу, с астеническими чертами личности: тревожной мнительностью, неуверенностью, повышенной ранимостью и эмоциональной лабильностью. Уменьшение или устранение тревоги, напряженности, соматических, вегетативных, когнитивных нарушений наблюдается на 5–7-й день лечения. Максимальный эффект достигается к концу 4-й нед. лечения и сохраняется после него в среднем в течение 1–2 нед.
Фабомотизол относится к «короткоживущим» препаратам. Время достижения максимальной концентрации в крови составляет 0,85±0,13 ч. Средняя величина максимальной концентрации — 0,13±0,073 мкг/мл. Среднее время удержания препарата в организме — 1,6±0,86 ч. Препарат интенсивно распределяется по хорошо васкуляризированным органам.
В отличие от большинства транквилизаторов фабомотизол можно применять одновременно с лекарственными препаратами других фармакотерапевтических групп, без риска отрицательного влияния на эффективность терапии сопутствующих соматических заболеваний. Фабомотизол применяется не только в психиатрической и неврологической практике, но и в терапевтической практике при тревожных состояниях у пациентов с сопутствующей соматической патологией. В клинических исследованиях и программах клинического наблюдения показана высокая эффективность фабомотизола при различных видах тревожных расстройств у большинства пациентов при отсутствии негативного влияния препарата на течение соматического заболевания, а также на эффективность и безопасность терапии сопутствующей патологии. Эффективность фабомотизола подтверждена при лечении тревожных расстройств у пациентов с заболеваниями сердечно-сосудистой системы (ишемической болезнью сердца, гипертонической болезнью, аритмиями) [9–17], кожи [18–21], желудочно-кишечного тракта [22], с бронхиальной астмой [23], гинекологическими [24, 25] и онкологическими [26] заболеваниями, системной красной волчанкой [27], нарушениями сна [28], алкогольным абстинентным синдромом [29].
Применение фабомотизола в комплексном лечении никотиновой зависимости
Для оценки эффективности фабомотизола в комплексном лечении никотиновой зависимости был проведен анализ динамики симптомов отмены в процессе лечения. В основную группу были включены 30 пациентов, в контрольную — 6. Для оценки анксиолитического действия фабомотизола использовали шкалу тревоги Гамильтона и госпитальную шкалу тревоги и депрессии. Поскольку симптомы отмены развиваются на 1–2-й день после прекращения употребления табака, достигая максимума на 5-й день, и длятся 3–4 нед., то и период наблюдения составил 4 нед. В исследование включили пациентов с высокой степенью никотиновой зависимости и высокой мотивацией к отказу от курения табака, в возрасте от 18 до 60 лет, не принимавших лекарственные средства, обладающие психотропной активностью, с выраженностью тревоги не менее 18 баллов по шкале Гамильтона и не менее 7 баллов по госпитальной шкале тревоги и депрессии [30]. Степень никотиновой зависимости определяли с помощью теста Фагерстрема, а степень мотивации к отказу от табака — с помощью теста Прохаски [30]. Критериями исключения являлись: психоорганические расстройства при первичных дегенеративных церебральных заболеваниях, признаки алкоголизма, лекарственной или наркотической зависимости, беременность, индивидуальная непереносимость препарата, повторное включение пациента в исследование. Лечение никотиновой зависимости у пациентов обеих групп проводили с использованием никотинзаместительной терапии, учитывая степень никотиновой зависимости (тест Фагерстрема) [31, 32]. Всем пациентам основной группы дополнительно назначали фабомотизол с первого дня отказа от табака в дозе 10 мг 3 р./сут в течение 30 дней. Оценку тревоги по шкале Гамильтона и госпитальной шкале тревоги и депрессии проводили за 1–2 дня до начала лечения, а также на 3, 14, 21 и 30-й дни лечения. Характеристика пациентов основной и контрольной групп приведена в таблице 1.

Как видно из таблицы 1, в обеих группах пациенты имели очень высокую степень никотиновой зависимости, очень высокую мотивацию бросить курить, субклинически выраженные тревогу и депрессию. Некоторые пациенты имели клинически выраженные проявления тревоги и депрессии (депрессивный аффект). Сравнение показателей шкалы Гамильтона у пациентов основной группы до начала лечения (1-й визит) с показателями, наблюдаемыми через 3 дня (2-й визит), 14 дней (3-й визит), 21 день (4-й визит) и 30 дней (5-й визит), приведено в таблице 2.
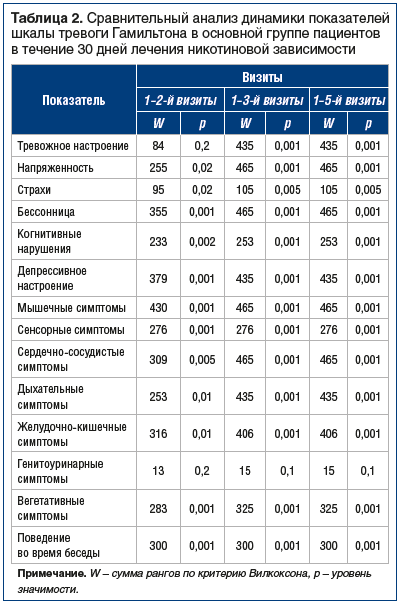
Как видно из таблицы 2, статистически значимая положительная динамика в процессе лечения фабомотизолом в основной группе наблюдалась уже на 3-й день лечения по всем показателям, кроме тревожного настроения и генитоуринарных симптомов. К 14-му дню лечения произошла полная редукция симптомов тревоги. В контрольной группе, в которой пациентам не проводилось лечение фабомотизолом, полная редукция симптомов тревоги наблюдалась только к 30-му дню лечения.
Динамика выраженности симптомов по госпитальной шкале тревоги и депрессии в основной группе представлена в таблице 3.

Как видно из таблицы 3, снижение степени выраженности тревоги при 95% достоверности с уровня «клинически выражена» происходило в интервале 85–100%, с уровня «субклинически выражена» — в интервале 88–100%. Достижение уровня нормы или отсутствия тревоги происходило в интервале 62–100%. Снижение степени выраженности депрессивного настроения с уровня «субклинически выражено» при 95% достоверности происходило в интервале 85–100%, достижение уровня нормы — в интервале 49–75%. Таким образом, полная редукция тревоги, определяемой по госпитальной шкале, при лечении фабомотизолом произошла к 3-й нед. лечения, а в контрольной группе — к 4-й нед., что подтверждено высоким уровнем достоверности.
Применение фабомотизола за 5 дней до даты полного отказа от курения
Анализ динамики выраженности тревоги у каждого пациента выявил, что субклинически выраженная тревога на 2-м визите (3-я нед. лечения) определялась у пациентов, у которых до начала лечения тревога имела степень «клинически выражена». Учитывая терапевтическое действие фабомотизола по уменьшению тревоги и других симптомов тревожных состояний на 5–7-й день лечения, можно ожидать, что эффективность лечения пациентов с выраженным проявлением тревоги может быть повышена за счет назначения фабомотизола за 5 дней до даты полного отказа от курения.
В исследование были включены 15 пациентов с признаками тревоги (не менее 18 баллов по шкале Гамильтона или 8 баллов по госпитальной шкале тревоги и депрессии), с высокой степенью никотиновой зависимости и высокой мотивацией к отказу от табака (табл. 4).

До начала лечения со всеми пациентами проводилась краткая мотивирующая беседа и устанавливалась дата полного отказа от курения табака. Всем пациентам начиная со дня отказа от курения назначали стандартный курс никотинзаместительной терапии в соответствии со степенью никотиновой зависимости (1-й визит) [31, 32]. Для лечения тревожных расстройств пациентам назначали препарат фабомотизол по 10 мг 3 р./сут в течение 30 дней, который они начинали принимать за 5 дней до даты отказа от курения. Эффективность раннего назначения фабомотизола оценивали по динамике показателей выраженности тревоги и депрессии в процессе лечения, определяемых до начала лечения и на 7-й (2-й день отказа от курения, 2-й визит), 14-й (9-й день отказа от курения, 3-й визит) и 30-й (25-й день отказа от курения, 4-й визит) дни лечения. Статистический анализ результатов исследования проводили с использованием критерия Вилкоксона для парных выборочных наблюдений и критерия знаков для двух связанных выборок. Динамика симптомов тревожного расстройства по шкале Гамильтона представлена в таблице 5, динамика симптомов тревоги и депрессии по госпитальной шкале — в таблице 6.


Как видно из таблицы 5, уже на 2-м визите, который соответствовал 7-му дню приема фабомотизола и 2-му дню полного отказа от курения, тяжелая и средняя степени тревоги по шкале Гамильтона не выявлялись. По показателям госпитальной шкалы (см. табл. 6) полная редукция симптомов тревоги и депрессии наблюдалась на 3-м визите, который соответствовал 14-му дню приема фабомотизола и 9-му дню полного отказа от курения. Оценка статистической значимости выявленной динамики проводилась при сравнении показателей, определяемых на 1-м и 2-м визитах, 2-м и 3-м визитах, 3-м и 4-м визитах (табл. 7, табл. 8).

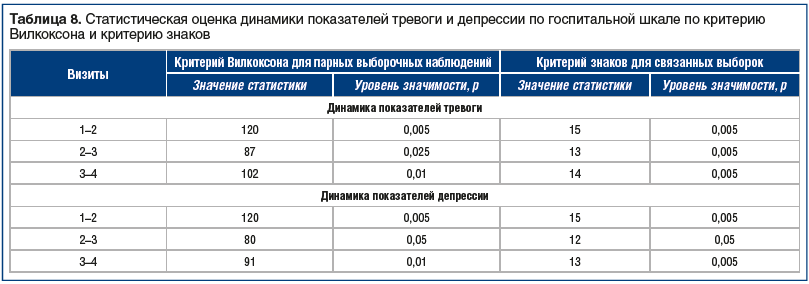
Как видно из таблиц 7 и 8, в процессе комплексного лечения, включающего фабомотизол, наблюдалась положительная динамика в виде снижения депрессии и тревоги по госпитальной шкале, а также тревоги по шкале Гамильтона при сравнении этих показателей между визитами. Выявленная динамика была статистически значимой, что подтверждено критерием Вилкоксона и критерием знаков. Таким образом, назначение фабомотизола за 5 дней до даты отказа от курения позволило к этой дате снизить выраженность тревожных расстройств и депрессивного аффекта и сохранить эту тенденцию на весь период отказа от курения, что важно и для профилактики их обострения при развитии симптомов отмены.
Пациенты хорошо переносили терапию фабомотизолом, нежелательных явлений, связанных с приемом препарата, не наблюдалось. Важно отметить, что на фоне отказа от курения у пациентов, принимавших фабомотизол в составе комплексной терапии, не отмечено статистически значимого изменения массы тела (исходная средняя масса тела — 75,73 кг, после завершения терапии — 75,06 кг). В то же время, по данным литературы, в течение первого месяца после отказа от курения среднее увеличение массы тела составляет 1,1 кг при отсутствии какой-либо терапии и 0,9 кг — при проведении никотинзаместительной терапии.
В результате описанных выше исследований синдром отмены при отказе от курения включили в инструкцию по применению фабомотизола в качестве одного из показаний к применению препарата. Никотиновая зависимость, развивающаяся при употреблении любых форм табака, с учетом выраженности симптомов отмены классифицируется в МКБ-10 как «Синдром зависимости от табака» (F17.2) и «Синдром отмены табака» (F17.3). В Российской Федерации утверждены Клинические рекомендации «Синдром зависимости от табака, синдром отмены табака у взрослых», в которых фабомотизол рекомендован к применению в качестве дополнения к базовой терапии для повышения эффективности устранения симптомов отмены в дозе 10 мг 3 р./сут с минимальной продолжительностью применения 1 мес. [33].
Заключение
Включение фабомотизола в комплексное лечение никотиновой зависимости повышает эффективность лечения за счет его терапевтического действия в отношении имеющихся тревожно-депрессивных проявлений, а также профилактического действия препарата, направленного на симптомы отмены во время отказа от курения. Назначение фабомотизола возможно в двух режимах: с первого дня полного прекращения курения и за 5 дней до первого дня. При обоих режимах назначения фабомотизола в комплексном лечении никотиновой зависимости синдром отмены купируется быстрее, чем у пациентов, у которых фабомотизол не входит в программу лечения.
При назначении фабомотизола за 5 дней до даты отказа от табакокурения у пациентов с повышенной тревожностью происходит редукция тревоги к дате отказа от курения, продолжающаяся на фоне дальнейшего проведения терапии. При назначении пациентам с исходно повышенным уровнем тревожности в комплексной программе лечения фабомотизола за 5 дней до даты отказа от табакокурения не наблюдалось увеличения тревоги к 3-му дню отказа от табакокурения как проявление симптомов отмены табака, в отличие от группы пациентов, в которой фабомотизол назначали с первого дня отказа от табакокурения. Подобные данные об эффективности фабомотизола получены по госпитальной шкале тревоги и депрессии. Выявлено снижение не только уровня тревоги, но и выраженности сопутствующего депрессивного аффекта к дню отказа от табакокурения, которое продолжалось на фоне дальнейшей терапии.
Таким образом, фабомотизол рекомендуется использовать в комплексном лечении пациентов с высокой степенью никотиновой зависимости. Для лиц с повышенной тревожностью, в т. ч. при сопутствующих депрессивных проявлениях, рекомендуется назначение фабомотизола за 5 дней до даты отказа от табакокурения. Редукция тревожного состояния и профилактика развития симптомов отмены (тревожных и депрессивных проявлений) позволяет увеличить эффективность комплексного лечения табачной зависимости.
Статья посвящается памяти видного российского ученого Бориса Львовича Медникова, доктора медицинских наук, профессора, организатора комплекса исследований, благодаря которым фабомотизол широко внедрен в клиническую практику, что повысило эффективность оказания медицинской помощи пациентам с тревожными расстройствами при различных соматических заболеваниях.












