Вопросы безопасности длительной заместительной терапии андрогенами инволютивных изменений традиционно были в сфере интересов практических врачей. Более того, ограничениями в широком использовании данного вида лекарственного воздействия долгие годы служили именно сведения об их побочных действиях. В последние годы благодаря разработке новых андрогенных препаратов и расширения показания к их применению вопрос безопасности гормональной терапии вновь приобрел свою актуальность.
Природной моделью для оценки безопасности андрогенотерапии являются пациенты с женским транссексуализмом (ТС) – типа женщина–мужчина. Эти лица вынужденно должны получать пожизненное лечение андрогенами [Bakker A. et al., 2002] с целью подавления конституциональных признаков генетического пола и приобретения черт, свойственных представителям противоположного пола [Калинченко С.Ю. и соавт., 2000; Gooren L., 2005].
В то же время многофакторное влияние андрогенов на организм обусловливает необходимость детального изучения их влияния на основные виды обменных процессов, минеральную плотность костной ткани и функциональное состояние жизненноважных органов.
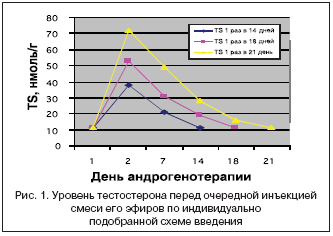
В исследование включены 73 пациента с женским ТС в возрасте от 19 до 46 лет (медиана возраста – 30 [27;34] лет), получающих терапию препаратами тестостерона пролонгированного действия – смесью эфиров тестостерона не менее 1 года (от 1 до 15 лет, медиана – 4 года). Препараты вводили внутримышечно по 1,0 мл 1 раз в 2–4 недели. Доза подбиралась индивидуально в зависимости от скорости метаболизма тестостерона. Уровень тестостерона определялся на 2, 7, 14, 18 и 21–й дни после введения разовой дозы препарата. Индивидуально подобранная доза не менялась на протяжении всего периода лечения.
До проведения настоящего исследования маскулинизирующая маммопластика была выполнена у всех 73 пациентов с женским ТС, у 52 – проведена операция удаления матки с яичниками. Фаллопластика была выполнена 23 лицам с женским ТС; 5 пациентам после проведенных гистерэктомии с двусторонней овариэктомией и фаллопластики была также выполнена и уретропластика.
Две группы контроля составили 20 здоровых мужчин с медианой возраста 35 [34;38] лет и 20 здоровых женщин с медианой возраста 31 [29,5;36,5] год, проходившие диспансеризацию в медицинском центре.
Статистическую обработку полученных данных проводили с использованием пакета прикладных программ Statistica (StatSoft Inc. США, версия 6.0).
Результаты гормонального обследования пациентов с женским ТС по сравнению со здоровыми мужчинами и женщинами представлены в таблице 1.
Как видно из данных таблицы 1, уровень тестостерона в группе обследованных пациентов с женским ТС превышал уровень тестостерона в контрольной группе женщин (17,3 [10,9;24,3] нмоль/л и 0,7 [0,35;0,9] нмоль/л соответственно, р<0,001) и не отличался в группе мужчин (рис. 1, 2).
Таким образом, длительная андрогенотерапия в индивидуально подобранных дозах оставалась адекватной на протяжении всего курса терапии. Ни у кого из обследованных лиц не возникало необходимости в уменьшении или увеличении дозы вводившегося препарата, а также интервалов между его введениями, что свидетельствует об отсутствии кумуляции.
Снижения чувствительности к вводимой дозе эфиров тестостерона не отмечалось, в связи с чем необходимости в повышении дозы ни у кого из пациентов с женским ТС не возникало. Развития толерантности к проводимой андрогенной терапии и побочных ее эффектов выявлено не было, что свидетельствует об отсутствии развития сенсибилизации к терапии андрогенами.
Об адекватности проводимой терапии свидетельствовало то, что у 42 пациентов с женским ТС оволосение было оценено как Р4, А4, Р5, у 31 – как Р2–3, А4, Р4, а показатели Р2–4, А4, Р4–5 – соответствовали выраженной андрогенизации организма.
Как видно из таблицы 2, окружность талии 80±1,5 см и индекс массы тела 22 кг/м2 [20;24] у 64 пациентов с женским ТС оказались в пределах нормальных значений; у 9 человек – она составила 100±1,5 см, что соответствует абдоминальному ожирению, а ИМТ при этом составил 25 кг/м2. В группе контроля здоровых женщин окружность талии (79±1,5 см) и ИМТ (24 кг/м2) находились в пределах нормальных значений [24;25], а в группе здоровых мужчин у 6 человек окружность талии и ИМТ составила 96±1,5 см и 26 кг/м2, что соответствует абдоминальному ожирению, а у 15 – 92±1,5 см и 25,5 кг/м2 [25;26], что соответствует норме. Таким образом, по сравнению с контрольной группой мужчин у пациентов с женским ТС не выявлено различий в распространенности ожирения. В то же время длительная андрогенотерапия существенно повышает представленность ожирения у пациентов с женским ТС по сравнению со здоровыми женщинами (р<0,001).
Как видно из представленных в таблице 3 данных, медиана уровня гемоглобина составила в основной группе 150 г/л [145;160], что достоверно (р<0,001) выше соответствующего показателя в группе здоровых женщин 134,5 г/л [130,5;141,5], но не отличается статистически значимо от контрольной группы мужчин 151,0 [142;155]. Уровни эритроцитов – 5,0х109/л [4,7;5,3] и гематокрита – 44% [42;48] также оказались в основной группе достоверно (р<0,001) выше, чем в группе здоровых женщин, но не отличались от соответствующих показателей здоровых мужчин. Несмотря на то, что средние значения анализируемых показателей у пациентов с женским ТС не отличались от здоровых мужчин, тем не менее у 18 (25%) пациентов с женским ТС наблюдалось повышение уровня гемоглобина выше верхней физиологической нормы мужчин, у 26 (36%) – эритроцитоз и у 9 (12%) – более высокий уровень гематокрита. При корреляционном анализе установлена прямая взаимосвязь между уровнями тестостерона и гемоглобина (r=0,29; р=0,04) и тестостерона с эритроцитами (r=0,33; р=0,02). Однако при той же статистической обработке выявлена достоверная отрицательная корреляция (r=–0,247175; p=0,035010) между уровнем гемоглобина и длительностью терапии андрогенами (табл. 4).
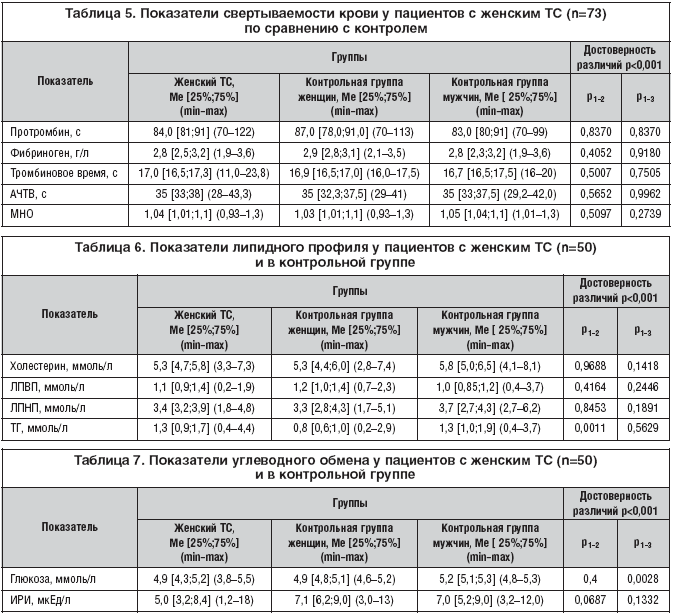
Как видно из представленных в таблице 5 данных, у всех 73 пациентов с женским ТС показатели фибринолиза соответствовали нормальным значениям и не отличались от обеих групп контроля. Как видно из таблицы 6, уровни холестерина, липопротеидов высокой и низкой плотности достоверно не отличались от соответствующих показателей в обеих группах контроля. В то же время уровень триглицеридов в основной группе составил 1,3 [0,9;1,7] ммоль/л, достоверно превышая соответствующий показатель только в группе здоровых женщин (0,8 [0,6;1,0]).
Уровень иммунореактивного инсулина, определенный у 50 пациентов с женским ТС, был в пределах нормальных значений 5,0 [3,2–8,4] мкЕд/мл и достоверно не отличался от значений в обеих контрольных группах (табл. 7). Уровень же глюкозы в основной группе был достоверно (p<0,001) ниже, чем в группе здоровых мужчин (5,2 [5,1;5,3]), и не отличался от соответствующего показателя в группе здоровых женщин.
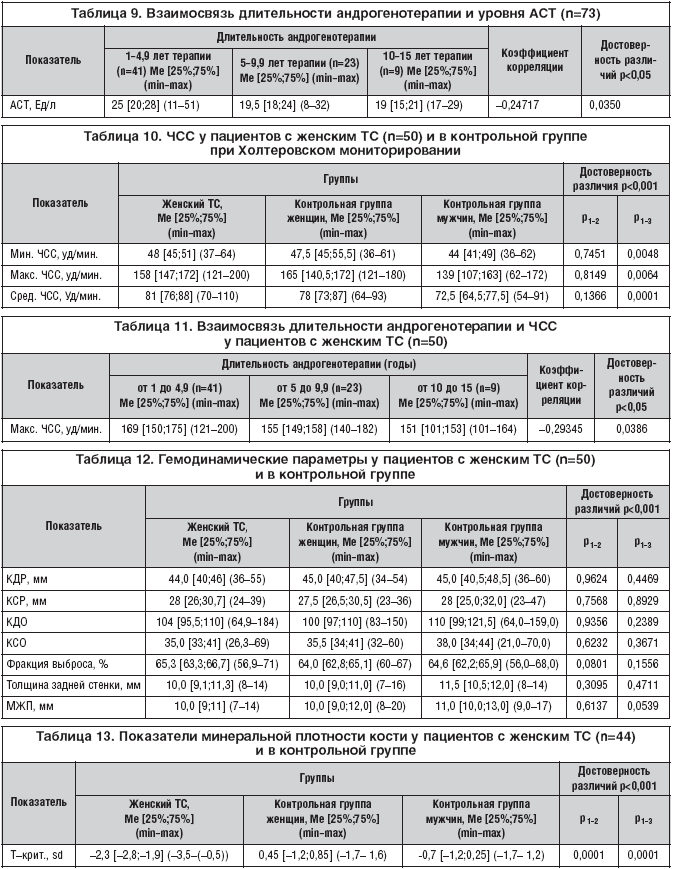
Уровень аспарагин–аминотрансферазы в обследованной группе пациентов с женским ТС (табл. 8) оказался достоверно (р<0,001) выше, чем в группе здоровых женщин, и ниже, чем в группе здоровых мужчин, соответственно 22 [18;27] Ед/л и 16,5 [13;22]. Уровень аланин–аминотрансферазы имел тенденцию к повышению в женской группе контроля (16,0 [14,5;20,0]) и был статистически значимо (р<0,001) ниже, чем в контрольной группе мужчин (29 [19,5;34,5]). Только у 3 обследованных пациентов с женским ТС повышение ферментов печени было незначительно выше нормы, у остальных 70 – уровни АСТ и АЛТ находились в пределах нормальных значений. Более того, предполагаемое гепатотоксическое влияние андрогенов при длительном их применении по данным корреляционного анализа не подтверждается (табл. 9).
Из 64 обследованных пациентов с женским ТС ультразвуковое исследование печени показало нормальные размеры и ее эхо–структуру у 43 человек; у 6 выявлены диффузные изменения печени, у 9 – признаки жировой инфильтрации, у 2 – умеренное уплотнение паренхимы, у 2 – капиллярная гемангиома, у 1 – деформация желчного пузыря и у 1 – калькулезный холецистит вне обострения. В контрольной группе мужчин нормальные размеры и эхо–структура печени отмечены у 13 человек; диффузные ее изменения – у 5, признаки жировой инфильтрации – у 2. В женской группе контроля у 14 человек размеры и эхо–структура печени были не изменены, у 4 человек выявлены диффузные изменения печени и у 2 – деформация желчного пузыря.
Ультразвуковое исследование органов малого таза, проведенное у 21 пациента с женским ТС, длительно получающего андрогены и с сохраненной маткой и яичниками выявило эхо–признаки инволютивных их изменений (уменьшения размеров матки и яичников), характерных для постменопаузального периода. В женской группе контроля у 17 человек признаков УЗИ патологии не выявлено; у 3 человек – односторонние кисты яичника, которые при УЗИ динамике носили функциональный характер.
При Холтеровском мониторировании у 50 пациентов с женским ТС значимых колебаний сегмента ST не выявлено. У 23 из них определялся синусовый ритм, у 19 – эпизоды синусовой аритмии, у 7 – миграция водителя ритма, у 6 – желудочковая и у 5 – наджелудочковая экстрасистолия. В единичных наблюдениях диагностированы синдром ранней реполяризации желудочков, наджелудочковая экстрасистолия с эпизодами неустойчивой пароксизмальной суправентрикулярной тахикардией.
Как видно из таблицы 10, достоверных отличий между ЧСС у пациентов с женским ТС и в контрольной группе женщин выявлено не было. В то же время по сравнению с контрольной группой мужчин у пациентов с женским ТС имелась достоверная тенденция к учащению сердечного ритма. И эта закономерность по данным корреляционного анализа (табл. 11) зависела от длительности андрогенотерапии (r=–0,293450; p=0,038612).
Как видно из представленных данных в таблице 12, эхокардиография не выявила статистически достоверных отличий основных гемодинамических параметров в исследуемой (n=50) и обеих контрольных группах. У 35 пациентов с женским ТС патологии не выявлено, пролапс митрального клапана 1 степени диагностирован у 6 пациентов, в том числе с регургитацией 1 степени у 2, у 9 – гипертрофия левого желудочка (толщина МЖП 13 мм, ЗСЛЖ 12 мм). Ни у одного пациента с выявленной гипертрофией миокарда левого желудочка не отмечено повышение АД, в том числе по данным АД–мониторирования.
В результаты проведенного полифункционального исследования наибольшие изменения у пациентов с женским ТС отмечено со стороны костной ткани (табл. 13). При этом было диагностировано высокодостоверное (p<0,001) снижение минеральной плотности кости: Т–критерий составил в основной группе –2,3sd [–2,8;–1,9], в группах женского и мужского контроля – соответственно 0,45sd [–1,2;0,85], –0,7sd [–1,2;0,25]. Остеопороз был диагностирован у 17 пациентов (38%), остеопения – у 24 (54%); в группах контроля среди женщин остеопения была выявлена у 5 человек (25%), среди мужчин – у 4 (20%).
Таким образом, выявленное у пациентов с женским ТС снижение минеральной плотности костной ткани может быть связано как с вынужденной гормональной перестройкой, так и влиянием непосредственно препаратов тестостерона на метаболизм костной ткани. В любом случае, это требует дальнейшего изучения и разработки соответствующего плана лечения и профилактики остеопороза у пациентов с женским ТС.
Выводы
1. У пациентов с женским транссексуализмом, как на модели природного гипогонадизма показана безопасность вынужденной длительной терапии андрогенами в отношении основных видов обмена, функционального состояния сердечно–сосудистой системы, печени и минеральной плотности костной ткани.
2. При длительной андрогенной терапии у пациентов с женским транссексуализмом не развивается кумуляция, сенсибилизация и толерантность к препаратам тестостерона.
3. У пациентов с женским транссексуализмом препараты тестостерона не оказывают стимулирующего действия на секрецию инсулина, не вызывают гипергликемию, не нарушают обмен липидов и гемостаз.
4. Терапия андрогенами не вызывает изменений со стороны функционального состояния сердечно–сосудистой системы и печени.
5. У подавляющего большинства пациентов с женским транссексуализмом выявлено снижение минеральной плотности костной ткани, что может быть обусловлено вынужденной гормональной перестройкой костного метаболизма под влиянием андрогенных препаратов.