–Я—А–Њ–±–ї–µ–Љ—Л, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б —И–Є—А–Њ–Ї–Є–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Э–Я–Т–Я, –љ–Њ—Б—П—В –Љ—Г–ї—М—В–Є–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –Є –Њ–±—Б—Г–ґ–і–∞—О—В—Б—П –≤ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –љ–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е [1, 2] –Є –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л—Е [3] –Ї–Њ–љ—Б–µ–љ—Б—Г—Б–∞—Е. –Ю—Б–Њ–±—Г—О –∞–Ї—В—Г–∞–ї—М–љ–Њ—Б—В—М –њ—А–Є–Њ–±—А–µ—В–∞–µ—В —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–µ –љ–µ–≥–∞—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Э–Я–Т–Я –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г –Ц–Ъ–Ґ. –Я—А–Є —Н—В–Њ–Љ –≥–∞—Б—В—А–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –≤—Л–Ј—Л–≤–∞—О—В –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –≤—Б–µ –Э–Я–Т–Я (—Б —А–∞–Ј–љ–Њ–є —З–∞—Б—В–Њ—В–Њ–є) –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –Є—Е —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В—А–Њ–µ–љ–Є—П, –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л –Є —Б–њ–Њ—Б–Њ–±–∞ –≤–≤–µ–і–µ–љ–Є—П. –Ґ–∞–Ї, –Њ–і–љ–Њ–Ї—А–∞—В–љ—Л–є –Є–ї–Є –і–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Є–µ–Љ –Э–Я–Т–Я –≤ 12–30% —Б–ї—Г—З–∞–µ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О —П–Ј–≤—Л –ґ–µ–ї—Г–і–Ї–∞ –Є –≤ 2–19% – —П–Ј–≤—Л –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є. –≠—А–Њ–Ј–Є–≤–љ–Њ-—П–Ј–≤–µ–љ–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –Ц–Ъ–Ґ –Њ—В–Љ–µ—З–∞–µ—В—Б—П, –њ–Њ –і–∞–љ–љ—Л–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –Є—Б—В–Њ—З–љ–Є–Ї–Њ–≤, —Г 20–40% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —А–µ–≥—Г–ї—П—А–љ–Њ –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е –Э–Я–Т–Я [4]. –Я–Њ –і–∞–љ–љ—Л–Љ –Р.–Х. –Ъ–∞—А–∞—В–µ–µ–≤–∞, –Т.–Р. –Э–∞—Б–Њ–љ–Њ–≤–Њ–є (2000), —З–∞—Б—В–Њ—В–∞ –≤—Л—П–≤–ї–µ–љ–Є—П —Н—А–Њ–Ј–Є–≤–љ–Њ-—П–Ј–≤–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е, –љ–∞–±–ї—О–і–∞–≤—И–Є—Е—Б—П –≤ –Ї–ї–Є–љ–Є–Ї–µ –Ш–љ—Б—В–Є—В—Г—В–∞ —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є –†–Р–Ь–Э –Є –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Э–Я–Т–Я –љ–∞ –Љ–Њ–Љ–µ–љ—В –њ—А–Њ–≤–µ–і–µ–љ–Є—П –≥–∞—Б—В—А–Њ—Б–Ї–Њ–њ–Є–Є, —Б–Њ—Б—В–∞–≤–Є–ї–∞ 33,8% [5]. –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ A. Lanas –Є —Б–Њ–∞–≤—В. (2006), –Э–Я–Т–Я –Є –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ (–Р–°–Ъ) —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В —А–Є—Б–Ї —П–Ј–≤–µ–љ–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П –≤ 3,5 –Є 3,1 —А–∞–Ј–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [6].
–Р–Ї—В—Г–∞–ї—М–љ–Њ—Б—В—М –і–∞–љ–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ—Л –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–Љ, –љ–Њ –Є —Б–Њ—Ж–Є–∞–ї—М–љ–Њ-—Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–Љ –∞—Б–њ–µ–Ї—В–Њ–Љ, —Б–≤—П–Ј–∞–љ–љ—Л–Љ —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –Є —Б–Љ–µ—А—В–µ–є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л—Е –Ї–∞–Ї –њ–Њ–±–Њ—З–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є –Э–Я–Т–Я, —В–∞–Ї –Є –≤–ї–Є—П–љ–Є–µ–Љ «–≥—А–Њ–Ј–љ—Л—Е» –Э–Я–Т–Я-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –љ–∞ —В–µ—З–µ–љ–Є–µ –Є –Є—Б—Е–Њ–і —В—П–ґ–µ–ї—Л—Е —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–∞—Ж–Є–µ–љ—В–∞. –Ф–∞–љ–љ—Л–µ J. Fries (1996), –Њ—Б–љ–Њ–≤–∞–љ–љ—Л–µ –љ–∞ –∞–љ–∞–ї–Є–Ј–µ –Э–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –±–∞–љ–Ї–∞ –і–∞–љ–љ—Л—Е ARAMIS, –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –µ–ґ–µ–≥–Њ–і–љ–Њ 1,6% –±–Њ–ї—М–љ—Л—Е —А–µ–≤–Љ–∞—В–Њ–Є–і–љ—Л–Љ –∞—А—В—А–Є—В–Њ–Љ, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Э–Я–Т–Я, –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–Є—А—Г—О—В—Б—П –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А—Л –≤ —Б–≤—П–Ј–Є —Б —В—П–ґ–µ–ї—Л–Љ–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П–Љ–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ, –њ—А–Є —Н—В–Њ–Љ 0,18% –µ–ґ–µ–≥–Њ–і–љ–Њ —Г–Љ–Є—А–∞—О—В [7]. –°–Њ–≥–ї–∞—Б–љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–љ—Л–Љ G. Singh —А–∞—Б—З–µ—В–∞–Љ, –µ–ґ–µ–≥–Њ–і–љ–Њ –≤ –°–®–Р –њ—А–Њ–≥–љ–Њ–Ј–Є—А—Г–µ—В—Б—П 107 —В—Л—Б. –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –Є 16 500 —Б–Љ–µ—А—В–µ–є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –Њ–њ–∞—Б–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –њ—А–Є–µ–Љ–Њ–Љ –Э–Я–Т–Я [5].
–°–µ—А—М–µ–Ј–љ–Њ—Б—В—М –њ—А–Њ–±–ї–µ–Љ—Л –Э–Я–Т–Я-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —В–∞–Ї–ґ–µ –µ–≤—А–Њ–њ–µ–є—Б–Ї–Є–Љ–Є —Г—З–µ–љ—Л–Љ–Є. –Ґ–∞–Ї, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –≤ –Ф–∞–љ–Є–Є L. Lipworth –Є —Б–Њ–∞–≤—В. (2004) –Є –њ–Њ—Б–≤—П—Й–µ–љ–љ–Њ–µ –∞–љ–∞–ї–Є–Ј—Г –њ—А–Є—З–Є–љ —Б–Љ–µ—А—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –Ф–∞–љ–Є–Є, –Ї–Њ—В–Њ—А—Л–Љ –±—Л–ї –љ–∞–Ј–љ–∞—З–µ–љ –Є–±—Г–њ—А–Њ—Д–µ–љ (n=113 538), –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –µ–≥–Њ –њ—А–Є–µ–Љ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї—Б—П —Б –њ–Њ—З—В–Є —В—А–µ—Е–Ї—А–∞—В–љ—Л–Љ –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л –ї–µ—В–∞–ї—М–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ –Њ—В –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ—Л—Е –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –µ–≤—А–Њ–њ–µ–є—Б–Ї–Њ–є –њ–Њ–њ—Г–ї—П—Ж–Є–µ–є [8]. –°–Њ–≥–ї–∞—Б–љ–Њ V. Merle –Є —Б–Њ–∞–≤—В. (2004), –≤–Њ –§—А–∞–љ—Ж–Є–Є –±–Њ–ї–µ–µ 25% –ї—О–і–µ–є —Б—В–∞—А—И–µ 40 –ї–µ—В –њ—А–Є–љ–Є–Љ–∞—О—В –Э–Я–Т–Я, –њ—А–Є —Н—В–Њ–Љ —А–Є—Б–Ї c–Љ–µ—А—В–Є –Њ—В –Ц–Ъ–Ґ-–Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –≤ 4 —А–∞–Ј–∞ [9]. –Я–Њ –і–∞–љ–љ—Л–Љ M. Tramer –Є —Б–Њ–∞–≤—В. (2000), –≤ –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є–Є –љ–µ –Љ–µ–љ–µ–µ 2 —В—Л—Б. –±–Њ–ї—М–љ—Л—Е –µ–ґ–µ–≥–Њ–і–љ–Њ —Г–Љ–Є—А–∞—О—В –Њ—В –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ—Л—Е –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–є –Є –њ–µ—А—Д–Њ—А–∞—Ж–Є–Є —П–Ј–≤, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –Э–Я–Т–Я [10]. –Т —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Є—Б–њ–∞–љ—Б–Ї–Є—Е –Є –Є—В–∞–ї—М—П–љ—Б–Ї–Є—Е —Г—З–µ–љ—Л—Е [Laporte J. –Є —Б–Њ–∞–≤—В., 2004], –њ–Њ—Б–≤—П—Й–µ–љ–љ–Њ–Љ –Є–Ј—Г—З–µ–љ–Є—О –≥–∞—Б—В—А–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –Э–Я–Т–Я, —Б—А–µ–і–Є –Њ–±—Й–µ–≥–Њ —З–Є—Б–ї–∞ –±–Њ–ї—М–љ—Л—Е (n=2813) —Б –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ—Л–Љ–Є –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П–Љ–Є 38% –њ—А–Є–љ–Є–Љ–∞–ї–Є –Э–Я–Т–Я [11].
–Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –њ—А–Є–µ–Љ –Э–Я–Т–Я –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–Ј–≤–Є—В–Є—О —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Њ—Б—В—А–Њ–≥–Њ –≥–∞—Б—В—А–Є—В–∞ –≤ —В–µ—З–µ–љ–Є–µ –љ–µ–і–µ–ї–Є –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П [4]. –£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Н—А–Њ–Ј–Є–Є —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –њ–Њ—Б–ї–µ –њ—А–Є–µ–Љ–∞ –Ї–∞–ґ–і–Њ–є –і–Њ–Ј—Л –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Э–Я–Т–Я, –∞ —Г 15–30% –±–Њ–ї—М–љ—Л—Е, –і–ї–Є—В–µ–ї—М–љ–Њ –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е –Э–Я–Т–Я, —П–Ј–≤—Л –ґ–µ–ї—Г–і–Ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–Є —Е–Њ—В—П –±—Л –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ [12].
–°–њ–µ–Ї—В—А –≥–∞—Б—В—А–Њ–Є–љ—В–µ—Б—В–Є–љ–∞–ї—М–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –њ—А–Є–µ–Љ–Њ–Љ –Э–Я–Т–Я, –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —И–Є—А–Њ–Ї –Є –≤–∞—А—М–Є—А—Г–µ—В –Њ—В –ї–µ–≥–Ї–Њ–є –і–Є—Б–њ–µ–њ—Б–Є–Є –і–Њ —А–∞–Ј–≤–Є—В–Є—П —Н—А–Њ–Ј–Є–є (—З–∞—Б—В–Њ –Љ–љ–Њ–ґ–µ—Б—В–≤–µ–љ–љ—Л—Е) –Є –њ–µ–њ—В–Є—З–µ—Б–Ї–Є—Е —П–Ј–≤. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Д–∞–Ї—В–Є—З–µ—Б–Ї–Є –Љ–љ–Њ–≥–Є–µ —Б–µ—А—М–µ–Ј–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –њ—А–Є–µ–Љ–Њ–Љ –Э–Я–Т–Я, –Љ–Њ–≥—Г—В –њ—А–Њ—В–µ–Ї–∞—В—М –±–µ–Ј —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –Љ–∞–љ–Є—Д–µ—Б—В–Є—А—Г—П –њ–µ—А—Д–Њ—А–∞—Ж–Є–µ–є –Є–ї–Є —В—П–ґ–µ–ї—Л–Љ –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Л–Љ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–µ–Љ [13, 14]. –Ю—В—Б—Г—В—Б—В–≤–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –Э–Я–Т–Я-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є –Ц–Ъ–Ґ (–љ–∞–ї–Є—З–Є–µ –≤ 70% —Б–ї—Г—З–∞–µ–≤ —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л—Е «–љ–µ–Љ—Л—Е —П–Ј–≤») –Ј–∞—З–∞—Б—В—Г—О –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Ї–∞–Ї —В–Њ—А–Љ–Њ–ґ–µ–љ–Є–µ–Љ –±–Є–Њ—Б–Є–љ—В–µ–Ј–∞ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ – –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –±–Њ–ї–Є –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, —В–∞–Ї –Є —Б—Г–≥—Г–±–Њ —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л–Љ–Є –Њ—Й—Г—Й–µ–љ–Є—П–Љ–Є, –њ—А–Њ—П–≤–ї—П—О—Й–Є–Љ–Є—Б—П –љ–µ –Є—Б—В–Є–љ–љ—Л–Љ –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–є, –∞ —В–µ–Љ, —З—В–Њ –ґ–∞–ї–Њ–±—Л, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Њ—Б–љ–Њ–≤–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ, –±–µ—Б–њ–Њ–Ї–Њ—П—В –њ–∞—Ж–Є–µ–љ—В–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –±–Њ–ї—М—И–µ, –љ–µ–ґ–µ–ї–Є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ. –°–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –љ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М —А–∞—Б—Ж–µ–љ–µ–љ–Њ –Ї–∞–Ї –Њ–і–љ–Њ–Ј–љ–∞—З–љ—Л–є –њ—А–Є–Ј–љ–∞–Ї –Њ—В—Б—Г—В—Б—В–≤–Є—П –њ–Њ—А–∞–ґ–µ–љ–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є.
–Ю–±—Й–µ–Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Э–Я–Т–Я-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л —Г–ї—М—Ж–µ—А–Њ–≥–µ–љ–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г –Ц–Ъ–Ґ. –Я—А–Є —Н—В–Њ–Љ, –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є —Н—А–Њ–Ј–Є–≤–љ–Њ-—П–Ј–≤–µ–љ–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —А–∞–Ј–≤–Є—В–Є–µ –і–≤—Г—Е –≤–∞—А–Є–∞–љ—В–Њ–≤ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞: –Ї–∞–Ї –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –≤–Њ –≤—А–µ–Љ—П –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –Э–Я–Т–Я (—З—В–Њ —Б–њ—А–∞–≤–µ–і–ї–Є–≤–Њ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Р–°–Ъ –Є –µ–µ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е), —В–∞–Ї –Є —Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ —Б –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Л (–¶–Ю–У) – –Ї–ї—О—З–µ–≤–Њ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ –≤ –Ї–∞—Б–Ї–∞–і–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л, –Ї–Њ—В–Њ—А–∞—П —П–≤–ї—П–µ—В—Б—П –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–Њ–Љ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–Њ–≤ –Є —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ–Њ–≤—В–Њ—А–љ–Њ–µ –њ–Њ–њ–∞–і–∞–љ–Є–µ –∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –Э–Я–Т–Я —Б –ґ–µ–ї—З—М—О –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–Ї—Б–Ї—А–µ—Ж–Є–Є –≤ –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ—Г—О –Ї–Є—И–Ї—Г –Є –ґ–µ–ї—Г–і–Њ–Ї –њ—А–Є –і—Г–Њ–і–µ–љ–Њ–≥–∞—Б—В—А–∞–ї—М–љ–Њ–Љ —А–µ—Д–ї—О–Ї—Б–µ. –Р—А–∞—Е–Є–і–Њ–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞, –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—П—Б—М –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –¶–Ю–У, –њ—А–µ–Њ–±—А–∞–Ј—Г–µ—В—Б—П –≤ —Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–µ —Н–љ–і–Њ–њ–µ—А–Њ–Ї—Б–Є–і—Л –Є –њ—А–µ–≤—А–∞—Й–∞–µ—В—Б—П –≤ —В–∞–Ї–Є–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П, –Ї–∞–Ї –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ—Л, –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ—Л –Є —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ—Л (–њ—А–Њ—Б—В–∞–љ–Њ–Є–і—Л). –¶–Ю–У-1 («–Ї–Њ–љ—Б—В–Є—В—Г—В–Є–≤–љ–∞—П» –Є–Ј–Њ—Д–Њ—А–Љ–∞) –њ–Њ—Б—В–Њ—П–љ–љ–Њ –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —В–Ї–∞–љ–µ–є, —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А—Г–µ—В –Ї–∞–Ї –њ–Њ—Б—В–Њ—П–љ–љ—Л–є –Ї–ї–µ—В–Њ—З–љ—Л–є —Д–µ—А–Љ–µ–љ—В –Є —А–µ–≥—Г–ї–Є—А—Г–µ—В —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤ –≤ —В–Ї–∞–љ—П—Е –Є –Њ—А–≥–∞–љ–∞—Е (–≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞ –Х1), –Ї–Њ—В–Њ—А—Л–µ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г—О—В –ґ–µ–ї—Г–і–Њ—З–љ—Г—О —Б–µ–Ї—А–µ—Ж–Є—О –Є –Ј–∞—Й–Є—Й–∞—О—В —Б–ї–Є–Ј–Є—Б—В—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г –Ц–Ъ–Ґ. –≠–Ї—Б–њ—А–µ—Б—Б–Є–Є –¶–Ю–У-2 («–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є» –Є–Ј–Њ—Д–Њ—А–Љ—Л) –≤ –љ–Њ—А–Љ–µ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —В–Ї–∞–љ–µ–є –љ–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В, –љ–Њ –µ–µ —Г—А–Њ–≤–µ–љ—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –њ—А–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–Є —В–Ї–∞–љ–µ–є –Є–ї–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–Є –≤ –Њ—В–≤–µ—В –љ–∞ –і–µ–є—Б—В–≤–Є–µ —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ (–§–Э–Ю-α, –Ш–Ы-1), —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ –Ї–Є—Б–ї–Њ—А–Њ–і–∞, —А—П–і–∞ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Њ—Б—В–∞ –≤ –Љ–∞–Ї—А–Њ—Д–∞–≥–∞—Е, —Б–Є–љ–Њ–≤–Є–Њ—Ж–Є—В–∞—Е, —Д–Є–±—А–Њ–±–ї–∞—Б—В–∞—Е, –≥–ї–∞–і–Ї–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А–µ, —Е–Њ–љ–і—А–Њ—Ж–Є—В–∞—Е –Є —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л—Е –Ї–ї–µ—В–Ї–∞—Е, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –¶–Ю–У-2 —Б—З–Є—В–∞—О—В –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ–є –Ј–∞ —А–∞–Ј–≤–Є—В–Є–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –±–Њ–ї–Є –Є –ї–Є—Е–Њ—А–∞–і–Ї–Є, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —З–µ–≥–Њ –Њ–±—А–∞–Ј—Г—О—В—Б—П –њ—А–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –Љ–µ–і–Є–∞—В–Њ—А—Л, –њ–Њ–≤—Л—И–∞—О—Й–Є–µ –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є –Є —А–∞—Б—И–Є—А—П—О—Й–Є–µ —Б–Њ—Б—Г–і—Л.
–Э—Л–љ–µ –Њ–±—Й–µ–њ—А–Є–Ј–љ–∞–љ–љ–Њ–є —П–≤–ї—П–µ—В—Б—П —В–Њ—З–Ї–∞ –Ј—А–µ–љ–Є—П, —Б–Њ–≥–ї–∞—Б–љ–Њ –Ї–Њ—В–Њ—А–Њ–є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞—В—М —А–∞–Ј–≤–Є—В–Є–µ –Э–Я–Т–Я-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є. –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ–Њ–±–Њ—З–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Э–Я–Т–Я –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –љ–µ —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є–љ–Є–Љ–∞—О—Й–Є—Е –і–∞–љ–љ—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞. –Ю–±—К—П—Б–љ–µ–љ–Є–µ –≤—Л—И–µ–љ–∞–Ј–≤–∞–љ–љ–Њ–≥–Њ —Д–µ–љ–Њ–Љ–µ–љ–∞ —Б–≤—П–Ј–∞–љ–Њ —Б –љ–∞–ї–Є—З–Є–µ–Љ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –Ц–Ъ–Ґ. –Т–∞–ґ–љ–µ–є—И–Є–Љ–Є —Б—А–µ–і–Є –љ–Є—Е —П–≤–ї—П—О—В—Б—П: –њ–Њ–ґ–Є–ї–Њ–є –≤–Њ–Ј—А–∞—Б—В (—Б—В–∞—А—И–µ 65 –ї–µ—В), —П–Ј–≤–µ–љ–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј (—Н–њ–Є–Ј–Њ–і –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є—П –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ), –њ—А–Є–µ–Љ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Э–Я–Т–Я –Є–ї–Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є –њ—А–Є–µ–Љ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Њ–є –≥—А—Г–њ–њ—Л (–≤ —В. —З. –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –Р–°–Ъ), —В—П–ґ–µ–ї—Л–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П – —В–∞–Ї–Є–µ –Ї–∞–Ї –Ј–∞—Б—В–Њ–є–љ–∞—П —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–є –њ—А–Є–µ–Љ –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤, –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤. –Ъ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–Љ —Д–∞–Ї—В–Њ—А–∞–Љ —А–Є—Б–Ї–∞ –Њ—В–љ–Њ—Б—П—В –љ–∞–ї–Є—З–Є–µ —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–≥–Њ –∞—А—В—А–Є—В–∞, –ґ–µ–љ—Б–Ї–Є–є –њ–Њ–ї, –Ї—Г—А–µ–љ–Є–µ, –њ—А–Є–µ–Љ –∞–ї–Ї–Њ–≥–Њ–ї—П [5, 15, 16]. –Ъ —Н—В–Њ–є –ґ–µ –≥—А—Г–њ–њ–µ –њ—А–Є—З–Є—Б–ї—П—О—В –Є –Є–љ—Д–µ–Ї—Ж–Є—О H. pylori [17].
–Я—А–Є —Н—В–Њ–Љ, –Њ—Ж–µ–љ–Ї–∞ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—Б—П —Б —Г—З–µ—В–Њ–Љ –Є—Е –≥—А–∞–і–∞—Ж–Є–Є –і–ї—П –Ї–∞–ґ–і–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ (—В–∞–±–ї. 1) [18].
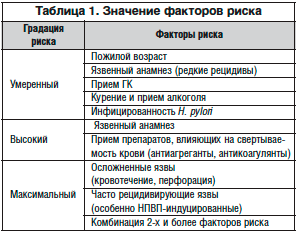
–Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –≤—Л–≤–Њ–і–∞–Љ–Є –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є (2002), –љ–Є–Ј–Ї–Є–є —А–Є—Б–Ї –≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –њ—А–Є–µ–Љ–Њ–Љ –Э–Я–Т–Я, –љ–∞–±–ї—О–і–∞–µ—В—Б—П —В–Њ–ї—М–Ї–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–µ –Є–Љ–µ—О—Й–Є—Е –љ–Є –Њ–і–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–Є—Б–Ї–∞.
–Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –≤—Б–µ –±–Њ–ї—М—И—Г—О –∞–Ї—В—Г–∞–ї—М–љ–Њ—Б—В—М –њ—А–Є–Њ–±—А–µ—В–∞—О—В –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –Є–Ј—Г—З–µ–љ–Є—П –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –≥–µ–љ–Њ–≤ (–≥–µ–љ–Њ–Љ–∞) —З–µ–ї–Њ–≤–µ–Ї–∞, —З—В–Њ —Б–Њ–Ј–і–∞–µ—В –њ—А–µ–і–њ–Њ—Б—Л–ї–Ї–Є –і–ї—П –њ–Њ–і–±–Њ—А–∞ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–є —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є–Є, –∞ —В–∞–Ї–ґ–µ –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є.
–Я–Њ–љ–Є–Љ–∞–љ–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –Ц–Ъ–Ґ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Э–Я–Т–Я –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г–≥–ї—Г–±–Є–ї–Њ—Б—М, —З—В–Њ –њ—А–Є–≤–µ–ї–Њ –Ї —А–∞–Ј—А–∞–±–Њ—В–Ї–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—Е–µ–Љ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –Э–Я–Т–Я-–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –≤–µ—А—Е–љ–Є—Е –Њ—В–і–µ–ї–Њ–≤ –Ц–Ъ–Ґ. –Э–∞–Є–±–Њ–ї–µ–µ —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –њ–Њ–і—Е–Њ–і–Њ–Љ —Б—З–Є—В–∞–µ—В—Б—П —Ж–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–∞—П —Н–љ–і–Њ—Б–Ї–Њ–њ–Є—З–µ—Б–Ї–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –њ–µ—А–≤–Є—З–љ–∞—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –Э–Я–Т–Я-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є —Б —Г—З–µ—В–Њ–Љ —А–∞—Б—Б–Љ–Њ—В—А–µ–љ–љ—Л—Е –≤—Л—И–µ —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, —З—В–Њ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ —Г–Љ–µ–љ—М—И–∞–µ—В —З–∞—Б—В–Њ—В—Г —В—П–ґ–µ–ї—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е –≥–∞—Б—В—А–Њ–Є–љ—В–µ—Б—В–Є–љ–∞–ї—М–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤.
–Ф–ї—П —А–µ—И–µ–љ–Є—П –≤–Њ–њ—А–Њ—Б–∞ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є, —Б–≤—П–Ј–∞–љ–љ–Њ–є —Б –њ—А–Є–µ–Љ–Њ–Љ –Э–Я–Т–Я, –≤ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П –Є–љ–≥–Є–±–Є—В–Њ—А—Л –њ—А–Њ—В–Њ–љ–љ–Њ–є –њ–Њ–Љ–њ—Л (–Ш–Я–Я). –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П–Љ –Р–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є (2002), –њ—А–Є –≤—Л—Б–Њ–Ї–Њ–Љ —А–Є—Б–Ї–µ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –≥–∞—Б—В—А–Њ–і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є –Ј–Њ–љ—Л –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Э–Я–Т–Я (–і–≤–∞ –Є –±–Њ–ї–µ–µ —Д–∞–Ї—В–Њ—А–∞ —А–Є—Б–Ї–∞, –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ) –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –≤–Љ–µ—Б—В–Њ –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є—Е (–љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е) –Э–Я–Т–Я –љ–∞–Ј–љ–∞—З–∞—В—М —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У-2 –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Ш–Я–Я, –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Њ–і–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–Є—Б–Ї–∞ –Љ–Њ–ґ–љ–Њ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞—В—М—Б—П —В–Њ–ї—М–Ї–Њ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–Љ –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ –¶–Ю–У-2, –∞ –њ—А–Є –љ–Є–Ј–Ї–Њ–Љ —А–Є—Б–Ї–µ (—Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –љ–µ—В) – –њ—А–Є–Љ–µ–љ—П—В—М –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є–µ –Э–Я–Т–Я.
–Т–∞–ґ–љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –≤—А–∞—З–∞-—В–µ—А–∞–њ–µ–≤—В–∞, –Ј–∞—З–∞—Б—В—Г—О –њ—А–Є—Е–Њ–і–Є—В—Б—П —Б—В–∞–ї–Ї–Є–≤–∞—В—М—Б—П —Б —Б–Њ—З–µ—В–∞–љ–љ—Л–Љ–Є –њ—А–Њ–±–ї–µ–Љ–∞–Љ–Є —А–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є–Є –Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є, –Ї–Њ–≥–і–∞ –Є–Љ–µ–µ—В –Љ–µ—Б—В–Њ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Њ–њ–Њ—А–љ–Њ-–і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞, –∞ —В–∞–Ї–ґ–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Э–Я–Т–Я. –Ю–±—Й–µ–Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Є–Љ–µ–љ–љ–Њ —В–Њ—А–Љ–Њ–ґ–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –¶–Ю–У-1 –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Њ–њ—А–µ–і–µ–ї—П–µ—В –≥–∞—Б—В—А–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л—Е (–љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е) –Э–Я–Т–Я. –Т —Н—В–Њ–є —Б–≤—П–Ј–Є, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ –Њ—В–і–∞–µ—В—Б—П –Є–љ–≥–Є–±–Є—В–Њ—А–∞–Љ –¶–Ю–У-2, –Њ–±–ї–∞–і–∞—О—Й–Є–Љ —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –Ї–Њ—В–Њ—А—Л–µ —П–≤–ї—П—О—В—Б—П –Љ–µ–љ–µ–µ —В–Њ–Ї—Б–Є—З–љ—Л–Љ–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л –ї–µ–Ї–∞—А—Б—В–≤ –Є —Б–Њ—З–µ—В–∞—О—В –≤ —Б–µ–±–µ –±—Л—Б—В—А–Њ–µ –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –Є –Љ–Њ—Й–љ—Л–є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В.
–Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –¶–Ю–У-2 —Б–љ–Є–ґ–∞—О—В —А–Є—Б–Ї —П–Ј–≤–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П, –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–∞ 2-—Е –Є –±–Њ–ї–µ–µ —Д–∞–Ї—В–Њ—А–Њ–≤ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –Ц–Ъ–Ґ —З–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –Э–Я–Т–Я-–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ—А–Є–±–ї–Є–ґ–∞–µ—В—Б—П –Ї –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ–Љ—Г –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—О –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Э–Я–Т–Я. –Ґ–∞–Ї, –њ–Њ –і–∞–љ–љ—Л–Љ –±—А–Є—В–∞–љ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є, —Г 9407 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —П–Ј–≤–∞–Љ–Є –ґ–µ–ї—Г–і–Ї–∞, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Э–Я–Т–Я, —Б–Њ—Е—А–∞–љ—П–ї—Б—П –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–є, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ—П–µ–Љ–Њ–≥–Њ –Э–Я–Т–Я [19]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ–Њ—П–≤–Є–≤—И–Є–µ—Б—П —Б–Њ–Њ–±—Й–µ–љ–Є—П –Њ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–∞—Е –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Є–Ј —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У-2 –љ–∞ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б–Є—Б—В–µ–Љ—Г –њ—А–Є–≤–µ–ї–Є –Ї –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—О –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –≤ —Н—В–Њ–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–Є –Є —И–Є—А–Њ–Ї–Њ–Љ—Г –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –Є—Е –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ [20].
–Э–µ–ї—М–Ј—П –љ–µ –Њ—В–Љ–µ—В–Є—В—М –Є —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –Є–Љ–µ—О—В—Б—П —А–∞–±–Њ—В—Л, –≤ –Ї–Њ—В–Њ—А—Л—Е –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –њ—А–Є—Б—Г—В—Б—В–≤–Є–µ –¶–Ю–У-2 –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —В–Ї–∞–љ—П—Е (–≥–Њ–ї–Њ–≤–љ–Њ–є –Є —Б–њ–Є–љ–љ–Њ–є –Љ–Њ–Ј–≥, –њ–Њ—З–Ї–Є, –Ї–Њ—Б—В–љ–∞—П —В–Ї–∞–љ—М) –≤ –Ї–∞—З–µ—Б—В–≤–µ «–Ї–Њ–љ—Б—В–Є—В—Г—В–Є–≤–љ–Њ–є» –Є–Ј–Њ—Д–Њ—А–Љ—Л [21]. –Я—А–Є —Н—В–Њ–Љ, –і–∞–љ–љ—Л–µ J.L. Wallace –Є —Б–Њ–∞–≤—В. —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ —Д–µ—А–Љ–µ–љ—В –¶–Ю–У-2 –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–µ–Њ–±—Е–Њ–і–Є–Љ –і–ї—П –Ј–∞—Й–Є—В—Л –ґ–µ–ї—Г–і–Ї–∞, –∞ –¶–Ю–У-1 – –њ—А–Є–љ–Є–Љ–∞—В—М —Г—З–∞—Б—В–Є–µ –≤ —А–∞–Ј–≤–Є—В–Є–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –Њ—Б–Њ–±–µ–љ–љ–Њ –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е [22].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г—З–Є—В—Л–≤–∞—П –≤—Л—И–µ—Б–Ї–∞–Ј–∞–љ–љ–Њ–µ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ –∞–Ї—В–Є–≤–љ—Л–є –љ–∞—Г—З–љ—Л–є –њ–Њ–Є—Б–Ї –Є —Б–Њ–Ј–і–∞–љ–Є–µ –љ–Њ–≤—Л—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –≤–µ—Й–µ—Б—В–≤, —Б–њ–Њ—Б–Њ–±–љ—Л—Е –Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ–Њ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М –¶–Ю–У-2. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —А–∞–Ј—А–∞–±–∞—В—Л–≤–∞—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В—Л, –Є–љ–≥–Є–±–Є—А—Г—О—Й–Є–µ –Ї–∞–Ї –¶–Ю–У-2, —В–∞–Ї –Є –ї–Є–њ–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Г (–њ–Њ—Б–ї–µ–і–љ—П—П, –Ї–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –љ–∞—А—П–і—Г —Б –¶–Ю–У –њ—А–Є–љ–Є–Љ–∞–µ—В —Г—З–∞—Б—В–Є–µ –≤ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–µ –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л). –Я—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П, —З—В–Њ –і–≤–Њ–є–љ–Њ–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –±—Г–і–µ—В –Љ–Є–љ–Є–Љ–Є–Ј–Є—А–Њ–≤–∞—В—М —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Э–Я–Т–Я-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –≥–∞—Б—В—А–Њ–њ–∞—В–Є–Є.
–Р–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л–Љ –њ–Њ–і—Е–Њ–і–Њ–Љ —П–≤–ї—П–µ—В—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ NO-–∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е –Э–Я–Т–Я. –Ю–Ї—Б–Є–і –∞–Ј–Њ—В–∞-–і–Њ–љ–Њ—А–љ—Л–µ –Э–Я–Т–Я (NO-–Э–Я–Т–Я) –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –љ–Њ–≤—Л–є –Ї–ї–∞—Б—Б —Б–Њ–µ–і–Є–љ–µ–љ–Є–є, —П–≤–ї—П—О—Й–Є—Е—Б—П –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ–Є –Њ—В –Њ–±—Л—З–љ—Л—Е –Э–Я–Т–Я, –Ї–Њ—В–Њ—А—Л–µ –±—Л–ї–Є –Є–Ј–Љ–µ–љ–µ–љ—Л –њ—Г—В–µ–Љ –і–Њ–±–∞–≤–ї–µ–љ–Є—П –Ї –љ–Є–Љ –Љ–Њ–ї–µ–Ї—Г–ї—Л –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞.
–§–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞ (NO) –Љ–љ–Њ–≥–Њ–≥—А–∞–љ–љ—Л. –≠—В–Њ –Є –≤–ї–Є—П–љ–Є–µ –љ–∞ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б–Є—Б—В–µ–Љ—Г, –Ї–Њ—В–Њ—А–Њ–µ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є –≥—Г–∞–љ–Є–ї–∞—В—Ж–Є–Ї–ї–∞–Ј—Л, –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ —Ж–У–Ь–§ –Є –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є –њ—А–Њ—В–µ–Є–љ–Ї–Є–љ–∞–Ј—Л G. NO –њ—А–Є–љ–Є–Љ–∞–µ—В —Г—З–∞—Б—В–Є–µ –≤ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞—Е —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ–Њ–є –Ї–ї–µ—В–Ї–Є, –≤—Л–Ј—Л–≤–∞—П –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є—О. –Я—А–Є –≤–і—Л—Е–∞–љ–Є–Є NO —А–∞—Б—Б–ї–∞–±–ї—П—О—В—Б—П –≥–ї–∞–і–Ї–Є–µ –Љ—Л—И—Ж—Л –±—А–Њ–љ—Е–Њ–≤. –Т–∞–ґ–љ—Г—О —А–Њ–ї—М NO –Є–≥—А–∞–µ—В –≤ –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–Є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞. –Ю–Ї–Є—Б—М –∞–Ј–Њ—В–∞ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Є —А—П–і –і—А—Г–≥–Є—Е —Н—Д—Д–µ–Ї—В–Њ–≤: —Г—З–∞—Б—В–≤—Г–µ—В –≤ –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–Є —Ж–µ–ї–Њ—Б—В–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є, —Б–љ–Є–ґ–∞–µ—В –∞–і–≥–µ–Ј–Є—О –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ –Ї —Н–љ–і–Њ—В–µ–ї–Є—О, —В–Њ—А–Љ–Њ–Ј–Є—В –Љ–Є–≥—А–∞—Ж–Є—О –Є –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Л—Е –Ї–ї–µ—В–Њ–Ї. –Э–µ–Љ–∞–ї–Њ–≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ NO —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П –Є–Љ–µ–µ—В –Є –≤ —А–µ–≥—Г–ї—П—Ж–Є–Є –≥–µ–Љ–Њ—Б—В–∞–Ј–∞: –њ–Њ–і–∞–≤–ї—П–µ—В –∞–і–≥–µ–Ј–Є—О –Є –∞–≥—А–µ–≥–∞—Ж–Є—О —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤. –Ю–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ NO —Б —Г—З–∞—Б—В–Є–µ–Љ –Є–љ–і—Г—Ж–Є—А—Г–µ–Љ–Њ–є NO-—Б–Є–љ—В–∞–Ј—Л –≤ –Љ–∞–Ї—А–Њ—Д–∞–≥–∞—Е, –ї–Є–Љ—Д–Њ—Ж–Є—В–∞—Е –Є –љ–µ–є—В—А–Њ—Д–Є–ї–∞—Е –Є–≥—А–∞–µ—В –Ј–љ–∞—З–Є–Љ—Г—О —А–Њ–ї—М –≤ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–Є –Є –Є–Љ–Љ—Г–љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є—П—Е, —З—В–Њ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –Є –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –≤ –±–∞–Ї—В–µ—А–Є—Ж–Є–і–љ–Њ–є, –њ—А–Њ—В–Є–≤–Њ–≤–Є—А—Г—Б–љ–Њ–є –Є –њ—А–Њ—В–Є–≤–Њ–Њ–њ—Г—Е–Њ–ї–µ–≤–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–∞–Ї—А–Њ—Д–∞–≥–Њ–≤. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П NO —В–Њ—А–Љ–Њ–Ј–Є—В –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є—О –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤ –Є –Њ—Б–ї–∞–±–ї—П–µ—В –Є–Љ–Љ—Г–љ–љ—Л–є –Њ—В–≤–µ—В –љ–∞ —З—Г–ґ–µ—А–Њ–і–љ—Л–µ –∞–љ—В–Є–≥–µ–љ—Л. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–љ–і—Г—Ж–Є—А—Г–µ–Љ–∞—П NO-—Б–Є–љ—В–∞–Ј–∞ –Љ–Њ–ґ–µ—В –Є–≥—А–∞—В—М —А–Њ–ї—М –≤ –њ—А–Њ—Ж–µ—Б—Б–∞—Е –∞–њ–Њ–њ—В–Њ–Ј–∞ [23].
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –Њ–Ї—Б–Є–і –∞–Ј–Њ—В–∞ —П–≤–ї—П–µ—В—Б—П –≤–∞–ґ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ –Ј–∞—Й–Є—В—Л —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞ –љ–∞—А—П–і—Г —Б –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞–Љ–Є. –Ъ –Њ—Б–љ–Њ–≤–љ—Л–Љ –Ј–∞—Й–Є—В–љ—Л–Љ —Н—Д—Д–µ–Ї—В–∞–Љ –Њ—В–љ–Њ—Б—П—В—Б—П —Б—В–Є–Љ—Г–ї—П—Ж–Є—П —Б–µ–Ї—А–µ—Ж–Є–Є —Б–ї–Є–Ј–Є, —А–µ–≥—Г–ї—П—Ж–Є—П –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–µ –Є –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –∞–і–≥–µ–Ј–Є–Є –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤ –Ї —Н–љ–і–Њ—В–µ–ї–Є—О —Б–Њ—Б—Г–і–Њ–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –љ–µ–Љ–∞–ї–Њ–≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –Њ–±–µ—Б–њ–µ—З–µ–љ–Є–µ –Љ–Њ—В–Њ—А–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –Ц–Ъ–Ґ, –∞ —В–∞–Ї–ґ–µ —А–µ–≥—Г–ї—П—Ж–Є–Є –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є—П –ґ–µ–ї—З–Є –≤ –Ї–Є—И–µ—З–љ–Є–Ї; –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, NO –≤—Л–Ј—Л–≤–∞–µ—В —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–Њ—В–Њ—А–Є–Ї–Є –Ц–Ъ–Ґ, —А–∞—Б—Б–ї–∞–±–ї–µ–љ–Є–µ —Б—Д–Є–љ–Ї—В–µ—А–∞ –Ю–і–і–Є –Є –љ–Є–ґ–љ–µ–≥–Њ –њ–Є—Й–µ–≤–Њ–і–љ–Њ–≥–Њ —Б—Д–Є–љ–Ї—В–µ—А–∞ [24, 25].
–Ю–±—Й–µ–Є–Ј–≤–µ—Б—В–µ–љ –Є —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –Ц–Ъ–Ґ –Є–Љ–µ–µ—В –Њ–±—И–Є—А–љ—Г—О –∞—Д—Д–µ—А–µ–љ—В–љ—Г—О –Є–љ–љ–µ—А–≤–∞—Ж–Є—О. –Я—А–Є —Н—В–Њ–Љ, —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–µ —В–µ—А–Љ–Є–љ–∞–ї–Є –≤—Л–њ–Њ–ї–љ—П—О—В –љ–µ —В–Њ–ї—М–Ї–Њ –∞—Д—Д–µ—А–µ–љ—В–љ—Г—О, –љ–Њ –Є –Љ–µ—Б—В–љ—Г—О —Н—Д—Д–µ–Ї—В–Њ—А–љ—Г—О —Д—Г–љ–Ї—Ж–Є—О. –Ч–∞ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –љ–∞–Ї–Њ–њ–ї–µ–љ–Њ –Љ–љ–Њ–≥–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ –≤ –њ–Њ–і–і–µ—А–ґ–Ї—Г –Љ–µ—Б—В–љ–Њ–є —Н—Д—Д–µ–Ї—В–Њ—А–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –Њ–Ї–Њ–љ—З–∞–љ–Є–є –≤ —А–µ–≥—Г–ї—П—Ж–Є–Є –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Њ–≤, —В—А–Њ—Д–Є—З–µ—Б–Ї–Є—Е –Є –Є–Љ–Љ—Г–љ–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –≥–∞–љ–≥–ї–Є–µ–≤ –Є –≥–ї–∞–і–Ї–Є—Е –Љ—Л—И—Ж –Ц–Ъ–Ґ [26, 27]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–Љ–Љ—Г–љ–Њ–≥–Є—Б—В–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є –≤ —Б–Њ—Б—В–∞–≤–µ –њ–µ—А–≤–Є—З–љ—Л—Е –∞—Д—Д–µ—А–µ–љ—В–Њ–≤ –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –±–Њ–ї—М—И–Њ–µ —З–Є—Б–ї–Њ –љ–µ–є—А–Њ–њ–µ–њ—В–Є–і–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —В—А–∞–љ–њ–Њ—А—В–Є—А—Г—О—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –≤ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–Љ, –љ–Њ –Є –≤ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–Љ –љ–∞–њ—А–∞–≤–ї–µ–љ–Є–Є (–∞–љ—В–Є–і—А–Њ–Љ–љ–Њ), –∞ —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±–љ—Л –љ–∞–Ї–∞–њ–ї–Є–≤–∞—В—М—Б—П –Є —Е—А–∞–љ–Є—В—М—Б—П –≤ –≤–µ–Ј–Є–Ї—Г–ї–∞—Е –≤ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е –љ–µ—А–≤–љ—Л—Е —В–µ—А–Љ–Є–љ–∞–ї—П—Е –Є –ї–Њ–Ї–∞–ї—М–љ–Њ –≤—Л–і–µ–ї—П—В—М—Б—П —Н–Ї–Ј–Њ—Ж–Є—В–Њ–Ј–Њ–Љ –њ—А–Є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е —В–µ—А–Љ–Є–љ–∞–ї–µ–є —А–∞–Ј–љ—Л–Љ–Є —Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –Є —Д–Є–Ј–Є—З–µ—Б–Ї–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є [28]. –Т–∞–ґ–љ—Л–Љ —Н–ї–µ–Љ–µ–љ—В–Њ–Љ –≤ —Н—В–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Њ–Ї–∞–Ј–∞–ї—Б—П –Ї–∞–њ—Б–∞–Є—Ж–Є–љ – –ґ–≥—Г—З–Є–є –Є–љ–≥—А–µ–і–Є–µ–љ—В –Њ—Б—В—А–Њ–≥–Њ –Ї—А–∞—Б–љ–Њ–≥–Њ –њ–µ—А—Ж–∞, –≤–њ–µ—А–≤—Л–µ –њ—А–Є–Љ–µ–љ–µ–љ–љ—Л–є –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –≤–µ–љ–≥–µ—А—Б–Ї–Є–Љ —Г—З–µ–љ—Л–Љ N. Jancso –±–Њ–ї–µ–µ 55 –ї–µ—В –љ–∞–Ј–∞–і. –Т–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ –µ–≥–Њ –і–µ–є—Б—В–≤–Є–Є –љ–∞ –њ–µ—А–≤–Є—З–љ—Л–µ –∞—Д—Д–µ—А–µ–љ—В—Л –њ—А–Є–і–∞–µ—В—Б—П –≤–∞–љ–Є–ї–Є–љ–Њ–≤–Њ–є –≥—А—Г–њ–њ–µ, –њ—А–µ–і—Б—В–∞–≤–ї—П—О—Й–µ–є, –њ–Њ —Б—Г—В–Є, —Е–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–љ—Л–є –≤ –Ї—Г–ї–Є–љ–∞—А–Є–Є –≤–∞–љ–Є–ї–Є–љ, –љ–µ –Њ–±–ї–∞–і–∞—О—Й–Є–є, –Ї–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –ґ–≥—Г—З–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Т 1997 –≥. –Ї–∞–њ—Б–∞–Є—Ж–Є–љ–Њ–≤—Л–µ (–≤–∞–љ–Є–ї–Њ–Є–і–љ—Л–µ) —А–µ—Ж–µ–њ—В–Њ—А—Л –≤–њ–µ—А–≤—Л–µ –±—Л–ї–Є –Ї–ї–Њ–љ–Є—А–Њ–≤–∞–љ—Л.
–°–ї–µ–і—Г–µ—В –Њ—Б–Њ–±–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –і–µ–є—Б—В–≤–Є—П –Ї–∞–њ—Б–∞–Є—Ж–Є–љ–∞, –Ї–Њ—В–Њ—А—Л–є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Є–Ј–±–Є—А–∞—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е —В–Њ–љ–Ї–Є—Е –љ–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –°-–≤–Њ–ї–Њ–Ї–Њ–љ –Є —З–∞—Б—В–Є—З–љ–Њ – –љ–∞ —В–Њ–љ–Ї–Є–µ –Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–µ –Р-–і–µ–ї—М—В–∞ –≤–Њ–ї–Њ–Ї–љ–∞ [29]. –Я—А–Є —Н—В–Њ–Љ –Њ–љ –љ–µ –≤–ї–Є—П–µ—В –љ–∞ —Н–љ—В–µ—А–∞–ї—М–љ—Л–µ –Є –∞–≤—В–Њ–љ–Њ–Љ–љ—Л–µ –љ–µ—А–≤—Л (—Е–Њ—В—П –≤ –≤—Л—Б–Њ–Ї–Є—Е –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П—Е –Љ–Њ–ґ–µ—В –Њ–Ї–∞–Ј—Л–≤–∞—В—М –љ–∞ –љ–Є—Е –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤–∞–љ–Є–ї–Њ–Є–і–љ—Л–µ (–Ї–∞–њ—Б–∞–Є—Ж–Є–љ–Њ–≤—Л–µ) —А–µ—Ж–µ–њ—В–Њ—А—Л —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В—Б—П —Б–µ–є—З–∞—Б –Ї–∞–Ї –Є–љ—В–µ–≥—А–∞—В–Њ—А—Л –±–Њ–ї–µ–≤—Л—Е –Є –Є–Њ–љ-–≤–Њ–і–Њ—А–Њ–і–љ—Л—Е —Б—В–Є–Љ—Г–ї–Њ–≤. –Я—А–Є —Н—В–Њ–Љ –≤–∞–ґ–љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –і–µ–є—Б—В–≤–Є–µ –Ї–∞–њ—Б–∞–Є—Ж–Є–љ–∞ –Ј–∞–≤–Є—Б–Є—В –Њ—В –і–Њ–Ј—Л –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є —Н–Ї—Б–њ–Њ–Ј–Є—Ж–Є–Є. –Ґ–∞–Ї, –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –Ї–∞–њ—Б–∞–Є—Ж–Є–љ–∞ –∞–Ї—В–Є–≤–Є—А—Г—О—В —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–µ —В–µ—А–Љ–Є–љ–∞–ї–Є, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —А–µ–ї–Є–Ј–Є–љ–≥—Г –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—В—В–µ—А–Њ–≤, —З–∞—Б—В—М –Є–Ј –Ї–Њ—В–Њ—А—Л—Е —Б–њ–Њ—Б–Њ–±–љ—Л —А–µ–Ј–Ї–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –ї–Њ–Ї–∞–ї—М–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –Є –Њ–Ї–∞–Ј—Л–≤–∞—В—М —В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Ф–∞–љ–љ–Њ–µ –Њ–±—Б—В–Њ—П—В–µ–ї—М—Б—В–≤–Њ –Њ–±—К—П—Б–љ—П–µ—В, –њ–Њ—З–µ–Љ—Г —Г –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б—В—А–∞–і–∞—О—Й–Є—Е —П–Ј–≤–µ–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ—М—О, –љ–∞—А—Г—И–∞—О—Й–Є—Е —Й–∞–і—П—Й—Г—О –і–Є–µ—В—Г –Є —Г–њ–Њ—В—А–µ–±–ї—П—О—Й–Є—Е –Њ—Б—В—А—Л–є –Ї—А–∞—Б–љ—Л–є –њ–µ—А–µ—Ж, –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г–ї—Г—З—И–µ–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –Є —Г—Б–Ї–Њ—А–µ–љ–љ–Њ–µ –Ј–∞–ґ–Є–≤–ї–µ–љ–Є–µ —П–Ј–≤. –£–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –Є/–Є–ї–Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є —Н–Ї—Б–њ–Њ–Ј–Є—Ж–Є–Є –Ї–∞–њ—Б–∞–Є—Ж–Є–љ–∞ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –∞–љ–∞–ї–≥–µ–Ј–Є—А—Г—О—Й–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ.
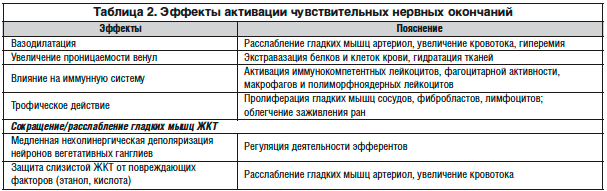
–§–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –∞–Ї—В–Є–≤–∞—Ж–Є–Є –Ї–∞–њ—Б–∞–Є—Ж–Є–љ-—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –Њ–Ї–Њ–љ—З–∞–љ–Є–є (—В–∞–±–ї. 2) –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П —А–µ–ї–Є–Ј–Є–љ–≥–Њ–Љ –љ–µ–є—А–Њ–њ–µ–њ—В–Є–і–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –≤ –љ–Є—Е –ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ—Л. –Ф–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–Њ—Б—В–Њ—П–љ–љ—Л–Љ–Є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є –і–∞–љ–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ —П–≤–ї—П—О—В—Б—П —В–∞—Е–Є–Ї–Є–љ–Є–љ—Л –Є –Ї–∞–ї—М—Ж–Є—В–Њ–љ–Є–љ – –≥–µ–љ —А–Њ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ–µ–њ—В–Є–і–∞. –Я–Њ—Б–ї–µ–і–љ–Є–є —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј —Б–∞–Љ—Л—Е –Љ–Њ—Й–љ—Л—Е –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А–Њ–≤ –Є –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ—А—П–Љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –љ–∞ –≥–ї–∞–і–Ї–Є–µ –Љ—Л—И—Ж—Л —Б–Њ—Б—Г–і–Њ–≤ (—Е–Њ—В—П –Є–Љ–µ—О—В—Б—П –і–∞–љ–љ—Л–µ –Њ —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –µ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —З–µ—А–µ–Ј —А–µ–ї–Є–Ј–Є–љ–≥ –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞ –≤ —А—П–і–µ –Ї—А—Г–њ–љ—Л—Е –Њ—А–≥–∞–љ–љ—Л—Е –∞—А—В–µ—А–Є–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤) [27]. –°—Г–±—Б—В–∞–љ—Ж–Є—П –† –Њ–±–ї–∞–і–∞–µ—В —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ —З–µ—А–µ–Ј —Н–љ–і–Њ—В–µ–ї–Є–є-–Ј–∞–≤–Є—Б–Є–Љ—Л–є —А–µ–ї–Є–Ј–Є–љ–≥ –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞, —Г–≤–µ–ї–Є—З–Є–≤–∞—П –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В—М —Б–Њ—Б—Г–і–Њ–≤ (–≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –њ–Њ—Б—В–Ї–∞–њ–Є–ї–ї—П—А–љ—Л—Е –≤–µ–љ—Г–ї), —З—В–Њ –ї–µ–ґ–Є—В –≤ –Њ—Б–љ–Њ–≤–µ –Ї–∞–Ї –≥–Є–і—А–∞—В–∞—Ж–Є–Є, —В–∞–Ї –Є –Є–Љ–Љ—Г–љ–Њ–Ј–∞—Й–Є—В—Л —В–Ї–∞–љ–µ–є (—З–µ—А–µ–Ј —Н–Ї—Б—В—А–∞–≤–∞–Ј–∞—Ж–Є—О –ї–Є–Љ—Д–Њ—Ж–Є—В–Њ–≤). –Ш–Љ–µ–љ–љ–Њ —А–µ–ї–Є–Ј–Є–љ–≥–Њ–Љ –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А–љ—Л—Е –љ–µ–є—А–Њ–њ–µ–њ—В–Є–і–Њ–≤ –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П —В–Ї–∞–љ–µ–є –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –Ј–∞—Й–Є—В—Г —Б–ї–Є–Ј–Є—Б—В–Њ–є –Ц–Ъ–Ґ –Њ—В –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ї–∞–њ—Б–∞–Є—Ж–Є–љ–∞, —З—В–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ [26, 29].
–Т—Л—И–µ–Њ–њ–Є—Б–∞–љ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞ –Є –Љ–µ—Е–∞–љ–Є–Ј–Љ –і–µ–є—Б—В–≤–Є—П –Ї–∞–њ—Б–∞–Є—Ж–Є–љ–Њ–≤—Л—Е (–≤–∞–љ–Є–ї–Њ–Є–і–љ—Л—Е) —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –ї–µ–≥–ї–Є –≤ –Њ—Б–љ–Њ–≤—Г —Б–Њ–Ј–і–∞–љ–Є—П –љ–Њ–≤–Њ–≥–Њ –Э–Я–Т–Я – –∞–Љ—В–Њ–ї–Љ–µ—В–Є–љ –≥—Г–∞—Ж–Є–ї–∞ (–Р–Ь–У). –Ф–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –њ–Њ–ї—Г—З–µ–љ —Б –њ–Њ–Љ–Њ—Й—М—О –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –Љ–µ—В–Њ–і–Є–Ї–Є —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ—В–µ–Ј–∞ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П —В–Њ–ї–Љ–µ—В–Є–љ–∞ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–Њ–є (–≥–ї–Є—Ж–Є–љ–Њ–Љ) –Є –≥–≤–∞—П–Ї–Њ–ї–Њ–Љ [30]. –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Р–Ь–У –Є–љ–≥–Є–±–Є—А—Г–µ—В –±–Є–Њ—Б–Є–љ—В–µ–Ј –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, –љ–Њ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Б —Н—В–Є–Љ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ—А—П–Љ–Њ–µ –Ј–∞—Й–Є—В–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ —Б—В–µ–љ–Ї—Г –ґ–µ–ї—Г–і–Ї–∞ –Ј–∞ —Б—З–µ—В —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є—П –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ—Л—Е –њ–µ–њ—В–Є–і–Њ–≤, –≤ —В. —З. –Ї–∞–ї—М—Ж–Є—В–Њ–љ–Є–љ-–≥–µ–љ-—Б–≤—П–Ј–∞–љ–љ–Њ–≥–Њ –њ–µ–њ—В–Є–і–∞, –∞ —В–∞–Ї–ґ–µ —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ї–∞–њ—Б–∞–Є—Ж–Є–љ–∞ (–≤–∞–љ–Є–ї–Њ–Є–і–љ—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л), —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞, –Ј–∞—Й–Є—Й–∞—О—Й–µ–≥–Њ —Б—В–µ–љ–Ї—Г –ґ–µ–ї—Г–і–Ї–∞ –Њ—В —А–∞–Ј—А—Г—И–µ–љ–Є—П [31, 32]. –Р–Ї—В–Є–≤–∞—Ж–Є—П —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ї–∞–њ—Б–∞–Є—Ж–Є–љ–∞ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ—А–Є –њ—А—П–Љ–Њ–Љ –Ї–Њ–љ—В–∞–Ї—В–µ –Љ–Њ–ї–µ–Ї—Г–ї —Н—В–Њ–≥–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ —Б–Њ —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Њ–є –ґ–µ–ї—Г–і–Ї–∞, –Є –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–µ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ –і–∞–љ–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Є –њ—А–Є–µ–Љ–µ –њ–Є—Й–Є –љ–∞—В–Њ—Й–∞–Ї.
–°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –љ–∞ –Ї—А—Л—Б–∞—Е, –Р–Ь–У, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я, –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Є—Е –Є–ї–Є –љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є –і–∞–ґ–µ –њ—А–Є –≤–љ—Г—В—А–Є–ґ–µ–ї—Г–і–Њ—З–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–Є –≤ –і–Њ–Ј–∞—Е, –≤ 6 —А–∞–Ј –њ—А–µ–≤—Л—И–∞—О—Й–Є—Е –і–Њ–Ј—Л, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–µ –і–ї—П —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –Ї–Њ–ґ–љ–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П [33]. –Т –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±—Л–ї–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ, —З—В–Њ –Р–Ь–У —Б–љ–Є–ґ–∞–µ—В —Б–µ–Ї—А–µ—Ж–Є—О –Ї–Є—Б–ї–Њ—В—Л –ґ–µ–ї—Г–і–Њ—З–љ–Њ–≥–Њ —Б–Њ–Ї–∞ –Є —Г–Љ–µ–љ—М—И–∞–µ—В –њ–Њ—А–∞–ґ–µ–љ–Є—П –ґ–µ–ї—Г–і–Ї–∞, –≤—Л–Ј–≤–∞–љ–љ—Л–µ –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ–Њ–Љ, —Г –Ї—А—Л—Б [34]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Р–Ь–У –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–≤—Л—И–∞–ї –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Є–љ—В–∞–Ј—Л –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞ –Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ NO –≤ –Ц–Ъ–Ґ, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –µ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є—В—Л (—В–Њ–ї–Љ–µ—В–Є–љ, MED5 –Є –≥–≤–∞—П–Ї–Њ–ї) –љ–µ –Њ–±–ї–∞–і–∞–ї–Є —В–∞–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О [35].
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ, —З—В–Њ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–є, –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–Є–є –Є –ґ–∞—А–Њ–њ–Њ–љ–Є–ґ–∞—О—Й–Є–є —Н—Д—Д–µ–Ї—В—Л –Р–Ь–У —Б—А–∞–≤–љ–Є–Љ—Л —Б —В–∞–Ї–Њ–≤—Л–Љ–Є –і–ї—П –љ–µ—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я [36–38].
–†–µ–Ј—Г–ї—М—В–∞—В—Л —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±–Ј–Њ—А–∞ –ї–Є—В–µ—А–∞—В—Г—А—Л (–Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л—Е –Є –љ–µ–Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Њ—Б—В–µ–Њ–∞—А—В—А–Є—В–∞, —А–µ–≤–Љ–∞—В–Њ–Є–і–љ–Њ–≥–Њ –∞—А—В—А–Є—В–∞ –Є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –љ–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є) –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –Р–Ь–У –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –і—А—Г–≥–Є–Љ–Є –Э–Я–Т–Я –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —З–∞—Б—В–Њ—В–∞ —Б–ї—Г—З–∞–µ–≤ —Б –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–Љ–Є —А–µ–∞–Ї—Ж–Є—П–Љ–Є –Є —А–∞–љ–љ–Є–Љ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є–µ–Љ –ї–µ—З–µ–љ–Є—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –љ–Є–ґ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–љ–Є–Љ–∞–ї–Є –Р–Ь–У, —З–µ–Љ –і—А—Г–≥–Є–µ –Э–Я–Т–Я [30]. –Я—А–Њ–≤–Њ–і–Є–ї—Б—П –∞–љ–∞–ї–Є–Ј 18 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤ —З–µ—В—Л—А–µ—Е –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –Р–Ь–У —Б—А–∞–≤–љ–Є–≤–∞–ї–Є —Б –і–Є–Ї–ї–Њ—Д–µ–љ–∞–Ї–Њ–Љ, –≤ –њ—П—В–Є – —Б —В–Њ–ї–Љ–µ—В–Є–љ–Њ–Љ, –≤ –і–≤—Г—Е – —Б –Є–љ–і–Њ–Љ–µ—В–∞—Ж–Є–љ–Њ–Љ, –≤ –і–≤—Г—Е – —Б –љ–∞–њ—А–Њ–Ї—Б–µ–љ–Њ–Љ, –≤ –і–≤—Г—Е – —Б –і–Є—Д–ї—Г–љ–Є—Б–∞–ї–Њ–Љ –Є –≤ –Њ–і–љ–Њ–Љ – —Б –Є–±—Г–њ—А–Њ—Д–µ–љ–Њ–Љ –Є —Д–ї—Г—А–±–Є–њ—А–Њ—Д–µ–љ–Њ–Љ. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—В–ї–Є—З–∞–ї–Є—Б—М –њ–Њ —Б–≤–Њ–µ–є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є – –Њ—В 1 –љ–µ–і. –і–Њ 150 –і–љ–µ–є, —З—В–Њ –љ–µ –њ–Њ–≤–ї–Є—П–ї–Њ –љ–∞ —А–∞–Ј–ї–Є—З–Є—П –і–∞–љ–љ—Л—Е.
–Ф–∞–љ–љ—Л–µ –і–≤—Г—Е –і—А—Г–≥–Є—Е –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј–Њ–≤ [30, 39] —В–∞–Ї–ґ–µ —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ —В–Њ, —З—В–Њ –њ—А–Є –њ—А–Є–µ–Љ–µ –Р–Ь–У –љ–∞–±–ї—О–і–∞–µ—В—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Љ–µ–љ—М—И–µ (7,2 –Є 28,3% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ) –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –ґ–µ–ї—Г–і–Ї–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–Љ–Є –Э–Я–Т–Я. –І–∞—Б—В–Њ—В–∞ –Є —Б—В–µ–њ–µ–љ—М —В—П–ґ–µ—Б—В–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є –ґ–µ–ї—Г–і–Ї–∞, –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —Н–љ–і–Њ—Б–Ї–Њ–њ–Є–Є, –±—Л–ї–∞ –Љ–µ–љ—М—И–µ–є –њ—А–Є –њ—А–Є–µ–Љ–µ –Р–Ь–У –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і—А—Г–≥–Є–Љ–Є –Э–Я–Т–Я, –Њ—В–љ–Њ—И–µ–љ–Є–µ —И–∞–љ—Б–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 0,3 (95% CI 0,1–0,7) –і–ї—П —В—П–ґ–µ–ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Є 0,1 (95% CI 0,1 to 0,4) – –і–ї—П —Б—А–µ–і–љ–µ–≥–Њ –Є —В—П–ґ–µ–ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Т –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ –Љ–Њ–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –і–ї—П –Р–Ь–У –±—Л–ї–Є –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ—Л –≥–∞—Б—В—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Э–Я–Т–Я [40].
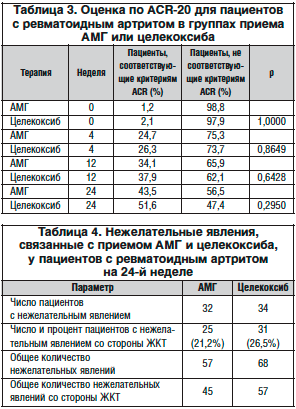
–Ш–љ—В–µ—А–µ—Б–љ—Л–Љ–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В—Л 24-–љ–µ–і–µ–ї—М–љ–Њ–≥–Њ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ –њ–∞—А–∞–ї–ї–µ–ї—М–љ—Л—Е –≥—А—Г–њ–њ–∞—Е –њ–Њ –Њ—Ж–µ–љ–Ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –і–ї—П –Ц–Ъ–Ґ –Р–Ь–У –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–Њ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–µ–≤–Љ–∞—В–Њ–Є–і–љ—Л–Љ –∞—А—В—А–Є—В–Њ–Љ [41]. –С—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 235 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є–Ј –љ–Є—Е 180 (85 – –≤ –≥—А—Г–њ–њ–µ –њ—А–Є–µ–Љ–∞ –Р–Ь–У –Є 95 – —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞) –Ј–∞–≤–µ—А—И–Є–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ. –Ъ–∞–ґ–і—Л–є –њ–∞—Ж–Є–µ–љ—В –њ—А–Є–љ–Є–Љ–∞–ї –µ–ґ–µ–і–љ–µ–≤–љ–Њ 2 —А./—Б—Г—В –Р–Ь–У –≤ –і–Њ–Ј–µ 600 –Љ–≥ –Є–ї–Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–± –≤ –і–Њ–Ј–µ 200 –Љ–≥. –С—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ—Б—В—М –Р–Ь–У –Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ —Б–Њ —Б—А–∞–≤–љ–Є–Љ–Њ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М—О –і–ї—П –Ц–Ъ–Ґ. –Т —В–∞–±–ї–Є—Ж–µ 3 –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ —Б—Е–Њ–ґ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–∞ 4, 12 –Є 24-–є –љ–µ–і. –њ—А–Є–µ–Љ–∞.
–І–∞—Б—В–Њ—В–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є —В–∞–Ї–ґ–µ –±—Л–ї–∞ —Б—Е–Њ–ґ–µ–є –і–ї—П –Њ–±–Њ–Є—Е –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П (—В–∞–±–ї. 4). –Я—А–Њ—Ж–µ–љ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–Љ–Є —П–≤–ї–µ–љ–Є—П–Љ–Є —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ, —Б–≤—П–Ј–∞–љ–љ—Л–Љ–Є —Б —В–µ—А–∞–њ–Є–µ–є –Э–Я–Т–Я, —Б–Њ—Б—В–∞–≤–Є–ї 21,2% – –і–ї—П –≥—А—Г–њ–њ—Л –њ—А–Є–µ–Љ–∞ –Р–Ь–У –Є 26,5% – –і–ї—П —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞.
–£—З–Є—В—Л–≤–∞—П –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–є —А–Є—Б–Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У-2, –∞–≤—В–Њ—А—Л –≤ –і–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –Є –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ —П–≤–ї–µ–љ–Є—П —Б–Њ —Б—В–Њ—А–Њ–љ—Л —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –Р–Ь–У –Є —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–Њ–Љ. –°–Њ–≥–ї–∞—Б–љ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –≠–Ъ–У, —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –љ–Є –њ—А–Є –Љ–µ–ґ–≥—А—Г–њ–њ–Њ–≤–Њ–Љ —Б—А–∞–≤–љ–µ–љ–Є–Є (—В–Њ—З–љ—Л–є —В–µ—Б—В –§–Є—И–µ—А–∞ –љ–∞ –Є—Б—Е–Њ–і–љ–Њ–Љ —Г—А–Њ–≤–љ–µ, p=0,6004 –Є –њ—А–Є –њ–Њ—Б–ї–µ–і–љ–µ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, —В–Њ—З–љ—Л–є —В–µ—Б—В –§–Є—И–µ—А–∞, p=1,0000), –љ–Є –њ—А–Є –≤–љ—Г—В—А–Є–≥—А—Г–њ–њ–Њ–≤–Њ–Љ —Б—А–∞–≤–љ–µ–љ–Є–Є (—В–µ—Б—В Mc-Nemar: p=0,5637 –Р–Ь–У –Є p=0,797 – –і–ї—П –≥—А—Г–њ–њ—Л –њ—А–Є–µ–Љ–∞ —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞).
–Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –¶–Ю–У-2-—Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Э–Я–Т–Я, –Ї–Њ—В–Њ—А—Л–µ –љ–µ –≤–ї–Є—П—О—В –љ–∞ –∞–≥—А–µ–≥–∞—Ж–Є—О —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ [42], –Р–Ь–У –Њ–±–ї–∞–і–∞–µ—В –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О in vitro –Є ex vivo, —Б—А–∞–≤–љ–Є–Љ–Њ–є —Б –і–µ–є—Б—В–≤–Є–µ–Љ –Р–°–Ъ [43]. –С–ї–∞–≥–Њ–і–∞—А—П —Н—В–Њ–Љ—Г —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ—Г —Н—Д—Д–µ–Ї—В—Г –і–∞–љ–љ—Л–є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В —П–≤–ї—П–µ—В—Б—П –±–Њ–ї–µ–µ –њ–Њ–і—Е–Њ–і—П—Й–Є–Љ, —З–µ–Љ —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є –Є–љ–≥–Є–±–Є—В–Њ—А –¶–Ю–У-2, –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ–і–љ–Є–Љ –Є–ї–Є –±–Њ–ї–µ–µ –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞.
–Я–Њ–і–≤–Њ–і—П –Є—В–Њ–≥ –≤—Л—И–µ—Б–Ї–∞–Ј–∞–љ–љ–Њ–Љ—Г, –Љ–Њ–ґ–љ–Њ –Ї–Њ–љ—Б—В–∞—В–Є—А–Њ–≤–∞—В—М, —З—В–Њ –Р–Ь–У —П–≤–ї—П–µ—В—Б—П –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –Њ–±–ї–∞–і–∞—П –љ–µ —В–Њ–ї—М–Ї–Њ —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л–Љ–Є —Б —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–Љ–Є –Э–Я–Т–Я –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ, –∞–љ–∞–ї–≥–µ—В–Є—З–µ—Б–Ї–Є–Љ –Є –∞–љ—В–Є–њ–Є—А–µ—В–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–∞–Љ–Є, –љ–Њ –Є —Е–Њ—А–Њ—И–Є–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –і–ї—П –Ц–Ъ–Ґ –Є —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Я—А–µ–і—Б—В–∞–≤–Є—В–µ–ї–µ–Љ –Р–Ь–У –љ–∞ —А–Њ—Б—Б–Є–є—Б–Ї–Њ–Љ —Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Њ–Љ —А—Л–љ–Ї–µ —П–≤–ї—П–µ—В—Б—П –њ–Њ—П–≤–Є–≤—И–Є–є—Б—П –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–і–∞–≤–љ–Њ –њ—А–µ–њ–∞—А–∞—В –Э–∞–є–Ј–Є–ї–∞—В, –Ї–Њ—В–Њ—А—Л–є, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –Ј–∞–є–Љ–µ—В –і–Њ—Б—В–Њ–є–љ—Л–µ –њ–Њ–Ј–Є—Ж–Є–Є –≤ —В–µ—А–∞–њ–Є–Є –±–Њ–ї–Є –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П, –∞ –њ–Њ –∞—Б–њ–µ–Ї—В—Г –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Љ–Њ–ґ–µ—В —Б—В–∞—В—М –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–Њ–є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л—Е –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –¶–Ю–У-2. –Ф–∞–љ–љ–Њ–µ –Њ–±—Б—В–Њ—П—В–µ–ї—М—Б—В–≤–Њ –њ—А–Є–Њ–±—А–µ—В–∞–µ—В –≤–∞–ґ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ —Г –њ–Њ–ї–Є–Љ–Њ—А–±–Є–і–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –ї–Є—Ж –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –Ї–Њ–≥–і–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ –і–ї–Є—В–µ–ї—М–љ—Л–є –њ—А–Є–µ–Љ –Э–Я–Т–Я.












