–Ю–і–љ–∞–Ї–Њ –і—А—Г–≥–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є –љ–µ –≤—Л—П–≤–Є–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Љ–µ–ґ–і—Г —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ –Є —А–∞–Ј–≤–Є—В–Є–µ–Љ —Б—В–Њ–є–Ї–Њ–є –Њ—Д—В–∞–ї—М–Љ–Њ–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –њ–Њ—Б–ї–µ –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ anti-VEGF [19вАУ22]. –С—Л–ї–∞ –≤—Л–і–≤–Є–љ—Г—В–∞ –≥–Є–њ–Њ—В–µ–Ј–∞ –Њ —В–Њ–Љ, —З—В–Њ —А–∞–Ј–≤–Є—В–Є–µ –Њ—Д—В–∞–ї—М–Љ–Њ–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –њ–Њ—Б–ї–µ –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ—Л—Е –Є–љ—К–µ–Ї—Ж–Є–є –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ —Б CD36 –≥–µ–љ–љ—Л–Љ –њ–Њ–ї–Є–Љ–Њ—А—Д–Є–Ј–Љ–Њ–Љ [23]. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–Љ–µ—О—Й–Є–µ—Б—П –і–∞–љ–љ—Л–µ –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л—Е –њ—А–Є—З–Є–љ–∞—Е –Є —Д–∞–Ї—В–Њ—А–∞—Е —А–Є—Б–Ї–∞, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–≤–Њ–і—П—В –Ї —Б—В–Њ–є–Ї–Њ–Љ—Г –њ–Њ–≤—Л—И–µ–љ–Є—О —Г—А–Њ–≤–љ—П –Т–У–Ф –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ anti-VEGF, –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л. –Т —Н—В–Њ–є —Б–≤—П–Ј–Є —Ж–µ–ї—М—О –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б—В–∞–ї–Њ –Є–Ј—Г—З–µ–љ–Є–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є —Г—А–Њ–≤–љ—П –Т–У–Ф –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –њ–Њ—Б–ї–µ –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–Њ–≤ anti-VEGF —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Є–Љ–Є –Є —Б–Ї—А—Л—В—Л–Љ–Є —Е–Њ—А–Є–Њ–Є–і–∞–ї—М–љ—Л–Љ–Є –љ–µ–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–Љ–Є –Љ–µ–Љ–±—А–∞–љ–∞–Љ–Є (–•–Э–Т).
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –љ–∞ –±–∞–Ј–µ –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–і–µ–ї–µ–љ–Є—П –§–Ъ–£ ¬Ђ–¶–µ–љ—В—А–∞–ї—М–љ—Л–є –≤–Њ–µ–љ–љ—Л–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –≥–Њ—Б–њ–Є—В–∞–ї—М –Є–Љ. –Я. –Т. –Ь–∞–љ–і—А—Л–Ї–∞¬ї –Ь–Є–љ–Њ–±–Њ—А–Њ–љ—Л –†–Њ—Б—Б–Є–Є –≤ –њ–µ—А–Є–Њ–і —Б –Љ–∞—П 2016 –њ–Њ —П–љ–≤–∞—А—М 2017 –≥. –§–Є–љ–∞–ї—М–љ—Л–є –њ—А–Њ—В–Њ–Ї–Њ–ї –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤–Ї–ї—О—З–∞–ї –і–∞–љ–љ—Л–µ 34 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (40 –≥–ї–∞–Ј) —Б ¬Ђ–≤–ї–∞–ґ–љ–Њ–є¬ї —Д–Њ—А–Љ–Њ–є –Т–Ь–Ф. –Т–µ—А–Є—Д–Є–Ї–∞—Ж–Є—П –і–Є–∞–≥–љ–Њ–Ј–∞, –≤–Ї–ї—О—З–∞—П –љ–∞–ї–Є—З–Є–µ —Е–Њ—А–Є–Њ–Є–і–∞–ї—М–љ–Њ–є –љ–µ–Њ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є, –±—Л–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ —Б –њ–Њ–Љ–Њ—Й—М—О —Д–ї—О–Њ—А–µ—Б—Ж–µ–љ—В–љ–Њ–є –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є–Є (–§–Р–У) –Є –Њ–њ—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ–≥–µ—А–µ–љ—В–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є (–Ю–Ъ–Ґ) –љ–∞ –њ—А–Є–±–Њ—А–µ —Б–њ–µ–Ї—В—А–∞–ї—М–љ–Њ–≥–Њ —В–Є–њ–∞ (Spectralis, Heidelberg Engineering, –У–µ—А–Љ–∞–љ–Є—П).–Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 2 –≥—А—Г–њ–њ—Л: 1-—О –≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л —Б –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Њ–є –•–Э–Т (19 –≥–ї–∞–Ј), 2-—О –≥—А—Г–њ–њ—Г вАФ –њ–∞—Ж–Є–µ–љ—В—Л —Б–Њ —Б–Ї—А—Л—В–Њ–є –•–Э–Т (21 –≥–ї–∞–Ј). –Т –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ—Л–µ –Є–љ—К–µ–Ї—Ж–Є–Є 0,05 –Љ–ї (0,5 –Љ–≥) –њ—А–µ–њ–∞—А–∞—В–∞ —А–∞–љ–Є–±–Є–Ј—Г–Љ–∞–± –і–≤—Г–Љ—П —Б–µ—А—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є —Е–Є—А—Г—А–≥–∞–Љ–Є. –Ъ—А–Є—В–µ—А–Є–µ–Љ –≤–Ї–ї—О—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –і–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –њ–Њ–Љ–Є–Љ–Њ –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –і–Є–∞–≥–љ–Њ–Ј–∞, –±—Л–ї–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є –≥–ї–∞—Г–Ї–Њ–Љ—Л. –£—А–Њ–≤–µ–љ—М –Т–У–Ф –Є–Ј–Љ–µ—А—П–ї–Є –Ј–∞ 1 —З –і–Њ –Є–љ—К–µ–Ї—Ж–Є–Є, —З–µ—А–µ–Ј 1 —З –њ–Њ—Б–ї–µ –љ–µ–µ, –∞ —В–∞–Ї–ґ–µ –љ–∞ 7-–є –і–µ–љ—М –Є —З–µ—А–µ–Ј 1 –Љ–µ—Б. –њ–Њ—Б–ї–µ –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П anti-VEGF –њ—А–µ–њ–∞—А–∞—В–∞ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Љ–µ—В–Њ–і–∞ —В–Њ–љ–Њ–Љ–µ—В—А–Є–Є –њ–Њ –Ь–∞–Ї–ї–∞–Ї–Њ–≤—Г (–≥—А—Г–Ј 10 –≥). –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Њ—Д—В–∞–ї—М–Љ–Њ—В–Њ–љ—Г—Б–∞ –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М –≤ –Ї–ї–Є–љ–Є–Ї–µ –≤ –Є–љ—В–µ—А–≤–∞–ї–µ –Њ—В 10:00 –і–Њ 12:00. –Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Њ—Б—В—А–Њ—В—Л –Ј—А–µ–љ–Є—П —Г –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –≤ —Б—В–∞–љ–і–∞—А—В–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –Њ—Б–≤–µ—Й–µ–љ–Є—П –њ–Њ —В–∞–±–ї–Є—Ж–∞–Љ –°–љ–µ–ї–ї–µ–љ–∞. –Э–∞–Є–ї—Г—З—И–∞—П –Ї–Њ—А—А–Є–≥–Є—А–Њ–≤–∞–љ–љ–∞—П –Њ—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П –њ—А–Њ–≤–µ—А—П–ї–∞—Б—М –≤ —Г—Б–ї–Њ–≤–Є—П—Е –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є. –°—А–Њ–Ї –љ–∞–±–ї—О–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –і–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –Њ–≥—А–∞–љ–Є—З–Є–≤–∞–ї—Б—П –Є–љ—В–µ—А–≤–∞–ї–Њ–Љ –љ–∞–±–ї—О–і–µ–љ–Є—П 35вАУ45 –і–љ–µ–є, —З—В–Њ –±—Л–ї–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–Њ –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ –і–Є–Ј–∞–є–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤—Б–ї–µ–і—Б—В–≤–Є–µ –њ–ї–∞–љ–Є—А–Њ–≤–∞–љ–Є—П –њ–Њ–≤—В–Њ—А–љ–Њ–є –Є–љ—К–µ–Ї—Ж–Є–Є anti-VEGF –њ—А–µ–њ–∞—А–∞—В–∞.
–Ь–µ—В–Њ–і—Л —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Њ–±—А–∞–±–Њ—В–Ї–Є
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –≤–љ–Њ—Б–Є–ї–Є—Б—М –≤ –Њ–±—Й—Г—О —В–∞–±–ї–Є—Ж—Г –і–∞–љ–љ—Л—Е –љ–∞ —Б–µ—А—В–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Њ–±–Њ—А—Г–і–Њ–≤–∞–љ–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –ї–Є—Ж–µ–љ–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ –∞–љ–∞–ї–Є–Ј–Є—А—Г–µ–Љ—Л—Е –і–∞–љ–љ—Л—Е –≤—Л–њ–Њ–ї–љ—П–ї–∞—Б—М –Њ–і–љ–Є–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–Љ —Б –њ–Њ–Љ–Њ—Й—М—О –њ—А–Њ–≥—А–∞–Љ–Љ—Л Statistica, –≤–µ—А—Б–Є—П 10.0 (StatSoft, Inc., –°–®–Р). –Я—А–Є–≤–Њ–і–Є–Љ—Л–µ –њ–∞—А–∞–Љ–µ—В—А—Л –њ—А–Њ–≤–µ—А—П–ї–Є—Б—М –љ–∞ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–µ –Ј–∞–Ї–Њ–љ—Г –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П (–Ї—А–Є—В–µ—А–Є–є –®–∞–њ–Є—А–Њ вАФ –£–Є–ї–Ї–∞, p>0,05). –І–Є—Б–ї–Њ–≤—Л–µ –і–∞–љ–љ—Л–µ, –Є–Љ–µ—О—Й–Є–µ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–µ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ, –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —Д–Њ—А–Љ–∞—В–µ: –Ь¬±ѕГ, –≥–і–µ –Ь вАФ —Б—А–µ–і–љ–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ, ѕГ вАФ —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ —Б—А–µ–і–љ–µ–≥–Њ –Ј–љ–∞—З–µ–љ–Є—П. –Я—А–Є —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–Є, –Њ—В–ї–Є—З–љ–Њ–Љ –Њ—В –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ (–Ї—А–Є—В–µ—А–Є–є –®–∞–њ–Є—А–Њ вАФ –£–Є–ї–Ї–∞, p<0,05), –і–∞–љ–љ—Л–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ –≤–Є–і–µ –Љ–µ–і–Є–∞–љ—Л –Є –Ї–≤–∞—А—В–Є–ї–µ–є (Me (25%; 75%)). –Я–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≤ –і–≤—Г—Е –Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≤—Л–±–Њ—А–Ї–∞—Е –≤ —А–∞–Ј–љ—Л–µ —Б—А–Њ–Ї–Є –≤–≤–µ–і–µ–љ–Є—П anti-VEGF –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б—А–∞–≤–љ–Є–≤–∞–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О –њ–∞—А–љ–Њ–≥–Њ –Ї—А–Є—В–µ—А–Є—П –£–Є–ї–Ї–Њ–Ї—Б–Њ–љ–∞. –Я–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≤ –і–≤—Г—Е –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≤—Л–±–Њ—А–Ї–∞—Е –њ—А–Є –љ–Њ—А–Љ–∞–ї—М–љ–Њ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–Є —Б—А–∞–≤–љ–Є–≤–∞–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О t-–Ї—А–Є—В–µ—А–Є—П –і–ї—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≤—Л–±–Њ—А–Њ–Ї, –і–ї—П —Б—А–∞–≤–љ–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ –і–≤—Г—Е –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л—Е –≤—Л–±–Њ—А–Ї–∞—Е –њ—А–Є –љ–µ–љ–Њ—А–Љ–∞–ї—М–љ–Њ–Љ —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є –Ї—А–Є—В–µ—А–Є–є –Ь–∞–љ–љ–∞ вАФ –£–Є—В–љ–Є.–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є –Њ–±—Б—Г–ґ–і–µ–љ–Є–µ
–°—А–µ–і–Є –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –±—Л–ї–Њ 61,8% –Љ—Г–ґ—З–Є–љ (21 —З–µ–ї–Њ–≤–µ–Ї) –Є 38,2% –ґ–µ–љ—Й–Є–љ (13 —З–µ–ї–Њ–≤–µ–Ї). –°—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –≤—Б–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ—Б—В–∞–≤–Є–ї 76,79¬±7,13 –≥–Њ–і–∞. –°—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –Љ—Г–ґ—З–Є–љ —Б–Њ—Б—В–∞–≤–Є–ї 76,00¬±7,27 –≥–Њ–і–∞, –ґ–µ–љ—Й–Є–љ вАФ 78,08¬±6,98 –≥–Њ–і–∞. –°—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ 1-–є –≥—А—Г–њ–њ–µ —Б–Њ—Б—В–∞–≤–Є–ї 78,06¬±6,92 –≥–Њ–і–∞, –≤–Њ 2-–є –≥—А—Г–њ–њ–µ вАФ 76,15¬±6,94 –≥–Њ–і–∞. –Ф–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –Њ—В–ї–Є—З–Є–є –њ–Њ –≤–Њ–Ј—А–∞—Б—В—Г —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ (p>0,05).
–Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–≥–Њ —А–∞–љ–µ–µ –і–Є–∞–≥–љ–Њ–Ј–∞ –љ–∞ –Љ–Њ–Љ–µ–љ—В –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤ 1-–є –≥—А—Г–њ–њ–µ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 11 (3; 24) –Љ–µ—Б., –≤–Њ 2-–є –≥—А—Г–њ–њ–µ вАФ 12 (7; 34) –Љ–µ—Б. –Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ—Л—Е –Є–љ—К–µ–Ї—Ж–Є–є anti-VEGF –њ—А–µ–њ–∞—А–∞—В–∞ –і–Њ –Љ–Њ–Љ–µ–љ—В–∞ –≤–Ї–ї—О—З–µ–љ–Є—П –≤ 1-–є –≥—А—Г–њ–њ–µ —Б–Њ—Б—В–∞–≤–Є–ї–Њ 2 (1; 3) –Є–љ—К–µ–Ї—Ж–Є–Є, –≤–Њ 2-–є –≥—А—Г–њ–њ–µ вАФ —В–∞–Ї–ґ–µ 2 (0; 3) –Є–љ—К–µ–Ї—Ж–Є–Є. –Ф–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –Њ—В–ї–Є—З–Є–є –њ–Њ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –і–Є–∞–≥–љ–Њ–Ј–∞ –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –њ—А–µ–і—Л–і—Г—Й–Є—Е –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ—Л—Е –Є–љ—К–µ–Ї—Ж–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ (p>0,05).
–Я–Њ –і–∞–љ–љ—Л–Љ –Ю–Ъ–Ґ, —В–Њ–ї—Й–Є–љ–∞ —Б–µ—В—З–∞—В–Ї–Є –≤ 1-–є –≥—А—Г–њ–њ–µ –і–Њ –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П anti-VEGF –њ—А–µ–њ–∞—А–∞—В–∞ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 353 (307; 460) –Љ–Ї–Љ, –≤–Њ 2-–є –≥—А—Г–њ–њ–µ вАФ 375 (312; 416) –Љ–Ї–Љ (—А–Є—Б. 1, 2). –Ъ–Њ—А—А–Є–≥–Є—А–Њ–≤–∞–љ–љ–∞—П –Њ—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 1-–є –≥—А—Г–њ–њ—Л –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ 0,2 (0,05; 0,3), –≤–Њ 2-–є –≥—А—Г–њ–њ–µ —Н—В–Њ—В –ґ–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –±—Л–ї —А–∞–≤–µ–љ 0,4 (0,2; 0,6), p=0,008. –Я–Њ—Б–ї–µ –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П anti-VEGF –њ—А–µ–њ–∞—А–∞—В–∞ –≤ 1-–є –≥—А—Г–њ–њ–µ —В–Њ–ї—Й–Є–љ–∞ —Б–µ—В—З–∞—В–Ї–Є –≤ –Љ–∞–Ї—Г–ї–µ —Б–љ–Є–Ј–Є–ї–∞—Б—М –і–Њ 316 (263; 428) –Љ–Ї–Љ, –≤–Њ 2-–є –≥—А—Г–њ–њ–µ вАФ –і–Њ 291 (268; 394) –Љ–Ї–Љ. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–є —А–∞–Ј–љ–Є—Ж—Л –Љ–µ–ґ–і—Г –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ ¬Ђ—В–Њ–ї—Й–Є–љ–∞ —Б–µ—В—З–∞—В–Ї–Є –≤ –Љ–∞–Ї—Г–ї–µ¬ї –і–Њ –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –Є —Н—В–Є–Љ –ґ–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –≤—Л—П–≤–ї–µ–љ–Њ –љ–µ –±—Л–ї–Њ (p>0,05). –Ъ–Њ—А—А–Є–≥–Є—А–Њ–≤–∞–љ–љ–∞—П –Њ—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є –њ–Њ–≤—Л—Б–Є–ї–∞—Б—М –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е: –≤ 1-–є –≥—А—Г–њ–њ–µ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 0,3 (0,05; 0,3), –≤–Њ 2-–є –≥—А—Г–њ–њ–µ вАФ
0,4 (0,4; 0,6), –Є —Н—В–Є —А–∞–Ј–ї–Є—З–Є—П –±—Л–ї–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ (p<0,001).

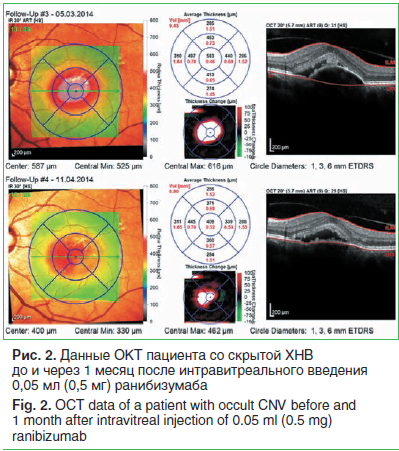
–£—А–Њ–≤–µ–љ—М –Т–У–Ф –≤ 1-–є –≥—А—Г–њ–њ–µ —З–µ—А–µ–Ј 1 —З –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є –њ–Њ–≤—Л—Б–Є–ї—Б—П –і–Њ 20 (17; 22) –Љ–Љ —А—В. —Б—В., –Њ–і–љ–∞–Ї–Њ –љ–∞ 7-–є –і–µ–љ—М –љ–∞—Е–Њ–і–Є–ї—Б—П —Г–ґ–µ –љ–∞ –Є—Б—Е–Њ–і–љ–Њ–Љ —Г—А–Њ–≤–љ–µ, –Ї–Њ—В–Њ—А—Л–є —Б–Њ—Е—А–∞–љ—П–ї—Б—П –Є —З–µ—А–µ–Ј 1 –Љ–µ—Б. –Ь–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–µ –Љ–µ—Б—В–љ–Њ–µ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –љ–µ –љ–∞–Ј–љ–∞—З–∞–ї–Њ—Б—М. –Т–Њ 2-–є –≥—А—Г–њ–њ–µ —Г—А–Њ–≤–µ–љ—М –Т–У–Ф –Њ—Б—В–∞–≤–∞–ї—Б—П —Б—В–∞–±–Є–ї—М–љ—Л–Љ –≤ —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ —Б—А–Њ–Ї–∞ –љ–∞–±–ї—О–і–µ-
–љ–Є—П. –†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф –і–Њ –Є –њ–Њ—Б–ї–µ –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П anti-VEGF –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 1.
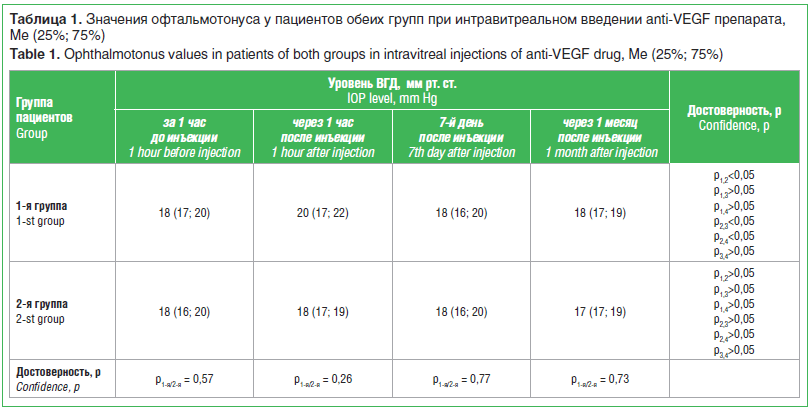
–Т 1-–є –≥—А—Г–њ–њ–µ –±—Л–ї–∞ –Њ–±–љ–∞—А—Г–ґ–µ–љ–∞ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П —А–∞–Ј–љ–Є—Ж–∞ –Љ–µ–ґ–і—Г —Г—А–Њ–≤–љ–µ–Љ –Т–У–Ф —З–µ—А–µ–Ј 1 —З –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є –Є —Г—А–Њ–≤–љ—П–Љ–Є –Њ—Д—В–∞–ї—М–Љ–Њ—В–Њ–љ—Г—Б–∞ –і–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞, –∞ —В–∞–Ї–ґ–µ —З–µ—А–µ–Ј 7 –і–љ–µ–є –Є 1 –Љ–µ—Б. –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є (p<0,05). –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —А–∞–Ј–љ–Є—Ж—Л –Љ–µ–ґ–і—Г –Є—Б—Е–Њ–і–љ—Л–Љ–Є –Ј–љ–∞—З–µ–љ–Є—П–Љ–Є –Њ—Д—В–∞–ї—М–Љ–Њ—В–Њ–љ—Г—Б–∞ –Є –Є—Е –Ј–љ–∞—З–µ–љ–Є—П–Љ–Є –≤ —В–µ—З–µ–љ–Є–µ 1 –Љ–µ—Б. –љ–∞–±–ї—О–і–µ–љ–Є—П –љ–µ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ (p>0,05). –Т–Њ 2-–є –≥—А—Г–њ–њ–µ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –Њ—В–ї–Є—З–Є–є –≤ —Г—А–Њ–≤–љ–µ –Т–У–Ф —З–µ—А–µ–Ј 1 —З, –љ–∞ 7-–є –і–µ–љ—М –Є —З–µ—А–µ–Ј 1 –Љ–µ—Б. –њ–Њ—Б–ї–µ –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–є –Є–љ—К–µ–Ї—Ж–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 2-–є –≥—А—Г–њ–њ—Л –љ–µ –≤—Л—П–≤–ї–µ–љ–Њ (p>0,05). –Я—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є —Г—А–Њ–≤–љ—П –Њ—Д—В–∞–ї—М–Љ–Њ—В–Њ–љ—Г—Б–∞ –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –љ–∞ —А–∞–Ј–љ—Л—Е —Б—А–Њ–Ї–∞—Е –љ–∞–±–ї—О–і–µ–љ–Є—П –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–є —А–∞–Ј–љ–Є—Ж—Л —Н—В–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ (p>0,05).
–°–Њ–≥–ї–∞—Б–љ–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–Љ –≤ —В–∞–±–ї–Є—Ж–µ –і–∞–љ–љ—Л–Љ, –Љ—Л –љ–µ –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є –њ–Њ–≤—Л—И–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф —З–µ—А–µ–Ј 7 –і–љ–µ–є –Є 1 –Љ–µ—Б. –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –љ–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П anti-VEGF –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —А–∞–љ–µ–µ –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л—Е –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ—Л—Е –≤–≤–µ–і–µ–љ–Є–є –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е —Б–Њ—Б—В–∞–≤–Є–ї–Њ –Њ—В 0 –і–Њ 6 –Є–љ—К–µ–Ї—Ж–Є–є. –Т —В–µ—З–µ–љ–Є–µ –≤—Б–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –љ–∞–±–ї—О–і–µ–љ–Є—П (1 –Љ–µ—Б., 4 –Є–Ј–Љ–µ—А–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф) –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Њ—Д—В–∞–ї—М–Љ–Њ—В–Њ–љ—Г—Б–∞ –љ–∞—Е–Њ–і–Є–ї–Є—Б—М –≤ ¬Ђ–Ї–Њ—А–Є–і–Њ—А–µ¬ї (min/max) –Њ—В 14 –і–Њ 21 –Љ–Љ —А—В. —Б—В. –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Њ–є –•–Э–Т –Є –≤ –Є–љ—В–µ—А–≤–∞–ї–µ –Њ—В 13 –і–Њ 24 –Љ–Љ —А—В. —Б—В. —Г –ї–Є—Ж —Б–Њ —Б–Ї—А—Л—В–Њ–є –•–Э–Т. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б —Г—З–µ—В–Њ–Љ —А–∞–Ј–ї–Є—З–Є–є ¬Ђ—В–Њ–љ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є—Е –Ї–Њ—А–Є–і–Њ—А–Њ–≤¬ї –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –Ї–Њ–ї–µ–±–∞–љ–Є–є –Њ—Д—В–∞–ї—М–Љ–Њ—В–Њ–љ—Г—Б–∞ —Г –ї–Є—Ж —Б–Њ —Б–Ї—А—Л—В–Њ–є –•–Э–Т —Б—Г—Й–µ—Б—В–≤—Г–µ—В, –љ–Њ –≤ –љ–∞—И–µ–Љ –љ–∞–±–ї—О–і–µ–љ–Є–Є, –і–∞–ґ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —И–µ—Б—В–Є–Ї—А–∞—В–љ—Л–Љ –≤–≤–µ–і–µ–љ–Є–µ–Љ —А–∞–љ–Є–±–Є–Ј—Г–Љ–∞–±–∞ –Є–Ј —Н—В–Њ–є –≥—А—Г–њ–њ—Л –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –њ–Њ–≤—Л—И–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф.
–Ю–≥—А–∞–љ–Є—З–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–°–ї–µ–і—Г–µ—В —Г—З–Є—В—Л–≤–∞—В—М, —З—В–Њ —Б—А–Њ–Ї –љ–∞–±–ї—О–і–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–ї—П–ї –≤—Б–µ–≥–Њ 1 –Љ–µ—Б. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤ –љ–∞—И–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–µ –±—Л–ї–Њ —А–∞–Ј–і–µ–ї–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ–ї–Њ—Й–∞–і–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–Є—П –•–Э–Т, –∞ —В–∞–Ї–ґ–µ —А–∞–Ј–і–µ–ї–µ–љ–Є—П –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —А–∞–љ–µ–µ –≤—Л–њ–Њ–ї–љ–µ–љ–љ—Л—Е –Є–љ—К–µ–Ї—Ж–Є–є –љ–∞ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ –њ–Њ–і–≥—А—Г–њ–њ—Л, –≤ —В. —З. –Њ—В–і–µ–ї—М–љ–Њ –љ–µ –≤—Л–і–µ–ї—П–ї–Є —В–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї–Њ–Љ—Г –Њ–љ–∞ –±—Л–ї–∞ —Б–і–µ–ї–∞–љ–∞ –≤–њ–µ—А–≤—Л–µ.–Т—Л–≤–Њ–і—Л
–£ –±–Њ–ї—М–љ—Л—Е —Б ¬Ђ–≤–ї–∞–ґ–љ–Њ–є¬ї —Д–Њ—А–Љ–Њ–є –Т–Ь–Ф –Є –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Њ–є –•–Э–Т –Њ—В–Љ–µ—З–µ–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Т–У–Ф —З–µ—А–µ–Ј 1 —З –њ–Њ—Б–ї–µ –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –Є–љ—В—А–∞–≤–Є—В—А–µ–∞–ї—М–љ–Њ–є –Є–љ—К–µ–Ї—Ж–Є–Є (p<0,05). –Э–∞ —Д–Њ–љ–µ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ anti-VEGF —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б ¬Ђ–≤–ї–∞–ґ–љ–Њ–є¬ї —Д–Њ—А–Љ–Њ–є –Т–Ь–Ф —Б –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Њ–є –Є —Б–Њ —Б–Ї—А—Л—В–Њ–є –•–Э–Т —Г—А–Њ–≤–µ–љ—М –Т–У–Ф –љ–µ –Є–Ј–Љ–µ–љ–Є–ї—Б—П –љ–∞ 7-–є –і–µ–љ—М –Є —З–µ—А–µ–Ј 1 –Љ–µ—Б. –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є (—А>0,05). –Э–∞–ї–Є—З–Є–µ –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Њ–є –•–Э–Т –Љ–Њ–ґ–µ—В —П–≤–ї—П—В—М—Б—П —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –і–ї—П –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–Є—П —Г—А–Њ–≤–љ—П –Т–У–Ф –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –њ–Њ–≤—В–Њ—А–љ–Њ–є anti-VEGF —В–µ—А–∞–њ–Є–Є –≤ –і–Њ–Ј–µ 0,05 –Љ–ї (0,5 –Љ–≥).–°—Г—Й–µ—Б—В–≤—Г–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Њ—Д—В–∞–ї—М–Љ–Њ—В–Њ–љ—Г—Б–∞ —Г –ї–Є—Ж —Б –Ї–ї–∞—Б—Б–Є—З–µ—Б–Ї–Њ–є –Є —Б–Ї—А—Л—В–Њ–є –•–Э–Т –Є —А–∞–Ј–љ—Л–Љ–Є –Є—Б—Е–Њ–і–љ—Л–Љ–Є —Г—А–Њ–≤–љ—П–Љ–Є –Т–У–Ф –љ–∞ —Д–Њ–љ–µ –њ–Њ–≤—В–Њ—А–љ—Л—Е –≤–≤–µ–і–µ–љ–Є–є anti-VEGF –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–°–≤–µ–і–µ–љ–Є—П –Њ–± –∞–≤—В–Њ—А–∞—Е: 1,2–Ъ—Г—А–Њ–µ–і–Њ–≤ –Р–ї–µ–Ї—Б–∞–љ–і—А –Т–ї–∞–і–Є–Љ–Є—А–Њ–≤–Є—З вАФ –і.–Љ.–љ., –њ—А–Њ—Д–µ—Б—Б–Њ—А, –љ–∞—З–∞–ї—М–љ–Є–Ї –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–і–µ–ї–µ–љ–Є—П; 3–Ч–∞—Е–∞—А–Њ–≤–∞ –Ь–∞—А–Є—П –Р–љ–і—А–µ–µ–≤–љ–∞ вАФ –Ї.–Љ.–љ., –≤—А–∞—З-–Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥; 1–У–∞–њ–Њ–љ—М–Ї–Њ –Ю–ї–µ—Б—П –Т–ї–∞–і–Є–Љ–Є—А–Њ–≤–љ–∞ вАФ –Ї.–Љ.–љ., –≤—А–∞—З-–Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥; 1–У–Њ—А–Њ–і–љ–Є—З–Є–є –Т–Є—В–∞–ї–Є–є –Т–ї–∞–і–Є–Љ–Є—А–Њ–≤–Є—З вАФ –≤—А–∞—З-–Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥. 1–§–Ъ–£ ¬Ђ–¶–Т–Ъ–У –Є–Љ. –Я. –Т. –Ь–∞–љ–і—А—Л–Ї–∞¬ї –Ь–Є–љ–Њ–±–Њ—А–Њ–љ—Л –†–Њ—Б—Б–Є–Є. 107014, –†–Њ—Б—Б–Є–є—Б–Ї–∞—П –§–µ–і–µ—А–∞—Ж–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, —Г–ї. –С. –Ю–ї–µ–љ—М—П, –і. 8–∞. 2–§–У–С–Ю–£ –Т–Ю –†–Э–Ш–Ь–£ –Є–Љ. –Э. –Ш. –Я–Є—А–Њ–≥–Њ–≤–∞ –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є. 117997, –†–Њ—Б—Б–Є–є—Б–Ї–∞—П –§–µ–і–µ—А–∞—Ж–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, —Г–ї. –Ю—Б—В—А–Њ–≤–Є—В—П–љ–Њ–≤–∞, –і. 1. 3–§–У–Р–£ –Э–Ь–Ш–¶ ¬Ђ–Ь–Э–Ґ–Ъ ¬Ђ–Ь–Є–Ї—А–Њ—Е–Є—А—Г—А–≥–Є—П –≥–ї–∞–Ј–∞¬ї –Є–Љ. –∞–Ї–∞–і. –°. –Э. –§–µ–і–Њ—А–Њ–≤–∞¬ї –Ь–Є–љ–Ј–і—А–∞–≤–∞ –†–Њ—Б—Б–Є–Є. 127486, –†–Њ—Б—Б–Є–є—Б–Ї–∞—П –§–µ–і–µ—А–∞—Ж–Є—П, –≥. –Ь–Њ—Б–Ї–≤–∞, –С–µ—Б–Ї—Г–і–љ–Є–Ї–Њ–≤—Б–Ї–Є–є –±—Г–ї—М–≤., –і. 59–∞. –Ъ–Њ–љ—В–∞–Ї—В–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П: –Ъ—Г—А–Њ–µ–і–Њ–≤ –Р–ї–µ–Ї—Б–∞–љ–і—А –Т–ї–∞–і–Є–Љ–Є—А–Њ–≤–Є—З, e-mail: akuroyedov@hotmail.com. –Я—А–Њ–Ј—А–∞—З–љ–Њ—Б—В—М —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є: –љ–Є–Ї—В–Њ –Є–Ј –∞–≤—В–Њ—А–Њ–≤ –љ–µ –Є–Љ–µ–µ—В —Д–Є–љ–∞–љ—Б–Њ–≤–Њ–є –Ј–∞–Є–љ—В–µ—А–µ—Б–Њ–≤–∞–љ–љ–Њ—Б—В–Є –≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е –Љ–∞—В–µ—А–Є–∞–ї–∞—Е –Є–ї–Є –Љ–µ—В–Њ–і–∞—Е. –Ъ–Њ–љ—Д–ї–Є–Ї—В –Є–љ—В–µ—А–µ—Б–Њ–≤ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В. –°—В–∞—В—М—П –њ–Њ—Б—В—Г–њ–Є–ї–∞ 14.11.2017.
About the authors: 1,2Aleksander V. Kuroyedov вАФ professor, –°hief of ophthalmology Department; 3Maria A. Zakharova вАФ PhD, ophthalmologist; 1Olesya V. Gaponko вАФ PhD, ophthalmologist; 1Vitaly V. Gorodnichy вАФ ophthalmologist. 1Central Military Clinical Hospital named after P. V. Mandryka. 8–Р, B. Oleniya str., Moscow, 107014, Russian Federation. 2Pirogov Russian National Research Medical University. 1, Ostrovityanova str., Moscow, 117997, Russian Federation. 3S. Fyodorov Eye Microsurgery Federal State Institution. 59–∞, Beskudnikovskaya str., Moscow, 127486, Russian Federation. Contact information: Aleksander V. Kuroyedov, e-mail: akuroyedov@hotmail.com. Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 14.11.2017.












