Введение
Сумма многочисленных факторов, включающих сложный патогенез заболевания, хронический прогредиентно текущий характер болезни с постепенным, но постоянным снижением эффективности любых методик лечения, старение населения в целом, необходимость пожизненного наблюдения при соблюдении значительного числа ограничений и условностей, должна приниматься во внимание при выборе стратегии лечебно-диагностического процесса для ее рационального использования [1–5]. С учетом вышесказанного, а также в силу изменения структуры патологии и традиционных медикаментозных назначений, произошедшего за последние 10–15 лет по причине появления новых местных антиглаукомных гипотензивных препаратов, включая отдельные формы без консервантов либо с присутствием альтернативных консервирующих составов, их комбинаций и развития рынка дженериков, практикующие врачи столкнулись с необходимостью переосмысления тактики ведения пациентов с ПОУГ [6–14]. В настоящее время обсуждаются необходимость дифференцированного подхода к лечению пациентов с разными стадиями заболевания на старте лечения, а также целесообразность применения агрессивных хирургических подходов у пациентов с разными уровнями внутриглазного давления (ВГД) и скоростью прогрессирования [15]. Не менее важными видятся горизонты персонализированных подходов к лечению, включающих динамическое наблюдение с использованием более совершенных приборов, а также применение дополнительных методик терапии [16–18]. Очевидно, что наряду с медицинскими проблемами при лечении ПОУГ большинство специалистов сталкиваются с социальными и личностными проблемами своих пациентов, которые накладывают отпечаток на специфику лечебно-диагностического процесса [19].По-прежнему ощущается недостаток клинико-эпидемиологических исследований, востребованность которых связана с возможностью использования для дальнейшего анализа большого массива материала, значительных выборок предикторов заболевания за продолжительный период наблюдения.
В этой связи целью настоящей работы стало установление структурных различий отдельных клинико-эпидемиологических показателей у пациентов с ПОУГ, поступавших на оперативное лечение в офтальмологический стационар ФКУ «ЦВКГ им. П.В. Мандрыка» МО РФ в 2005–2006 гг. и 2015–2016 гг.
Материал и методы
В итоговый протокол выборочного научно-клинического ретроспективного исследования были включены данные 204 человек (204 глаза; женщин – 51 (25%), мужчин – 153 (75%)). Для работы были использованы данные пациентов с начальной, развитой и далеко зашедшей стадиями ПОУГ, поступавших в 2005–2006 гг. и 2015–2016 гг. для проведения оперативного лечения вследствие отсутствия стабилизации процесса. За период 2005–2006 гг. были отобраны данные 108 пациентов (108 глаз (52,9%)), составивших 1-ю группу, за период 2015–2016 гг. – данные 96 больных (96 глаз (47,1%)), составивших 2-ю группу. Все оперативные вмешательства были выполнены 4 хирургами с разным уровнем профессиональной подготовки, опытом работы и индивидуальными предпочтениями, используемыми при оперативном лечении. Пациенты, включенные в исследование, находились на диспансерном наблюдении в диспансерном отделении госпиталя и других поликлиниках МО РФ. Для заполнения базы данных были использованы лицензированные персонализированные возможности таблицы Excel (Microsoft, США) с предварительной кодировкой результатов для исключения нарушения норм действующего законодательства.Были проанализированы следующие клинико-эпидемиологические показатели: пол; возраст на момент постановки диагноза, на момент выполнения первой антиглаукомной операции (если при настоящей госпитализации планировалось выполнение повторной хирургии глаукомы, а также количество таких операций в анамнезе) и возраст на момент поступления в стационар; количество сопутствующих соматических заболеваний; отдельные биохимические показатели крови (общий холестерин и глюкоза); наличие хрусталика или артифакия; уровень ВГД на момент поступления в стационар и при выписке; количество антиглаукомных препаратов (группы) и продолжительность медикаментозной гипотензивной терапии на момент поступления в стационар; морфофункциональные характеристики: толщина слоя нервных волокон сетчатки (СНВС), площадь и объем нейроретинального пояска (НРП), показатели статической автоматической периметрии; тип проведенного оперативного вмешательства; день недели проведения операции; продолжительность нахождения в стационаре; наличие и количество ранних послеоперационных осложнений.
Отдельно были проанализированы диагнозы направления и стационара, а также проведен дополнительный экспертный анализ диагнозов для исключения ошибок заполнения документации. Стадия глаукомы на момент заполнения истории болезни устанавливалась по данным медицинской документации поликлинического учреждения (на основании данных тонометрии, офтальмоскопии и разных видов периметрии). При этом в стационаре в указанные периоды наблюдения также выполнялась однократно статическая автоматическая периметрия (САП). Оценка уровня ВГД производилась согласно данным тонометрии, проведенной тонометром Маклакова (груз 10 г). Структурные параметры диска зрительного нерва (ДЗН) и СНВС исследовались при помощи гейдельбергской ретинальной томографии (HRT 3, Heidelberg Engineering, Германия). При анализе результатов САП устанавливали среднюю светочувствительность сетчатки (MD) и ее стандартное отклонение (PSD). Исследование вышеуказанных параметров проводилось на компьютерных периметрах Humphrey 740i и 750i (Carl Zeiss-Meditec Inc., США).
Экспертное заключение по отношению к диагнозу заболевания во всех случаях выполнялось в соответствии с системой дифференциальной диагностики заболеваний и было подтверждено специальными методами исследования, проводилось двумя квалифицированными специалистами. Результаты этого заключения фиксировались в протоколе и во всех случаях принимались в качестве последней инстанции при определении стадии заболевания.
Критерии включения и исключения, используемые при оценке медицинской документации
Критерии включения: наличие в документации результатов необходимых исследований; данные пациентов европеоидной расы с начальной, развитой или далеко зашедшей стадиями ПОУГ (с псевдоэксфолиативным синдромом (ПЭС) или без него, с разной степенью открытия угла передней камеры и документально подтвержденной не менее полугода от момента установления диагноза; на момент финального обследования пациенты могли получать любую антиглаукомную гипотензивную терапию или не получать ее по причине успешно выполненной ранее антиглаукомной операции; возраст пациентов – от 45 до 89 лет (средний, пожилой и старческий возраст, согласно классификации Всемирной организации здравоохранения от 2012 г., www.who.int/ru); клиническая рефракция ±6,0 диоптрии и астигматизм ±3,0 диоптрии; наличие хрусталика или артифакия.Критерии исключения: отсутствие документации, необходимой для ретроспективного анализа; пациенты с любой другой формой ПОУГ и клинической рефракцией, нежели указано выше; пациенты с любыми другими заболеваниями сетчатки (например, возрастная макулодистрофия, «сухая» форма (начиная со II стадии по классификации AREDS (2001)), состояния после окклюзий и осложнений диабетической ретинопатии, макулодистрофия, «влажная» форма, в т. ч. на фоне интравитреальных инъекций препаратами – ингибиторами ангиогенеза и др.); пациенты с травмами и заболеваниями органа зрения в анамнезе, проведение тонометрии у которых могло искажать результаты; пациенты после интракапсулярной экстракции катаракты, «классической» экстракапсулярной экстракции катаракты или факоэмульсификации, прошедших с осложнениями (например, частичная потеря стекловидного тела или наличие послеоперационного астигматизма более ±3 диоптрий); пациенты с любой формой отслойки сетчатки (оперированная или неоперированная); пациенты с общими (системными) заболеваниями, требующими гормональной терапии, как это принято согласно методике проведения клинических исследований .
Методы статистического анализа
Обработка полученных данных проводилась одним исследователем с использованием программы Statistica (версии 8.0, StatSoft Inc., США). Приводимые параметры, имеющие нормальное распределение, представлены в формате М±m, где М – среднее значение, m – стандартная ошибка среднего значения. Распределение количественных параметров приведено в соответствии с W-критерием Шапиро – Уилка. Параметры, имеющие распределение, отличное от нормального, представлены в формате Мe (Q25%; Q75%), где Мe – медиана, а Q25% и Q75% – квартили. При нормальном распределении параметров для сравнения двух независимых групп или повторных внутригрупповых изменений использовался t-критерий Стьюдента. При отличном от нормального распределении параметров при сравнении нескольких независимых выборок использовался анализ для попарного сравнения двух независимых выборок – Z-аппроксимация U-критерия Манна – Уитни, для повторных внутригрупповых сравнений применялась Z-аппроксимация T-критерия Вилкоксона. Для проверки равенства медиан нескольких выборок применяли H-критерий Краскела – Уоллеса. Критический уровень значимости при проверке статистических гипотез принимался равным <0,05.Результаты и обсуждение
Средний возраст пациентов обеих групп на момент установления диагноза составил 65,35±8,87; 66 (59,5; 71,5) лет и 65,66±8,37; 66 (59,0; 72,0) лет соответственно, и этот показатель не имел статистически значимых отличий (p>0,05). Следует подчеркнуть, что возраст пациентов на момент установления диагноза «глаукома» отличался от среднестатистических показателей, опубликованных, в том числе и с нашим участием, ранее [6–13, 17]. В этом исследовании наши пациенты были старше в среднем на 5–7 лет. Продолжительность жизни пациентов, находящихся на учете в ФКУ «ЦВКГ им. П.В. Мандрыка» МО РФ, превышает среднюю по стране вследствие использования рациональной системы диспансерного наблюдения [21].На момент проведения оперативного лечения возраст пациентов составил 71,63±8,35; 69,5 (64,5;76,0) года и 75,06±7,61; 74 (68,0; 79,6) года соответственно, и установленные межгрупповые различия были статистически значимыми (p<0,004). В таблице 1 приведены возрастные характеристики пациентов обеих групп с разными стадиями заболевания.
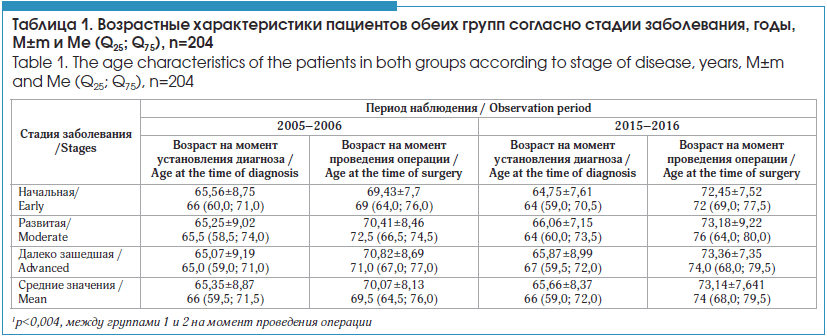
Согласно полученным результатам, глаукома по-прежнему диагностируется в сопоставимом возрасте, независимо от установленной стадии заболевания, но оперативное лечение в последние годы проводилось более возрастным пациентам. Вместе с тем, несмотря на более пожилой возраст таких пациентов на момент проведения оперативного лечения, количество сопутствующих заболеваний у лиц 2-й группы было сопоставимо с результатами лиц 1-й группы (3,38±1,78; 3 (2,00; 4;00) и 3,63±1,61; 4 (3,00; 4,00) соответственно, p>0,05), что свидетельствует в пользу применяемой системы динамического наблюдения в учреждении. Установленные различия биохимических показателей крови носили разнонаправленный характер: у больных 1-й группы были более высокие показатели общего холестерина (6,1±0,15; 6,00 (5,5; 7,0) ммоль/л и 5,3±0,13; 5,15 (4,5; 6,2) ммоль/л соответственно, p<00001)) и более низкие значения глюкозы крови (5,55±0,11; 5,4 (5,0; 5,8) ммоль/л и 5,9±0,11; 5,79 (5,3; 6,4) ммоль/л соответственно (p<00001)).
Остановимся более подробно на анализе сравнения стадий заболевания, диагностированных у пациентов по данным направления поликлиники, по данным стационарной истории болезни и согласно экспертному заключению. Эти данные приведены в таблице 2.
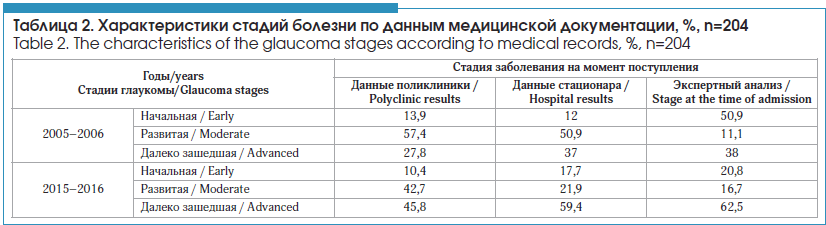
Ретроспективный экспертный анализ свидетельствует о преобладании начальной стадии заболевания у лиц, поступавших на оперативное лечение в 2005–2006 гг. Установленные различия между диагнозами направления/стационара и экспертным заключением, на наш взгляд, связаны в первую очередь с только внедрявшейся на тот момент (и по большей части экспериментальной) классификацией глаукомы, основанной на результатах САП [22, 23]. Ретроспективный экспертный анализ показал, что в основном различия в диагнозах отмечались именно между начальной и развитой стадиями глаукомы. По данным поликлиники и стационарной истории болезни имела место более продвинутая стадия заболевания. В поздний период наблюдения (2015–2016 гг.) различия в диагнозах при определении стадии болезни врачами поликлиники/стационара и экспертами находились в диапазоне от 3,1% до 5,2%, что подтверждает поэтапное внедрение новых знаний.
Развитие микрохирургических технологий привело к значительному увеличению числа пациентов, оперированных по поводу катаракты, из числа больных, поступавших для оперативного лечения глаукомы. Так, в 2005–2006 гг. таких пациентов было всего 11 (10,2%), тогда как в 2015–2016 гг. их стало 60, или 62,5% от общего числа больных. В основном артифакия была определена у лиц 2–й группы с далеко зашедшей стадией глаукомы (37,5%), что согласуется с возрастными характеристиками пациентов и прогрессированием катаракты в случае уже ранее выполненной антиглаукомной операции. В таблице 3 приведены данные, касающиеся наличия искусственного хрусталика глаза у больных, поступающих на оперативное лечение глаукомы согласно стадии заболевания.
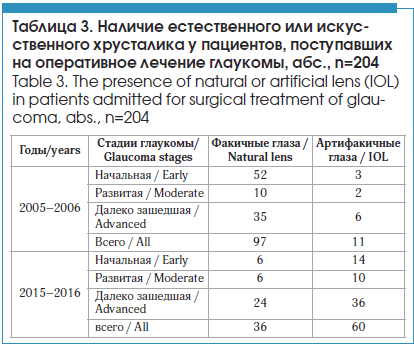
Глаукома – хроническое заболевание с прогредиентным течением, и в подавляющем большинстве случаев терапевтические подходы лечения сменяются один на другой (в силу нарушения толерантности к основным режимам применения гипотензивных антиглаукомных препаратов) и чередуются с проведением оперативного лечения. Анализ показал, что в 1-й группе среднее число оперированных ранее лиц составило 0,23±0,47; 0 (0,00; 2,00), а во 2-й группе – 0,46±0,78; 0 (0,00;4,00), p<0,035. Это указывает на изменение характеристик рефрактерности заболевания и подчеркивает востребованность оперативного лечения как одного из основных направлений терапии глаукомы. В то же время межгрупповое изменение структуры этой характеристики предполагает невысокую эффективность даже хирургического метода лечения глаукомы. В свою очередь анализ медикаментозных режимов инстилляций установил различия, существующие при выборе количества групп антиглаукомных препаратов, произошедшие за 10 лет (рис. 1). Так, среднее число препаратов, которые получали больные с глаукомой на момент поступления в стационар для оперативного лечения в 2005–2006 гг., составило 1,57±0,67; 2 (1,00; 2,00) единицы, и с течением времени это значение
достоверно увеличилось до 2,31±0,92; 2 (2,00; 3,00) единиц, p<0,00001.

В рамках этого исследования не подразумевалось проведение детального анализа отдельных групп антиглаукомных препаратов. Установлено, что в более ранний период времени большинство пациентов поступали на операцию, получая 1 или 2 препарата (90%), в то время как в последние годы число таких пациентов снизилось почти в 2 раза (до 50%), но значительно выросла доля больных, получавших 3 и более препаратов (с 10% до 50%, или в 5 раз в абсолютном исчислении). В таблице 4 приведены данные о количестве препаратов в зависимости от стадии заболевания в разные периоды наблюдения.

Продолжением оценки эффективности местной медикаментозной гипотензивной терапии стало определение сроков до момента выполнения первой операции. Установлено, что такие сроки за последние годы кардинально изменились. Было подсчитано, что средний срок, в течение которого пациенты получают медикаментозную терапию, прежде чем направляются на операцию, в 2005–2006 гг. составил 2 (1,00; 7,00) года, а в последнее время он достоверно увеличился – до 5,5 (2,00; 11,00) года, p<0,0009. Такие различия были получены в основном за счет результатов пациентов с начальной стадией глаукомы: сроки для них составили 2 (1,00; 7,00) года и 5 (4,00;10,00) лет соответственно, p<0,02. У больных с продвинутыми стадиями заболевания полученные результаты сравнения вышеуказанных сроков наблюдения были достоверно незначимыми (p>0,05). Последнее косвенно указывает на две очевидные вещи: во-первых, терапевтические подходы в силу развития фармакологического рынка все же могут являться вполне эффективным инструментом лечения больных с глаукомой; во-вторых, специалисты и пациенты стали крайне осторожны при выборе хирургической тактики у лиц с начальной стадией глаукомы.
При анализе морфофункциональных составляющих в первую очередь следует отметить различия в показателях ВГД, которые у больных 2-й группы в целом стали ниже. В таблице 5 приведены данные офтальмотонуса больных обеих групп.
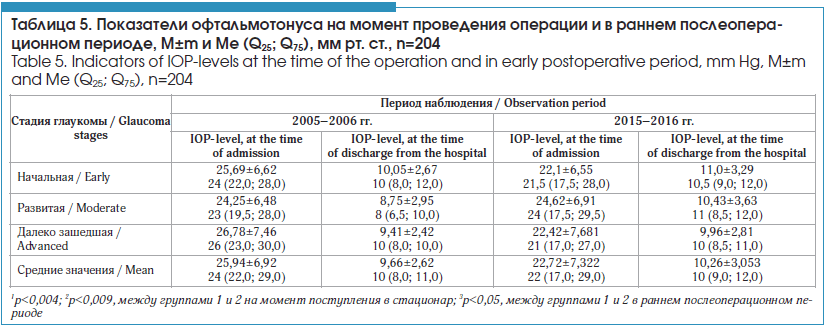
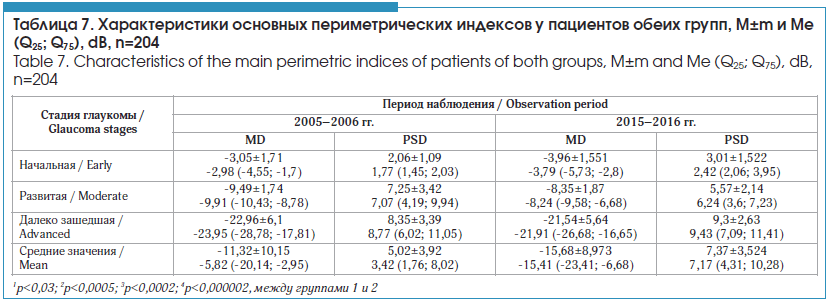
Из приведенных в таблице 5 данных следует, что пациенты, которые поступали на лечение в 2015–2016 гг., имели более низкий уровень офтальмотонуса (за счет больных с 3-й стадией глаукомы и в целом) благодаря приему большего количества гипотензивных препаратов (p<0,004). Но вместе с тем послеоперационный уровень ВГД в раннем послеоперационном периоде был выше, что, вероятнее всего, определяется естественным течением заболевания у лиц, которые более длительное время получают медикаментозную терапию (p<0,05). В таблицах 6 и 7 приведены результаты морфофункциональных исследований пациентов обеих групп, включающие состояние структуры зрительного нерва (площадь и объем НРП), СНВС и основные показатели САП.
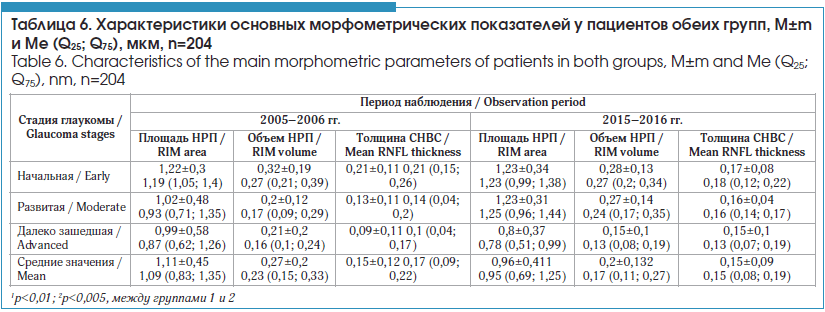
Было установлено, что пациенты 2-й группы имели более выраженные изменения морфометрической структуры, что было характерно для площади НРП (p<0,01) и его объема (p<0,005). В то же время состояние СНВС у пациентов обеих групп было сопоставимым (p>0,5).
Изменения периметрических индексов были статистически достоверны вследствие различий у пациентов с начальной стадией глаукомы (p<0,03 p<0,0005) и в целом (p<0,0002 и p<0,000002). Установленные межгрупповые изменения морфофункциональных характеристик могут быть следствием как указанных выше возрастных различий, так и утяжеления стадии заболевания в более поздний период наблюдения. В целом морфофункциональные характеристики соответствовали стадийности глаукомного процесса.
Различные типы антиглаукоматозных операций имеют свои показания в зависимости от формы и, конечно, от стадии глаукомы. При открытоугольной форме глаукомы применяются многочисленные модификации проникающих и непроникающих оперативных вмешательств. При анализе типов проведенных оперативных вмешательств было установлено, что в 2005–2006 гг. в 52,8% случаев использовались фистулизирующие оперативные пособия, а в 47,2% – операции непроникающего типа. В второй период наблюдения операции фистулизирующего типа составили лишь 14,6% случаев, в то время как хирургическое лечение с выполнением непроникающих операций проводилось в 85,4% случаев. Во всех случаях применялись различные модификации указанных выше оперативных вмешательств. По нашему мнению, предпочтительный выбор операций непроникающего типа был связан с большим количеством дополнительных дренажей и аддитивным применением лазерных технологий, используемых при выполнении этого типа операции, а также с осторожностью хирургов, пытавшихся обезопасить пациента от ранних послеоперационных осложнений. Вместе с тем предпочтения в выборе типа оперативного вмешательства, наряду с изменением тяжести глаукомного процесса в сторону увеличения количества больных с далеко зашедшей стадией глаукомы, повлияли негативно на изменение числа ранних послеоперационых осложнений, таких как гифема, отслойка сосудистой оболочки и синдром мелкой передней камеры. Так, в 2005–2006 гг. ранние осложнения были отмечены в 4,6% случаев, а в 2015–2016 гг. их число увеличилось почти в 4 раза, составив 17,7%. Мы не исключаем, что в более ранний период наблюдения такие осложнения документально фиксировались в меньшей степени. В пользу этого свидетельствует тот факт, что даже несмотря на изменения характеристик течения послеоперационного процесса средние сроки продолжительности нахождения в стационаре достоверно уменьшились: с 8 (6,5; 11,0) дней в 2005–2006 гг. до 7 (5,0; 10,0) дней в 2015–2016 гг. (p<0007).
Анализируя выбор дня недели для проведения оперативного лечения в обеих группах наблюдения, следует выделить понедельник (21,3% и 31,3% от всех оперативных вмешательств), далее следуют четверг (31,5% и 24%), среда (26,9% и 21,9%) и вторник (20,4% и 24%). Преобладание первого и четвертого дней недели, скорее всего, связано с естественным «накоплением» пациентов за четверг – пятницу предыдущей недели и понедельник – среду недели текущей.
Ограничения исследования
В итоговый протокол пациентов с далеко зашедшей стадией глаукомы обеих групп были включены данные пациентов, периметрические индексы которых превышали рекомендованные значения для этой стадии. Такие исключения были сделаны в силу сохранности остроты зрения у вышеуказанных больных в обеих группах.В проведенном исследовании не был выполнен анализ групповой структуры препаратов, которые пациенты получали в разные периоды наблюдения. Вполне возможно, что именно появление и активное внедрение в практику новых антиглаукомных препаратов позволило более выраженно понизить уровень ВГД у больных с начальной стадией глаукомы, а это, в свою очередь, способствовало более позднему направлению пациентов на оперативное лечение.
Заключение
Было установлено, что независимо от стадии болезни глаукома диагностируется в сопоставимом возрасте, но в последнее время мы стали больше оперировать пациентов старших возрастных групп с далеко зашедшей стадией заболевания, в т. ч. чаще повторно и на артифакичных глазах.Пациенты, поступавшие на лечение в 2015–2016 гг., более продолжительно лечились при помощи антиглаукомной медикаментозной терапии с использованием 3 и 4 гипотензивных препаратов и имели более низкий уровень офтальмотонуса до момента выполнения операции, таким образом, изменились не только структура назначений, но и подходы к терапии в целом.
Согласно приведенной статистике изменился характер операций в отделении за счет значительного увеличения числа непроникающих вмешательств (и их многочисленных модификаций, в т. ч. и использования лазерных технологий), вместе с этим увеличилось количество ранних операционных осложнений, что коррелирует с утяжелением стадии заболевания на момент поступления, но за счет более быстрого купирования осложнений уменьшилась продолжительность койко-дня.
Обращает на себя внимание несоответствие в стадиях заболевания на разных этапах (поликлиника – стационар – экспертный анализ), особенно в начале – середине 2000–х гг., что, на наш взгляд, связано как с недостаточной распространенностью современных приборов для диагностики и мониторинга заболевания на тот момент времени, так и со структурно-функциональными несоответствиями самого заболевания, а также с использованием устаревшей классификации заболевания и отсутствием в новых федеральных рекомендациях четких указаний на использование современных приборов при определении стадии болезни.
Результаты данной работы могут быть использованы при анализе эффективности лечения больных глаукомой. Исследование предполагает продолжение с целью оценки эффективности проведенного лечения и диспансерного наблюдения в отдаленные периоды.
Сведения об авторах: 1,2 Куроедов Александр Владимирович – д.м.н., профессор; 2Криницына Екатерина Аркадьевна – врач-ординатор; 3Сергеева Валерия Михайловна – врач-ординатор; 1Городничий Виталий Владимирович – врач-офтальмолог. 1ФКУ «Центральный военный клинический госпиталь им. П.В. Мандрыка» МО РФ. 107014, Российская Федерация, Москва, ул. Б. Оленья, 8А; 2ФГБОУ ВО «РНИМУ им. Н.И. Пирогова» Минздрава России. 117997, Российская Федерация, Москва, ул. Островитянова, 1. 3ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова (Сеченовский Университет)» Минздрава России. 119991, Российская Федерация, Москва, ул. Трубецкая, 8-2. Контактная информация: Куроедов Александр Владимирович, e-mail: akuroyedov@hotmail.com. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 12.09.2017.
About the authors: 1,2Alexander V. Kuroedov – professor; 2Ekaterina A. Krunitsyna – resident; 3Valeria M. Sergeeva – resident; 1Vitaly V. Gorodnichiy - ophthalmologist. 1Central Military Clinical Hospital named after P.V. Mandrykа. 8A, B. Olenya str., Moscow, 107014, Russian Federation. 2Russian National Research Medical University named after N.I. Pirogov. 1, Ostrovityanova str., Moscow, 117997, Russian Federation. 3First Moscow State Medical University named after I.M. Sechenov. 8-2, Trubetskaya str., Moscow, 119991, Russian Federation. Contact information: Alexander V. Kuroedov, e-mail: akuroyedov@hotmail.com Financial Disclosure: no author has a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 12.09.2017.








.gif)



