Введение
Неутешительная медицинская статистика свидетельствует о том, что заболевания коленного сустава по-прежнему представляют собой серьезную проблему. Наиболее распространенные из них — остеоартроз (ОА) и дегенеративные разрывы менисков (ДРМ), которые характерны для пациентов возрастной группы старше 35 лет, а у больных с ОА их частота достигает 75–95% [1–4]. ДРМ не ассоциированы с острой травмой, они могут провоцироваться на фоне дегенерации и ослабления прочности ткани на микроуровне и обусловлены старением либо ОА [4, 5]. С возрастом частота дегенеративных повреждений менисков прогрессивно возрастает, причем у большинства (около 60%) обследованных клинические симптомы отсутствуют, а повреждения являются случайной находкой при проведении магнитно-резонансной томографии (МРТ) [6, 7].
В настоящее время в лечении пациентов с ДРМ на фоне ОА предпочтение отдают артроскопическим вмешательствам с целью частичной менискэктомии [8, 9]. В то же время высокая распространенность разрывов менисков у пациентов с ОА, которые часто протекают бессимптомно, не позволяет достоверно определить, вызваны ли клинические проявления заболевания непосредственно разрывом, ОА или и тем и другим вместе. В связи с этим вопрос выбора тактики лечения остается дискутабельным: следует ли лечить пациентов с ДРМ на фоне ОА хирургическим путем или разумнее отдать предпочтение консервативному лечению [3, 10–14]. Несмотря на то, что многие пациенты пожилого возраста, страдающие ОА, сообщают о симптоматическом облегчении после артроскопии коленного сустава, рандомизированные плацебо-контролируемые исследования достоверно не подтверждают этого [2, 3, 10–14]. В то же время анализ результатов двухлетнего наблюдения пациентов после артроскопической парциальной менискэктомии, выполненной по поводу ДРМ на фоне тяжелого ОА, сопровождавшегося острой болью, показал снижение болезненности у 65% прооперированных и отсутствие прогрессирования ОА [15].
Согласно клиническим рекомендациям лечение дегенеративных заболеваний коленного сустава заключается в комплексном воздействии, которое включает в себя немедикаментозные и медикаментозные методы, а при необходимости и хирургическое вмешательство [16]. В качестве лекарственных средств используются симптоммодифицирующие препараты быстрого действия, влияющие на клинические симптомы заболевания (боль, воспаление), — нестероидные противовоспалительные препараты (НПВП) [16] и симптоммодифицирующие препараты замедленного действия (Symptomatic Slow-Acting Drugs for OsteoArthritis — SYSADOA), эффект которых проявляется медленно, но сохраняется после окончания лечения [17, 18]. К сожалению, НПВП могут вызывать серьезные побочные эффекты, прежде всего со стороны желудочно-кишечного тракта (ЖКТ) и сердечно-сосудистой системы, поэтому предпочтение следует отдавать селективным ингибиторам ЦОГ-2, при применении которых риск развития гастро- и энтеропатии значительно ниже [19]. Ярким представителем таких препаратов является целекоксиб (Симкоксиб), доказавший свою эффективность при низкой частоте побочных эффектов.
Препараты из группы SYSADOA, к которым относятся глюкозамина сульфат (ГС) и хондроитина сульфат (ХС), вызывают симптоматическое улучшение, сходное с эффектом «простых» анальгетиков и НПВП, предотвращают прогрессирование структурных изменений. О перспективности применения комбинации ГС и ХС свидетельствуют как экспериментальные, так и клинические данные [20–22]. КОНДРОнова® — один из первых комбинированных препаратов (класс рекомендаций 1A), продемонстрировавший хорошую переносимость даже у пациентов с сопутствующими заболеваниями и непереносимостью стандартных НПВП [23].
Появление в последние годы более безопасных препаратов, в т. ч. оказывающих модифицирующее действие на хрящ, а также совершенствование реабилитационных методов лечения, с одной стороны, и неоднозначные результаты хирургических вмешательств — с другой, подталкивают исследователей к поиску более эффективных и безопасных подходов к лечению пациентов с дегенеративными изменениями коленного сустава.
Цель исследования: оценить эффективность консервативного лечения у пациентов с ДРМ на фоне ОА в качестве альтернативы комбинированному лечению.
Материал и методы
В когортное проспективное сравнительное исследование было включено 236 человек (из них 70 мужчин), получавших лечение по поводу дегенеративного разрыва одного из менисков на фоне ОА коленного сустава в период с 01.06.2020 по 01.02.2021.
Критерии включения: возраст 45–65 лет; признаки разрыва мениска на фоне ОА, обнаруженные с помощью МРТ; боль при движении по визуально-аналоговой шкале (ВАШ) не менее 40 мм на протяжении последних 2 нед.; неприменение любых препаратов из групп SYSADOA и НПВП в течение 3 нед.; добровольное согласие на участие в исследовании и готовность к адекватному сотрудничеству.
Критерии исключения: аллергические реакции на препараты; противопоказания к применению препаратов; отказ от участия в исследовании; онкологические заболевания любой локализации; заболевания печени с печеночной недостаточностью; хронические заболевания почек с почечной недостаточностью.
Обследование включало сбор жалоб, анамнеза, оценку антропометрических показателей и ортопедического статуса, оценку боли по ВАШ и оценку по WOMAC (боль, скованность и функциональность), МРТ и рентгенографию коленного сустава.
В исследование были включены пациенты с ДРМ, подтвержденным данными МРТ, на фоне ОА коленного сустава I–III стадии по рентгенологической классификации Келлгрена — Лоуренса. В зависимости от метода лечения пациенты были разделены на 2 группы.
В 1-ю группу вошли 122 пациента (из них 86 женщин), которым было проведено комбинированное лечение, включающее артроскопическое оперативное вмешательство по поводу разрыва мениска коленного сустава и комплексную терапию в послеоперационном периоде (НПВП, препарат из группы SYSADOA, лечебная физкультура, физиотерапевтическое лечение).
Артроскопические вмешательства на коленном суставе выполняли c использованием стандартных портов. Осуществляли парциальную менискэктомию, при повреждении хряща вмешательство дополняли хондропластикой. С первых суток после вмешательства разрешали ходьбу с полной нагрузкой на оперированную конечность.
Вторую группу составили 114 пациентов (из них 80 женщин), которые отказались от операции, в связи с чем им был проведен только курс комплексного консервативного лечения, аналогичный таковому в 1-й группе.
Терапия включала назначение препаратов Симкоксиб и КОНДРОнова®. Симкоксиб в дозе 200 мг назначали по 1 капсуле 2 р/сут, длительность терапии зависела от индивидуальной клинической ситуации, непрерывный прием препарата составлял от 14 до 30 дней. Препарат КОНДРОнова® назначали внутрь по 2 капсулы 3 р/сут, длительность курса лечения составила 60 дней.
Немедикаментозные мероприятия включали: лечебную физкультуру, обучение пациента использованию ортопедических приспособлений для передвижения и иммобилизации сустава, физиотерапевтическое лечение.
Пациенты были обследованы повторно через 10 нед. и 20 нед. после начала лечения. При каждом визите проводили ортопедический осмотр, обследование по ВАШ и WOMAC. Первичной конечной точкой оценки эффективности терапии было уменьшение выраженности боли в суставах по ВАШ, а также динамика индекса WOMAC. Дополнительно оценивали удовлетворенность пациентов лечением (по шкале от 1 до 5, где «1» — полное отсутствие улучшения или ухудшение, а «5» — превосходный результат лечения) и качество жизни по опрос-нику EQ-5D. Эффективность лечения оценивалась как отличная, хорошая, удовлетворительная и как отсутствие эффекта. Переносимость медикаментозной терапии оценивали по частоте развития побочных эффектов и определяли как отличную, хорошую, удовлетворительную и плохую.
Cтатистическую обработку проводили с использованием пакета программ Statistica 12.0, SPSS. Определяли среднее арифметическое (M), дисперсию, ошибку среднего арифметического (m). Достоверность различий оценивали с помощью непараметрического U-критерия Манна — Уитни. Различия считали значимыми при p<0,05. Корреляционный анализ проведен с использованием рангового коэффициента корреляции Спирмена (r). Для оценки тесноты связей использовали шкалу Чеддока. Статистическую значимость коэффициента корреляции оценивали при помощи t-критерия Стьюдента. Корреляционную связь считали статистически значимой при p<0,05.
Результаты исследования
Пациенты групп исследования были сопоставимы по возрасту, длительности заболевания, интенсивности суставного синдрома, степени нарушения функции сустава, активности и рентгенологической стадии заболевания. Выявлены статистически значимые различия (p<0,05) между мужчинами и женщинами в каждой из обследуемых групп по индексу массы тела (ИМТ), сопутствующим соматическим заболеваниям. Данные МРТ показали преобладание в обеих группах пациентов с признаками ДРМ и ОА II стадии по классификации Келлгрена — Лоуренса независимо от пола. Результаты по ВАШ и опроснику WOMAC выявили статистически значимые отличия (p<0,05), показывающие, что женщины определяют выраженность болевого синдрома выше, чем мужчины, что связано с преобладанием у них эмоциональной составляющей. Показатели скованности и функциональности сустава по WOMAC были сопоставимы в обеих группах и не зависели от половой принадлежности (табл. 1).

Через 10 нед. после начала лечения у большинства пациентов обеих групп независимо от пола и возраста отмечалось значимое уменьшение боли по ВАШ, которое сохранялось и даже увеличивалось к 20-й неделе наблюдения. Несмотря на то, что исходно боль была больше выражена у женщин, динамика боли на обоих сроках наблюдения не зависела от пола.
Динамика показателей по WOMAC через 10 нед. и 20 нед. наблюдения в обеих группах показала значимое уменьшение всех параметров (боли, скованности и функциональности) уже к 10-й неделе, и показатели прогрессивно продолжали снижаться к 20-й неделе и не зависели от пола, возраста, сопутствующей патологии и вида лечения (табл. 2).

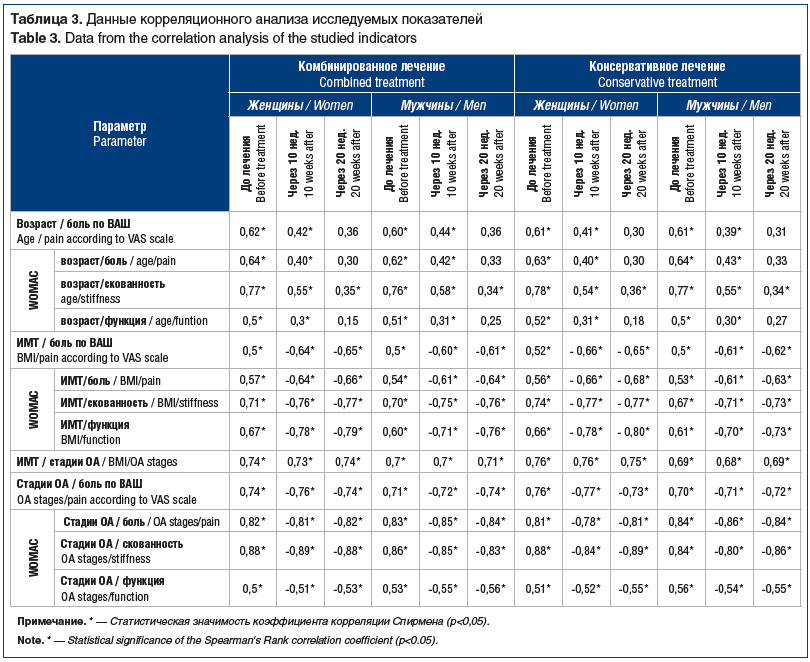
Для выявления факторов эффективности терапии проведен корреляционный анализ. Определены достоверные умеренные корреляционные связи между возрастом, ИМТ, стадией ОА и всеми показателями по ВАШ и WOMAC, а также достоверные сильные корреляционные связи между полом и болью по ВАШ (r=0,92, p<0,05) и субшкале WOMAC (r=0,82, p<0,05).
Анализ корреляционных взаимодействий по коэффициенту корреляции рассматривали в тех случаях, где он присутствовал у обследуемых пациентов и до лечения. При этом было отмечено, что корреляция по сравнению с исходными показателями сохранялась или изменялась на всех сроках наблюдения. Это говорит о том, что в нормальном состоянии существуют определенные взаимосвязи между показателями состояния коленного сустава, необходимые для функционирования.
С увеличением срока наблюдения отмечено ослабление корреляционной связи между полом и болью по ВАШ и субшкале WOMAC, так как женщины определяют выраженность болевого синдрома выше, чем мужчины, что обусловлено преобладанием у них эмоциональной составляющей. Ослабление корреляционных связей между возрастом и показателями по ВАШ и WOMAC в обеих группах свидетельствует об отсутствии влияния возраста на эффективность лечения. С увеличением периода наблюдения отмечается изменение направления и усиление связей между ИМТ и показателями по ВАШ и WOMAC, что говорит об обратной зависимости эффективности проводимого лечения и функционального индекса от ИМТ. Также корреляционный анализ показал, что эффективность комбинированного и консервативного лечения находится в обратной зависимости от стадии ОА по классификации Келлгрена — Лоуренса (табл. 3).
Анализ удовлетворенности лечением показал, что пациенты после консервативного лечения дали более высокую оценку общего состояния, чем пациенты после комбинированного лечения, что, возможно, связано с неоправдавшимися надеждами на лучший исход оперативного лечения, особенно у женщин. По мнению врачей, состояние наблюдаемых пациентов не вернулось к исходному значению, оставаясь после лечения достоверно лучше (табл. 4).

Основным следствием изменений состояния опорно-двигательного аппарата при ОА является изменение качества жизни пациентов. Результатом комбинированного лечения стало улучшение качества жизни по опроснику EQ-5D к 10-й неделе на 38% (p<0,05), к 20-й неделе — на 49% (p<0,05); у 102 пациентов 2-й группы качество жизни улучшилось на 40% (p<0,05) и на 51% (p<0,05) соответственно, у 12 пациентов — только на 11% (p<0,05). Ни у одного из наблюдаемых пациентов в обеих группах качество жизни после лечения не снизилось до прежнего уровня.
Подавляющее большинство пациентов дали высокую, хорошую или отличную оценку результатам комплексной медикаментозной терапии. Умеренный ответ на лечение был отмечен у 20% пациентов, низкий ответ — у 10% пациентов 2-й группы, которые продолжали принимать НПВП до 4 нед.
У 12 пациентов (7 женщин и 5 мужчин) 2-й группы эффект от лечения к 20-й неделе оказался недостаточным, по мнению и пациентов, и врачей. В ходе наблюдения периодически выявлялись механические симптомы в коленном суставе, в основном кратковременные блокады сустава, устраняющиеся самопроизвольно, а также болезненные щелчки. Через 25 нед. от начала терапии этим пациентам проведено хирургическое лечение. При артроскопической ревизии у них были выявлены значительная хондромаляция мыщелков, свободные внутрисуставные тела, а также нестабильные, чаще всего лоскутные повреждения менисков. Ожидать отличного результата только от консервативных мероприятий у этих пациентов было излишне оптимистично. После операции все пациенты отметили значительное снижение выраженности боли и увеличение объема движений в коленном суставе.
Переносимость препаратов Симкоксиб и КОНДРОнова® была хорошей. Ни один из пациентов не прервал лечение из-за нежелательных реакций.
Обсуждение
Вопрос о характере связи между ДРМ и ОА коленного сустава до сих пор не нашел однозначного ответа. По одним данным, начавшаяся дегенерация мениска приводит к потере его функции, повышению давления на суставные хрящи и подлежащую субхондральную кость и в итоге обусловливает развитие ОА коленного сустава [1, 4]. По другим данным, при развитии ОА в дегенеративный процесс вовлекаются и мениски, т. е. ДРМ возникает вторично [24].
Дискуссию также вызывает вопрос относительно связи болевого синдрома в коленном суставе с наличием ДРМ у пациента. Убедительных доказательств того, что боль в коленном суставе, особенно пораженном ОА, напрямую связана с ДРМ, нет, однако пациенты этой группы часто подвергаются артроскопическому вмешательству, и среди них, а также среди врачей распространено убеждение об уменьшении симптомов в коленном суставе после операции [7–9].
Полученные в ходе проведенного нами исследования результаты свидетельствуют о высокой эффективности выбранных препаратов в лечении дегенеративных заболеваний коленного сустава и согласуются с данными метаанализа 36 РКИ (n=17 206), согласно которым целекоксиб в дозировке 200 мг эффективнее, чем плацебо, снижал боль в среднем на 16% и превосходил по эффективности другие НПВП в среднем на 11% (p<0,05) [16]. В работе [23] монотерапия препаратом КОНДРОнова® в течение 3,8±0,7 мес. обусловила уменьшение боли в покое на 33,3%, при движении — на 60%, при пальпации — на 47,1% от исходной. Пациенты отмечали увеличение объема движений, уменьшение хруста, утренней скованности, снижение числа болезненных суставов.
Минимальные различия между группами по динамике показателей боли и функциональности коленного сустава указывают на целесообразность отказа от хирургических методов лечения ДРМ на фоне ОА до тех пор, пока не будет проведена адекватная комплексная терапия. Это предположение подтверждается данными литературы, согласно которым различия в клинических исходах после артроскопического хирургического вмешательства по сравнению с консервативным лечением отсутствуют [10–14].
При проведении консервативного лечения у пациентов старшей возрастной группы, особенно при применении НПВП, особое внимание следует уделять безопасности. На протяжении всего нашего исследования ни у одного больного не были зарегистрированы побочные эффекты, которые потребовали бы снижения дозы или отмены препарата. Комплексная терапия с использованием препаратов Симкоксиб и КОНДРОнова® хорошо переносилась пациентами и показала свою безопасность.
Высокая селективность целекоксиба к ЦОГ-2 снижает риск гастроинтестинальных осложнений, обусловленных влиянием на ЦОГ-1. Это подтверждают данные других исследований. В метаанализе 52 РКИ (n=51 048) сравнивали безопасность целекоксиба, плацебо и неселективных НПВП. Оценивался суммарный индекс негативного влияния на ЖКТ, включавший частоту кровотечений и перфораций желудка и кишечника, развития язв и анемии, связанной с кишечной кровопотерей. Частота этих осложнений составила 1,0, 0,9 и 2,3 эпизода на 100 пациентов-лет [25].
Не меньшие опасения при использовании НПВП вызывают кардиоваскулярные осложнения. Преимущества целекоксиба показаны в масштабном исследовании [26], в котором препарат продемонстрировал минимальный риск кардиоваскулярных катастроф (относительный риск 1,06; 95% доверительный интервал (95% ДИ) 0,83—1,34). Для других селективных НПВП этот показатель был выше: для мелоксикама — 1,24 (95% ДИ 0,99–1,55), для нимесулида — 1,69 (95% ДИ 1,43–1,99), а для этерококсиба значительно выше — 2,21 (95% ДИ 1,18–4,14).
Данных о развитии серьезных побочных эффектов при применении препарата КОНДРОнова® и веществ, входящих в его состав, в мировой литературе нами не найдено. Достоверное улучшение качества жизни и общего состояния пациентов по оценке врачей на 39,1±1,5% к 10-й неделе и на 42,0±3,7% к 20-й неделе наблюдения свидетельствует о высокой эффективности подобранного под конкретного пациента комбинированного или консервативного лечения.
Подводя итоги, можно заключить, что выполнение артроскопической парциальной менискэктомии в качестве первой ступени лечения ДРМ не оправданно. Результаты нашего исследования свидетельствуют, что на первом этапе следует проводить консервативное лечение, включающее курс НПВП в сочетании с препаратами из группы SYSADOA и реабилитационную программу, направленную на улучшение функционального состояния мышц нижней конечности. Артроскопическая менискэктомия показана при неэффективности неоперативного подхода, которая в нашем исследовании понадобилась лишь 12 пациентам (7 женщинам и 5 мужчинам).
Выводы
Комплексная терапия, включающая применение симптоммодифицирующих препаратов быстрого (Симкоксиб) и медленного (КОНДРОнова®) действия в рекомендованных дозах в комбинации с немедикаментозными методами лечения продемонстрировала высокую эффективность и безопасность при лечении пациентов с ДРМ на фоне ОА.
Артроскопическую парциальную менискэктомию не следует предлагать пациентам в качестве первого этапа лечения ДРМ. Основными причинами боли в коленном суставе при ДРМ, по данным литературы, скорее всего, являются синовит, развивающийся в период обострения ОА, а также избыточное давление на суставной хрящ и субхондральную кость, которое возникает в связи со снижением амортизирующих свойств мениска при его дисфункции. Выраженность этих процессов напрямую коррелирует со стадией ОА. В связи с этим удаление части мениска в большинстве случаев стабильных дегенеративных разрывов не приведет к купированию болевого синдрома.
Показанием к раннему проведению артроскопической операции может быть только нестабильное повреждение мениска с наличием механических симптомов (болезненных щелчков и периодически возникающей блокады коленного сустава).
Благодарность
Редакция благодарит ООО «ПанБио Фарм» за оказанную помощь в технической редактуре настоящей публикации.
Acknowledgment
Editorial Board is grateful to LLC PBF for the assistance in technical edition
of this publication.
Сведения об авторах:
Бессараб Максим Сергеевич — к.м.н., врач травматологического отделения ГБУЗ «ГКБ им. Ф.И. Иноземцева ДЗМ»; 105187, Россия, г. Москва, ул. Фортунатовская, д. 1; ORCID iD 0000-0002-6781-0310.
Краснов Генрих Олегович — врач травматологического отделения ГБУЗ «ГКБ им. Ф.И. Иноземцева ДЗМ»; 105187, Россия, г. Москва, ул. Фортунатовская, д. 1; ORCID iD 0000-0002-8148-2237.
Чарчян Артак Михайлович — к.м.н., заведующий травматологическим отделением ГБУЗ «ГКБ им. Ф.И. Иноземцева ДЗМ»; 105187, Россия, г. Москва, ул. Фортунатовская, д. 1; ORCID iD 0000-0003-0813-4647.
Хорошков Сергей Николаевич — д.м.н., профессор кафедры травматологии, ортопедии и медицины катастроф ФГБОУ ВО МГМСУ им. А.И. Евдокимова Минздрава России; 127473, Россия, г. Москва, ул. Делегатская, д. 20/1; ORCID iD 0000-0003-3452-5166.
Контактная информация: Бессараб Максим Сергеевич, e-mail: fulcrum666@gmail.com. Прозрачность финансовой деятельности: никто из авторов не имеет финансовой заинтересованности в представленных материалах или методах. Конфликт интересов отсутствует. Статья поступила 22.02.2021, поступила после рецензирования 15.03.2021, принята в печать 31.03.2021.
About the authors:
Maxim S. Bessarab — Cand. of Sci. (Med.), doctor of the Department of Traumatology, F.I. Inozemtsev City Clinical Hospital; 1, Fortunatovskaya str., Moscow, 105187, Russian Federation; ORCID iD 0000-0002-6781-0310.
Genrikh O. Krasnov — doctor of the Department of Traumatology, F.I. Inozemtsev City Clinical Hospital;
1, Fortunatovskaya str., Moscow 105187, Russian Federation; ORCID iD 0000-0002-8148-2237.
Artak M. Charchyan — Cand. of Sci. (Med.), Head of the Department of Traumatology, F.I. Inozemtsev City Clinical Hospital; 1, Fortunatovskaya str., Moscow, 105187, Russian Federation; ORCID iD 0000-0003-0813-4647.
Sergey N. Khoroshkov — Dr. of Sci. (Med.), Professor of the Department of Traumatology, Orthopedics and Emergency Medicine, A.I. Yevdokimov Moscow State University of Medicine and Dentistry; 20/1, Delegatskaya str., Moscow, 127473, Russian Federation; ORCID iD 0000-0003-3452-5166.
Contact information: Maxim S. Bessarab, e-mail:
fulcrum666@gmail.com. Financial Disclosure: no authors have a financial or property interest in any material or method mentioned. There is no conflict of interests. Received 22.02.2021, revised 15.03.2021, accepted 31.03.2021.








.gif)



